BCR-ABL酪氨酸激酶抑制劑的研究進(jìn)展
王偉,鄒志紅
(東南大學(xué)化學(xué)化工學(xué)院,江蘇南京 210009)
人體9號(hào)染色體上的癌基因c-ABL鏈接到22號(hào)染色體上的斷點(diǎn)簇集區(qū)(BCR),形成p210 BCR-ABL融合基因和p185 BCR-ABL融合基因,這兩種融合基因使相應(yīng)的BCR-ABL酪氨酸激酶持續(xù)激活,引起細(xì)胞增殖、黏附和生存性質(zhì)的改變,分別導(dǎo)致產(chǎn)生慢性粒細(xì)胞白血病(CML)和急性粒細(xì)胞白血病(ALL)[1]。之前治療這類(lèi)疾病主要依靠單克隆抗體藥物,直到2001年美國(guó)FDA批準(zhǔn)了第一個(gè)治療CML的BRCABL酪氨酸激酶抑制劑伊馬替尼后,尋找小分子化合物抑制BRC-ABL酪氨酸激酶以治療上述疾病逐漸成為人們關(guān)注的熱點(diǎn)。本文擬就BRC-ABL酪氨酸激酶抑制劑的研究進(jìn)展作一綜述。
1 第一代BCR-ABL酪氨酸激酶抑制劑
20世紀(jì)90年代初,在Zimmermann的帶領(lǐng)下,合成了一系列以2-苯氨基嘧啶為主體的小分子化合物,經(jīng)過(guò)篩選發(fā)現(xiàn)伊馬替尼(Imatinib,STI571)能夠特異性的抑制BCR-ABL酪氨酸激酶的活性[2]。其結(jié)構(gòu)式見(jiàn)圖1。2001年5月10日美國(guó)FDA批準(zhǔn)了諾華公司(Novartis)的伊馬替尼用于治療CML,這是首個(gè)治療CML的BCR-ABL酪氨酸激酶抑制劑,具有劃時(shí)代的意義,被美國(guó)《科學(xué)》雜志列入2001年度十大科技新聞[3]。現(xiàn)已明確,伊馬替尼并非絕對(duì)特異的酪氨酸抑制劑,除抑制BCR-ABL酪氨酸激酶活力外,對(duì)血小板衍化生長(zhǎng)因子 β(PDGF-β)受體酪氨酸激酶和干細(xì)胞因子(SCF)的c-kit配體酪氨酸激酶活力也存在同等程度的抑制[4]。然而,隨后的臨床研究表明,BCRABL基因發(fā)生了包括Y253H、E255V、E255K、F359V、T315I、G250E、F317L、E355G、H396P、M351T、M253H、L248V、Q252H、Y253H和Y253C等15種突變,BCRABL基因的突變導(dǎo)致伊馬替尼出現(xiàn)耐藥性[5]。
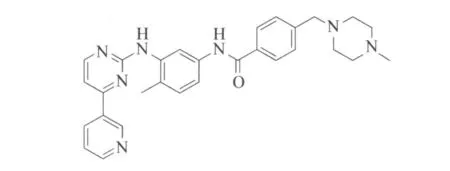
圖1 Imatinib結(jié)構(gòu)式
2 第二代BCR-ABL酪氨酸激酶抑制劑
由于伊馬替尼耐藥性的出現(xiàn),開(kāi)發(fā)新的BCR-ABL酪氨酸激酶抑制劑迫在眉睫。目前,第二代BCR-ABL酪氨酸激酶抑制劑已經(jīng)上市,主要藥物有達(dá)沙替尼和尼洛替尼。
2.1 達(dá)沙替尼
達(dá)沙替尼(Dasatinib,BMS-354825),結(jié)構(gòu)式見(jiàn)圖2,是由美國(guó)百時(shí)美施貴寶公司(Bristol-Myers Squibb)研發(fā)的一種口服BCR-ABL酪氨酸激酶抑制劑,于2006年6月28日通過(guò)美國(guó)FDA審批,用于治療CML和費(fèi)城染色體陽(yáng)性的急性淋巴細(xì)胞性白血病(ph+ALL)[6]。人們認(rèn)為該藥既可以與ABL酪氨酸的活性部位又可與其非活性部位連接,比伊馬替尼更有藥效但不會(huì)致死靜止的干細(xì)胞群[7]。在哺乳動(dòng)物中,其口服生物利用度14%~34%,其差異可能是與藥物的不能完全吸收以及首過(guò)效應(yīng)有關(guān)。藥代動(dòng)力學(xué)數(shù)據(jù)顯示達(dá)沙替尼主要是通過(guò)氧化代謝消除,對(duì)大部分伊馬替尼耐藥性的突變都有效[8]。
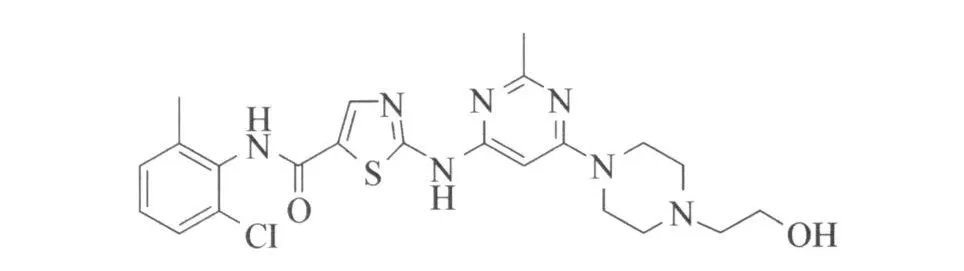
圖2 Dasatinib結(jié)構(gòu)式
2.2 尼洛替尼
苯胺嘧啶類(lèi)衍生物——尼洛替尼(Nilotinib,AMN107)在臨床上開(kāi)發(fā)為一種單鹽酸鹽形式,結(jié)構(gòu)式見(jiàn)圖3。這個(gè)分子結(jié)構(gòu)與伊馬替尼相關(guān)并且是通過(guò)伊馬替尼-ABL結(jié)合物的晶體結(jié)構(gòu)與藥物化學(xué)的關(guān)系研究而發(fā)現(xiàn)的[9]。尼洛替尼是一種選擇性的BCR-ABL酪氨酸激酶抑制劑,其有效性是伊馬替尼的20~50倍,能抑制除T315I外的伊馬替尼耐藥性BCR-ABL突變[10]。該藥于2007年10月29日經(jīng)美國(guó)FDA批準(zhǔn)用于治療CML。
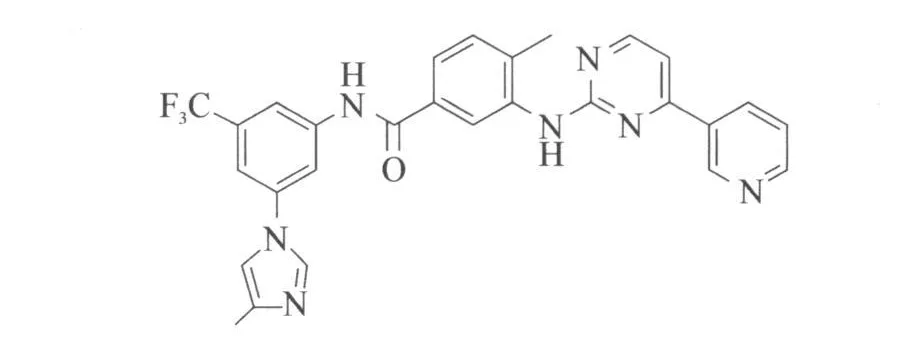
圖3 Nilotinib結(jié)構(gòu)式
雖然達(dá)沙替尼和尼洛替尼顯示出令人鼓舞的初步成效,但一些研究者報(bào)道它們使用后將在ABL激酶區(qū)引發(fā)新的突變。Ray等[11]已鑒別出17種在該激酶區(qū)上的突變,其中包括6種已知的伊馬替尼耐藥性突變(L248V、Q252H、Y253/C、E255K和T315I)和11種另外增加的突變(K247N、E282K、K285N、V289L、L273F、E292K、N297T、H375P、T406I、W430L和E431G)。
3 新近開(kāi)發(fā)的BCR-ABL酪氨酸激酶抑制劑
由于第二代BCR-ABL酪氨酸激酶抑制劑耐藥性的出現(xiàn),開(kāi)發(fā)出更新的BCR-ABL酪氨酸激酶抑制劑是很有必要的,目前正在開(kāi)發(fā)的主要有以下這些。
3.1 伯舒替尼
伯舒替尼(Bosutinib,SKI-606),結(jié)構(gòu)式見(jiàn)圖4,由惠氏制藥(Wyeth)開(kāi)發(fā),是SRC和BCR-ABL雙重抑制劑,該化合物對(duì)血小板源性生長(zhǎng)因子的酪氨酸激酶沒(méi)有活性[12],但能抑制BCR-ABL和LYN(一個(gè)芽殖期的內(nèi)褶蛋白質(zhì))轉(zhuǎn)磷酸化和細(xì)胞增殖作用。伯舒替尼對(duì)Y253H、E255V、E255K和F359V突變的BCR-ABL有效,在小鼠實(shí)驗(yàn)中顯示出有抑制K562異種移植物增生的作用[13],但對(duì)T315I突變依然沒(méi)有效果。在Ⅰ-Ⅱ期臨床研究中,69位伊馬替尼耐藥的CML或ph+ALL病人用伯舒替尼治療后癥狀都得到了好轉(zhuǎn),其副作用有腹瀉、惡心和嘔吐等[14]。
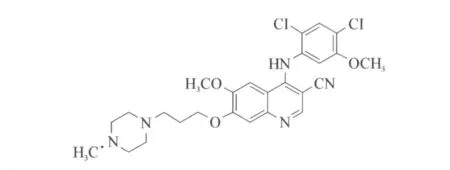
圖4 Bosutinib結(jié)構(gòu)式
3.2 INNO-406
INNO-406(CNS-9/NS-187),結(jié)構(gòu)式見(jiàn)圖5,由紐約因奴白制藥公司(Innovive Pharmaceutical,Inc.)開(kāi)發(fā),該化合物對(duì)BCR-ABL酪氨酸激酶的抑制活性是伊馬替尼的25~55倍,并且還能抑制達(dá)沙替尼耐藥的T315A,F317L和F317V BCR-ABL突變[15-16]。然而,該化合物對(duì)T315I突變依然沒(méi)有效果。INNO-406在大鼠模型中有口服活性并且是一種ATP競(jìng)爭(zhēng)性抑制劑。在Ⅰ期臨床試驗(yàn)中,受試病人至少有兩種其它酪氨酸激酶抑制劑的耐藥性,經(jīng)過(guò)INNO-406治療后已經(jīng)有了血液學(xué)和細(xì)胞遺傳學(xué)反應(yīng)[17]。
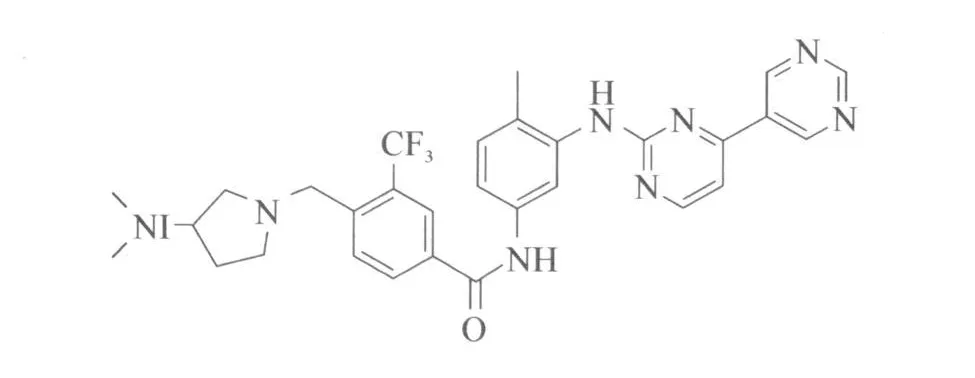
圖5 INNO-406結(jié)構(gòu)式
3.3 AP系列
Ariad公司研發(fā)的AP系列抗腫瘤化合物中,核心化合物AP23464已在臨床前研究中,結(jié)構(gòu)式見(jiàn)圖6,該化合物在低濃度時(shí)就可以通過(guò)抑制BCR-ABL的自磷酸化和細(xì)胞增殖來(lái)抑制BCR-ABL酪氨酸激酶[18],并且能抑制發(fā)生了Q252H、Y253F、E255K、M351H和H396P突變的BCR-ABL酪氨酸激酶,但該化合物依然不能抑制T315I突變。可喜的是同系列化合物AP23846和AP24534能抑制T315I突變,這兩種化合物臨床效果還有待于進(jìn)一步研究[19]。
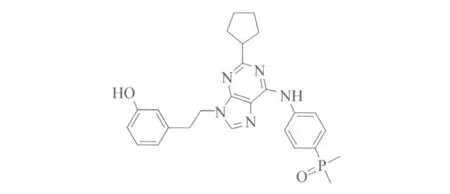
圖6 AP23464結(jié)構(gòu)式
3.4 PD系列
美國(guó)德州大學(xué)西南醫(yī)療中心的科學(xué)家對(duì)PD(乙酰吡啶[2,3-d]并嘧啶)系列化合物進(jìn)行了研究,其中核心化合物有PD173955、PD180970和PD166326,結(jié)構(gòu)式見(jiàn)圖7。通過(guò)這些化合物與ABL激酶結(jié)合物的晶體結(jié)構(gòu),推理得出它們與激酶區(qū)的活性ATP連接點(diǎn)結(jié)合產(chǎn)生活性,但這類(lèi)化合物與其他酶的類(lèi)似活性位點(diǎn)也結(jié)合,所以也能抑制表皮生長(zhǎng)因子(EGF)、EphB4、成纖維細(xì)胞生長(zhǎng)因子(FGF)、c-Kit、PDGF和血管內(nèi)皮細(xì)胞生長(zhǎng)因子(VEGF)受體酪氨酸激酶[20]。
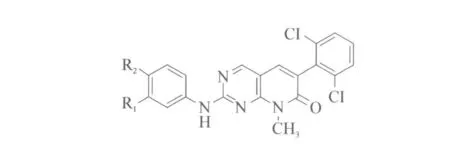
圖7 PD系列結(jié)構(gòu)式
這些化合物能夠抑制許多伊馬替尼耐藥性的BCR-ABL突變,但對(duì)T315I突變依然難以控制。Bubnoff等[21]評(píng)價(jià)了PD166326引起的突變,研究表明PD166326的耐藥性突變產(chǎn)生頻率要比伊馬替尼小,但其ABL激酶區(qū)的點(diǎn)突變卻比伊馬替尼多,第9位氨基酸殘基涵蓋了總共的14個(gè)點(diǎn)突變,包含最常見(jiàn)的G250E、Y253H、E255K(V)、T315I、F317L和E355G突變。然而,當(dāng)PD166326的濃度達(dá)到500 nM時(shí),這些突變了(除了T315I)的激酶活性能夠被抑制。由于現(xiàn)在的PD系列化合物溶解性低,口服利用度小,該系列化合物還未進(jìn)入臨床研究,因此開(kāi)發(fā)該類(lèi)型中新的化合物來(lái)克服這些缺點(diǎn)也是有必要的。
3.5 AZD0530
阿斯利康制藥公司(Astra Zeneca)開(kāi)發(fā)的BCRABL/SRC雙重酪氨酸激酶抑制劑AZD0530已進(jìn)入Ⅱ期臨床研究,其結(jié)構(gòu)式見(jiàn)圖8。結(jié)構(gòu)里有一個(gè)5-取代的喹唑啉環(huán)使得該分子對(duì)SRC家族激酶有很好的選擇性,也保持了抑制BCR-ABL的活性,并且抑制BCRABL激酶的耐藥性變異還未見(jiàn)報(bào)道,Ⅰ期臨床顯示該化合物可以很好地被人體吸收,且耐受劑量高,藥效持續(xù)時(shí)間長(zhǎng)[22]。AZD0530對(duì)人類(lèi)乳腺轉(zhuǎn)移MDA-MB231細(xì)胞具有活性,在胰臟和膀胱癌的大鼠模型中,AZD0530能夠在不影響源腫瘤細(xì)胞的情況下抑制腫瘤細(xì)胞轉(zhuǎn)移和預(yù)防Y530F SRC-轉(zhuǎn)染的NIH-3T3異種移植物的皮下轉(zhuǎn)移生長(zhǎng)[23]。目前,阿斯利康公司對(duì)AZD0530抑制SRC活性也做了臨床前研究[24]。
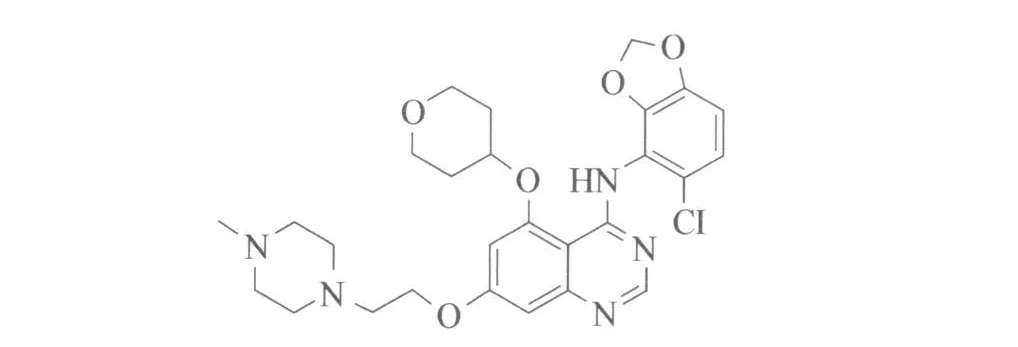
圖8 AZD0530結(jié)構(gòu)式
3.6 MK-0457
絲氨酸-蘇氨酸激酶的極光家族對(duì)有絲分裂過(guò)程是必需的,該家族的所有成員有可以確認(rèn)的ATP-連接位點(diǎn)并且通過(guò)遺傳的不穩(wěn)定性感應(yīng)來(lái)連接到腫瘤基因。默克公司(Merck)和維泰士公司(Vertex)共同研發(fā)的MK-0457(VX680),結(jié)構(gòu)式見(jiàn)圖9,是極光激酶抑制劑的一種并且在一些腫瘤細(xì)胞系中產(chǎn)生了抗增殖和促凋亡活性[25]。例如,用MK-0457作用后的細(xì)胞能進(jìn)入有絲分裂或通過(guò)S期繼續(xù)分化,但不會(huì)分裂開(kāi)。令人欣喜的是,MK-0457能與BCR-ABL活性部位連接并且有抗T315I突變的活性。這種抑制劑已經(jīng)進(jìn)入伊馬替尼耐藥性的CML和ph+ALL的Ⅱ臨床研究中。初始報(bào)告顯示3例有伊馬替尼耐藥性和T315I突變的病人出現(xiàn)了血液學(xué)反應(yīng),并且其中兩例病人中,突變體克隆的濃度也下降了[26]。
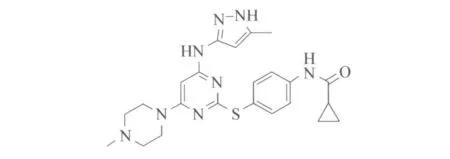
圖9 MK-0457結(jié)構(gòu)式
3.7 其他
Warmuth等[27]研究得出原來(lái)作為原癌基因SRC編碼的非受體型酪氨酸激酶抑制劑的CGP70630也能阻止BCR-ABL酪氨酸磷酸化,減緩腫瘤細(xì)胞的生長(zhǎng)和存活,但不能阻止T315I突變激酶的磷酸化。Lindsay等[28]研究了非-ATP競(jìng)爭(zhēng)型抑制劑ON012380,研究表明該化合物能降低BCR-ABL的自磷酸化和下游層的磷酸化,并且不管是在體內(nèi)還是體外該化合物抑制T315I突變的活性是伊馬替尼的10 000倍。Adrian等[29]研究得出GNF-2可通過(guò)一種變構(gòu)的非-ATP競(jìng)爭(zhēng)性機(jī)制抑制BCR-ABL激酶。Carter等[30]研究表明BIRB-796與T315I突變連接,但是相對(duì)于其他突變的BCR-ABL蛋白沒(méi)有活性。Chandra等[31]報(bào)道Adaphostin能誘導(dǎo)產(chǎn)生伊馬替尼耐藥性突變的BCR-ABL酪氨酸激酶氧化應(yīng)激來(lái)抑制其活性。Radi等[32]報(bào)道,他們發(fā)現(xiàn)一系列噻二唑衍生物,這些化合物是有效BCR-ABL酪氨酸激酶抑制劑,能抑制伊馬替尼耐藥的獨(dú)立BCR-ABL白血病細(xì)胞。Wang等[33]報(bào)道,一些新的N9-芳乙烯基嘧啶化合物可以作為有效的SRC/ABL酪氨酸激酶的雙重抑制劑。
4 結(jié) 語(yǔ)
對(duì)伊馬替尼耐藥的BCR-ABL突變體生物學(xué)結(jié)構(gòu)的了解使得BCR-ABL酪氨酸激酶抑制劑的研發(fā)有了新進(jìn)展。在確定病人有伊馬替尼耐藥的BCR-ABL突變后僅僅3年時(shí)間,兩種抑制該突變的新藥物——達(dá)沙替尼和尼洛替尼已經(jīng)上市。雖然這兩個(gè)藥物對(duì)T315I突變依然無(wú)效,但最近有抗T315I突變活性的化合物已被發(fā)現(xiàn)。隨著抑制現(xiàn)有BCR-ABL突變的新藥物不斷被研發(fā)出來(lái),分辨出不同類(lèi)型病人的最適合藥物變得越來(lái)越重要了。目前,新近開(kāi)發(fā)的BCR-ABL抑制劑越來(lái)越有效,并且聯(lián)合用藥也可增強(qiáng)治療效果,如Weisberg等[34]研究表明伊馬替尼和尼洛替尼聯(lián)合用于CML衍生的細(xì)胞系時(shí)有協(xié)同作用。進(jìn)一步研究BCR-ABL酪氨酸激酶作用機(jī)制和耐藥機(jī)制,開(kāi)發(fā)出全面的BCR-ABL酪氨酸激酶抑制劑是人們所期盼的。
[1]白亞軍.抗癌藥物伊馬替尼(Imatinib)堿的合成研究[D].西安:西北大學(xué),2007.
[2]潘耀柱,白海,王存邦.酪氨酸激酶抑制劑抑制骨髓瘤細(xì)胞的增殖及粘附[J].中國(guó)現(xiàn)代醫(yī)學(xué)雜志,2008,18(13):1863-1866.
[3]DAGHER R,COHEN M,WILLIAMS G,et al.Approval summary:imatinib mesylate in the treatment of metastatic and/or unresectable malignant gastrointestinal stromal tumors[J].Clin Cancer Res,2002,8(10):3034-3038.
[4]COHEN M H,WILLIAMSG,JOHNSONJ R,et al.Approval summary for imatinib mesylate capsules in the treatment of chronic myelogenous leukemia[J].Clin Cancer Res,2002,8(5):935-942.
[5]JABE F APPERLEY.Part II:Management of resistance to imatinib in chronic myeloid leukaemia[J].Lancet Oncol,2007,8(12):1116-1128.
[6]KANTARJIAN H,JABBOUR E,GRIMLEY,et al.Dasatinib[J].Nature Rev Drug Discov,2006,10(5):717-718.
[7]COPLAND M,HAMILTON A,EIRICK L J,et al.Dasatinib(BMS-354825)targets an earlier progenitor population than imatinib in primary CML but does not eliminate the quiescent fraction[J].Blood,2006,107(11):4532-4539.
[8]MULLER M C,ERBEN P,SCHENK T,et al.Response to dasatinib after imatinib failure according to type of preexisting BCR-ABL mutations[J].Blood,2006,108(1):225-260.
[9]CARLO G P,ROCCO P,MAURIZIO D.Bcr-Abl mutations,resistance to imatinib,and imatinib plasma levels[J].Blood,2003,102(5):1933-1935.
[10]KANTARJIANH,CORTESJ.New tyrosinekinaseinhibitors in chronic myeloid leukemia(CML)[J].Leukemia Res,2007,31(2):S16-S19.
[11]RAY A,COWAN-JACOB S W,MANLEY P W,et al.I-dentification of BCR-ABL point mutations conferring resistance to the Abl kinase inhibitor AMN107(nilotinib)by a random mutagenesis study[J].Blood,2007,109(11):5011-5015.
[12]GOLASJM,ARNDTK,ETIENNE C,et al.SKI-606,a 4-anilino-3-quinolinecarbonitrile dual inhibitor of Src and Abl kinases,is a potent antiproliferative agent against chronic myelogenous leukemia cells in culture and causes regression of K562 xenografts in nude mice[J].Cancer Res,2003,63(2):375-381.
[13]GRAFONE T,MANCINI M,OTTACIANI E,et al.A novel 4-anilino-3-quinolinecarbonitrile dual Src and Abl kinase inhibitor(SKI-606)has in vitro activity on CML Ph+blast cells resistant to imatinib[J].Proc Am Assoc Cancer Res,2005,46(5):1408-1413.
[14]GAMBACORTI-PASSERINI C,BLUMMEDORF T,KANTARJIAN H,et al.Bosutinib(SKI-606)exhibits clinical activity in patients with Philadelphia chromosome positive CML or ALL who failed imatinib[J].J Clin Oncol,2007,25(s1):33-47.
[15]DONATON J,WU JY,STAPLEY J,et al.BCR-ABL independence and LYNkinaseoverexpression in chronic myelogenous leukemia cells selected for resistance to STI571[J].Blood,2003,101(2):690-698.
[16]YASUYKI D A,SHINYA K,EISHI A.Comparison of imatinib,dasatinib,nilotinib and INNO-406 in imatinib-resistant cell lines[J].Leukemia Res,2008,32(6):980-983.
[17]NAITOH,KIMURA S,NAKAYA Y,et al.In vivoantiproliferative effect of NS-187,a dual Bcr-Abl/Lyn tyrosine kinase inhibitor,on leukemic cells harbouring Abl kinase domain mutations[J].Leukemia Res,2006,30(11):1143-1146.
[18]O'HARE T,POLLOCK R,STOFFREGEN E P,et al.Inhibition of wild-type and mutant Bcr-Abl by AP23464,a potent ATP-based oncogenic protein kinase inhibitor:implications for CML[J].Blood,2004,104(8):2532-2539.
[19]AZAM M,NARDIV,SHAKESPEARE WC,et al.Activity of dual SRC-ABL inhibitors highlights the role of BCR/ABL kinase dynamics in drug resistance[J].Proc Natl Acad Sci USA,2006,103(24):9244-9249.
[20]WISSING J,GODL K,BREHMER D,et al.Chemical proteomic analysis reveals alternative modes of action for pyrido[2,3-d]pyrimidine kinase inhibitors[J].Mol Cell Proteomics,2004,3(12):1181-1193.
[21]von BUBNOFF N,VEACH D R,MILLERW T,et al.Inhibition of wild-type and mutant Bcr-Abl by pyrido-pyrimidinetype small molecule kinase inhibitors[J].Cancer Res,2003,63(19):6395-6404.
[22]LOCKTON JA,SMETHURST D,MACPHERSON M,et al.Phase I ascending single and multiple dose studies to assess the safety,tolerability and pharmacokinetics of AZD0530,a highly selective,dual specific Src-Abl inhibitor[J].J Clin Oncol,2005,23(16S):3125-3130.
[23]HISCOX S,BARROW D,GREENT,et al.Adhesion-independent focal adhesion kinase activation involves Src and promotes cell adhesion and motility in tamoxifen-resistant MCF-7 cells and is inhibited by the Src/Abl kinase inhibitor,AZD0530[J].Proc Am Assoc Cancer Res,2005,46(3):62-63.
[24]TIMP G,MIKE F,RONINW.Preclinical anticancer activity of the potent,oral Src inhibitor AZD0530[J].Molecular Oncol,2009,3(3):248-261.
[25]SEIICHI O,TETSUZOT,JUNKO H O.Mechanism of MK-0457 efficacy against BCR-ABL positive leukemia cells[J].Biochem Biophys Res Commun,2009,380(4):775-779.
[26]GILESF J,CORTESJ,JONESD,et al.MK-0457,a novel kinase inhibitor,is active in patients with chronic myeloid leukemia or acute lymphocytic leukemia with the T315I BCRABL mutation[J].Blood,2007,109(2):500-502.
[27]WARMUTH M,SIMON N,MITINA O,et al.Dual-specific Src and Abl kinase inhibitors,PP1 and CGP76030,inhibit growth and survival of cells expressing imatinib mesylate-resistant Bcr-Abl kinases[J].Blood,2003,101(2):664-672.
[28]LINDSAY O K,CAMPBELL M.Non-ATP competitive protein kinase inhibitors as anti-tumor therapeutics[J].Biochem Pharmacol,2009,77(10):1561-1571.
[29]ADRIANF J,DINGQ,SIMT,et al.Allosteric inhibitors of Bcr-abl-dependent cell proliferation[J].Nat Chem Biol,2006,2(2):95-102.
[30]CARTER T A,WODICKA L M,SHAH N P,et al.Inhibition of drug-resistant mutants of ABL,KIT,and EGF receptor kinases[J].Proc Natl Acad Sci USA,2005,102(31):11011-11016.
[31]CHANDRA J,TRACY J,LOEGERING D,et al.Adaphostin-induced oxidative stress overcomes BCR/ABL mutationdependent and-independent imatinib resistance[J].Blood,2006,107(6):2501-2506.
[32]RADI M,CRESPAN E,BOTTA G,et al.Discovery and SAR of 1,3,4-thiadiazole derivatives as potent Abl tyrosine kinase inhibitors and cytodifferentiating agents[J].Bio&Med Chem Let,2008,18(3):1207-1211.
[33]WANG Y H,SHAKESPERAREW C,HUANGW S,et al.Novel N9-arenethenyl purines as potent dual Src/Abl tyrosine kinase inhibitors[J].Bio&Med Chem Let,2008,18(17):4907-4912.
[34]WEISBERG E,CATLEY L,WRIGHT R D,et al.Beneficial effects of combining nilotinib and imatinib in preclinical models of BCR-ABL+leukemias[J].Blood,2007,109(5):2112-2120.

