新疆地區老年退行性心臟瓣膜病的危險因素分析
劉 靜,張向陽,黃 定
老年退行性心臟瓣膜病 (SDHVD)又稱老年鈣化性心臟瓣膜病、老年心臟鈣化綜合征。SDHVD的發生機制一直被認為是被動的、自然衰老的過程,但國外許多報道證實 SDHVD的病理改變與動脈粥樣硬化相似,為黏液樣變性及脂質聚集,繼而鈣鹽沉積[1],引起瓣膜及其附屬物的功能異常。目前,隨著人均壽命的延長,SDHVD的發病率明顯升高,由于 SDHVD起病隱匿,進展緩慢,狹窄和 (或)關閉不全較輕時血流動力學改變較小,無癥狀的亞臨床期可長達幾十年,一旦出現胸悶、心悸、勞力性呼吸困難等臨床癥狀后,病程進展加速,可出現心力衰竭、心律失常,甚至猝死等[2]。因此,加強對SDHVD危險因素的認識,爭取早期干預治療,以延緩 SDHVD的發生、發展,有重要的臨床和社會意義。
1 資料與方法
1.1 一般資料 選擇 2008年 1月—2009年 8月來我院住院且年齡≥60歲的患者為研究對象。根據有無心臟瓣膜鈣化分為鈣化組 178例,平均年齡 (71±6)歲;對照組 182例,平均年齡 (69±5)歲。所有病例均除外風濕性心臟病、先天性心臟病、肺源性心臟病、膠原病、梅毒及感染性心內膜炎等所致的瓣膜病變,無貧血、甲狀腺功能亢進、甲狀旁腺功能亢進、無慢性腎功能不全等鈣磷代謝紊亂的疾病,無自身免疫性疾病病史,無置換瓣膜史。
1.2 研究方法 選用 Philips公司的 iE33-N型彩色超聲診斷儀,探頭頻率為 2.5 MHz。患者左側臥位,于常規切面進行探測。SDHVD診斷標準:超聲心動圖心瓣膜及瓣環有回聲增厚或局限性致密強回聲,邊緣較為規則,活動度下降。頻譜多普勒觀察各瓣膜狹窄或關閉不全的情況[3]。
1.3 統計學方法 采用 SPSS 17.0統計軟件進行統計學分析,計量資料采用 (x±s)表示,并進行正態性及方差齊性檢驗,組間比較采用獨立樣本 t檢驗,計數資料采用 χ2檢驗;檢驗水準定為 α=0.05。影響因素采用 Logistic回歸分析,并計算出優勢比 (OR)及 95%可信區間 (CI)。
2 結果
2.1 鈣化組和對照組一般臨床資料比較 兩組患者的年齡及吸煙、高血壓、高脂血癥、頸動脈粥樣硬化患者比例間差異均有統計學意義 (P<0.05);兩組患者的性別及冠心病、糖尿病患者比例間差異均無統計學意義 (P>0.05,見表 1)。

表1 鈣化組和對照組一般臨床資料比較Table 1 Comparison of clinical data between valve calcification group and control group
2.2 鈣化組和對照組實驗室檢查結果 瓣膜鈣化組的總膽固醇水平明顯高于對照組,差異有統計學意義 (P<0.05);其余檢測指標間差異均無統計學意義 (P>0.05,見表 2)。

表2 鈣化組和對照組實驗室檢查結果比較 (mmol/L)Table 2 Comparison of clinical and biochemical indicators between valve calcification group and control group
2.3 SDHVD發病危險因素的判定 以瓣膜是否鈣化為因變量,16項可能與之相關的影響因素為自變量,進行多因素 Logistic回歸分析,年齡因素按每 10歲分級賦值:60~69,0;70~79,1;80歲以上,2。回歸結果顯示:SDHVD的危險因素為年齡、吸煙、高血壓、高脂血癥;年齡每增加 10歲,SDHVD的危險增加 1.570倍,吸煙者比不吸煙者 SDHVD的危險增加 1.931倍;有高血壓、高脂血癥者比無高血壓、高脂血癥者 SDHVD的風險分別高 2.062、1.705倍;其他因素冠心病、糖尿病、性別等經回歸分析顯示對 SDHVD總的發病率的影響無統計學意義 (見表 3)。
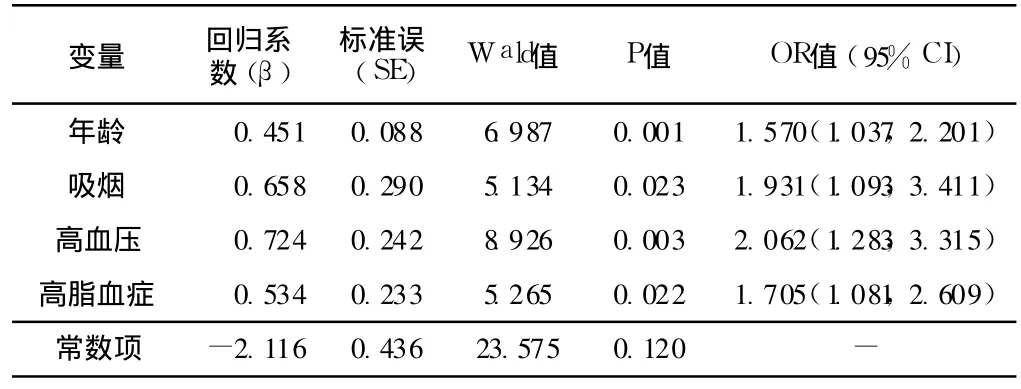
表3 多因素 Logistic回歸有意義結果Table 3 Results of multivariate Logistic regression meaningful
3 討論
本組資料顯示,年齡每增長 10歲,SDHVD的發病危險增高了 1.570倍,進一步證實了 SDHVD是隨年齡增長而發生的瓣膜退行性改變。分析原因可能是隨著年齡增長,衰老心臟處于低氧血癥和酸中毒狀態,容易引起心臟瓣膜、瓣環的膠原纖維斷裂,形成的間隙與鈣鹽結合導致心臟瓣膜、瓣環的鈣化。關于 SDHVD的性別差異目前尚無定論,有報道認為老年女性左房室瓣鈣化為老年男性的 2.5倍[4]。本研究顯示,SDHVD的發病率男女性別之間無統計學差異,還需進一步大樣本量的研究。
據報道尼古丁通過刺激肥大細胞來源的促炎性因子及促纖維化介質釋放,并通過增加成纖維細胞表達 TGF-β1,作用于瓣膜局部,能夠加速瓣膜狹窄的進展[5]。本研究進一步發現,吸煙者比不吸煙者 SDHVD的危險增加 1.931倍。
國外研究發現體內總膽固醇水平增高與瓣膜鈣化相關[6]。本組資料顯示,瓣膜鈣化組患者總膽固醇水平較對照組明顯升高,高脂血癥作為獨立的危險因素,使 SDHVD的危險增加了1.705倍,分析原因可能為高膽固醇血癥易使脂質沉積于瓣環及瓣膜的內膜,形成脂質斑塊,隨著脂質斑塊的增大,營養得不到充分供給,與沉積的鈣質結合使瓣膜鈣化。
有文獻報道顯示,纖維蛋白原水平與 SDHVD有關[7]。其可能機制是纖維蛋白原能特異性的與血小板膜糖蛋白 IIb/IIIa受體結合,促進血小板的聚集,影響血液的凝結性、粘滯性和流變性,影響瓣膜內皮細胞功能,使鈣鹽易于沉積內膜下及纖維組織。但本組資料未顯示兩組患者的纖維蛋白原水平無統計學差異,可能與樣本量小有關。
有報道顯示,原發性甲狀旁腺功能亢進患者中主動脈瓣鈣化發病率為 46%,左房室瓣環鈣化發病率為 39%,復合病變者發病率為 25%,提示 SDHVD可能與鈣磷代謝異常有關[8]。本組數據顯示,兩組患者的血鈣和血磷水平無統計學差異,其臨床意義還有待于進一步研究。
對于高血壓促使 SDHVD的風險增高,分析原因可能是高血壓使體循環壓力增高,心臟后負荷增大,容易引起膠原纖維斷裂,暴露的位點可以和鈣結合而引起鈣鹽沉積,造成瓣膜鈣化。
總之,影響瓣膜退行性鈣化是多種因素共同決定的,盡早對 SDHVD的危險因素進行干預,對延緩 SDHVD的發生、發展有重要意義。
1 Rajamannan NM,Bonow RO,Rohimtoola SH.Calcific aortic stenosis:an update[J].Nat Clin Pract Cardiovasc Med,2007,26(4):254-262.
2 段軍,鄒鳳軍,丁五麟,等 .老年主動脈瓣膜鈣化患者與冠心病關系的探討 [J].中華老年心腦血管病雜志,2008,10(2):93-95.
3 李陽,孫軼,彭世義.老年退行性心臟瓣膜病超聲心動圖分析[J].實用老年醫學,2010,24(4):303-305.
4 公茂磊,鄭素霞.老年人的主動脈瓣硬化癥 [J].國外醫學老年醫學分冊,2004,25(1):222-224.
5 Gerber Y,Goldbourt U,Feinberg MS,et al.Are triglyceride-rich lipoproteins associated with aortic valve sclerosis?A preliminary report[J].Atherosclerosis,2003,17(6):301-305.
6 Chui MC,Newby DE,Panarelli M,et al.Association between calcific aortic stenosis and hypercholesterolemia:is there a need for a randomized controlled trial of cholesterol lowering theapy[J].Clin Cardiol,2001,24(4):52-55.
7 曹淑玉,楊玉蘭,郭云,等 .纖維蛋白原與退行性心臟瓣膜病關系的研究 [J].中華老年學雜志,2001,21(2):415-416.
8 Thomas S,Claudette A,Herbert F,et al.Cardiac abnormalities in patients with primary hyperparathyroidism implications for follow-up[J].J Clinical Endocrinol Metab,1997,82(8):106-112.

