脂肪酶催化藥物合成的研究進展
脂肪酶(Lipase,EC3.1.1.3)可以水解三酸甘油酯產生脂肪酸、單甘油酯、雙甘油酯及甘油,在有機溶劑(包括超臨界流體)中,亦可催化逆水解反應,例如酯化、交酯化、氨解、交流酯化及肽解等反應。脂肪酶已廣泛應用于食品、造紙、皮革、洗滌劑、化工材料和醫藥合成等諸多領域,其中,藥物合成一直是脂肪酶研究領域的熱點。
目前,臨床上超過60%的常用藥物為手性藥物。通常的化學工藝對手性分子的合成并不理想,存在反應路徑長、重金屬催化劑殘留和收率低等缺點;而脂肪酶對底物具有高度的立體選擇性,只需單步反應就可以高效率地制備出手性產物,這使得脂肪酶在光學純化合物制備和藥物手性轉換中具有獨特的優勢。非水酶學的建立和發展,使脂肪酶的這種特性在手性藥物及其中間體合成中的地位更加突出。
同時,脂肪酶作為生物催化劑具有高度的區域選擇性,特別適合于一般化學方法難以實現的多功能化合物的合成,能很好地避免多取代產物等副產物的產生。脂肪酶催化反應除具有高度的立體選擇性和區域選擇性、副反應少等特點外,還具有催化反應條件溫和、無環境污染等優越性,可以保證產物的光學純度和收率。脂肪酶作為生物催化劑,為化學過程提供了更為清潔和高效的途徑。
近年來,研究人員通過新脂肪酶的篩選、酶固定化、反應介質的改變、酰基供體的選擇和反應條件(如溫度、水活度、底物摩爾比例和真空氣壓等)的優化,構建了許多脂肪酶催化藥物合成的優化工藝,脂肪酶在藥物合成領域的研究得到不斷拓展和創新。作者在此對近5年來脂肪酶催化合成抗炎鎮痛藥物、抗抑郁藥物、抗菌藥物、抗腫瘤藥物、維生素類藥物及其中間體的最新研究進展進行了綜述。
1 脂肪酶催化合成抗炎鎮痛藥物
非甾體類抗炎鎮痛藥物(Nonsteroidal antiinflammatory drugs,NSAIDs)是一類具有解熱、鎮痛、抗炎、抗風濕和血小板聚集作用的藥物,主要用于治療多種疾病引起的持續性發炎、疼痛和發燒[1]。此類藥物大多因手性中心的存在而具有對映體,比如萘普生、酮洛芬、布洛芬和氟比洛芬等。最近研究人員利用脂肪酶在手性藥物拆分中具有的優勢,對合成這四種藥物的工藝進行了優化,獲得了較好的結果。
1.1 脂肪酶催化合成(S)-萘普生
萘普生[(+)α-甲基-6-甲氧基-2-萘乙酸]是世界上應用最多的非甾體類抗炎鎮痛藥物。臨床研究表明,(S)-萘普生的生理活性是其對映體的28倍,并作為單一對映體藥物用于人體。在有機溶劑中水解(R,S)-萘普生甲酯是合成(S)-萘普生的理想途徑(圖1)。
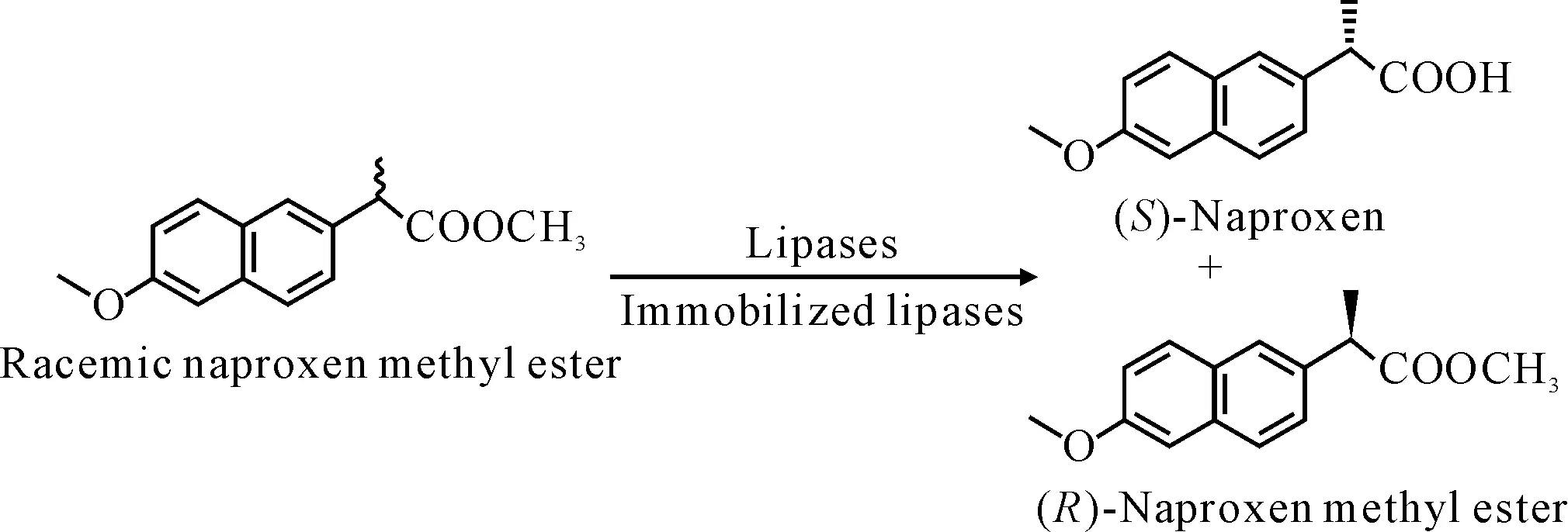
圖1 立體選擇性水解(R,S)-萘普生甲酯
Salgin等[2]用皺褶假絲酵母脂肪酶(CRL)在超臨界二氧化碳存在下的含水緩沖溶液/異辛烷反應體系中立體選擇性水解消旋萘普生甲酯。結果發現,對映體比率隨著反應時間的延長而升高,對映體選擇率(E)為236,轉化率(x)為41.6%,產物對映體過剩值(eep)為98.2%,底物對映體過剩值(ees)為70.0%。在超臨界二氧化碳中選擇合適的反應體系和實驗條件,產物對映體過剩值、對映體比率、轉化率、酶活性和穩定性均能達到較好的水平。Takac等[3]研究了在水-有機二相體系中催化水解消旋萘普生甲酯合成(S)-萘普生的一系列參數對CRL立體選擇性的影響,并獲得了(S)-萘普生的最高對映體比率,E為171.1,x為49.8%,eep為95.7%。Sahin等[4]比較了不同類型添加劑對包裹在四乙氧基硅烷和辛基三乙氧基硅烷中的CRL的立體選擇性的影響。結果顯示,加入氨基杯[4,6]芳烴和羧基杯[6]芳烴添加劑的包裹脂肪酶與不加添加劑的包裹脂肪酶相比具有更高的轉化率和立體選擇性。因此,選擇適宜的添加劑對脂肪酶的立體選擇性具有重要的影響。Kwon等[5]對南極假絲酵母脂肪酶B(CALB)催化的消旋萘普生酯交換反應在真空、水、己烷和超臨界二氧化碳中的穩定性進行了研究。結果表明,CALB-(S)-萘普生復合物的氫鍵比CALB-(R)-萘普生復合物的氫鍵更加穩定,此外,與普通條件下相比,在超臨界條件下可在更短的反應時間里具有最小能量值,得到更高的產率。
1.2 脂肪酶催化合成(S)-酮洛芬
酮洛芬(α-甲基-3-苯甲酰基-苯乙酸)的羧基α-碳是手性中心,存在(R)-和(S)-對映體。然而,(S)-酮洛芬和(R)-酮洛芬卻顯示了不同的藥理活性[6]。(S)-對映體可用于減緩炎癥和減輕疼痛,而(R)-對映體活性很低,甚至在有些情況下,還有不必要的生理副作用和毒性。
最近,Long等[7]克隆了粘質沙雷菌ECU1010的一種脂肪酶,并在大腸桿菌中表達,這種重組脂肪酶能立體選擇性水解(R,S)-酮洛芬酯合成(S)-酮洛芬(圖2),eep達到91.6%,E達到63,x高達48.2%。重組脂肪酶也表現了很高的立體選擇性,這為得到具有更高活性的脂肪酶提供了另外一條途徑。
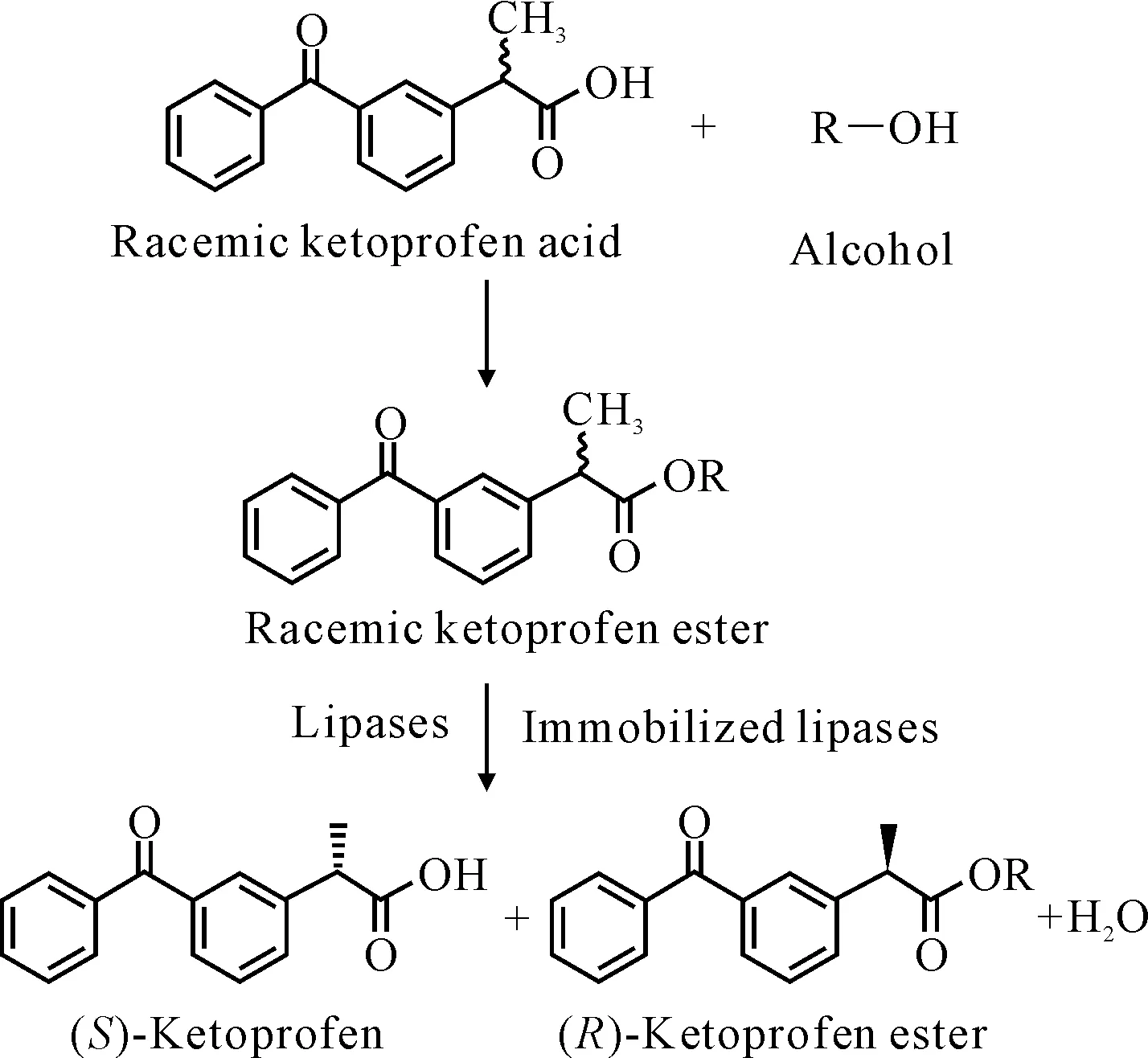
圖2 立體選擇性水解(R,S)-酮洛芬酯
Wu等[8]在用大孔丙烯酸樹脂吸附的南極假絲酵母脂肪酶催化水解酮洛芬乙酯的實驗過程中,偶然發現45℃下這種酶制劑在強酸環境(pH值1.0)比在中性環境中水解酮洛芬乙酯顯示了更高的對映選擇性。這是由于在強酸環境下,酶構象的改變提高了其立體選擇性。Ong等[9]將CALB于酶膜反應器中固定,與游離CALB相比,固定化CALB降低了對映分離(R,S)-酮洛芬的酶量,eep和E分別提高到87.8%和27。
1.3 脂肪酶催化合成(S)-布洛芬
布洛芬[2-(4-異丁基苯基)丙酸]是常用的非甾體類抗炎鎮痛藥物,廣泛用于治療頭痛和輕微的疼痛。消旋布洛芬的兩個對映體只有(S)-對映體具有抗炎的特性[10]。有報道稱(S)-布洛芬酸的鎮痛作用是(R)-對映體的160多倍,(R)-布洛芬不僅沒有活性并且還可能引起副作用[11]。
為了合成光學純的(S)-布洛芬,很多研究者對脂肪酶催化消旋布洛芬的酯交換反應進行了研究。Wang等[12]在親水醋酸纖維素/疏水聚四氟乙烯薄膜復合材料中設計了一種特殊的微結構作為脂肪酶的載體,手性拆分消旋布洛芬,產物對映體過剩值和對映體選擇率均比自由脂肪酶催化體系顯著提高,這種固定化載體改善了脂肪酶的立體選擇性和穩定性。Gottemukkala等[13]研究了溶劑十八烷烴的側鏈甲基位置和水活度對CRL催化布洛芬酯交換的對映選擇性的影響(圖3)。結果顯示, CRL在40℃下水活度為0.73的異辛烷中,催化反應達到最好的效果,起始反應速率和對映選擇性均較好。
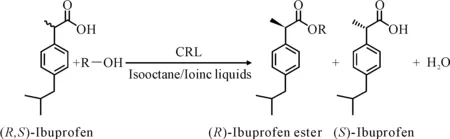
圖3 皺褶假絲酵母脂肪酶動力學拆分(R,S)-布洛芬
Foresti等[14]利用商業脂肪酶Novozym 435,在無其它溶劑存在條件下催化(R,S)-布洛芬和乙醇的酯交換反應,并將實驗數據作為分子模型進行深入的計算分析。在最佳反應條件下,產物對映體過剩值達到54%,布洛芬轉化率達到63%。Liu等[15]在0.1 mol·L-1磷酸緩沖溶液(pH值8)中,用來自子囊菌酵母的胞外脂肪酶LIP催化水解(S)-布洛芬酯,得到了高純度的(S)-布洛芬,ee達到98%。
1.4 脂肪酶催化合成(S)-氟比洛芬
與當前使用的大多數芳基丙酸類NSAIDs相比,氟比洛芬[2-(2-氟-4-聯苯)-丙酸]是以R(-)-體和S(+)-體的混合形式被人體吸收的。越來越多的研究表明,R(-)-氟比洛芬和S(+)-氟比洛芬具有不同的藥理學活性。
Shin等[16,17]用脂肪酶催化合成光學純的(S)-氟比洛芬,獲得了極高的ee(98%)和x(48%)。Bae等[18]用來自粘質沙雷菌ES-2的脂肪酶立體選擇性水解(R,S)-氟比洛芬乙酯合成(S)-氟比洛芬(圖4)。反應24 h后,在獲得較高轉化率的同時,ee、x和E分別高達98.5%、45.1%和332,顯示該酶在合成(S)-氟比洛芬方面具有良好的應用前景。
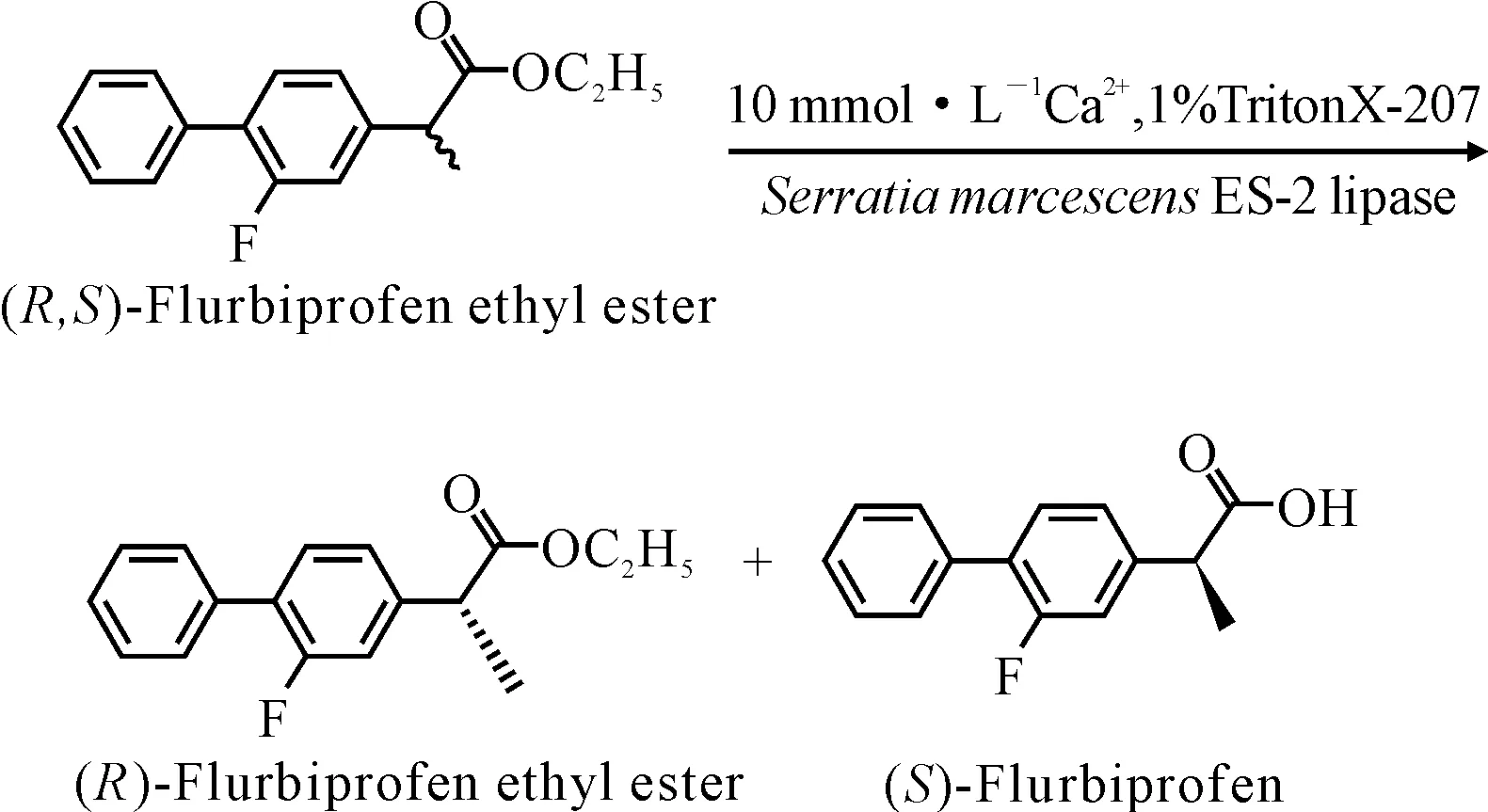
圖4 立體選擇性水解(R,S)-氟比洛芬乙酯
2 脂肪酶合成抗抑郁藥物及其中間體
達泊西汀、氟西汀、度洛西汀和西酞普蘭是治療抑郁癥的臨床常用藥,它們均因具有手性中心而存在(S)-對映體和(R)-對映體,進而具有不同藥理和生理學活性,其結構式見圖5。
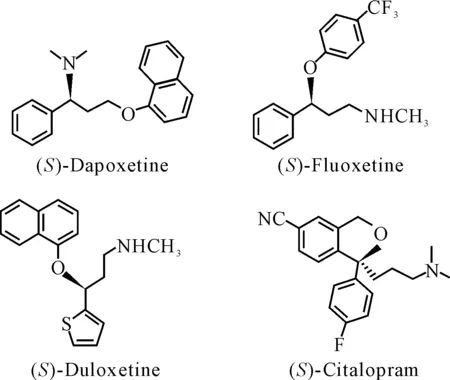
圖5 抗抑郁藥物化學結構
Torre等[19]用南極假絲酵母脂肪酶A(CALA)拆分3-氨基-3-苯基-1-丙醇(化合物Ⅰ),得到了合成(S)-達泊西汀的重要中間體N-(O-3-丁基二甲硅烷基-3-羥基-1-苯丙基)甲氧基乙酰胺(圖6),合成的(S)-達泊西汀有較高的產率(72%)和ee(93%)。
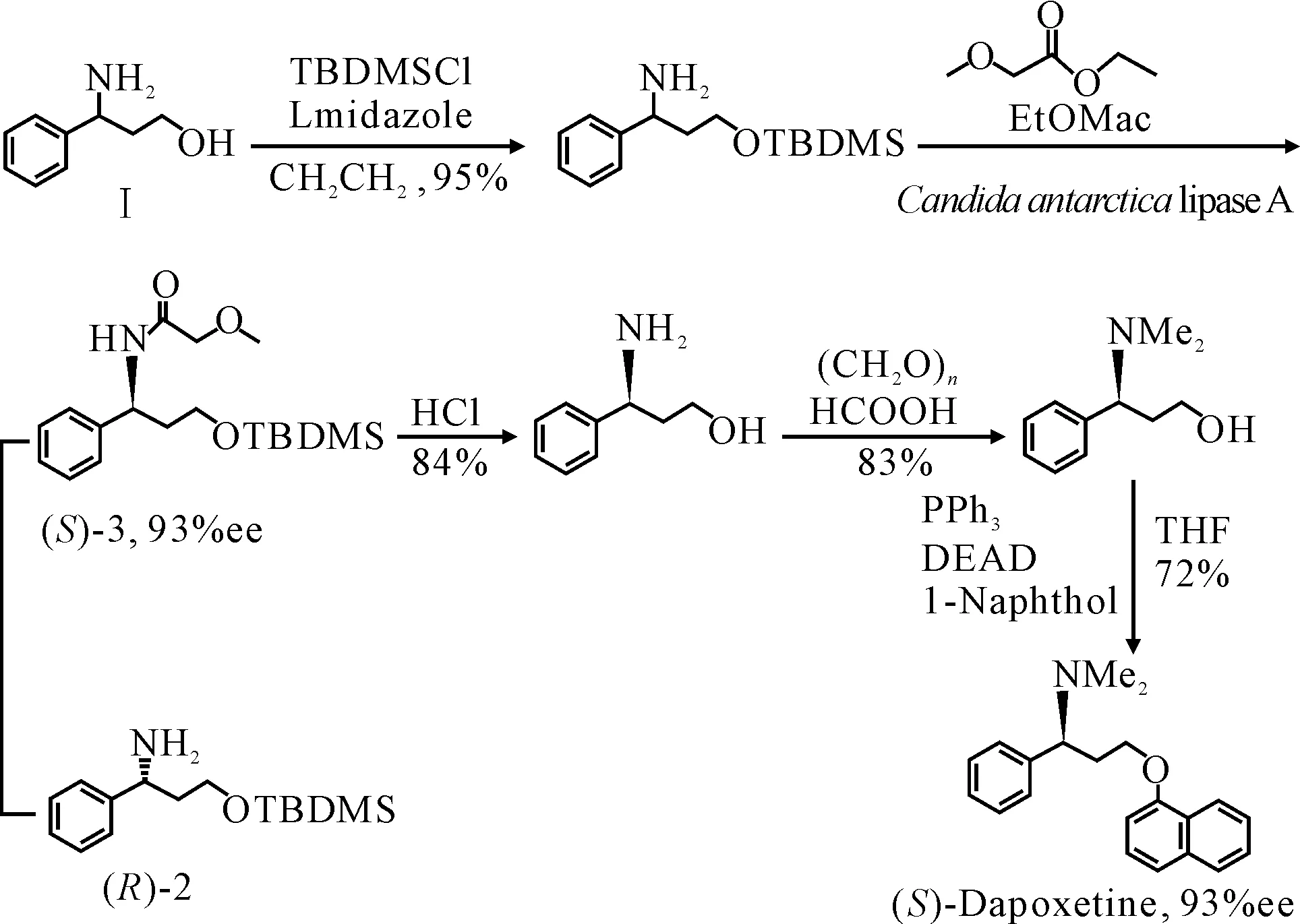
圖6 由3-氨基-3-苯基-1-丙醇合成(S)-達泊西汀
Chaubey等[20]研究證實固定化的節桿菌屬螺菌脂肪酶(ABL)在動力學拆分氟西汀中間體時具有極好的特性。在固定化酶催化反應中,轉化率、對映體過剩值和對映選擇性等均顯著提高。Kamal等[21]研究了固定化洋蔥假單胞桿菌脂肪酶催化γ-疊氮醇類乙酸鹽的水解和醇解反應,動力學拆分得到的對映純γ-疊氮醇類,可以用于抗抑郁藥(S)-氟西汀和(S)-度洛西汀的合成。Wang等[22,23]在以乙酰乙烯酯為酰基供體的無溶劑體系中,研究了固定化南極假絲酵母脂肪酶B催化拆分S-4-[(4-二甲氨基)-1-(4-氟苯)-1-羥基-1-丁基]-3-羥甲基-苯基腈(西酞普蘭中間體)的動力學模型,(S)-二醇的純度達到99.5%,產率達到86.2%(圖7)。
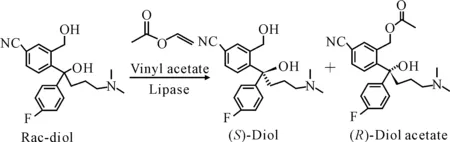
圖7 脂肪酶催化二醇和乙酰乙烯酯的不對稱酯交換反應
3 脂肪酶催化合成抗菌藥物及其中間體
甲霜林[N-(2,6-二甲苯基)-N-2-(甲氧乙酰基)丙氨酸甲酯]是丙氨酰胺的一種,體內實驗表明其具有很好的殺菌活性,并且沒有毒副作用[24]。然而只有(R)-甲霜林具有殺菌活性[25]。Park等[26]用固定在丁基纖維素上的洋蔥假單胞桿菌脂肪酶高效合成了殺菌劑(R)-甲霜林的重要中間體2-甲氧乙基-(R)-N-(2,6-二甲苯基)丙氨酸[(R)-2],獲得了較高的產率(34%)和ee(96%)(圖8)。
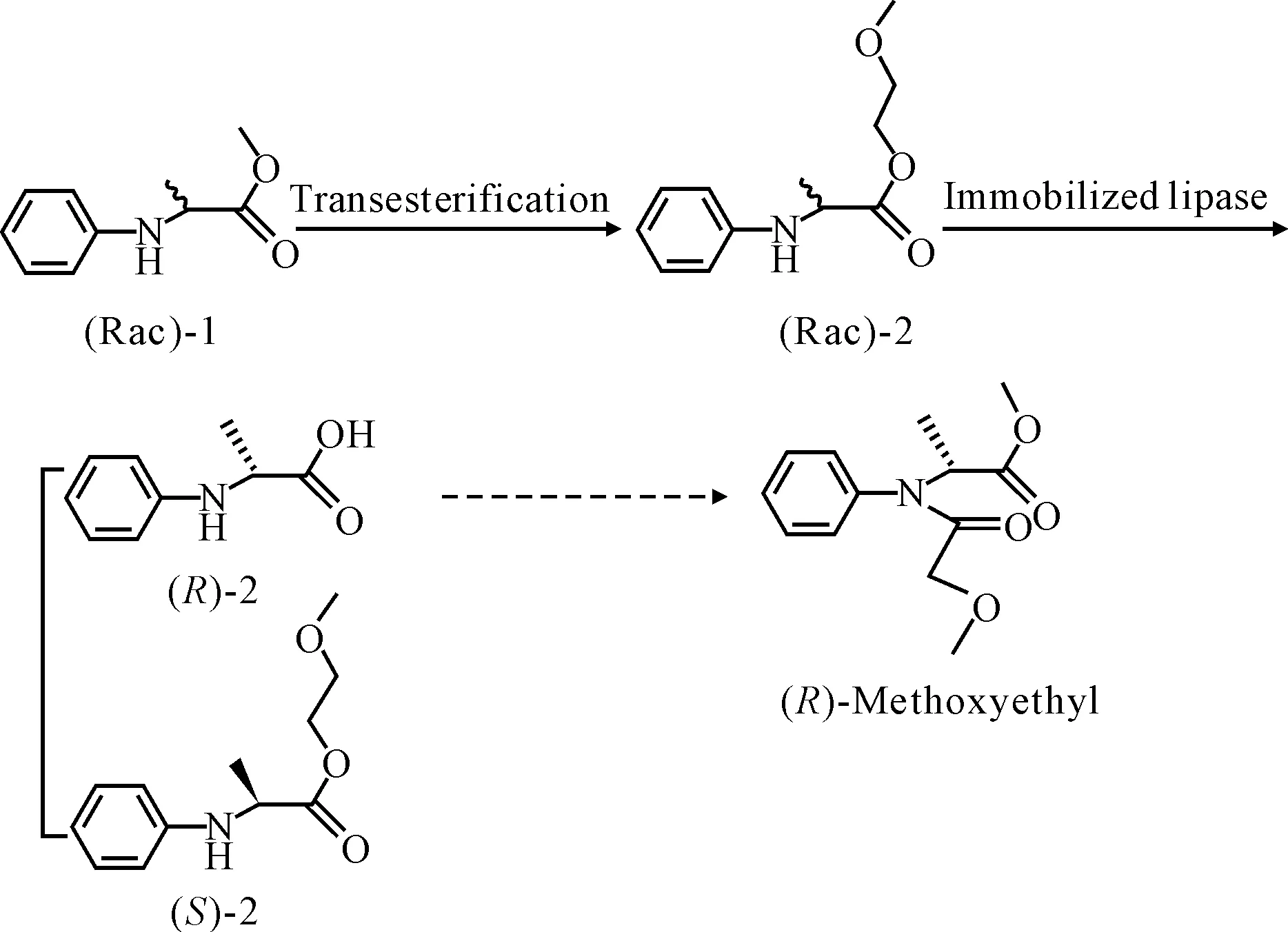
圖8 脂肪酶催化外消旋酯水解

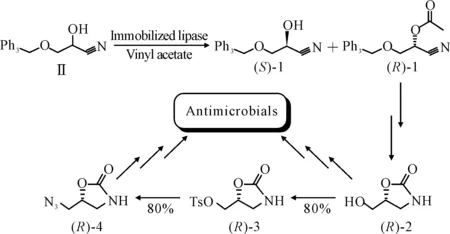
圖9 固定化脂肪酶合成唑烷酮類抗菌藥物中間體
辣椒辣素(反-8-甲基-N-香草基-6-壬酰胺)及其類似物是辣椒中辣椒素一類的化合物,其中已有很多作為藥物應用于臨床。酶催化合成辣椒辣素類似物也越來越受到人們的關注。N-香草壬酰胺(VAN)是辣椒辣素的取代物,和辣椒辣素具有相似的化學結構和藥理作用,能抑制細菌的繁殖[28]。Liu[29]在超臨界二氧化碳中用脂肪酶催化鹽酸香蘭素胺成功合成N-香草壬酰胺,產率很高(圖10)。研究發現,N-香草壬酰胺具有抗大腸桿菌的性能,可以作為食品防腐的潛在抗菌藥物。
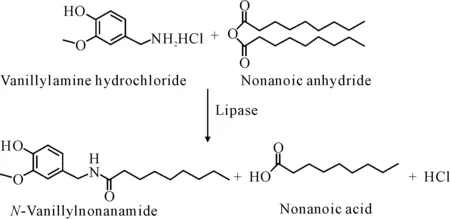
圖10 超臨界二氧化碳中脂肪酶催化合成N-香草壬酰胺
穿心蓮內酯是草藥穿心蓮的主要活性成分,具有抗菌活性[30],多年來被廣泛用于治療多種疾病,比如細菌和病毒感染。Chen等[31]將洋蔥伯霍爾德桿菌脂肪酶固定化后在丙酮中催化穿心蓮內酯制備14-乙酰基穿心蓮內酯,產率達到95%(圖11)。為在非水介質體系中脂肪酶催化穿心蓮內酯獲得更多的穿心蓮內酯類似物提供了良好的啟示。
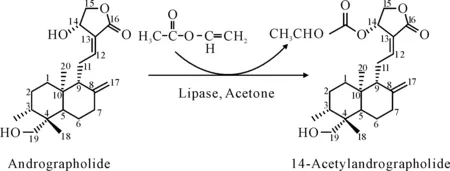
圖11 脂肪酶在丙酮中催化穿心蓮內酯與乙酸乙烯酯的區域選擇性酰化
4 脂肪酶催化合成抗腫瘤藥物
6-氮尿苷和5-氟尿苷因具有細胞毒性,可以用于治療結腸癌、直腸癌、白血病等。通過合成各種6-氮尿苷和5-氟尿苷衍生物,可以克服藥物的不良理化性質,并降低其毒副作用。比如5′-O-酰基-6-氮尿苷和5′-O-酰基-5-氟尿苷衍生物的抗腫瘤活性都比自身高,且降低了化療時的毒副作用[32,33]。但傳統化學合成方法的區域選擇性差,所以合成得到的大部分都是酰化混合物。
近年來,研究者選擇脂肪酶合成了一系列6-氮尿苷和5-氟尿苷的單一酰化衍生物,產率較高。Wang等[34,35]和Zong等[36]首次分別利用CALB和嗜熱棉毛菌脂肪酶高效區域選擇性酰化合成6-氮尿苷的5′-O-單酯(圖12)。研究表明,選擇不同類型的酰基供體,對CALB和嗜熱棉毛菌脂肪酶的活性具有重要的影響,以乙酸乙烯酯作為酰基供體時反應速率、底物轉化率和區域選擇性都很高。
Zinni等[37]利用CALB的區域選擇性醇解合成了一系列新的2′,3′-6-氮尿苷雙酰化衍生物,產率均較高,合成的親水和親脂性衍生物可以用作6-氮尿苷的前藥。Wang等[38]以月桂酸乙烯酯為酰化試劑,用嗜熱棉毛菌脂肪酶Lipozyme TL IM選擇性合成了5-氟尿苷酯的衍生物5′-O-酰基-5-氟尿苷,其抗腫瘤效果比5-氟尿苷更好。研究了水活度、底物摩爾比、反應溫度和攪拌速度對反應的影響,在最適反應條件下反應6 h,底物轉化率達到94.8%,選擇性超過99%。由于氟尿苷存在一級羥基基團5′-OH和二級羥基基團3′-OH,兩者成酯后都會對抗腫瘤效果有影響。Xia等[39]根據脂肪酶的區域選擇性,用CALB在乙腈中合成了5′-O-酰基-5-氟尿苷衍生物,用來自洋蔥假單胞菌的固定化脂肪酶(PSL-C)在四氫呋喃中合成了3′-O-酰基-5-氟尿苷衍生物,兩種酶的選擇性和催化產率均很高。
5 脂肪酶催化合成維生素類藥物
維生素是一類具有生物活性的低分子有機物,是人體進行正常物質代謝、維持正常生理功能所必不可少的類活性藥物。如果長期缺乏某種維生素,就會引起人體生理機能障礙。
將維生素酯化合成維生素酯類衍生物不僅能得到更多的維生素類藥物,還能克服維生素自身存在的缺點。Yin等[40]用固定化假絲酵母脂肪酶催化維生素A醋酸酯和棕櫚酸反應合成維生素A棕櫚酸酯。研究了脂肪酶種類、底物摩爾比、反應溫度和水活度等因素對反應的影響,結果表明,25℃下在己烷中,維生素A醋酸酯和棕櫚酸的摩爾比為1∶3,以100 mg 固定化假絲酵母脂肪酶催化反應12 h,維生素A棕櫚酸酯的產率達到81%。Zhang等[41,42]用南極假絲酵母脂肪酶B(Novozyme 435)區域選擇性催化酯交換反應合成了維生素B6單酯5-O-乙酰吡哆醇(5-AcPN)(圖13)。
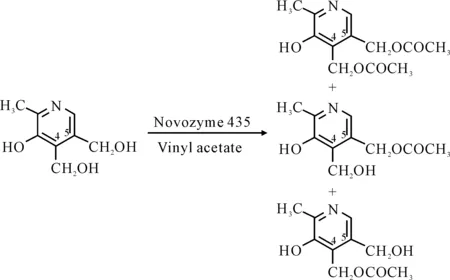
圖13 吡哆醇的酯交換反應
在酯交換反應中,不同的酰基供體不僅影響著反應的轉化率,而且也影響到區域選擇性。Zhang等對影響反應的參數進行了研究。結果顯示,在乙腈中,醋酸乙烯酯作為酰基供體,南極假絲酵母脂肪酶B(Novozyme 435)催化合成5-O-乙酰吡哆醇(5-AcPN)的最大轉化率達到99%,區域選擇性達到93%。Bai等[43]也對該反應的影響參數進行了研究,得到了與Zhang等類似的結果。
維生素 E 經酯化修飾轉化成其衍生物形態,可改善其穩定性、水溶性和表面活性等。Torres等[44]首次用酶催化維生素E的酰化反應。在2-甲基-2-丁烯(2M2B)中,分別用吸附于離子交換樹脂、生物可降解聚合物聚乙交酯和聚丙烯上的南極假絲酵母脂肪酶B,催化醋酸乙烯酯與維生素E進行酯交換反應,結果顯示吸附于離子交換樹脂的南極假絲酵母脂肪酶B(Novozym 435)催化效果最好。
6 展望
作為應用最為廣泛的生物催化劑之一的脂肪酶,近年來在藥物及藥物中間體合成領域的研究熱度仍持續升高。但是,在實際應用中仍存在許多問題需要解決,如脂肪酶的種類不夠豐富、酶活性不穩定、回收困難、成本昂貴、固有的最大動力學拆分效率只能達到50%等,這些因素在一定程度上限制了脂肪酶的應用范圍,因而成為研究人員重點關注的問題。
隨著基因工程技術、蛋白質工程技術和發酵工程技術的飛速發展并日趨成熟,輔以酶工程、底物工程和介質工程等技術手段的交叉引入,為脂肪酶的研究提供了前所未有的發展機遇和空間,在降低脂肪酶成本的同時,脂肪酶的穩定性、活性和選擇性進一步提高,反應機理也更加明確。更多新型的脂肪酶獲得了成功應用,新的脂肪酶催化藥物合成工藝也不斷地被成功構建和優化。可以預測,隨著研究工作者的不斷努力,脂肪酶在藥物合成領域的應用將會更加深入、系統,同時,脂肪酶的應用領域必將進一步擴大并在工業應用中發揮越來越重要的作用。
參考文獻:
[1] Cash J,Klippel J.Second-line drug therapy for rheumatoid arthritis[J].The New England Journal of Medicine,1994,330(19):1368-1375.
[2] Salgin U,Salgin S,Taka S.The enantioselective hydrolysis of racemic naproxen methyl ester in supercritical CO2usingCandidarugosalipase[J].The Journal of Supercritical Fluids,2007,43(2):310-316.
[3] Takac S,Mutlu D.A parametric study on biphasic medium conditions for the enantioselective production of naproxen byCandidarugosalipase[J].Appl Biochem Biotechnol,2007,141(1):15-26.
[4] Sahin O,Erdemir S,Uyanik A,et al.Enantioselective hydrolysis of(R/S)-naproxen methyl ester with sol-gel encapculated lipase in presence of calix[n]arene derivatives[J].Applied Catalysis A:General,2009,369(1-2):36-41.
[5] Kwon C,Jeong J,Kang J.Molecular modeling and experimental v-erification of lipase-catalyzed enantioselective esterification of racemic naproxen in supercritical carbon dioxide[J].Korean Journal of Chemical Engineering,2009,26(1):214-219.
[6] Hutt A,Caldwell J.The importance of stereochemistry in the clinical pharmacokinetics of the 2-arylpropionic acid non-steroidal anti-inflammatory drugs[J].Clinical Pharmacokinetics,1984,9(4):371-373.
[7] Long Z D,Xu J H,Zhao L L,et al.Overexpression ofSerratiamarcescenslipase inEscherichiacolifor efficient bioresolution of racemic ketoprofen[J].Journal of Molecular Catalysis B:Enzymatic,2007,47(3-4):105-110.
[8] Wu J,Ho P,Poh T,et al.Enhanced enantioselectivity of immobilizedCandidaantarcticalipase for hydrolysis of ketoprofen ethyl ester at pH 1[J].Korean Journal of Chemical Engineering,2007,24(4):648-650.
[9] Ong A,Kamaruddin A,Bhatia S,et al.Enantioseparation of(R,S)-ketoprofen usingCandidaantarcticalipase B in an enzymatic membrane reactor[J].Journal of High Resolution Chromatography,2008,31(13):2476-2485.
[10] Mustranta A.Use of lipases in the resolution of racemic ibuprofen[J].Applied Microbiology and Biotechnology,1992,38(1):61-66.
[11] Adams S,Bresloff P,Mason C.Pharmacological differences between the optical isomers of ibuprofen:Evidence for metabolic inversion of the(-)-isomer[J].The Journal of Pharmacy and Pharmacology,1976,28(3):256-257.
[12] Wang Y,Hu Y,Xu J,et al.Immobilization of lipase with a special microstructure in composite hydrophilic CA/hydrophobic PTFE membrane for the chiral separation of racemic ibuprofen[J].Journal of Membrane Science,2007,293(1-2):133-141.
[13] Gottemukkala V V,Saripella K K,Kadari A K,et al.Effect of methyl branching of C8H18alkanes and water activity on lipase-catalyzed enantioselective esterification of ibuprofen[J].Electronic Journal of Biotechnology,2008,11(1):1-8.
[14] Foresti M,Galle M,Ferreira M,et al.Enantioselective esterification of ibuprofen with ethanol as reactant and solvent catalyzed by immobilized lipase:Experimental and molecular modeling aspects[J].Journal of Chemical Technology Biotechnology,2009,84(10):1461-1473.
[15] Liu Y,Wang F,Tan T.Cyclic resolution of racemic ibuprofen via coupled efficient lipase and acid-base catalysis[J].Chirality,2009,21(3):349-353.
[16] Shin G S,Lee K W,Kim T K,et al.Lipase-catalyzed production of optically active (S)-flurbiprofen in aqueous phase reaction system containing chiral succinyl [β]-cyclodextrin[J].Journal of Molecular Catalysis B:Enzymatic,2005,33(3-6):93-98.
[17] Shin G S,Lee K W,Lee Y H.Fed-batch production of (S)-flurbiprofen in lipase-catalyzed dispersed aqueous phase reaction system induced by succinyl [β]-cyclodextrin and its extractive purification[J].Journal of Molecular Catalysis B:Enzymatic,2005,37(1-6):109-111.
[18] Bae H A,Lee K W,Lee Y H.Enantioselective properties of extracellular lipase fromSerratiamarcescensES-2 for kinetic resolution of (S)-flurbiprofen[J].Journal of Molecular Catalysis B:Enzymatic,2006,40(1-2):24-29.
[19] Torre O,Gotor-Fernández V,Gotor V.Lipase-catalyzed resolution of chiral 1,3-amino alcohols:Application in the asymmetric synthesis of (S)-dapoxetine[J].Tetrahedron:Asymmetry,2006,17(5):860-866.
[20] Chaubey A,Parshad R,Koul S,et al.Enantioselectivity modulation through immobilization ofArthrobactersp.lipase:Kinetic resolution of fluoxetine intermediate[J].Journal of Molecular Catalysis B:Enzymatic,2006,42(1-2):39-44.
[21] Kamal A,Malik M S,Shaik A A,et al.Lipase mediated resolution of [γ]-azidoalcohols in aqueous and organic media:Synthesis of (R)-and (S)-fluoxetine and duloxetine[J].Journal of Molecular Catalysis B:Enzymatic,2009,58(1-4):132-137.
[22] Wang S Z,Wu J P,Xu G,et al.Kinetic modelling of lipase-catalyzed remote resolution of citalopram intermediate in solvent-free system[J].Biochemical Engineering Journal,2009,45(2):113-119.
[23] Wang S Z,Wu J P,Xu G,et al.Separation of citalopram intermediate from its acetate by solvent extraction[J].Separation and Purification Technology,2009,68(1):65-69.
[24] Ramos Tombo G,Bellus D.Chirality and crop protection[J].Angewandte Chemie.International Edition in English,1991,30(10):1193-1215.
[25] Blaser H,Spindler F.Enantioselective catalysis for agrochemicals.The case histories of (S)-metolachlor,(R)-metalaxylandclozylacon[J].Topics in Catalysis,1997,4(3):275-282.
[26] Park O J,Lee S H,Park T Y,et al.Enzyme-catalyzed preparation of methyl (R)-N-(2,6-dimethylphenyl)alaninate:A key intermediate for (R)-metalaxyl[J].Tetrahedron:Asymmetry,2005,16(6):1221-1225.
[27] Kamal A,Khanna G B R,Krishnaji T,et al.Lipase-mediated resolution of 3-hydroxy-4-trityloxybutanenitrile:Synthesis of 2-amino alcohols,oxazolidinones and GABOB[J].Tetrahedron:Asymmetry,2006,17(8):1281-1289.
[28] Buck S,Burks T.The neuropharmacology of capsaicin:Review of some recent observations[J].Pharmacol Reviews,1986,38(3):179-226.
[29] Liu K J.Lipase-catalyzed synthesis and antibacterial activity ofN-vanillylnonanamide[J].Journal of Molecular Catalysis B:Enzymatic,2009,58(1-4):181-186.
[30] Gupta S,Choudhry M,Yadava J,et al.Antidiarrhoeal activity of diterpenes ofAndrographispaniculata(kal-Megh)againstEscherichiacolienterotoxin ininvivomodels[J].Pharmaceutical Biology,1990,28(4):273-283.
[31] Chen Z G,Tan R X,Huang M.Efficient regioselective acylation of andrographolide catalyzed by immobilizedBurkholderiacepacialipase[J].Process Biochemistry,2010,45(3):415-418.
[32] Ozaki S,Akiyama T,Morita T,et al.5-Fluorouracil derivatives.XX.Synthesis and antitumor activity of 5′-O-unsaturated acyl-5-fluorouridines[J].Chemical & Pharmaceutical Bulletin,1990,38(11):3164-3166.
[33] Crosasso P,Brusa P,Dosio F,et al.Antitumoral activity of liposomes and immunoliposomes containing 5-fluorouridine prodrugs[J].Journal of Pharmaceutical Sciences,1997,86(7):832-839.
[34] Wang Z Y,Zong M H.Recognition of acyl donors by lipase CAL-B in the acylation of 6-azauridine[J].Biotechnology Progress,2009,25(3):784-791.
[35] Wang Z Y,Li N,Zong M H.A simple procedure for the synthesis of potential 6-azauridine prodrugs byThermomyceslanuginosuslipase[J].Journal of Molecular Catalysis B:Enzymatic,2009,59(1-3):212-219.
[36] Zong M H,Wang Z Y.Highly efficient regioselective acylation of 6-azauridine catalyzed byThermomyceslanuginosuslipase[J].Journal of Biotechnology,2008,136(S1):S380.
[37] Zinni M A,Iglesias L E,Iribarren A M.Preparation of potential 3-deazauridine and 6-azauridine prodrugs through an enzymatic alcoholysis[J].Journal of Molecular Catalysis B:Enzymatic,2007,47(1-2):86-90.
[38] Wang H,Zong M H,Wu H,et al.Novel and highly regioselective route for synthesis of 5-fluorouridine lipophilic ester derivatives by lipozyme TL IM[J].Journal of Biotechnology,2007,129(4):689-695.
[39] Xia A,Wu Q,Liu B,et al.Two-step synthesis of structure-diverseD-galactose conjugates and polymeric prodrugs of floxuridine via controllable regioselective enzymatic acylation of 3′-or 5′-OH group of floxuridine[J].Enzyme and Microbial Technology,2008,42(5):414-420.
[40] Yin C,Liu T,Tan T.Synthesis of vitamin A esters by immobilizedCandidasp.lipase in organic media[J].Chinese Journal of Chemical Engineering,2006,14(1):81-86.
[41] Zhang D H,Bai S,Sun Y.Lipase-catalyzed regioselective synthesis of monoester of pyridoxine(vitamin B6)in acetonitrile[J].Food Chemistry,2007,102(4):1012-1019.
[42] Zhang D H,Bai S,Dong X,et al.Optimization of lipase-catalyzed regioselective acylation of pyridoxine(vitamin B6)[J].Journal of Agricultural and Food Chemistry,2007,55(11):4526-4531.
[43] Bai S,Ren M,Wang L,et al.Regioselective acylation of pyridoxine catalyzed by immobilized lipase in ionic liquid[J].Frontiers of Chemical Engineering in China,2008,2(3):301-307.
[44] Torres P,Reyes-Duarte D,López-Cortés N,et al.Acetylation of vitamin E byCandidaantarcticalipase B immobilized on different carriers[J].Process Biochemistry,2008,43(2):145-153.

