乙酰基二茂鐵亞胺的合成研究
黃淮學院化學化工系 徐成
乙酰基二茂鐵亞胺的合成研究
黃淮學院化學化工系 徐成

亞胺是指含有亞甲氨基(Azomthine group)-RC=N-并通常是由伯胺與活潑羰基化合物所形成的一類化合物。由于亞胺類化合物(Schiff Base)是研究環金屬化合物的一個很好的配體,因此,我們在研究二茂鐵亞胺環金屬化合物時,對多種二茂鐵亞胺的合成進行了研究。
根據亞胺結構的不同,其合成方法大致有以下3種。Kozov等人采用加熱回流甲酰基二茂鐵和芳胺的乙醇溶液的方法得到了二茂鐵醛亞胺(Ferrocenylaldimine);二茂鐵酮亞胺需在催化劑的存在下進行縮合才能得到;Cully和Watts先后合成二茂鐵亞胺鹽,然后脫去質子,得到二茂鐵醛亞胺和酮亞胺,筆者主要采用了乙酰二茂鐵來進行二茂鐵亞胺的合成。
一、二茂鐵亞胺的合成
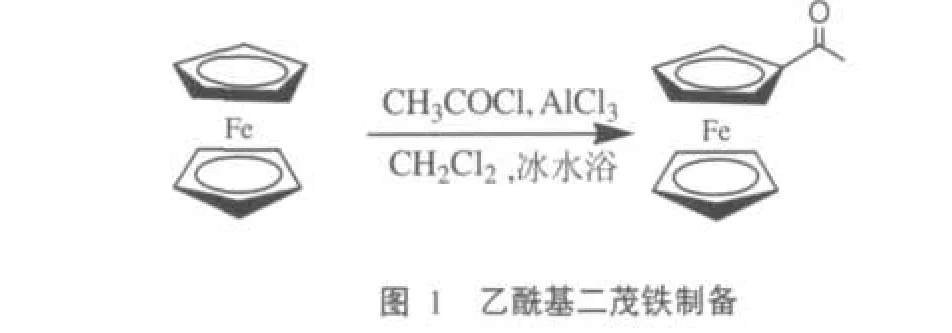
1.乙酰基二茂鐵的制備。低溫下,利用二茂鐵和乙酰氯進行催化,發生傅克酰基化反應制得乙酰基二茂鐵,如圖1所示。二氯甲烷中,冰水浴冷卻至0℃條件下,滴加2.5mL乙酰氯,分批加入無水氯化鋁4.2g(少量多次,間隔2~5min,10次加完),控制溫度在0℃度左右(最高不超過5℃)。加完后攪拌2.5h,倒入20mL冰水中,攪拌0.5h后,分出有機相,水層用二氯甲烷萃取,合并有機相,飽和食鹽水洗2次,用無水碳酸鉀干燥一夜,將有機相濃縮后,用二氯甲烷作洗脫劑,經層析柱分離,收集第二帶,濃縮,得橙紅色晶體。測得熔點為81~83℃。
3.乙酰二茂鐵亞胺的合成。將乙酰二茂鐵分別與2-氨基吡啶、對甲氧基苯胺、對甲苯胺、對氯苯胺按1∶1.5的比例加入三口瓶中,用無水甲苯作溶劑,在N2保護下,150℃加熱回流,劇烈反應后,每隔2h加入少量烘干的Al2O3粉末。定時用紅外儀監測反應進程,當羰基峰消失或很小時,停止反應。將反應液過濾,除去氧化鋁殘渣,并用石油醚洗滌。再把過濾后的溶液旋轉蒸發,蒸除溶劑,得深紅色的固體物質,若產品不純,得到油狀物,冷凍后可得到深紅色固體,在二氯甲烷:石油=1∶2中重結晶2~3次,得到產物。
三、結果與討論
二茂鐵亞胺3b-3d經比對熔點和紅外光譜進行了鑒定,均與文獻報道一致。3a由于產率比較低,分離不夠完全,含有部分雜質,數值與文獻報道有一定偏差。它們其產率、熔點數據列于表1。
2.二茂鐵亞胺的合成。在甲苯回流溫度下,以乙酰基二茂鐵為原料合成二茂鐵亞胺,如圖2所示。
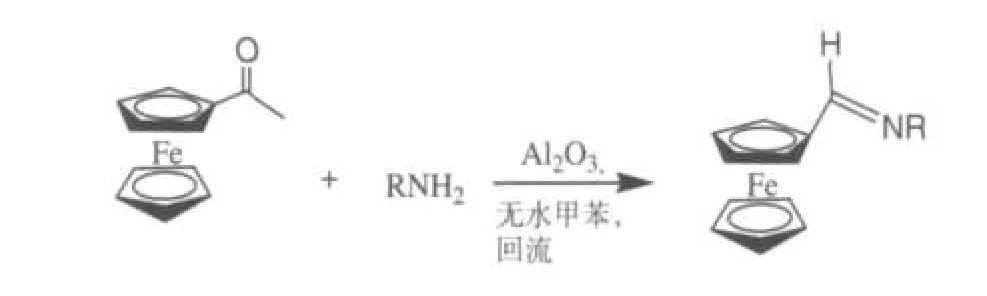
R-C5H4N(3a)/C7H7O(3b)/C7H7(3c)/C6H4Cl(3d)
二、實驗部分
1.試劑與儀器。熔點用WC-1型顯微熔點儀測定,溫度未經校正;紅外光譜用Perkin Elmer FTIR1750型紅外光譜儀測定,KBr壓片;薄層色譜板用青島海洋化工廠生產的硅膠GF254與縮甲基纖維素鈉(3.5%水溶液)調勻后鋪板;Al2O3在120℃活化2h制得;無水甲苯由分析純甲苯與金屬鈉回流制得;對甲氧基苯胺、對甲苯胺、對氯苯胺、2-氨基吡啶均未經處理,直接使用;乙酰二茂鐵按如下步驟制備。
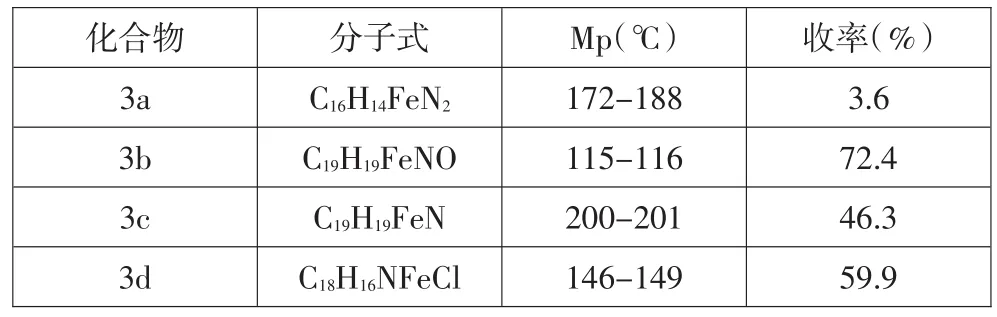
表1 化合物3a-3d的物理常數
紅外光譜表明,3a-3d二茂鐵亞胺在1100cm-1和1000cm-1附近均出現單取代二茂鐵的特征吸收峰,C=N伸縮振動出現在1 610~1 630cm-1范圍內為一單吸收峰。N-苯環上的取代基對二茂鐵茂環質子的化學位移影響不大,表明取代基效應沒有作用到二茂鐵部分,即共軛效應未貫通與整個分子。因此,苯環與茂環應該不在同一平面。
我們用Al2O3催化縮合方法合成3a,反應進行了4天,經紅外檢測發現,仍然只有少量亞胺產生。3a產率較低的原因可能是吡啶環上的N原子具有較大的電負性而減小了氨基上的電子云密度,從而降低了其親核能力,相當部分的雜環氨基不能有效地與酰基二茂鐵縮合形成二茂鐵亞胺化合物。因此,我們認為在合成其亞胺環金屬化合物時,可以先進行環金屬化反應,然后進行

