失血性休克大鼠血清TXB2等內源性介質水平變化及意義
許會彬,王化芬,王 青,王永清,劉文清,崔 慶
失血性休克(hemorrhagic shock,HS)是引起急診創傷患者死亡的首要因素,大量研究表明“炎性瀑布”及多器官功能衰竭是導致患者死亡的主要因素之一。在休克的發展過程中內源性介質起著重要的作用,它們相互影響、相互作用,共同促進休克的發生和發展。近年來,有關介質作用的研究受到廣泛關注,已成為研究休克的熱點[1-4]。本研究擬對不同程度HS及中度HS不同時相的大鼠血清TXB2、6-keto-PGF1α及8-iso-PGF2α水平進行檢測(由于重度HS存活時間相對較短,本文未就重度HS不同時相大鼠的相關指標進行觀測),以探討TXB2、6-keto-PGF1α及8-iso-PGF2α水平與休克程度及時相的相關性。
1 材料與方法
1.1 動物分組與模型制作 雄性Wistar大鼠50只,體重(250±10)g,由軍事醫學科學院動物中心提供。隨機分為5組(每組10只):正常對照(SHS)組;重度失血性休克 (RHS)組;中度失血性休克(MHS),按休克后采血時間的不同再將MHS組分為休克 30 min(MHS-30 min)組、休克 60 min(MHS-60 min)組及休克 120 min(MHS-120 min)組。各休克組以1%戊巴比妥鈉(35 mg/kg,ip)麻醉,左側股動脈插管連于恒流泵以備放血,1 kU/kg肝素鈉左側股靜脈注射使全血肝素化,手術燈照射給動物保溫。以控壓梯度放血模式,分三階段放血。動物手術后穩定10 min,開始快速放血,此時記為失血模型的 0 min。RHS組第一階段:放血(10±1)min使平均動脈壓降至(35±1) mmHg(1 mmHg=0.133 kPa),微量調整失血量維持血壓穩定10 min;第二階段:微量調整失血量維持血壓在(40±1)mmHg,穩定15 min;第三階段:微量調整失血量維持血壓在(45±1) mmHg,穩定 30 min,三階段放血完畢,制成RHS模型。模型制成60 min后,快速從股動脈采血。MHS組三階段血壓分別控制在(55±1)mmHg、(60±1) mmHg及(65±1)mmHg。 MHS 組按模型制成后采血時間的不同又分為三組,即在模型制成后,分別在30、60和120 min快速從股動脈采血。SHS組除不通過股動脈放血致休克處理外,其余同HS組。1.2 儀器與試劑 酶標儀由BIO-RAD公司生產,TXB2、6-keto-PGF1α 及 8-iso-PGF2α 試劑盒由美國ADL公司生產。
1.3 檢測方法 TXB2、6-keto-PGF1α 及 8-iso-PGF2α檢測均應用ELISA方法。
1.4 統計學處理 用SPSS11.5軟件處理數據。數據求出均數±標準差(±s),各組間比較采用t檢驗。
2 結果
2.1 各組 TXB2、6-keto-PGF1α 及 8-iso-PGF2α 水平及 (T/K) 比值 ①MHS組及 RHS組 TXB2、6-keto-PGF1α及8-iso-PGF2α水平均顯著高于SHS組(P 均<0.01);②RHS 組與 MHS 組比較,TXB2及8-iso-PGF2α 水平顯著升高(P<0.01),6-keto-PGF1α水平顯著降低 (P<0.05);MHS組及RHS組T/K比值顯著高于SHS組(P均<0.01),RHS組較MHS組T/K比值顯著升高(P<0.01)。見表1。
2.2 MHS 三不同時相組之間 TXB2、6-keto-PGF1α及8-iso-PGF2α水平及(T/K)比值 ①TXB2水平呈上升-下降-上升的趨勢(三組水平均高于SHS組),三組間兩兩比較,TXB2水平均具有顯著性差異(P<0.01),MHS-120 min 組水平最高; ②6-keto-PGF1α水平呈上升-上升-下降的趨勢 (三組水平均高于SHS組),三組間兩兩比較,6-keto-PGF1α水平均具有顯著性差異(P<0.01),MHS-60 min組水平最高;③8-iso-PGF2α水平隨休克時間的延長呈持續上升的趨勢,三組間兩兩比較,8-iso-PGF2α水平均具有顯著性差異(P<0.01);④T/K比值呈上升-下降-上升的趨勢(三組水平均高于SHS組),三組間兩兩比較,T/K比值均具有顯著性差異(P<0.01),MHS-120 min組T/K比值最高。見表2。
表 1 MHS組、RHS組及SHS組血漿脂類介質水平±s)
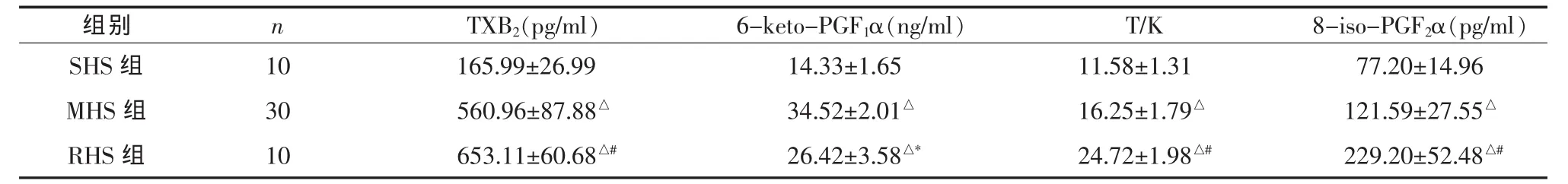
表 1 MHS組、RHS組及SHS組血漿脂類介質水平±s)
與 SHS 組比較,△P<0.01;與 RHS 組比較,#P<0.01;與 RHS 組比較,*P<0.05
組別 n TXB2(pg/ml) 6-keto-PGF1α(ng/ml) T/K 8-iso-PGF2α(pg/ml)SHS 組 10 165.99±26.99 14.33±1.65 11.58±1.31 77.20±14.96 MHS 組 30 560.96±87.88△ 34.52±2.01△ 16.25±1.79△ 121.59±27.55△RHS 組 10 653.11±60.68△# 26.42±3.58△* 24.72±1.98△# 229.20±52.48△#
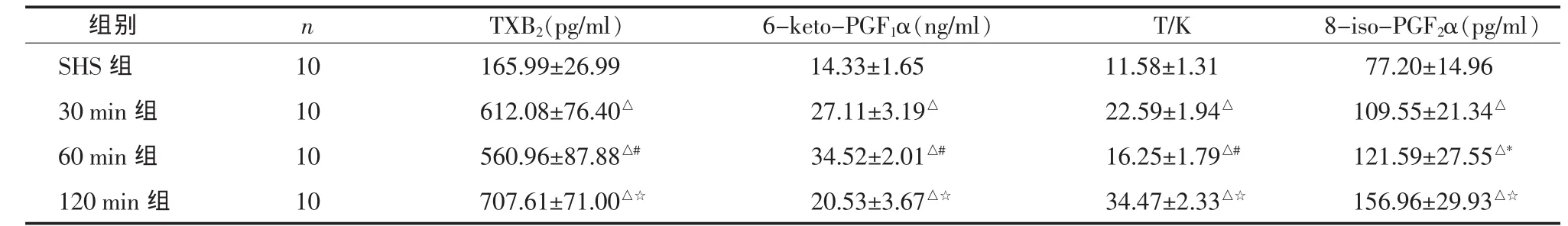
與 SHS 比較,△P<0.01;與 MHS-60 比較,#P<0.01;與 MHS-60 比較,*P<0.05;與 MHS-120 比較,☆P<0.01
3 討論
HS是一個危急的進行性的病理過程,救治時機至關重要。HS的有效救治時間為傷后1 h,稱為“黃金時間”(Golden Hour),很多傷者因為超過了救治的“黃金時間”而死亡。這主要是因為在急性失血性休克條件下會造成機體應激反應過度,從而引發一系列的“炎性連鎖反應”,機體會產生大量的炎性細胞因子,進而產生自由基等物質,全身血液灌注障礙,血流減緩又會造成微循環障礙[5,6]。由于細胞損傷的不斷加重,出現多器官功能障礙,造成休克的惡性循環,此時全身血管反應性降低,使休克向難治性階段不可逆發展,亦即轉變成了使用常規治療失血性休克的方法和手段都無效的難治性休克[7]。而炎性損傷、自由基損傷及其導致的多器官功能障礙成為創傷和休克的常見并發癥和主要死亡原因。因此在急性失血的早期及時監測機體的炎癥反應,給予有效的抗炎、抗自由基損傷的藥物,阻斷炎性瀑布的啟動,打斷休克的惡性循環,防止休克后器官功能障礙成為臨床工作人員及科研工作者關注的熱點。
血栓素 A2(thromboxane,TXA2)是一種強烈的縮血管物質,主要來源于血小板。LDL、白三烯B4和D4等都可刺激內皮細胞合成TXA2。該產物非常不穩定,在體液中的壽命僅30 s,而迅速變成穩定產物TXB2。 前列環素(prostacyclin PGI2)為花生四烯酸代謝產物,它是血管內皮細胞產生的一種前列腺素族物質,具有強烈的舒張血管與抑制血小板功能的作用。PGI2的半衰期只有6 min,它在血漿中迅速代謝為6-酮-PGF1α。正常情況下,兩者處于動態平衡之中,從而保持血管一定的緊張性并控制著血小板的聚集與血栓形成。因此,測定TXB2、6-keto-PGF1α的含量可以反映TXA2和PGI2的變化。8-異前列腺素 F2α(8-iso-PGF2α)是細胞生物膜的花生四烯酸經自由基脂質過氧化作用后產生的特異性產物,屬非酶催化的脂質過氧化物,是衡量機體氧化應激、脂質過氧化損傷強度的理想指標[8,9]。同時8-iso-PGF2α還具有多種重要的生物學活性:①促進炎癥反應;②促進血管內皮細胞粘附分子的表達和中性粒細胞的活性及粘附力;③具有較強的極性,氧化損傷后細胞膜上8-iso-PGF2α增多,使細胞膜的完整性進一步受到破壞,流動性發生改變,導致細胞的結構、功能受損,甚至引起細胞死亡;④促進自由基的產生及血小板的粘附、聚集和變形[10-13]。
本研究對HS大鼠血漿TXB2、6-keto-PGF1α及8-iso-PGF2α進行了檢測,同時對TXB2/6-keto-PGF1α(T/K)比值進行了比較。結果顯示:(1)各組TXB2水平比較:①MHS各組及RHS組TXB2水平均顯著高于SHS組(P均<0.01);②RHS組與MHS組比較,TXB2水平顯著升高(P<0.01);③MHS 三不同時相組之間比較:TXB2水平呈上升-下降-上升的趨勢,三組間兩兩比較,TXB2水平均具有顯著性差異(P<0.01),MHS-120 min組水平最高;該結果提示隨著HS的加重,機體炎癥反應增強;在HS早期機體就出現了較強烈的炎癥反應;隨后機體出現代償反應,炎性反應有所緩解;而隨著HS持續時間的延長,機體可能出現失代償,導致炎性反應進一步加劇;(2)各組6-keto-PGF1α水平比較:①MHS各組及RHS組6-keto-PGF1α水平均顯著高于SHS組(P均<0.01);②RHS組與 MHS組比較,6-keto-PGF1α 水平顯著降低(P<0.05);③MHS三不同時相組之間比較:6-keto-PGF1α水平呈上升-上升-下降的趨勢,三組間兩兩比較,6-keto-PGF1α水平均具有顯著性差異(P<0.01),MHS-60 min組水平最高;該結果提示HS狀態,機體在炎癥刺激下,出現應激反應,機體抗炎機制啟動;而隨著HS程度的加重,機體的抗炎反應減弱,說明在HS早期機體就出現了較強的抗炎反應,以緩解炎性刺激;而隨著HS持續時間的延長,機體的抗炎反應開始減弱;(3)各組8-iso-PGF2α水平比較:①MHS各組及RHS組8-iso-PGF2α 水平均顯著高于SHS組 (P均<0.01);②RHS組與MHS組比較,8-iso-PGF2α水平顯著升高(P<0.01);③MHS三不同時相組之間比較:8-iso-PGF2α水平隨休克時間的延長呈持續上升的趨勢,三組間兩兩比較,8-iso-PGF2α水平均具有顯著性差異(P<0.01),提示細胞膜的損傷隨著HS程度的加重或/和HS時間的延長而加劇;另一方面,高水平的8-iso-PGF2α具有多種生物學功能,可能進一步加重炎癥反應,加劇細胞結構及功能的損傷;(4)各組 TXB2/6-keto-PGF1α(T/K)比值比較:①MHS 各組及 RHS組 T/K比值顯著高于 SHS組 (P均<0.01);②RHS組與MHS組比較,T/K比值顯著升高(P<0.01);③MHS三不同時相組之間比較:T/K比值呈上升-下降-上升的趨勢,三組間兩兩比較,T/K比值均具有顯著性差異(P<0.01),MHS-120 min組T/K比值最高,提示HS時,由于組織缺氧,組胺釋放,補體系統的激活等因素作用,粘附聚集的PLT產生TxA2增多;同時血管內皮因缺氧,酸中毒或內毒素作用而受損,PGI2生成減少,導致TxA2占優勢的TxA2-PGI2平衡失調而促進PLT進一步聚集,微血管形成,加重組織損傷,引起血壓下降。另一方面在HS起始階段機體即出現了強烈的炎癥反應;隨后機體出現代償反應,在抗炎性機制啟動后,炎性反應有所緩解;隨著HS時間的持續,抗炎機制減弱,炎癥反應進一步增強。TXB2、6-keto-PGF1α及8-iso-PGF2α均為生物膜上花生四烯酸的代謝產物,與HS狀態機體的炎癥反應密切相關;另一方面,它們均發揮多種生物學功能,對HS狀態花生四烯酸的代謝可能進行反饋調節。
綜上說明,檢測 TXB2、6-keto-PGF1α 及 8-iso-PGF2α的變化對了解HS狀態機體炎癥反應具有重要意義,為失血性休克的救治提供新的思路和干預靶點。
[1]Yamanashi Y,Mori M,Terajima K,et al.A transient inflammatory reaction in the lung after experimental hemorrhagic shock and resuscitation with a hemoglobin-vesicles solution compared with rat RBC transfusion.ASAIO J,2009,55(5):478-483.
[2]Wang P,Li Y,Li J.Protective roles of hydroxyethyl starch 130/0.4 in intestinal inflammatory response and oxidative stress after hemorrhagic shock and resuscitation in rats.Inflammation,2009,32(2):71-82.
[3]Sato H,Kasai K,Tanaka T,et al.Role of tumor necrosis factoralpha and interleukin-1beta on lung dysfunction following hemorrhagic shock in rats.Med Sci Monit,2008,14(5):BR79-87.
[4]Arikan AA,Yu B,Mastrangelo MA,et al.Interleukin-6 treatment reverses apoptosis and blunts susceptibility to intraperitoneal bacterial challenge following hemorrhagic shock.Crit Care Med,2006,34(3):771-777.
[5]Altavilla D,Saitta A,Guarini S,et al.Oxidative stress causes nuclear factor-kappaB activation in acute hypovolemic hemorrhagic shock.Free Radic Biol Med,2001,30(10):1055-1066.
[6]Theoharides TC,Cochrane DE.Critical role of mast cells in inflammatory diseases and the effect of acute stress.J Neuroimmunol,2004,146(1):1-12.
[7]Resnic FS,Wainstein M,Lee MK,et al.No-reflow is an independent predictor of death and myocardial infarction after percutaneous coronary intervention.Am Heart J,2003,145(1):42-46.
[8]Wood LG,Fitzgerald DA,Gibson PG,et al.Increased plasma fatty acid concentrations after respiratory exacerbations are associated with elevated oxidative stress in cystic fibrosis patients.Am J Clin Nutr,2002,75(4):668-675.
[9]Dietrich M,Block G,Hudes M,et al.Antioxidant supplementation decreases lipid peroxidation biomarker F(2)-isoprostanes in plasma of smokers.Cancer Epidemiol Biomarkers Prev,2002,11(1):7-13.
[10]Kumar A,Kingdon E,Norman J.The isoprostane 8-iso-PGF2αlpha suppresses monocyte adhesion to human microvascular endothelial cells via two independent mechanisms.FASEB J,2005,19(3):443-445.
[11]Varma S,Janesko KL,Wisniewski SR,et al.F2-isoprostane and neuron-specific enolase in cerebrospinal fluid after severe traumatic brain injury in infants and children.J Neurotrauma,2003,20(8):781-786.
[12]Inder T,Mocatta T,Darlow B,et al.Elevated free radical products in the cerebrospinal fluid of VLBW infants with cerebral white matter injury.Pediatr Res,2002,52(2):213-218.
[13]Brault S,Martinez-Bermudez AK,Marrache AM,et al.Selective neuromicrovascular endothelial cell death by 8-Iso-prostaglandin F2αlpha:possible role in ischemic brain injury.Stroke,2003,34(3):776-782.

