小麥籽粒多酚氧化酶活性變化研究
陳 軍,高貴珍,曹穩(wěn)根,馬傳喜
(1.宿州學(xué)院化學(xué)與生命科學(xué)系,安徽宿州234000;2.安徽農(nóng)業(yè)大學(xué)農(nóng)學(xué)院,安徽合肥230036)
小麥生產(chǎn)在我國國民經(jīng)濟中占有重要地位,其中面制食品是我國人民的主食之一。而在面制食品的加工和儲藏過程中經(jīng)常會出現(xiàn)褐變現(xiàn)象。有不少研究表明,小麥中多酚氧化酶(Polyphenol Oxidase,PPO)是影響褐變的主要原因[1~3]。
PPO是一類廣泛分布于植物體內(nèi)能催化多酚類氧化成醌類的質(zhì)體金屬酶,它的底物(酚類物質(zhì))存在于液泡中,且這種酶與底物的區(qū)域分布使得PPO在完整細(xì)胞內(nèi)的生理功能難以確定。生物體內(nèi)的PPO分布是不均勻的,具有時間和空間特異性。在小麥中,從幼苗到植株以及成熟籽粒中都含有多酚氧化酶,但種類及活性有所差異。一些研究表明,小麥籽粒中的PPO主要存在于麩皮層中,面粉中PPO活性隨著出粉率的增加而提高[4],且不同小麥類型和品種間PPO均有一定差異;對同一品種而言,發(fā)育成熟的大籽粒PPO高于發(fā)育不完全的小籽粒。硬粒小麥多酚氧化酶活性最低,普通白粒小麥多酚氧化酶活性低于硬紅冬、硬紅春及軟紅冬小麥,但是硬紅冬和軟紅冬小麥、硬紅冬和硬紅春小麥間多酚氧化酶活性差異較小[5]。大量研究表明,成熟籽粒PPO主要存在于種皮中,胚中無PPO[6,7],但小麥籽粒發(fā)育及萌發(fā)過程中PPO動態(tài)性的變化規(guī)律還不是很清楚。
本研究選取不同類型小麥品種,對籽粒發(fā)育及萌發(fā)過程中PPO活性進行研究,以期找出小麥籽粒PPO活性變化規(guī)律,為小麥PPO遺傳改良提供理論依據(jù)。
1 材料和方法
1.1 試驗材料
發(fā)育期供試材料為:安農(nóng)95081-8、安農(nóng)95083-6-1、安農(nóng) 0309、鄭麥 9023、安農(nóng) 9267 和煙農(nóng)19 6個品種,于2006—2007年種植于安徽農(nóng)業(yè)大學(xué)試驗田。
萌發(fā)期供試材料為:宿麥553、徐麥856、皖麥 50、皖麥 52、煙農(nóng) 19、邯 6172、連麥 2號 7個品種,于2007—2008年種植于宿州市農(nóng)科所試驗田。
以上材料均采用小區(qū)撒播種植,田間管理與大田一致。
1.2 試驗方法
1.2.1 樣品處理
1.2.1.1 發(fā)育期籽粒的處理 各品種在盛花期選取同時開花且大小一致的200穗掛牌標(biāo)記。4月28日第1次取樣,每品種分別取15穗放于冷凍冰箱(-70℃)中待測。以后每隔5 d取樣1次,直至成熟收獲。
1.2.1.2 萌發(fā)期籽粒的處理 (1)每個品種稱取相同質(zhì)量的籽粒21份,每份1.000 g。(2)將上述樣品浸于一個培養(yǎng)皿里,于25℃、空氣濕度95%的人工可編程氣候箱內(nèi)培養(yǎng),且要定時翻動籽粒。(3)萌發(fā)期分 7 個階段取樣,即 0,12,24,36,48,60,72 h(每隔 12 h取樣1次)。將培養(yǎng)好的小麥籽粒冰浴研碎備用。
1.2.2 PPO活性檢測方法
1.2.2.1 發(fā)育期籽粒PPO活性檢測 參照Anderson[8]和Morris[9]的方法。未成熟籽粒(干質(zhì)量為0.300 0 g)放于研缽中冰浴研碎后轉(zhuǎn)入50 mL小燒杯中;成熟籽粒用瑞典產(chǎn)旋風(fēng)磨制備全麥粉(過0.5 mm篩)。稱取0.300 0 g全麥粉放入50 mL小燒杯中,加入7.5 mL反應(yīng)試劑(50 mmol/L,pH=6.5的MOPS緩沖液;10 mmol/L L-DOPA,左旋多巴作為PPO反應(yīng)底物),恒溫水浴振蕩器上振蕩5 min(振蕩器速度設(shè)為100 r/min,溫度設(shè)為37℃),樣品充分暴露在空氣中,之后迅速將反應(yīng)后的樣品放在冰塊上終止反應(yīng)(1 min),并迅速混勻樣品,用中速定量濾紙進行過濾。以反應(yīng)試劑(空白L-DOPA/MOPS,左旋多巴與MOPS的混合液)為對照,在475 nm下測定濾液的吸光度ΔA(ΔA為5 min內(nèi)吸光值的變化),每克籽粒每分鐘吸光值上升0.001定義為一個酶活單位(單位AU,absorbance unit)。PPO的活性表示為ΔA×103AU/(min·g)。
1.2.2.2 萌發(fā)期籽粒PPO活性檢測 在比色皿中依次加入2.8 mL磷酸緩沖液,1 mL 0.1 mol/L鄰苯二酚。用移液管加入0.3 mL粗酶液,混勻,迅速放入37℃水浴鍋中,水浴5 min后測OD420。每克籽粒每分鐘吸光值上升0.001定義為一個酶活單位(單位 AU,absorbance unit)。PPO的活性表示為ΔA×103AU/(min·g)。
1.3 數(shù)據(jù)分析
運用Excel和SAS統(tǒng)計分析程序?qū)?shù)據(jù)進行分析處理。
2 結(jié)果與分析
2.1 PPO活性變異方差分析
由表1可知,基因型與發(fā)育時期互作PPO活性變異的方差分析中,籽粒發(fā)育的不同階段PPO活性差異極顯著,不同基因型和基因型與發(fā)育時期互作PPO活性差異都不顯著。因此,基因型對籽粒發(fā)育過程中PPO活性不具有顯著影響,基因型與發(fā)育時期互作對PPO活性也不具有顯著影響,而籽粒發(fā)育的不同階段對PPO活性有顯著影響,且發(fā)育時期間的PPO活性差異遠(yuǎn)大于品種間的差異。這表明籽粒發(fā)育的不同時期是影響PPO活性的主要因素。
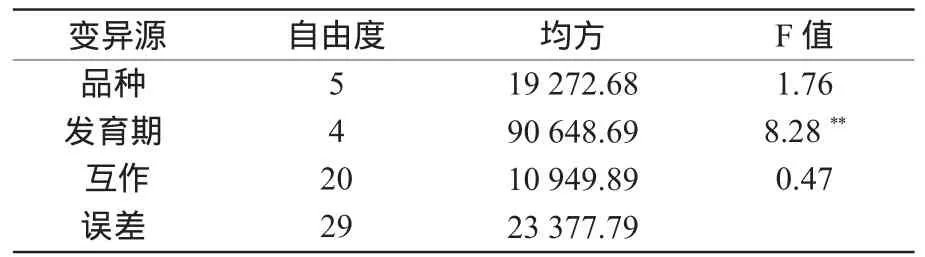
表1 基因型與發(fā)育時期互作PPO活性變異的方差分析
從不同品種與萌發(fā)期互作PPO活性變異方差分析(表2)可看出,品種間PPO活性差異極顯著,不同萌發(fā)階段PPO活性差異也達(dá)到極顯著水平,而品種與萌發(fā)期互作PPO活性差異不顯著。這表明在小麥籽粒萌發(fā)過程中,品種和萌發(fā)期對PPO活性都有顯著影響。
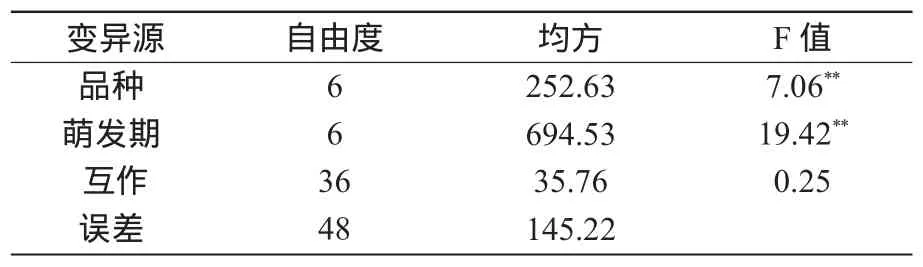
表2 基因型與萌發(fā)期互作PPO活性變異方差分析
2.2 PPO活性的變化
圖1結(jié)果表明,籽粒發(fā)育過程PPO活性變化大致趨勢是先降低后升高,但品種間變化幅度不同。安農(nóng)95083-6-1和安農(nóng)0309 2個品種開始時PPO活性較高然后大幅度下降,下降后又漸漸升高;安農(nóng)95081-8、安農(nóng)9267、煙農(nóng)19和鄭麥9023這4個品種PPO活性的變化趨勢較為平緩。
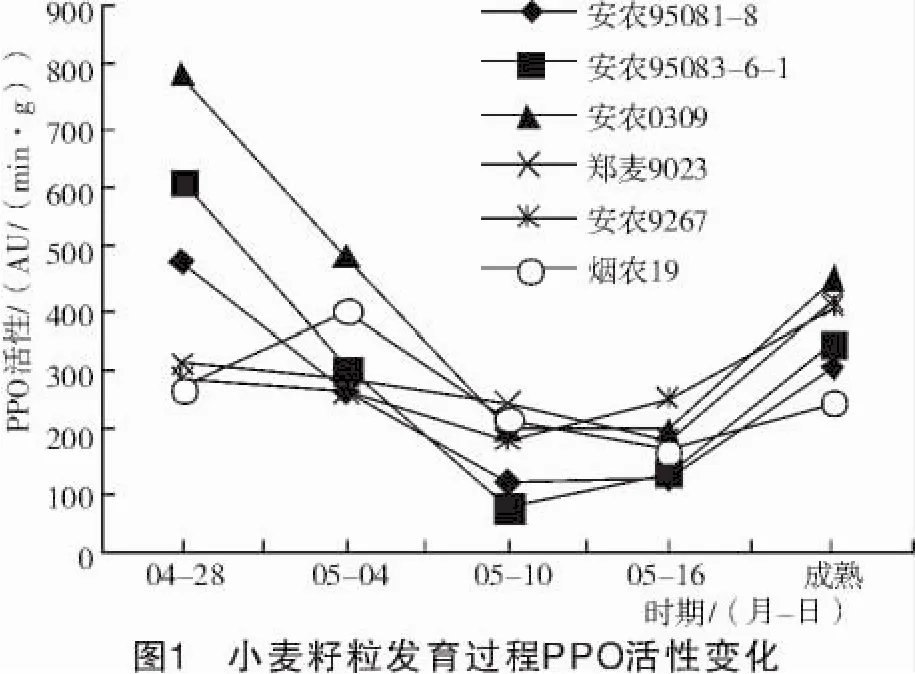
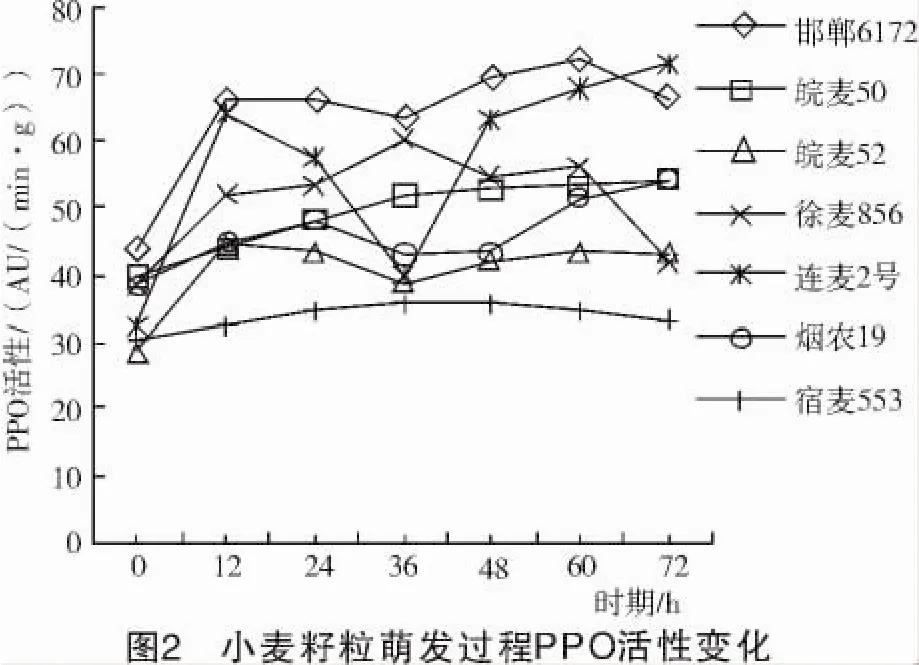
由圖2可知,各品種PPO活性的變化趨勢和幅度不盡相同,宿麥553變化幅度較小,其余6個品種變化幅度較大;徐麥856 PPO活性變化呈先升高后降低的趨勢;連麥2號、邯鄲6172、皖麥52 3個品種PPO活性呈升高后降低接著再升高又降低的變化。這說明小麥籽粒萌發(fā)過程中PPO活性是不穩(wěn)定的,但小麥籽粒萌發(fā)過程中成熟干籽粒(0 h)PPO活性最低。
3 結(jié)論與討論
小麥籽粒發(fā)育及萌發(fā)過程中PPO活性呈動態(tài)變化趨勢,存在著極其復(fù)雜的表達(dá)調(diào)控機制。通過對不同品種PPO活性的研究,不同發(fā)育期間的PPO活性差異遠(yuǎn)大于品種間的差異,籽粒發(fā)育過程中不同品種的不同發(fā)育時期間PPO活性變異水平不同,其PPO活性變化是開始時較高然后降低接著又升高,不同品種間這種變化幅度不同,一些品種變化幅度較大;萌發(fā)過程中PPO活性也是不穩(wěn)定的,各品種PPO活性的變化趨勢和幅度不盡相同,在小麥籽粒萌發(fā)過程中品種和萌發(fā)期對PPO活性都有顯著影響。現(xiàn)已知道PPO是一種質(zhì)體酶,存在于葉綠體、白色體等質(zhì)體中,生理狀態(tài)下與底物嚴(yán)格隔離[10],但在小麥籽粒萌發(fā)過程中,PPO易于釋放進而與底物接觸,這可能會導(dǎo)致萌發(fā)過程PPO活性較高。
一些研究發(fā)現(xiàn),在植物組織或器官中,幼嫩部位的PPO活性較高,而成熟或衰老部位的PPO活性低,但PPO的生理功能還不清楚[11,12]。由于PPO主要位于正常細(xì)胞的質(zhì)體中,其作為氧化還原酶被認(rèn)為與呼吸鏈末端電子傳遞有關(guān),能消除氧自由基的傷害與催化植物或動物的色素形成[13,14]。小麥植株P(guān)PO活性因感染病蟲而升高,因此PPO可能與植物自身防御功能有關(guān),但缺乏直接的證據(jù)。此外,PPO與植物的生長發(fā)育可能有關(guān),可促進乙烯的代謝。因此,本研究所得結(jié)果的原因可能有2個方面:一是籽粒本身抗性的需要,二是不同品種的小麥表達(dá)PPO的水平不同。
大量研究表明,PPO與植物抗病性密切相關(guān),PPO活性升高是小麥抵抗病原侵入和擴展的一種保護反應(yīng)。然而面制食品需要的是低PPO活性的小麥,以減輕面制食品的褐變,因而,在選育品種時,應(yīng)選擇籽粒發(fā)育期PPO活性高成熟后PPO活性低的品種。至于小麥籽粒發(fā)育和萌發(fā)期PPO活性變化是否存在內(nèi)在關(guān)系,這還有待于進一步研究。但本研究得出的籽粒發(fā)育的不同時期是影響PPO活性的主要因素,籽粒萌發(fā)過程中品種和萌發(fā)期對PPO活性都有顯著影響,這一結(jié)論可為小麥品質(zhì)改良提供重要信息。
[1] Baik BK,Czuchajowska Z,Pomeranz Y.Discoloration of dough for oriental noodles[J].Cereal Chemistry,1995,72:198-205.
[2] Bhattacharya M,Luo Q,Corke H.Time-dependent changes in dough color in hexaploid wheat landraces differingin polyphenol oxidase activity[J].Journal of Agricultural and Food Chemistry,1999,47(9):3579-3585.
[3] Feillet P,Autran J C,Verniere C L.Pasta brownness:an assessment[J].Journal of Cereal Science,2000,32:215-233.
[4] Hatcher DW,Kruger JE.Distribution of polyphenoloxidases in flour mill streams of Canadian common wheat classes milled to threeextraction rates[J].Cereal Chemistry,1993,70:51.
[5] Lamkin WM,Miller BS,Nelson SW,et al.Polyphenol oxidase activities of hard red winter,soft red winter,hard red spring,white common,club and durum wheat cultivars [J].Cereal Chemistry,1981,58(1):27-31.
[6] Kruger JE.Changesin thepolyphenol oxidases of wheat during kernel growth and maturation[J].Cereal Chem,1976,53(2):201-213.
[7] Taneja SR,Abrol Y P,Sachar RC.Modulation of o-diphenolase and monophenolase enzymes during wheat grain development[J].Cereal Chemistry,1974,51(2):457-465.
[8] Anderson JV,Morris CF.An improved whole-seed assay for screening wheat germplasm for polyphenol oxidase activity[J].Crop Science,2001,41:1697-1705.
[9] Morris CF,Anderson JV.Distribution of PPOactivity amonga large number of hexaploid wheat genotypes using an improved L-DOPA assay[J].Cereal Foods World,1998,43:518-520.
[10] W J,Shelton D R,Martin T J,et al.Variation in polyphenol Oxidase Activite and Quality Characteristic Among Hard White and Hard Winter Wheat Sample[J].Cereal Chem,1997,74(1):7-11.
[11] 金善寶.中國小麥學(xué)[M].北京:中國農(nóng)業(yè)出版社,1996.
[12] 蓋均益.作物栽培學(xué) [M].北京:中國農(nóng)業(yè)出版社,1994:98-123.
[13] 薛俊杰,王永琳,張淑改,等.泡桐叢枝病過氧化物酶和多酚氧化酶的研究[J].山西農(nóng)業(yè)科學(xué),2000,28(1):62-64.
[14] 云興福,崔世茂,霍秀文.黃瓜組織中幾種酶活性與其對雙霉病抗性的關(guān)系[J].華北農(nóng)學(xué)報,1995,10(1):92-98.

