左側偏癱患者上肢運動腦激活區與健康人對比的功能磁共振研究1)
董 培,崔方圓,譚中建,蔣根娣,張 華,鄒憶懷
臨床上,腦梗死有很高的致殘率,但同時也發現,在梗死發生后的一段時間,受損的神經功能會有一定程度的恢復。現代基礎研究將這種腦自行修復的能力歸結為腦的可塑性,其機制很復雜,與年齡、功能康復訓練、梗死位置等諸多因素相關。本研究通過對健康人與腦梗死后痙攣期患者左側上肢運動的BOLD-fMRI對照研究,試圖說明在運動通路損傷后,肢體運動所反應的激活腦區的特異性改變,進而初步探討腦梗死后腦功能重塑在痙攣期的特點及其機制。
1 資料與方法
1.1 臨床資料 偏癱組:偏癱患者6例,均為2008年3月—2009年3月于北京中醫藥大學附屬東直門醫院神經內科住院患者。其中男5例,女1例,年齡43歲~85歲。均為左側痙攣性偏癱者。經頭顱CT或磁共振成像(MRI)診斷為腦梗死,病程2周至6個月,均為首次發作腦血管病,病灶均在右側基底節和(或)放射冠,無意識障礙及視聽障礙,Brunnstrom分級在1級~4級(上肢)。另設正常組為對照組。以上兩組受試在試驗前均無不適,除偏癱組1例男性患者在試驗過程中出現煩躁、壓抑感而脫落外,余受試在試驗過程中均未出現明顯不適,配合完成試驗任務。受試前均簽署知情同意。
1.2 試驗方法 應用東直門醫院Simens Novus 1.5T超導磁共振掃描儀采用組塊設計模式進行掃描。在試驗前被告知試驗目的與方法,講解左上肢運動的方法、力度、幅度及頻率,
Brunnstrom分級在1級~2級的患者進行被動運動,Brunnstrom分級在3級~4級的患者進行主動運動,受試者主動或被動左上肢運動的頻率為從平臺上勻速自然抬起角度約45°~60°,經過前期訓練30 s內約運動 8次。受試者靜息休息10 min~15 min后進入核磁室,平臥位,視聽封閉狀態,線圈固定,保持頭位不動。首先進行結構像掃描,然后進行連續不間斷的左上肢主動或被動運動任務的fMRI的掃描。三維結構成像掃描采用 T1WI序列,掃描全腦。
1.3 Bold fMRI圖像處理及分析 采用BrainVoyager軟件對fMRI數據進行隨機效應模式統計處理。首先進行頭動校正,對處理過的圖像進行統計學分析,計算各像素的t值,P<0.05同時 voxel≥4的像素被認為有統計學意義。
2 結 果
2.1 正常組隨機效應模式分析 可見左上肢主動運動的激活腦區在小腦的分布以左側為主,包括小結、蚓部、后葉;右小腦激活區域以前葉、小腦扁桃體為主。在大腦皮層的激活區域以右側中央前回(BA4)、中央后回(BA2,3,4,5,40)為主,而左側大腦皮層未見明顯激活簇。詳見表1。
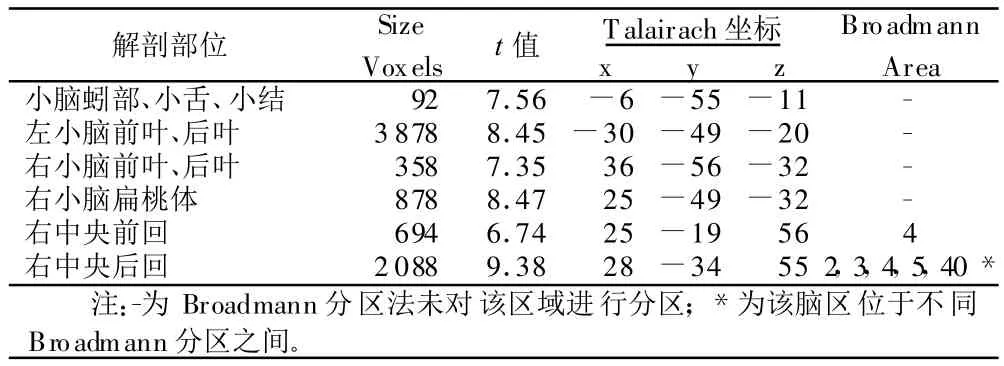
表1 正常組左上肢運動腦激活區像素數與t值
正常組左上肢主動運動腦功能抑制區以左右兩側邊緣系統為主,包括前扣帶回(BA24)、扣帶回(BA23,31,32)、后扣帶回(BA23,29,30,31)、海馬(BA19,27,34,35,36,37,38)、杏仁核;左側大腦皮層分布包括額下回(BA8,9)、中央前回(BA6,9)、頂枕楔前葉(BA7,23,31,39)、頂葉角回(BA39)、枕葉楔葉(BA18,30)、枕顳內側回(BA19,22)、顳葉(BA13,20,21,22,41)、島葉(BA13,22),激活簇較小;右側大腦皮層包括額中回(BA6,8)、頂枕楔前葉(BA 23,31)、顳上回(BA 38),激活簇較小。詳見表2。
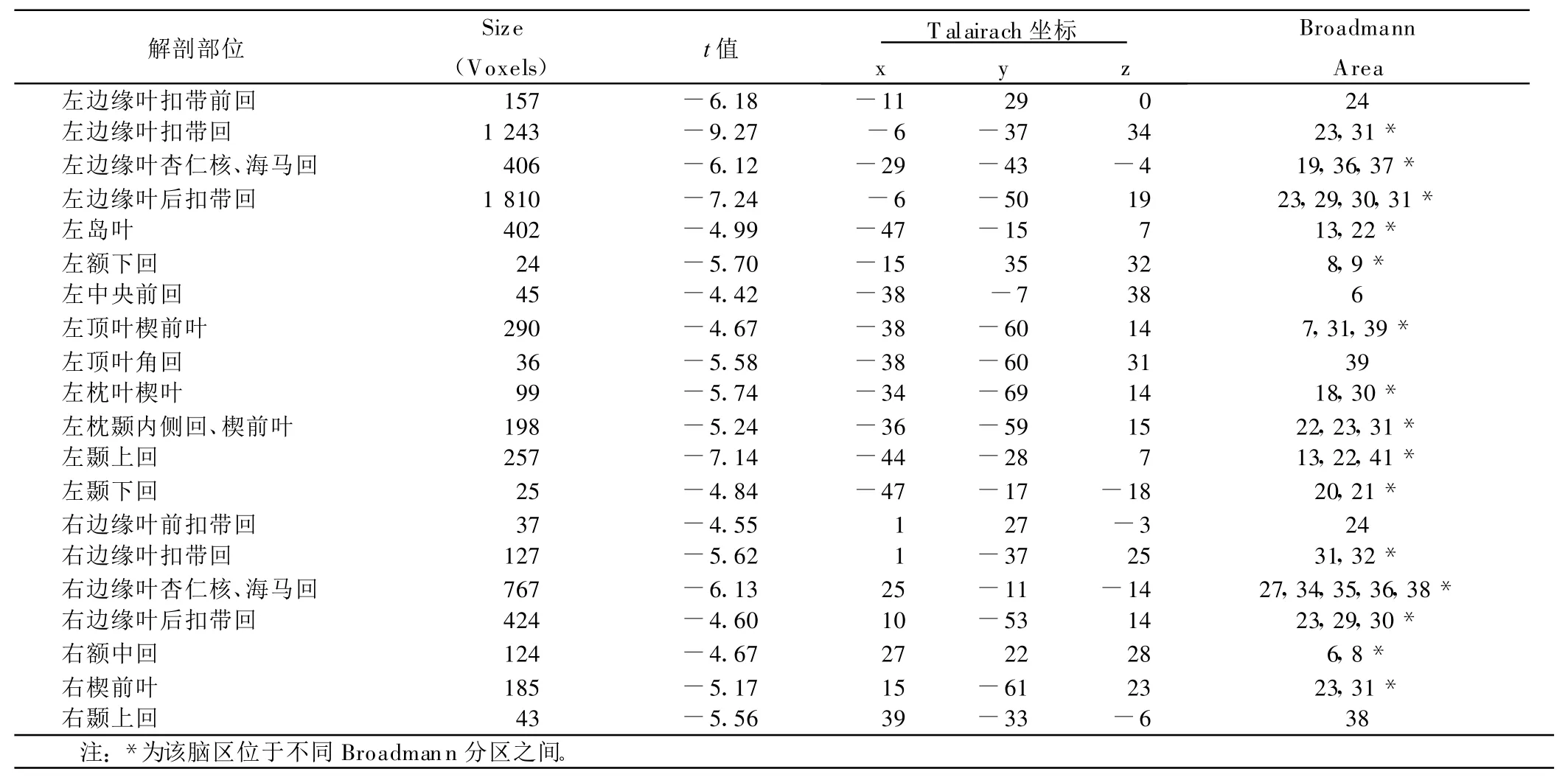
表2 正常組左上肢運動腦抑制區像素數與t值
2.2 對偏癱組隨機效應模式分析 可見左上肢運動的激活區包括:小腦蚓部、左小腦前后葉有明顯激活,右小腦后葉有較小激活簇;邊緣葉扣帶回有較小激活簇;左右蒼白球、殼核、左右丘腦及左島葉(BA13)有明顯激活;左側大腦皮層激活簇分布于左中央前回、中央后回(BA2,3,4)、頂下小葉(BA40)、枕葉楔葉(BA17,18,19,23)、顳葉上、中回(BA21,22);右側大腦皮層分布區為頂下小葉(BA40)、頂葉下部(BA40),上述區域激活程度較高,右枕葉楔葉和舌回(BA17,18)有少量激活。詳見表3、圖3。
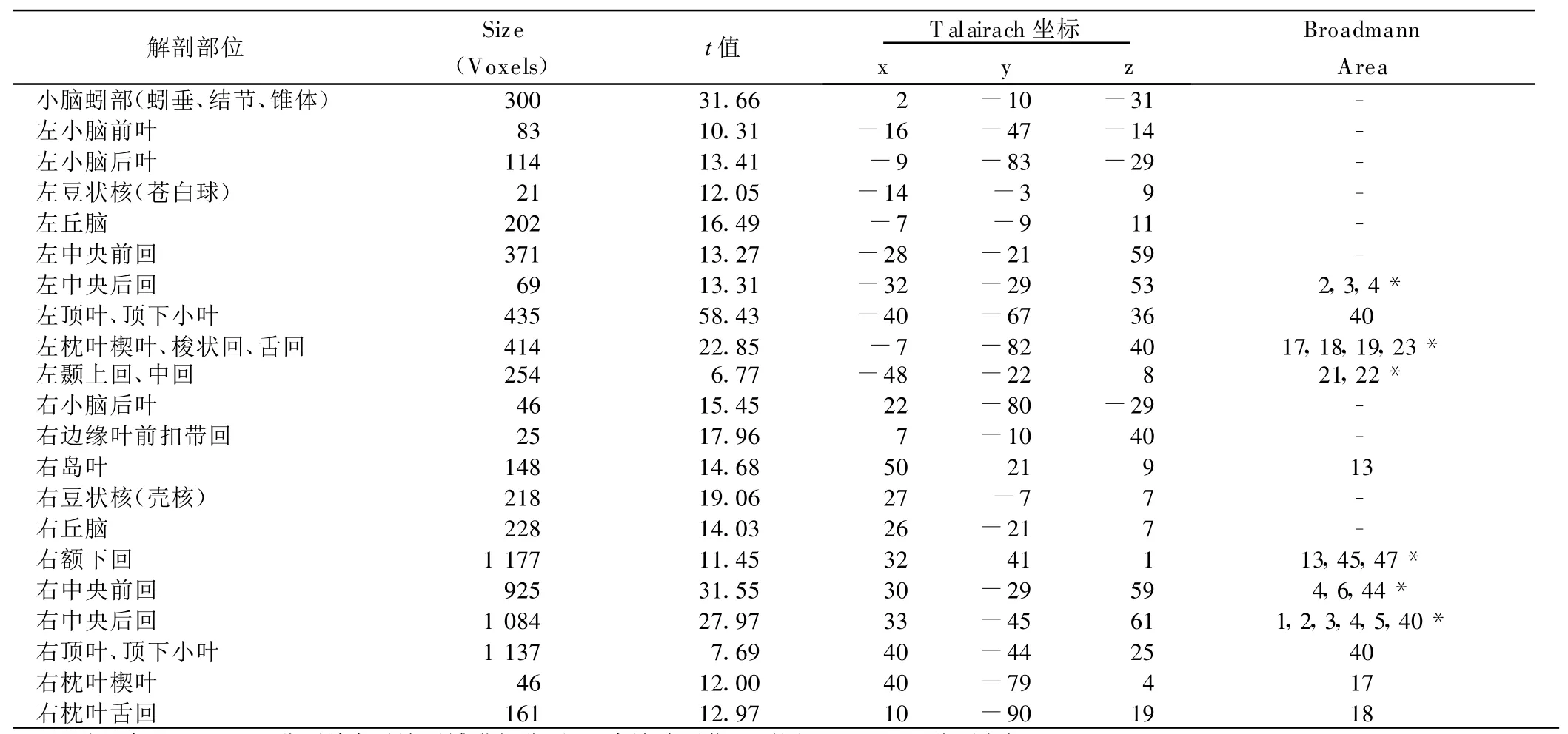
表3 偏癱組左上肢運動腦激活區像素數與t值
對偏癱組左上肢活動抑制區分析可見,腦干髓質、左尾狀核體和左島葉(BA13)有少量負激活簇。詳見表4。
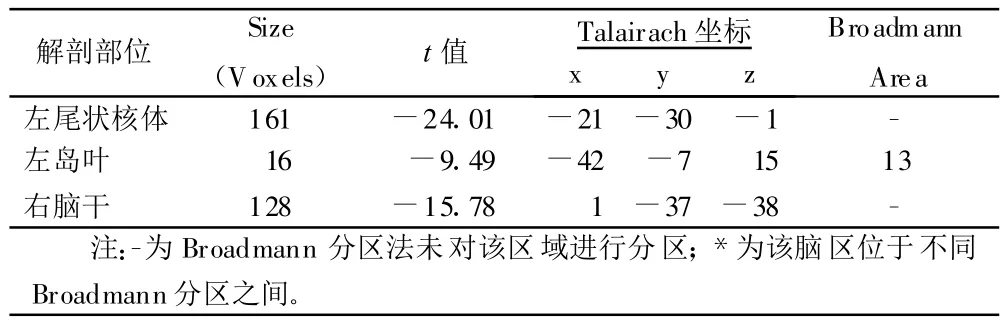
表4 偏癱組左上肢運動腦抑制區像素數與t值
兩組受試在執行左上肢運動任務在中央前回、后回(BA3,4區)有共同激活簇。應用BrainVoyager軟件中的ANOVA random effects analysis(F檢驗),對兩組的腦激活體素與兩組的刺激和靜息基線進行統計學分析發現,激活區分布于每組內分析結果相符合。詳見表5~表7。
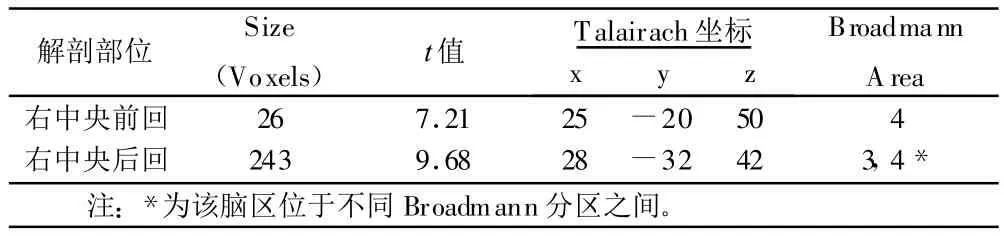
表5 兩組左上肢運動共同腦激活區
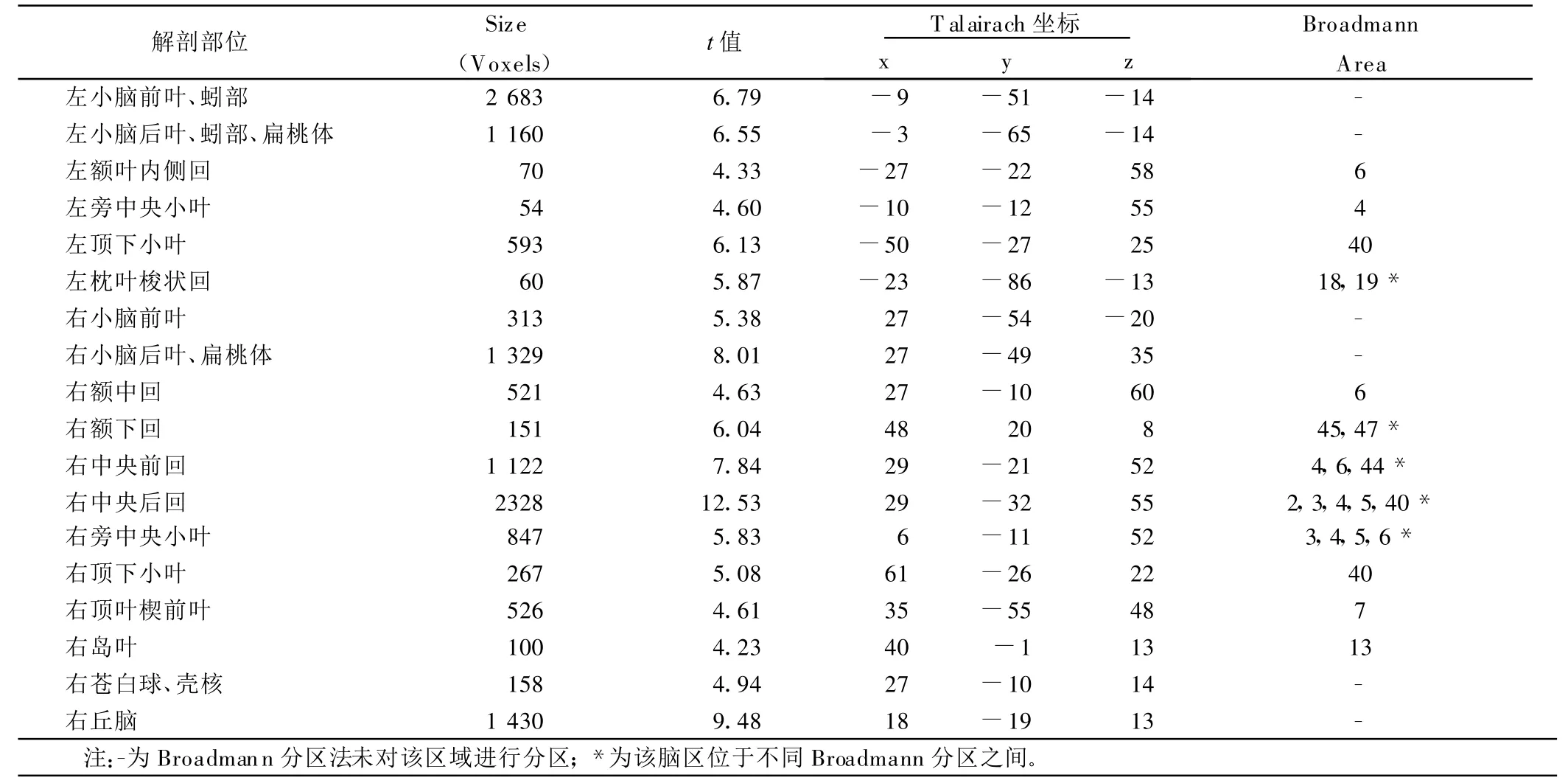
表6 兩組左上肢運動興奮腦區
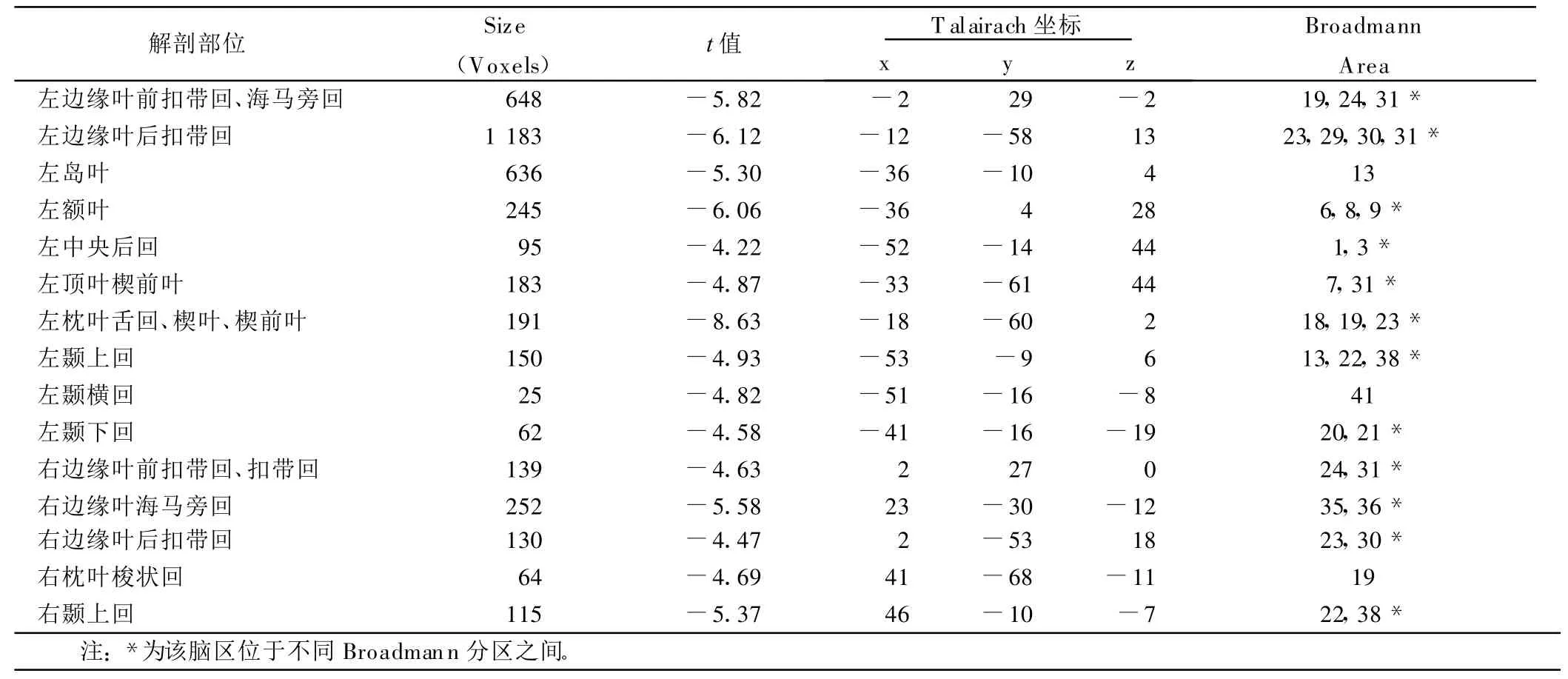
表7 兩組左上肢運動抑制腦區
3 討 論
正常組左上肢主動運動腦激活區主要分布在右側初級感覺運動皮層(SM1)及左側小腦。另外,次級軀體感覺皮層(BA5區)及后頂葉皮層(BA40區)亦見大面積激活簇。本試驗中,左上肢主動運動在右側SM1有明顯激活,并且沿中央前后回中上1/3分布,符合已知的皮層軀體定位排列方式。位于優勢半球的BA5區屬于次級軀體感覺皮層的一部分,其作用是整合到達初級感覺皮層的信息,并與原有記憶信息對比而成為經驗的一部分。由于本試驗設計為組塊設計,此區的激活可能與運動任務的重復性相關。頂葉皮層的BA40區在優勢半球被認為是較高的第三級聯合區,推測運動覺、觸覺、前庭覺、視覺、聽覺在此進行最高水平的整合,并且此區可發出纖維直接投射到運動前區(BA6區),從而形成與錐體系和錐體外系的直接和間接聯系[1]。這與已有研究認為的一些原來只參與運動準備的次級運動區,如輔助運動區(SMA)、前運動皮層(PMC)、次級運動區(PPC)也參與運動的執行[2]的結果相符。在小腦激活區中以左側舊小腦為著。舊小腦主要接受來自脊髓小腦通路的傳入沖動,而其傳出的沖動可以調節抗重力肌群的活動,提供運動時維持平衡的肌張力強度。由于本試驗采用左上肢抬舉運動,并要求運動保持一定的頻率和速度,因而肢體運動過程中需要維持一定的肌張力,這可能是舊小腦激活的原因。
雖然多數研究表明同側半球運動皮層在運動協調和運動控制方面起作用,如SMA在利手和非利手運動時都表現雙側激活[3],同側半球可能有控制精確運動的作用[4],并且左側優勢半球的作用更強[5]。更有研究發現右利手者即使在左手運動時左腦的激活程度強于右腦。這與本試驗結果略有差異,考慮原因:首先不同于其他試驗,本試驗任務為左上肢的抬舉運動,而非精細的對指運動,因此優勢半球沒有發揮較強的協調作用;其次,為了避免單個人的左側半球激活簇小而且分散的情況,本試驗分析采取嚴格的組群隨機效應的方法,從而造成左側大腦激活效應被剔除。
偏癱組左上肢主動運動引起雙側大腦運動皮層的明顯激活,激活區包括雙側初級感覺運動皮層、運動前區和次級運動區,雙側丘腦、小腦蚓部、右側小腦、右側島葉、殼核,以及健側大腦的蒼白球、扣帶回。與正常組相比,偏癱組的激活區域出現明顯泛化的情況,而且為雙側激活。這與以往的研究結果相符,如Kim等[6]發現卒中患者患側手運動會引起雙側初級感覺運動皮層的激活。Butefisch等[7]發現卒中患者患肢運動時引起雙側運動前區和初級運動皮層的激活。兩組左上肢主動運動時還出現了一些負激活的腦區,分布于扣帶回后部(BA31)、楔前葉(BA7)、左側 BA39、左側 BA19、左額葉背外側(BA8)等腦區。以上腦區被認為是靜息態腦活動網絡的一部分[8-10],其確切功能尚不清楚,但與大腦對內外環境的監測、情節記憶及自我意識相關。
由于大腦是個復雜的聯絡體系,各功能區間存在功能以及解剖結構上的聯系,因此,當某一腦區受損后,大腦皮層出現動態的功能重組以適應這一變化。目前研究認為主要存在三種皮層重組的類型:一是患側受累及的主要運動區發生移位;二是患側未受累及的主要運動區仍有激活;三是非主要運動區的功能明顯激活[11]。結合本研究分析其原因:腦梗死后患者運動功能的恢復有賴于錐體系以及錐體外系的共同作用,在隨意運動恢復的過程中,張力、運動協調、控制能力起到關鍵作用。本研究中偏癱組均為痙攣性偏癱患者,與正常組相比,偏癱組在執行運動任務時需要中樞神經系統更多的協調、控制作用,因此相應的腦區出現較多激活;本研究中偏癱組的運動激活區出現了何運動感覺皮層后方移動的現象,根據Ziemann等[13]的研究,這可能與本研究選取的病灶部位均在皮層下相關。
腦梗死后腦功能的重塑依賴于皮層功能的有機重組,受到多方面因素的影響。本研究發現偏癱組較正常組出現更多的錐體外系及次級運動區的激活,從而推測腦梗死后腦功能重塑的機制在于通過功能區的轉移和次級功能區的功能代償,這與以往的研究結果相符。但研究中也出現了一些無法用已有知識解釋的激活或負激活區域,如靜息態腦網絡相關的腦區,這需要大樣本的研究以闡明其機制。
[1] Cavada C,Goldman-Rakic PS.Posterior parietal cortex in rhesus monkey,Ⅱ:Evidence for segregated corticocortical networks linking sensory and limbic areas with the frontal lobe[J].Comp Neurol,1989,287:422.
[2] Weng XC,Li EZ,Zang YF,et al.Neural co rrelates of sequential finger movements revealde by event-related fMRI[J].Neuro Image,2000,11:920-927.
[3] Hlustikp,Solodkin A,Gullapallir P,et al.Functional lateralization of the human premotor cortex during sequential movements[J].Brain Cogn,2002,49(1):54-62.
[4] Ehrsson HH,Fagergren A,Jonsson T,et al.Cortical activity in precision-versus power-grip tasks:An fMRI study[J].Neurophy siol,2000,83(1):528-536.
[5] Jancke L,Specht K,Mirzazade S,et al.T he effect of finger movement speed of the dominant and the subdominant hand on cerebellar activation:A functional magnetic resonance imaging study[J].Neuro Image,1999,9(5):497-507.
[6] Kim YH,Jang SH,Byun WM,et al.Ipsilateral motor pathway confirmed by combined brain mapping of a patient with hemiparetic stroke:A case report[J].Arch Phy s Med Rehabil,2004,85(8):1351-1353.
[7] Butefisch CM,Kleiser R,Korber B,et al.Recruitment of contralesional motor cortex in stroke patients with recovery of hand function[J].Neurology,2005,64(6):1067-1069.
[8] Raichle M E,MacLeod AM,Snyder AZ,et al.A default mode of brain function[J].PNAS,2001,98(2):676-682.
[9] Mazoyer B,Zago L,Mellet E,et al.Cortical network fo r working memory and executive function sustain the conscious resting state in man[J].Brain Res Bull,2001,54(3):287-298.
[10] Greicius MD,K rasnow B,Resis AL,et al.Functional connectivity in the resting brain:A network analysis of the default mode hypothesis[J].PNAS,2003,100(1):253-258.
[11] Alkadhi H,Kollias SS,Crelier GR,et al.Plasticity of the humanmotor cortex in patients with arteriovenous malformations:A functional MR imaging study[J].AJNR,2000,21:1423-1428.
[12] Ziemann U,Iliac TV,Pauli C,et al.Learning modifies subsequent induction of long-term potentiation-like and long-term depressionlike plasticity in human motor cortex[J].Neuroscience,2004,24:1666-1672.

