5-甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃的合成及其與牛血清白蛋白的相互作用
李 艷,翟海燕,孫紹發(fā)
(1.咸寧學(xué)院化學(xué)與生命科學(xué)學(xué)院,湖北咸寧437100;2.廣西質(zhì)量技術(shù)工程學(xué)校,南寧替換為 530022)
5-甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃的合成及其與牛血清白蛋白的相互作用
李 艷1,翟海燕2,孫紹發(fā)1
(1.咸寧學(xué)院化學(xué)與生命科學(xué)學(xué)院,湖北咸寧437100;2.廣西質(zhì)量技術(shù)工程學(xué)校,南寧替換為 530022)
合成了一種新型的5-甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃有機(jī)化合物,通過核磁共振、紅外光譜及質(zhì)譜等對其結(jié)構(gòu)進(jìn)行了表征;應(yīng)用熒光光譜及紫外可見光譜法研究了該化合物(CAF)與牛血清白蛋白(BSA)之間在不同溫度下的相互作用.實(shí)驗(yàn)表明,CAF能強(qiáng)烈猝滅BSA的內(nèi)源熒光,猝滅機(jī)理為動態(tài)猝滅.在此基礎(chǔ)上計算了二者相互作用的結(jié)合常數(shù)、結(jié)合位點(diǎn)數(shù)及熱力學(xué)參數(shù)等,結(jié)果表明,CAF與BSA分子以摩爾比1∶1結(jié)合,其結(jié)合反應(yīng)主要是熵驅(qū)動,主要作用力是疏水力.
5-甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃(CAF);合成;表征;牛血清白蛋白;熒光猝滅;熱力學(xué)參數(shù)
近幾十年來,雜環(huán)化合物在醫(yī)藥和農(nóng)藥中的不斷出現(xiàn),使得雜環(huán)化合物日益成為生物活性物質(zhì)研究的重點(diǎn)[1],據(jù)文獻(xiàn)報道,已發(fā)現(xiàn)一些雜環(huán)胺類化合物表現(xiàn)出很高的抑菌活性,如噌啉衍生物,該類藥劑在防治稻瘟病方面表現(xiàn)出突出的特點(diǎn)[2].已有許多專利和文獻(xiàn)報道呋喃衍生物的合成及其具有良好的殺菌及抗癌等生物活性[3].
血清白蛋白是血液中含量最豐富的蛋白質(zhì),具有許多重要的生理功能,能和許多內(nèi)源及外源性化學(xué)物質(zhì)以各種方式結(jié)合,并攜帶著這些物質(zhì)通過血液在體內(nèi)進(jìn)行轉(zhuǎn)運(yùn)、運(yùn)輸、分配和代謝[4].因此,從不同的角度研究以白蛋白為代表的蛋白質(zhì)與具有生物活性小分子間的相互作用,了解藥物的作用機(jī)制,已成為一個非常活躍的研究課題.研究藥物小分子與蛋白質(zhì)作用的方法有很多,其中熒光光度法因?yàn)榫哂徐`敏度高、選擇性好、操作簡便易行等特性,得到廣泛應(yīng)用[5].
本文研究了運(yùn)用原料易得、條件溫和及收率較高的反應(yīng)來合成新型呋喃胺類化合物5-甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃(CAF)[6],并應(yīng)用熒光猝滅法研究其與BSA的相互作用.
1 合成部分
1.1 主要儀器與試劑
儀器:400型400MHz核磁共振儀(Varian Mercury公司,TMS為內(nèi)標(biāo))、X4型熔點(diǎn)儀(北京第三光學(xué)儀器廠,溫度未經(jīng)校正)、Perkin-Elemer PE-983紅外光譜儀(KBr壓片)、帶恒溫系統(tǒng)的 F-4500熒光分光光度計(日本日立公司)、UV-2300紫外可見分光光度計(北京普析通用儀器有限公司)、AU Y120電子分析天平.
藥品:氯代乙酰乙酸乙酯,丙二腈,對氯苯甲醛,醋酸,硼氫化鈉等試劑均為市售分析純和化學(xué)純.乙醇用金屬鈉處理后重新蒸餾,三乙胺新蒸餾后用 KOH干燥,甲醇新蒸餾;BSA(Sigma公司)、Tris(生化試劑)、鹽酸、NaCl(分析純)等,BSA溶解在 Tris-HCl(0.05 moL/L Tris,0.10 moL/L NaCl,p H=7.4)緩沖溶液,白蛋白溶液在開始實(shí)驗(yàn)前15分鐘配制,實(shí)驗(yàn)用水為二次亞沸水.
1.2 合成路線[6]
合成路線見圖1.
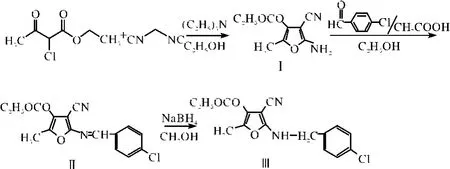
圖1 CAF的合成路線圖Fig.1 The road map of synthesis of CAF
1.3 合成步驟
1.3.15 -甲基-4-乙氧羰基-3-腈基-2-氨基呋喃 Ⅰ的制備 參考文獻(xiàn)方法[6],在冰水浴條件下,應(yīng)用丙二腈、氯代乙酰乙酸乙酯,在乙醇中,三乙胺催化反應(yīng),制得5-甲基-4-乙氧羰基-3-腈基-2-氨基呋喃Ⅰ,白色固體,產(chǎn)率約90%,m.p.224~225℃.
1.3.25 -甲基-4-乙氧羰基-3-腈基呋喃 Schiff堿Ⅱ的制備 向干燥的圓底燒瓶中加入Ⅰ(2 g),無水乙醇(20 mL),芳醛(10 mmol),冰醋酸(8~10滴),在磁力攪拌的作用下加熱回流24小時后,冷卻到室溫,即析出5-甲基-4-乙氧羰基-3-腈基呋喃Schiff堿 Ⅱ,黃色晶體,產(chǎn)率 80%,m.p.153~154℃.1H NMR(CDCl3,400 MHZ)δ:8.14~8.35(m,4H,Ar—H),8.83(s,1H,—CH=N —),4.37~4.43(m,2H,—CH2O),2.66(s,3H,—CH3),1.37~ 1.42(m,3H,CH3—CH2—);IR(KBr)υ:1634(C=N),1715(C=O),1607,1553 cm-1;MS(70 eV)m/z(%):318(M+,11),304(5),216(24),165(15),125(100),105(98),77(16).
1.3.35 -甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃(CAF)Ⅲ的合成 向(100 mL)干燥的圓底燒瓶中加入(3 mmol)SchiffⅡ,再加入10 mL新蒸的無水甲醇,快速加入NaBH4(3 mmol),在圓底燒瓶口安上防氫氣外逸的塑料袋(或氣球),冰水浴下攪拌1 h,分兩次補(bǔ)加NaBH4(3 mmol),移開冰水浴,3小時后,點(diǎn)樣,若反應(yīng)完全,將圓底燒瓶的混合液體緩慢倒入配有磁力攪拌器的冰水浴中,減壓抽濾,得到白色固體,用乙醇重結(jié)晶得目標(biāo)化合物Ⅲ,白色晶體,產(chǎn)率70%,m.p.104~105℃.1H NMR(CDCl3,400 MHZ)δ:7.25~7.35(m,4H,Ar—H),5.21(s,1H,—NH —),4.53~4.54(m,2H,—CH2N),4.29~4.33(m,2H,—CH2O),2.45(m,3H,—CH3),1.35~1.37(m,3H,CH3—CH2—);MS(70 eV)m/z(%):320(M+,11),306(5),206(24),167(15),127(100),107(98),79(16).
2 光譜法研究5-甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃(CAF)與牛血清白蛋白(BSA)的相互作用
2.1 實(shí)驗(yàn)方法
溶液的配制:配制不同溫度(T=298,302,306,310 K)下p H=7.4的 Tris-HCl緩沖溶液;在2 cm的比色皿中分別加入2 mL 1×10-5mol/L的BSA溶液和不同量的化合物CAF,得到化合物CAF與BSA之間不同物質(zhì)的量之比的系列溶液.
吸收光譜:分別測定化合物 CAF、BSA及1∶1的CAF-BSA溶液的吸收光譜.
熒光光譜:測定各溶液在不同溫度下的熒光光譜,選定激發(fā)和發(fā)射狹縫均為 2.5 nm,以λ=295 nm激發(fā),繪制295~450 nm的熒光光譜圖.
2.2 熒光光譜特征
BSA分子中色氨酸,酪氨酸和苯丙氨酸的存在使其具有內(nèi)源性熒光.以λex=295 nm激發(fā)BSA,在295 nm附近有很強(qiáng)的熒光峰,而相同條件下化合物CAF溶液在295 nm附近則沒有熒光峰,證明CAF不會發(fā)生與BSA相互干擾的熒光.固定BSA的量,隨著體系中化合物CAF的濃度的增加,BSA的內(nèi)源熒光進(jìn)行有規(guī)律的猝滅,如圖2所示(Fig.2).

圖2 CAF對BSA熒光光譜的影響Fig.2 Quenching of BSA fluorescence spectra by adding CAF
2.35 -甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃(CAF)猝滅BSA機(jī)理的推斷
熒光猝滅機(jī)理通常分為動態(tài)猝滅和靜態(tài)猝滅兩種.動態(tài)猝滅是猝滅劑和熒光物質(zhì)的激發(fā)態(tài)分子之間的相互作用引起的,其猝滅依賴于擴(kuò)散,由于溫度升高會導(dǎo)致擴(kuò)散系數(shù)增大,因此熒光物質(zhì)的猝滅常數(shù)將隨溫度的升高而增大.其過程遵循Stern-Volmer方程[7].

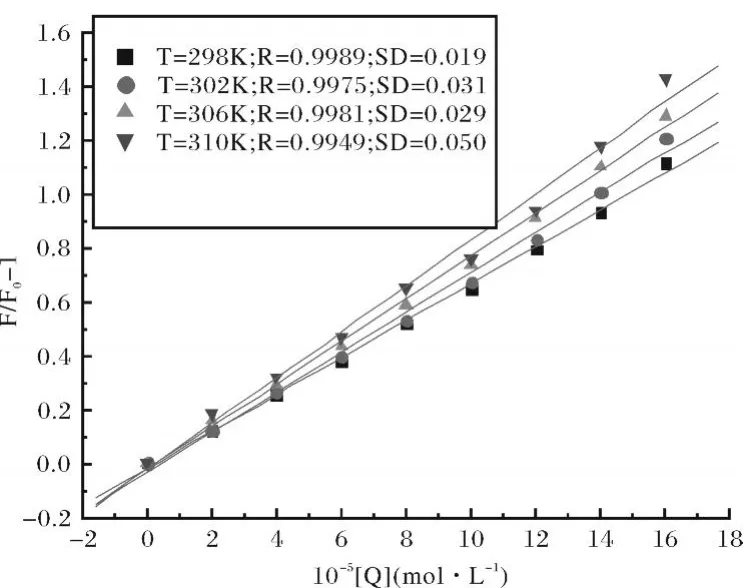
圖3 CAF對BSA熒光猝滅的Stern-Volmer圖Fig.3 Stern-Volmer plots at four different temperatures
式(1)中 F0和 F分別表示不存在和存在猝滅劑時熒光物質(zhì)的熒光強(qiáng)度;[Q]為猝滅劑的濃度,KSV是Stern-Volmer猝滅常數(shù).
靜態(tài)猝滅是猝滅劑與熒光物質(zhì)分子在基態(tài)時生成不發(fā)光的配合物,從而導(dǎo)致熒光物質(zhì)熒光強(qiáng)度降低的過程,溫度升高則導(dǎo)致基態(tài)配合物穩(wěn)定性下降,因此靜態(tài)猝滅常數(shù)將隨溫度的升高而減小,其過程可用下式描述:

分別測定了四個不同溫度(T=298,302,306和310 K)條件下,5-甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃(CAF)對BSA的熒光猝滅情況.圖3(Fig.3)為一定濃度范圍內(nèi)不同溫度下的[(F0/F)-1]-[Q]關(guān)系圖.從圖3可以看到,不同溫度下,猝滅常數(shù)不同,且隨溫度升高 KSV增大,表明上述猝滅為動態(tài)猝滅機(jī)理.
2.4 作用力類型的確定
藥物和生物活性分子之間的相互作用力包括氫鍵、靜電作用力、范德華力、疏水力四種.假設(shè)在測定溫度范圍內(nèi)焓變變化不大,則它的值和熵變ΔS可以從Vant Hoff方程求得[8].
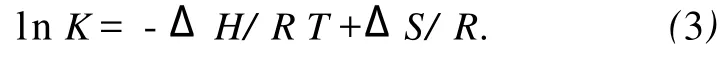
這里 K類似于在相應(yīng)溫度下的Stern-Volmer中的猝滅常數(shù) K[8]SV.自由能變ΔG由下式求得.
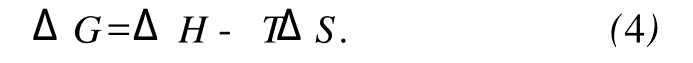
通過lnKSV對1/T作圖得圖4(Fig.4).
由式(4)計算得自由能變(ΔG)列于表 1.從ΔG的值可以看出SDA與BSA的相互作用是自發(fā)的.同時其相互作用的焓變及熵變是增大,表明CAF與BSA的結(jié)合主要是熵驅(qū)動的,其主要作用力類型為疏水力.
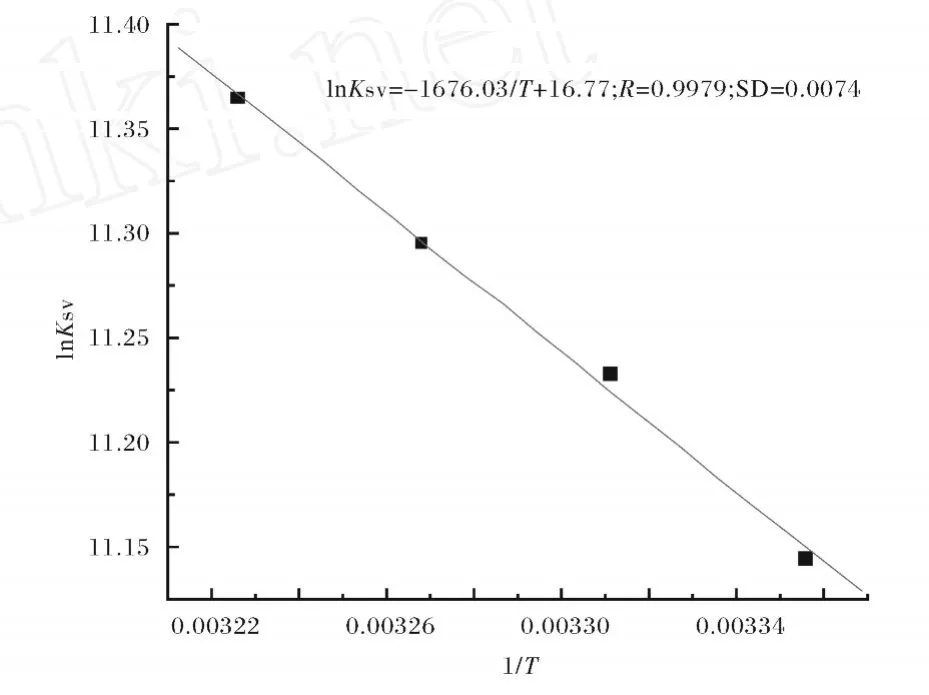
圖 4 Van’t-Hoff曲線圖Fig.4 Van’t-Hoff plot,p H=7.40,

表1 Stern-Volmer動態(tài)猝滅常數(shù) KSV及相關(guān)熱力學(xué)參數(shù)Tab.1 Stern-Volmer quenching constantKSVand relative thermodynamic parameters
2.5 表觀結(jié)合常數(shù)及結(jié)合位點(diǎn)數(shù)
當(dāng)小分子與大分子結(jié)合時其結(jié)合常數(shù)與結(jié)合位點(diǎn)數(shù)由下式求出:

這里 n為結(jié)合位點(diǎn)數(shù),Kb為表觀結(jié)合常數(shù),由(5)式作 lg[(F0/F)-1]~lg[Q]圖(見圖 5),依直線的斜率和截距即可求出CAF與BSA結(jié)合位點(diǎn)數(shù)n及表觀結(jié)合常 Kb.對于不同溫度下相關(guān)數(shù)據(jù)的計算結(jié)果列于表2.

圖5 lg[(F0/F)-1]~lg[Q]曲線圖Fig.5 Van’t-Hoff plot,lg[(F0/F)-1]~ lg[Q]
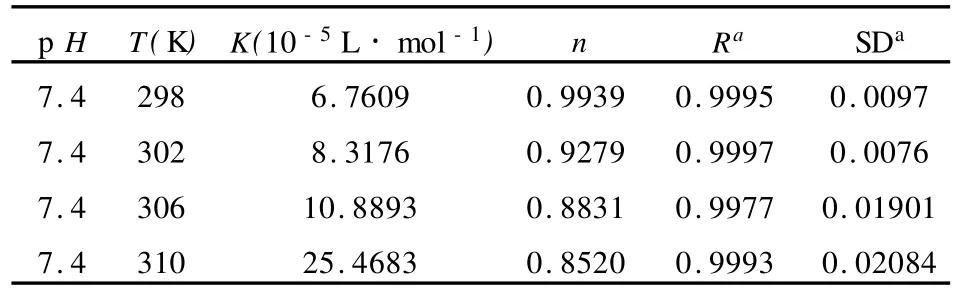
表2 不同溫度下的表觀結(jié)合常數(shù) Kb和結(jié)合位點(diǎn)數(shù)nTab.2 Binding constantKand Binding sitesn at different temperatures
在按近人體生理?xiàng)l件(p H=7.4,T=310 K)時,相關(guān)系數(shù) R大于0.99,結(jié)合位點(diǎn)數(shù) n接近1,說明CAF與BSA易以1∶1形成復(fù)合物;且溫度變化對結(jié)合常數(shù)影響比較小,說明了CAF與BSA之間有較強(qiáng)的結(jié)合作用,可以被蛋白質(zhì)所貯存和運(yùn)輸.
2.6 結(jié)合距離
按 F?rster的無輻射能量轉(zhuǎn)移理論可以求得CAF與BSA結(jié)合時結(jié)合位置與蛋白質(zhì)分子中熒光發(fā)射基團(tuán)之間的距離[9].

這里 r是給體(BSA)和受體(CAF)之間的距離,R0是轉(zhuǎn)移效率為50%時的臨界距離,可由下式求出
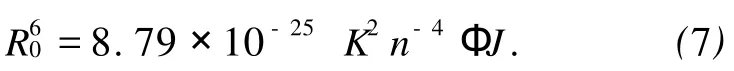
(7)式中 K2為偶極空間取向因子,n為介質(zhì)的折射指數(shù),Ф為給體的熒光量子產(chǎn)率,J為給體的熒光發(fā)射光譜(a)與受體吸收光譜(b)的光譜重疊積分 ,即:
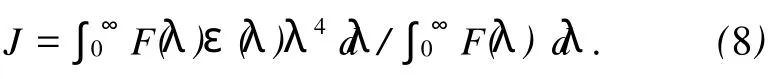
(8)式中 F(λ)為熒光受體在波長λ處的熒光強(qiáng)度,ε(λ)為受體在波長λ處的摩爾吸光系數(shù).圖6為CAF與BSA的摩爾比為1∶1時,化合物M的吸收光譜與熒光發(fā)射光譜的重疊圖.將圖中的光譜重疊部分按式(8)求出 J.在上述實(shí)驗(yàn)條件下,取K2=2/3,n=1.36,Ф=0.15,將這些數(shù)值代入式(7)可出 R0=3.37 nm;通過式(6)求出能量轉(zhuǎn)移效率 E=0.166,根據(jù) R0、E的值,由式(6)算出BSA內(nèi)色氨酸殘基與CAF分子間的距離 r=2.5 nm,符合能量轉(zhuǎn)移理論.說明CAF與BSA是足夠靠近(r<7nm),其結(jié)合是通過無輻射能量轉(zhuǎn)移而促使蛋白質(zhì)的熒光猝滅.
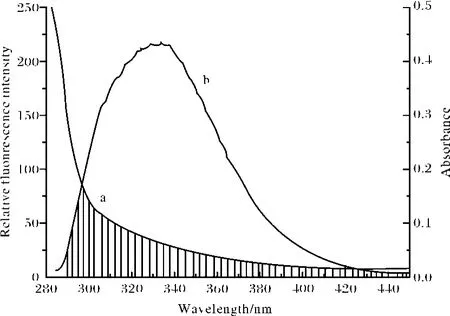
圖6 為CAF與BSA的摩爾比為1∶1時,化合物的吸收光譜與熒光發(fā)射光譜的重疊圖Fig.6 Spectral overlap of the fluorescence of
3 結(jié)論
實(shí)驗(yàn)合成了化合物 5-甲基-4-乙氧羰基-3-腈基-2-對氯苯甲胺基呋喃(CAF),并通過核磁共振儀、質(zhì)譜儀、紅外光譜儀對合成的產(chǎn)物進(jìn)行鑒定是成功的.應(yīng)用熒光光譜法、紫外吸收光譜法研究CAF與BSA的相互作用.研究結(jié)果表明CAF對BSA的熒光猝滅機(jī)理是動態(tài)猝滅過程,從結(jié)合位點(diǎn)常數(shù)值能斷定CAF與BSA以摩爾比1∶1結(jié)合,從計算出焓變和熵變值中,其中焓變值為常數(shù),熵變值為正,可表明此結(jié)合反應(yīng)主要是熵驅(qū)動,反應(yīng)中主要作用力是疏水力.
[1]Ding M W,Yang S J,Zhu J.New efficient synthesis of 2-substituted 5,6,7,8-tetrahydro benzothieno[2,3-d]pyrimidin-4(3H)-ones[J].Synthesis,2004,33(1):75-79.
[2]Liang Y,Ding M W,Liu ZJ,Liu X P.A facile and selective synthesis of 2-alkylamino-4(3H)-quinazolinones[J].Synth Commun,2003,33(6):2843-2848.
[3]周雅琴,宋增福,肖枚英,等.呋喃衍生物的合成[J].北京大學(xué)學(xué)報:自然科學(xué)版,1996,32(1):51-53.
[4]馬貴斌,楊 頻.熒光法研究血清白蛋白與藥物的結(jié)合作用[J].生物化學(xué)雜志,1992(5):624-630.
[5]王麗芳,楊斌盛.羥基-2-萘甲酸與牛血清白蛋白的作用[J].山西大學(xué)學(xué)報,2006,29(2):171-174.
[6]Hu Y G,Li G H,Ding M W.Efficient synthesis of furo[2,3-d]pyrimidin-4(3H)-ones[J].Arkivoc,2008(8):151-158.
[7]Cyril L,Earl J K,Sperry W M.Biochemists Handbook[M].London:Epon Led Press,1961:84.
[8]Hu YJ,Liu Y,Shen X S,et al.Studies on the interation between 1-hexylcarbamoyl-5 fluorouracil and bovone serum albumin[J].Molecular Structure,2005,738:143-174.
[9]Lakowicz J R.Principles of Fluorescence Spectroscopy[M].New York:Plenum Press,1999:237-265.
[10]孫紹發(fā),於敏敢,朱先軍.光譜法研究一種咪唑啉酮類衍生物與牛血清白蛋白的相互作用[J].華中師范大學(xué)學(xué)報:自然科學(xué)版,2007,41(3):171-174.
Abstract:a new compound 5-methyl-4-ethoxycarbonyl-3-cyano-2-parachlorobenzyl aminofuran has been synthesized and characterized by1H NMR,IR and MS.The interaction between 5-methyl-4-ethoxycarbonyl-3-cyano-2-parachlorobenzyl aminofuran(CAF)and Bovine Serum Albumin(BSA)was investigated by fluorescence and absorption spectroscopy.The experimental results showed that the fluorescence quenching of BSA by CAF was a result of the formation of the CAF-BSA complex and dynamic quenching occurred in the fluorescence quenching.The binding sites numbern,apparent corporation constant Kand corresponding thermodynamic parametersΔH,ΔG,ΔSwere calculated.The research results indicated that CAF bound BSA with molar ratio of 1∶1 and the binding reaction was mainly entropy-driven and hydrophobic interactions forces played major role in the reaction.
Key words:5-methyl-4-ethoxycarbonyl-3-cyano-2-parachlorobenzyl aminofuran;synthes;characterizition;Bovine Serum Albumin;fluorescence quenching;thermodynamic parameters
Synthesis and interaction with Bovine Serum Albumin of 5-methyl-4-ethoxycarbonyl-3-cyano-2-parachlorobenzyl aminofuran
LI Yan1,ZHAI Haiyan2,SUN Shaofa1
(1.Department of Chemistry and Life Science,Xianning College,Hubei,Xiangning 437000;2.School of Guangxi Quality and Technical Engineering,Nanning 530022)
S482
A
1000-1190(2010)04-0624-05
2010-06-27.
湖北省教育廳重點(diǎn)項(xiàng)目(D20092840).
*E-mail:liyan750606@yahoo.com.cn.

