飼用α-半乳糖苷酶穩定性及酶學特性的研究
中國農業大學動物科技學院 王春林 陸文清
α-半乳糖苷酶是消除飼料原料中α-半乳糖苷聚糖類抗營養因子的飼用外源酶類 (張麗英,2000;Leske和 Coon,1999)。但酶在加工應用過程中先經受原料混合加工、高溫制粒、運輸和儲存等環節后,才在動物胃腸道溶解發生作用,所以酶制劑的穩定性倍受關注。α-半乳糖苷酶理化性質的研究對其在飼料中的應用具有指導意義。本試驗對α-半乳糖苷酶粗制品的耐酸、耐溫和耐儲存性能進行了測定,體外研究了動物消化液對酶活力的影響,探討了粗酶-底物作用的動力學特征。
1 材料與方法
1.1 酶樣與酶活測定 酶樣取自青霉菌(Penicillium sp.MAFIC-6)固態發酵生產的α-半乳糖苷酶粗酶制劑,測試樣品為原酶干粉或原酶稀釋液。酶活分析方法參照Wang等(2004)。
1.2 pH對酶活力及穩定性的影響 用醋酸-醋酸鈉緩沖溶液 (pH 3.6 ~ 5.6,0.05 mol/L)、NaH2PO4-Na2HPO4緩沖溶液 (pH 5.7 ~8.0,0.10 mol/L)、Tris-鹽酸緩沖溶液 (pH 6.8 ~9.2,0.10 mol/L)和 Na2CO3-NaHCO3緩沖溶液(pH 9.2~10.7,0.10 mol/L)配制pH為2.5~12.5的緩沖體系,測定相同酶液在不同pH條件下的酶活力,確定最適pH。為觀察酶的pH穩定性,用pH 2.5~12.5反應液在40℃分別孵育酶液1、2 h和12 h,再按常規方法測定殘余酶活力。
1.3 溫度對酶活力及穩定性的影響 將酶液置于30~100℃溫度下反應測定不同溫度下的酶活力,確定酶作用的最適溫度。為了解酶在濕熱下的穩定性,將相同的稀釋酶液分別在30~100℃下處理30 min和60 min,冷卻后按常規方法測定殘余酶活力。為了解酶在干熱下的穩定性,用金屬鋁盒稱取干酶粉2.0 g左右,置于30~100℃溫度處理30 min和60 min,冷卻后測定殘余酶活力。結果表示為相對酶活力。
1.4 金屬離子對酶活力的影響 分別配制10×10-3mol/L的金屬離子(見表1)溶液,用酶液混合稀釋使離子在體系中的終濃度為1×10-3mol/L或1×10-4mol/L,于 40 ℃保溫 30 min,然后按常規方法測定α-半乳糖苷酶活力。結果表示為相對于未經金屬離子處理的酶活力的百分比例。
1.5 豬消化液對酶活力的影響 選取6頭體重(20±0.5)kg健康的達蘭豬,屠宰后分別從胃幽門部和小腸空腸部位取內容物,迅速用8層紗布過濾,4℃下4000 r/min離心20 min,取上清液裝棕色瓶-20℃冷凍保存備用。分別用醋酸緩沖溶液(pH 5.5)、胃液(pH 4.0 ~ 4.3)和小腸液(pH 6.1 ~6.3)混合原酶液(V/V 為 9∶1),放置 12 h 和 24 h。其中部分樣品用胃液處理12 h后繼續用腸液處理12 h。最終在統一條件下測定混合液殘余酶活力。以醋酸緩沖液的酶活力為對照,其他酶活與之相比的百分數為相對酶活力。
1.6 酶的耐儲藏試驗 選取起始酶活不同的兩個中試干燥酶樣品 (水分 <8%)。在常溫15~30℃和相對濕度 <50%條件下密封保存9個月,分別在3、6月和9月時取樣測定α-半乳糖苷酶活力,每個樣取6個平行。
2 結果與討論
2.1 pH對酶活的影響 酶的活性受所在環境pH的影響。pH改變能影響酶分子活性部位上有關基團的解離。在非最適pH時,活性基團的解離狀態發生改變,酶底物的結合力降低,因而酶促反應速度降低。此外,環境過酸、過堿能使酶蛋白本身變性失活。酶作為一種活性蛋白質,酶-底物體系的酸堿度影響到酶分子結構域、酶與底物的離子化程度及其間的親和力,一定的解離狀態最適合其催化反應,極端pH條件對酶可引起不可逆的破壞,使酶失活(沈同和王鏡巖,1991)。圖1表明,α-半乳糖苷酶最適pH為4.5。酶在不同pH反應體系中分別保溫1、2 h和12 h后,剩余酶活力呈現了相似的變化趨勢。以pH 4.5的相對酶活力為100%,當pH超過6.5時,3個時間的酶活力均保持在67%左右,隨后酶活迅速下降,到7.5時酶活保持依次為22.46%、20.51%和20.50%,到pH 8.5時,酶活均下降到10.5%以下。在pH 3.5以下時,3個時間點的酶活依次為16.82%、80.18%和53.04%,說明該酶具有較強的耐酸性能。由此可見,該酶的穩定pH在3.5~6.5。
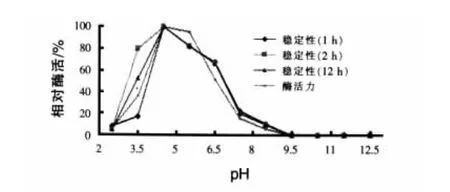
圖1 pH對酶活力及穩定性影響
2.2 溫度對酶活穩定性的影響 酶是一種生物活性催化劑,具有一般催化劑的性質,即其催化效率在一定范圍隨溫度升高而增加,但酶蛋白又會隨溫度升高逐漸變性而喪失催化活性。酶作用最適溫度是這兩種效應的綜合體現。圖2表明,酶的最適溫度在50~60℃。以30℃的相對酶活力為100%,在反應液中,酶在60℃保持30 min和60 min時的相對酶活力仍保持在90.67%和85.95%,但到70℃時,酶活迅速消失。圖3表明,酶在干熱條件下穩定性比濕熱高,超過80℃處理30 min或60 min,酶活仍保持在80%以上,顯然熱處理時間越長,酶活損失越快。因此,認為酶在70℃以下時是穩定的。
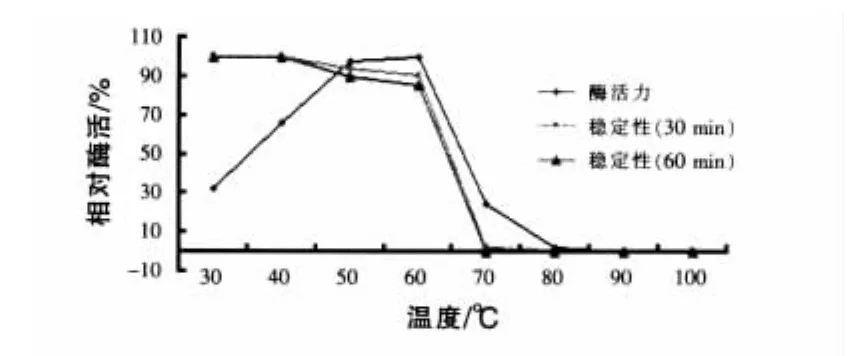
圖2 濕熱對酶活力及穩定性的影響
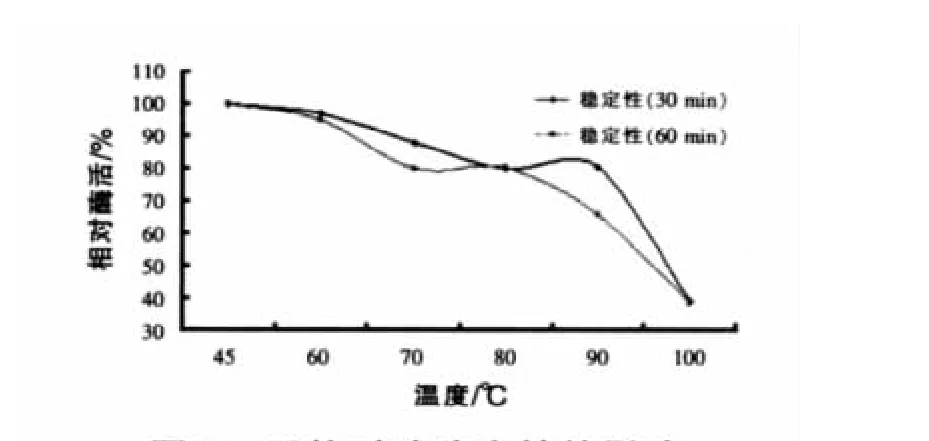
圖3 干熱對酶穩定性的影響
2.3 金屬離子對酶活力的影響 結果如表2所示。在離子濃度較高(1×10-3mol/L)時,各種金屬離子均不同程度地抑制了酶活;在低離子濃度(1×10-4mol/L) 時,Co2+和 Mn2+對酶活力有輕微的促進作用,Zn2+、Sn2+和Ca2+幾乎無影響。兩種濃度的Ag+和Hg2+均強烈抑制了酶活。
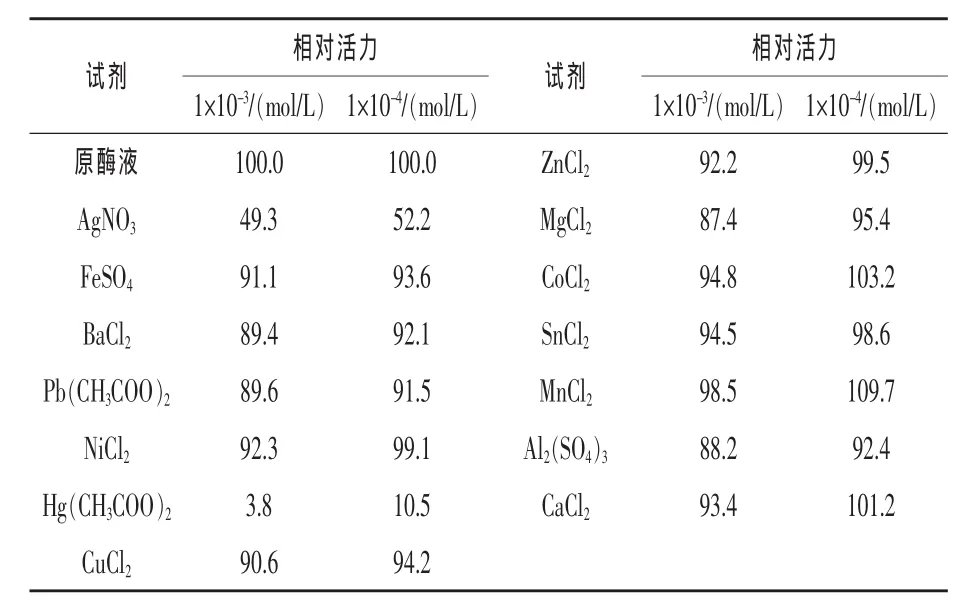
表2 金屬離子對酶活力的影響 %
2.4 豬消化液對酶活的影響 表3結果表明,酶經過胃液、腸液和二者連續的處理后,酶活力較對照組均顯著下降(P<0.05),但酶活力在胃液中最高,12 h達90.74%,24 h達86.87%,可能是胃液的pH最接近該酶最適pH范圍的緣故。在小腸液或胃液+小腸液中酶活下降較快,但經過12 h處理仍保持在70%以上。隨著時間延長各處理酶活均顯著降低(P<0.05)。由此證明α-半乳糖苷酶在動物胃腸道內仍能較穩定地發揮活性。
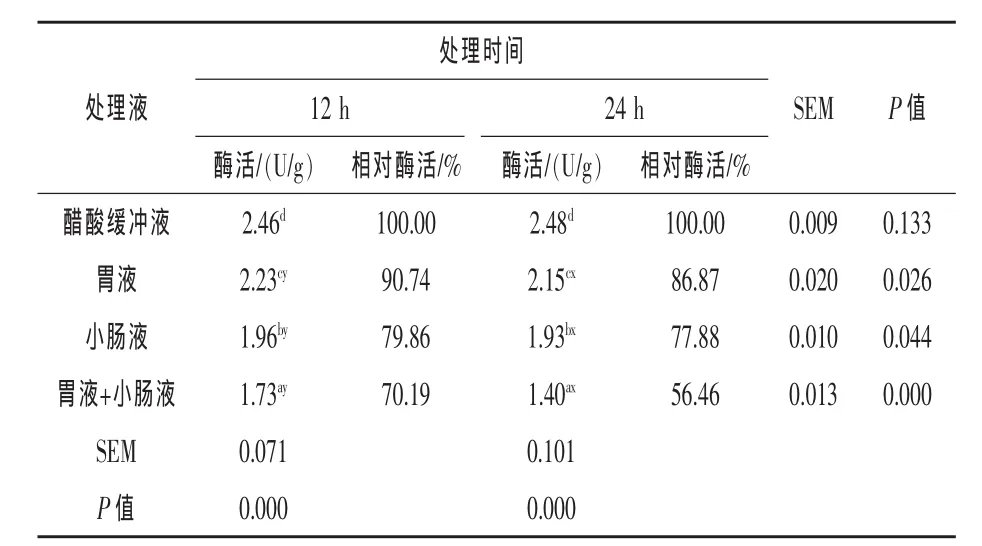
表3 豬消化液對α-半乳糖苷酶活力及穩定性的影響
2.5 儲存時間對酶活的影響 固態發酵的原酶樣,經過3、6個月和9個月的常規儲存后測定α-半乳糖苷酶活力,結果表明(見表4),在0~4℃冷藏9個月酶活力不受影響。在常溫15~30℃保存時,3月之內酶活不受影響,但隨后活力損失顯著(P<0.05),但到6個月時仍保留有原始活力的90.30%,到9個月時有80.58%,可見酶活在儲存條件下比較穩定,能夠適應生產實際中儲存的需要。
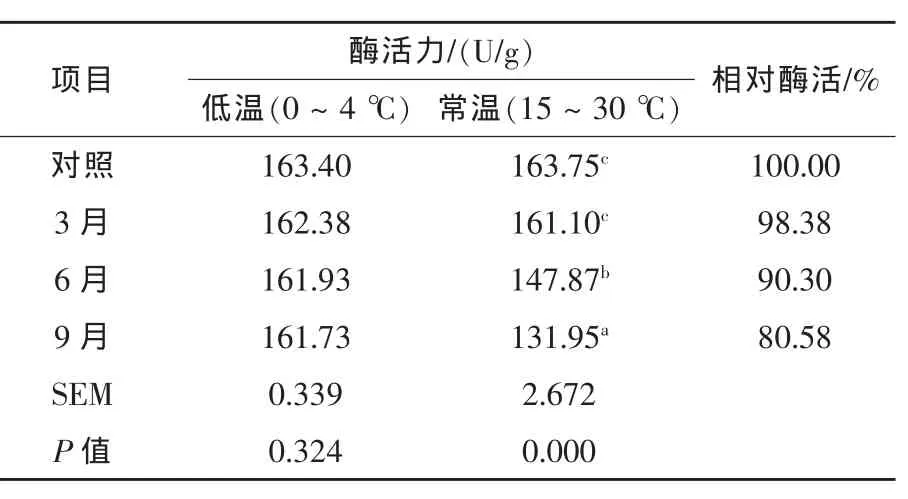
表4 儲存時間對酶活的影響
3 小結
通過對α-半乳糖苷酶粗酶制劑的理化性質研究表明,該酶的適宜pH在酸性范圍 (3.5~6.5),適宜的溫度在70℃以下,能夠耐受豬胃腸液12 h,貨架期長。
[1]沈同,王鏡巖.生物化學(上冊)[M].北京:高等教育出版社(第二版),1991.232~328.
[2]張麗英.大豆寡糖對斷奶仔豬抗營養作用及機理的研究:[博士學位論文][D].北京:中國農業大學,2000.
[3]Leske,K L,Coon C N.Hydrogen gas production of broiler chicks in response to soybean meal and α -galactoside free,ethanol-extracted soybean meal[J].Poult Sci,1999,78:1313 ~ 1316.
[4]Wang,C L,Li D F,Lu W Q,et al.Influence of cultivating conditions on the α-galactosidase biosynthesis from a novel strain of Penicillium sp.in SSF[J].Lett App Microb,2004,39:369 ~ 375.

