桑色素與溶菌酶相互作用的熒光光譜法研究
黃 威,田 皎,趙 楠,張國文,2,*
(1.南昌大學生命科學與食品工程學院,江西南昌330031;2.南昌大學食品科學與技術國家重點實驗室,江西南昌330047)
桑色素與溶菌酶相互作用的熒光光譜法研究
黃 威1,田 皎1,趙 楠1,張國文1,2,*
(1.南昌大學生命科學與食品工程學院,江西南昌330031;2.南昌大學食品科學與技術國家重點實驗室,江西南昌330047)
在生理酸度(pH7.4)條件下,應用熒光光譜法研究了桑色素與溶菌酶(LYS)相互作用的光譜特性。研究發現,桑色素對溶菌酶的內源熒光產生強烈的猝滅作用,其熒光機理為靜態與動態并存的復合猝滅方式。求出了不同溫度下桑色素與溶菌酶作用的結合常數和結合位點數。由Van’t Hoff方程式計算了桑色素與溶菌酶反應的熱力學參數:焓變(ΔH)和熵變(ΔS)值分別為-30.26kJ/mol和26.76(J/mol·K),表明桑色素與溶菌酶之間的作用力以靜電引力為主。根據F?rster非輻射能量轉移理論,求出了桑色素與溶菌酶色氨酸殘基之間的結合距離為4.05nm。同步熒光光譜顯示,桑色素使得溶菌酶的構象發生了變化。
桑色素,溶菌酶,熒光光譜,熱力學參數
溶菌酶(lysozyme,縮寫LYS)是一種廣泛存在于生物體內的小分子堿性蛋白,由129個氨基酸殘基組成,包含6個色氨酸(Trp)和3個酪氨酸(Tyr)殘基,其中Trp-62和Trp-108是最主要的熒光團。溶菌酶是生物體內不可缺少的非特異性體液免疫因子,具有抗菌、消炎、抗病毒等諸多的生理功能[1]。溶菌酶能與許多藥物分子結合,從而協同發揮藥效。近年來,對藥物與溶菌酶相互作用的研究相當活躍[2-4]。桑色素(Morin,結構式如圖1)是從黃桑木、桑橙樹和許多中草藥中提取的一種黃酮類化合物,具有抗氧化、抗炎和抗腫瘤等藥理活性[5]。本文采用熒光光譜法研究了生理酸度(pH 7.4)條件下桑色素與溶菌酶的相互作用,測定其動態猝滅常數、結合常數、結合位點數和給體-受體間結合距離,探討了兩者結合主要驅動力的類型和桑色素對溶菌酶構象的影響。該研究為從分子水平上了解桑色素與溶菌酶相互作用機制提供重要信息,為進一步尋求相關新藥的發現、食用功能因子的開發等奠定了實驗基礎。
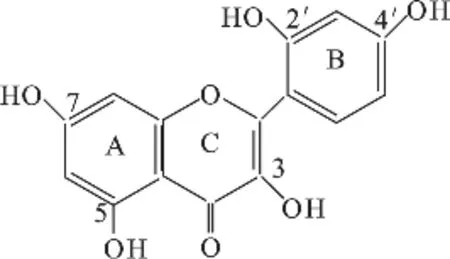
圖1 桑色素的結構式
1 材料與方法
1.1 材料與儀器
桑色素標準品 用無水甲醇配制成3.004× 10-3mol/L溶液,使用時根據所需進行稀釋,中國藥品生物制品檢定所產品;溶菌酶 用0.05mol/L的NaCl溶液配制成7.86×10-5mol/L的貯備液,溶液保存于4℃的冰箱中備用,北京華美生物工程有限公司產品;pH7.4的 Tris-HCl緩沖溶液;0.10mol/L的NaCl;其他試劑 均為分析純;實驗用水 均為二次蒸餾水。
F-4500型熒光光度計 日本日立公司;UV-2450紫外-可見分光光度計 日本島津公司;pHS-3C型酸度計 上海雷磁儀器廠。
1.2 實驗方法
在10mL的比色管中,依次加入2.0mL pH7.4的Tris-HCl緩沖溶液,2.0mL 0.10mol/L的NaCl溶液,128μL 7.857×10-5mol/L的溶菌酶溶液,以二次蒸餾水定容至10mL。準確移取3.0mL該溶液于石英熒光池中,用可調式移液器逐次加入一定體積的桑色素溶液(桑色素的累加體積為90μL),混合均勻并靜置5min。在熒光光度計上記錄熒光發射光譜和同步熒光光譜。在熒光猝滅實驗中,λex=280nm;同步熒光掃描時取Δλ=15nm和60nm(熒光激發和發射狹縫均為5nm)。
2 結果與討論
2.1 桑色素對溶菌酶熒光的猝滅作用
在溶菌酶結構中,Trp-62和Trp-108是最主要的熒光團,它們位于溶菌酶的底部結合區。當藥物分子與溶菌酶發生作用,主要體現在Trp-62殘基熒光強度的變化[2]。圖2可以看出,固定溶菌酶的濃度,隨著溶液中桑色素濃度的不斷增加,溶菌酶在344nm左右的內源熒光被逐漸猝滅,并產生一定的藍移,同時桑色素在510nm附近的熒光強度逐漸增加,而且在449nm處有一個等發射點,這些現象表明,桑色素與溶菌酶之間發生相互作用,使氨基酸殘基所處微環境發生變化[6]。
2.2 熒光猝滅機理
一般情況下,產生熒光猝滅作用的原因主要有動態猝滅和靜態猝滅[6]。為了進一步闡明熒光猝滅機理,用Stern-Volmer方程對熒光實驗數據進行分析:F0/F=1+Kqτ0[Q]=1+Ksv[Q],式中F0和F分別為未加入和加入桑色素時溶菌酶的熒光強度,Kq為雙分子猝滅過程速率常數,Ksv為動態猝滅常數,τ0為沒有猝滅劑存在下熒光分子平均壽命,生物大分子熒光壽命約10-8s[6],[Q]為桑色素的濃度。作出F0/F-[Q]關系圖(見圖3),并計算出不同溫度下的動態猝滅常數(見表1)。若桑色素對溶菌酶的熒光猝滅機理為單一的動態或靜態猝滅方式,F0/F與[Q]間應存在線性關系。由圖3可見,猝滅曲線并未表現出線性關系,Ksv隨溫度升高有降低趨勢,表明桑色素對溶菌酶的熒光猝滅機理并非單一的靜態猝滅,而是靜態和動態猝滅并存的復合猝滅機理[6-7]。

圖2 不同濃度的桑色素對溶菌酶熒光光譜的影響
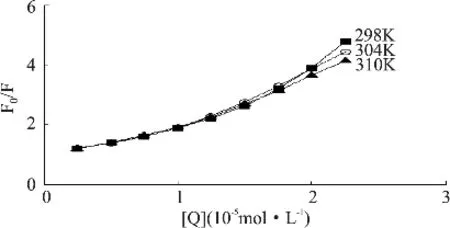
圖3 桑色素對溶菌酶熒光猝滅的Stern-Volmer圖
2.3 結合常數和結合位點數
有機小分子與生物大分子任一位點發生作用時,體系中發生作用的小分子與未作用的小分子之間處于一種平衡狀態,這種平衡關系可以用以下方程描述[8]:lg[(F0-F)/F]=lgK+nlg[Q],式中K為結合常數,n為結合位點數。以lg[(F0-F)/F]對lg[Q]進行一元線性回歸,由直線的截距和斜率求得桑色素與溶菌酶作用的結合常數K和結合位點數n,結果列于表1中。結合常數達106量級,表明桑色素與溶菌酶存在較強的結合,溫度升高使結合能力稍微減弱,溶菌酶與桑色素間有一個結合位點。
2.4 作用力類型
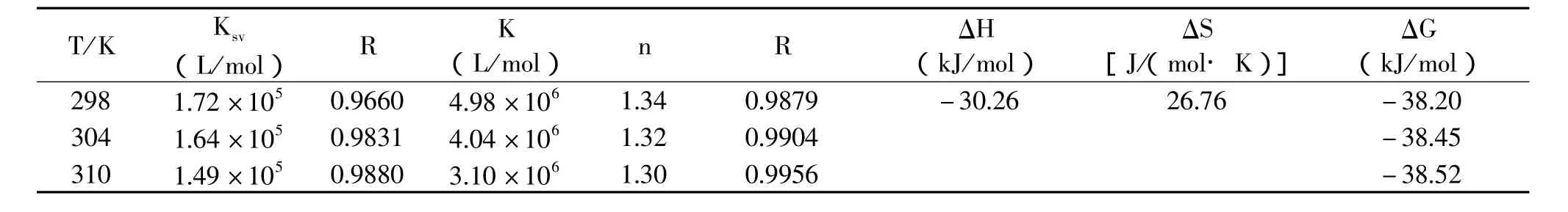
表1 不同溫度下桑色素與溶菌酶作用的猝滅常數Ksv、結合常數K、結合位點數n及熱力學參數
有機小分子和蛋白質等生物大分子之間的相互作用力主要有疏水作用力、氫鍵、范德華力和靜電引力等。當溫度變化范圍不大時,作用過程的焓變隨溫度的改變可忽略不計,根據熱力學參數之間的關系式lgK=-ΔH/2.303RT+ΔS/2.303R(式中K為對應溫度下的結合常數,R為氣體常數),以lg K對1/T進行一元線性回歸,由直線的斜率和截距計算出反應的焓變(△H)和熵變(△S),再由ΔG=ΔH-TΔS計算出結合反應的自由能變(ΔG),結果見表1。Ross[9]總結出小分子與生物大分子反應的熱力學參數與主要作用力類型的關系。即當ΔS>0,ΔH>0為典型的疏水作用力;ΔH<0,ΔS<0為氫鍵和范德華力;當ΔH<0,ΔS>0時,主要存在靜電相互作用。由表1可見,ΔG<0,H<0,△S>0,表明桑色素與溶菌酶的作用過程是一個熵增加、Gibbs自由能降低的自發過程,其作用力主要為靜電引力。
2.5 構象研究
同步熒光光譜可以提供熒光發色基團附近微環境的變化信息,同步熒光波長Δλ=15nm和60nm時所測得的同步熒光光譜分別為酪氨酸殘基和色氨酸殘基的光譜特征[10],根據酪氨酸和色氨酸殘基同步熒光光譜的變化可得出其微環境的變化,進而可推斷蛋白質構象的變化。研究發現,當 Δλ分別為15nm和60nm時,增加桑色素的濃度,酪氨酸殘基的最大發射波長發生了輕微的紅移(移動了2.4nm),如圖4A所示,說明桑色素與溶菌酶的結合使得酪氨酸殘基附近微環境的極性增大、疏水性降低[11],而色氨酸殘基的最大發射波長沒有明顯的移動(圖4B),表明在結合過程中色氨酸殘基附近的微環境沒有明顯的改變。
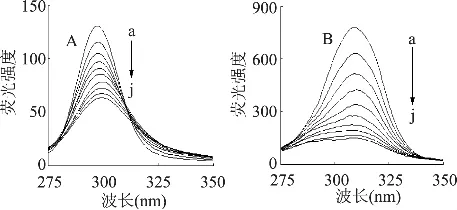
注:cLYS=1.00×10-6mol/L;cmorin=0,0.25,0.50,0.75,1.00,1.25,1.50,1.75,2.00,2.25×10-5mol/L for curves a→j;pH=7.4,T=298K;(A)Δλ=15nm;(B)Δλ=60nm。
2.6 結合距離
由F?rster非輻射能量轉移理論[12]和能量轉移效率E與供能體-受能體間距離r以及臨界能量轉移距離R0的關系式:E=1-F/F0=R60(/R60+r6);R60= 8.8×10-25K2n-4ΦDJ;J=∑F(λ)ε(λ)λ4Δλ/∑F(λ)Δλ。式中R0為E=50%時的臨界距離;K2為偶極空間取向因子,可取供能體-受能體各向隨機分布的平均值2/3;n為介質的折射指數,一般取水和有機物折射指數的平均值1.336;ΦD為供能體的熒光量子產率,通常取0.15[13];F(λ)為熒光供能體在波長λ處的熒光強度,ε(λ)為受能體在波長λ處的摩爾吸光系數,J是供能體的熒光發射光譜和受能體的吸收光譜之間的光譜重疊積分。圖5為溶菌酶的熒光光譜與桑色素的紫外吸收光譜的重疊圖譜。根據上述公式分別求得光譜的重疊積分 J=2.225×10-14cm3· L/mol,R0=2.92nm,E=0.122以及桑色素在溶菌酶中的結合部位距62位色氨酸殘基間的距離r =4.05nm。

圖5 溶菌酶熒光光譜(a)和桑色素吸收光譜(b)的重疊圖譜
3 結論
靜態與動態并存的復合猝滅方式是桑色素對溶菌酶的內源熒光產生猝滅作用的主要原因;桑色素與溶菌酶之間存在較強的結合作用,且有一個結合位點,桑色素在溶菌酶中的結合部位距62位色氨酸殘基間的距離為4.05nm,靜電引力是結合作用的主要驅動力;桑色素與溶菌酶結合使得酪氨酸殘基附近的微環境發生了變化,進而導致溶菌酶構象的改變。
[1]朱奇,陳彥.溶菌酶及其應用[J].生物學通報,1998,33(10):9-10.
[2]Wang Z,Li D J,Jin J.Study on the interaction of puerarin with lysozyme by spectroscopic methods[J].Spectrochim,Acta Part A,2008,70:866-870.
[3]Li D J,Zhu J F,Jin J.Spectrophotometric studies on the interaction between nevadensin and lysozyme[J].J Photoch Photobio A:Chem,2007,189:114-120.
[4]張國文,陳秀霞,郭金保,等.熒光法研究橙皮苷、淫羊藿苷與溶菌酶的相互作用[J].光譜學與光譜分析,2009,29(1):184-187.
[5]Fang S H,Hou Y C,Chang W C,et al.Morin sulfates/ glucuronides exertanti-inflammatory activity on activated macrophages and decreased the incidence of septic shock[J].Life Science,2003,74:743-756.
[6]陳國珍,黃賢智,許金鉤,等.熒光分析法[M].第二版.北京:科學出版社,1990.
[7]Lakowicz J R.Principles of Fluorescence Spectroscopy,second ed[M].Plenum Press,New York,1999:237-265.
[8]Hu Y J,Liu Y,Wang J B,et al.Study of the interaction between monoammonium glycyrrhizinate and bovine serum albumin[J].J Pharm Biomed Anal,2004,36(4):915-919.
[9]Ross D P,Subramanian S.Thermodynamics of protein association reaction:contributing to stability[J].Biochemistry, 1981,20:3096-3099.
[10]Lakowicz J R,Weber G.Quenching of protein fluorescence by oxygen,detection of structural fluctuations in proteins on the nanosecond time scale[J].Biochemistry,1973,12:4171-4179.
[11]Wang Y Q,Zhang H M,Zhang G C,et al.Interaction of the flavonoid hesperidin with bovine serum albumin:A fluorescence quenching study[J].J Lumin,2007,126:211-218.
[12]楊頻,高飛,馬貴斌.生物無機化學導論[M].西安:西安交通大學出版社,1991.
[13]Hu Y J,Liu Y,Shen X S,et al.Studies on the interaction between 1-hexylcarbamoyl-5-fluorouracil and bovine serum albumin[J].J Mol Struct,2005,738:143-147.
Study on the interaction of morin with lysozyme by fluorescence spectroscopy
HUANG Wei1,TIAN Jiao1,ZHAO Nan1,ZHANG Guo-wen1,2,*
(1.College of Life Science and Food Engineering,Nanchang University,Nanchang 330031,China;2.State Key Laboratory of Food Science and Technology,Nanchang University,Nanchang 330047,China)
The spectroscopic character between morin and lysozyme(LYS)was studied using fluorescence spectroscopy under the simulative physiological condition(pH7.4).lt was observed that there was a strong fluorescence quenching reaction of morin to lysozyme,the quenching mechanism was suggested as both static and dynamic quenching for morin-LYS system.The binding constants K and number of binding sites n of morin with lysozyme were obtained by fluorescence quenching method.The thermodynamic parameters of the interaction between morin and lysozyme were measured according to the Van’t Hoff equation.The enthalpy change(△H)and the entropy change(△S)were calculated to be-30.26kJ·mol-1,26.76J·mol-1·K-1respectively,which indicated that the interaction of morin with lysozyme was driven mainly by electrostatic interactions.The binding locality was an area 4.05nm away from tryptophan residue in lysozyme based on F?rster nonradiation energy transfer mechanism.The results of synchronous fluorescence spectra showed that the binding of morin to lysozyme induced conformational changes in lysozyme.
morin;lysozyme;fluorescence spectroscopy;thermodynamic parameters
TS201.1
A
1002-0306(2010)11-0088-04
2009-11-04 *通訊聯系人
黃威(1987-),男,本科生,研究方向:食品化學。
國家大學生創新性實驗計劃項目(081040308);江西省自然科學基金項目(2007GZH1924)。

