Conophylline——新型的骨髓干細胞植物誘導劑*
劉 俏 張 楠 浙江大學醫學院附屬邵逸夫醫院 杭州 310000
隨著移植醫學的發展,肝、腎及骨髓等的移植都獲得了相當大的成功,有人提出進行胰腺或者胰島的移植從而根治糖尿病的設想。經過大量的努力,目前這一方面的工作已經取得了一定的進展。2000年加拿大的 Edmonton研究小組就連續取得了 7例 1型糖尿病患者胰島移植的成功[1]。但是,供體的來源不足和排斥反應這兩大問題大大限制了胰腺和胰島移植的發展。因此,為了糖尿病治療的發展,需要尋找一種更好的胰島素分泌細胞的來源。
1 骨髓干細胞
目前,干細胞研究方興未艾。干細胞具有自我更新和多向分化的潛能,因而成為許多細胞治療和基因治療的重點研究對象,比如骨髓中造血干細胞的移植已經在臨床上用于白血病等血液系統疾病治療多年。而骨髓組織中除了造血干細胞外,還含有另外一種間充質干細胞。間充質干細胞不僅可以分化成為成骨細胞、成軟骨細胞、脂肪細胞、成肌細胞等間充質細胞譜系,在一定條件下,它還具有向非間充質細胞譜系如神經細胞分化的多潛能特性。因此,將骨髓間充質干細胞誘導分化為神經細胞用于神經系統疾病的治療,誘導分化為心肌細胞用于心肌梗死的搶救,誘導分化為成骨細胞促進骨缺損的修復,誘導分化為肝細胞進行自體干細胞移植從而挽救肝硬化患者的生命等,這些方面的研究都正在火熱的進行之中。那間充質細胞能否分化成胰島素分泌細胞呢?目前,已經有一些相關的研究,并取得了肯定的成果[2~4]。因此,可以設想如果能將從自體骨髓提取出的干細胞誘導分化成胰島素分泌細胞,再移植入患者體內,不僅解決了供體來源的問題,還完全不會有排斥反應的發生,這成為許多糖尿病患者的新希望。
2 Conophylline誘導骨髓干細胞體外分化成胰島素分泌細胞
Conophylline是從熱帶植物小葉狗牙花中提取出來的一種長春花堿類的小分子物質。研究顯示,在鼠的胰腺退化器官的培養中,Conophylline可抑制腺泡結構的形成以及增加胰島素陽性細胞的數量,并且顯著增加胰島素mRNA的表達和胰十二指腸同源異型盒-1陽性細胞的數量[5]。體內實驗還表明,當給予糖尿病模型的新生小鼠 Conophylline,它們的血糖水平和葡萄糖耐量都會顯著改善[5]。另外,有研究顯示,Conophylline具有誘導胰腺前體細胞模型—AR 42J細胞體外分化成胰島素分泌細胞的能力,并且和 activin A相比,Conophylline不會誘導細胞凋亡,被認為是一種神奇的植物誘導劑[6]。
那么,究竟為什么Conophylline具有這樣神奇的誘導活性呢?有研究者從馬來群島的一種名叫 T.divaricata的植物中分離出三種與 Conophylline結構類似的長春花堿類物質—Conophyllidine、Conofoline和 Conophyllinine,見圖 1。 實驗顯示,Conophyllidine具有和 Conophylline相似的引起胰腺腺泡癌細胞 AR 42J發生類似神經細胞的形態學改變的活性,Conophyllinine的這種活性要弱一點,而 Conofoline則完全沒有這種活性[7]。引起 AR 42J細胞發生類似神經細胞的形態學改變的 Conophylline最終誘導這些細胞分化成胰島素分泌細胞,從而證明二聚體aspidosperma中心的二氫呋喃結構是其分化誘導活性所必需的[7]。
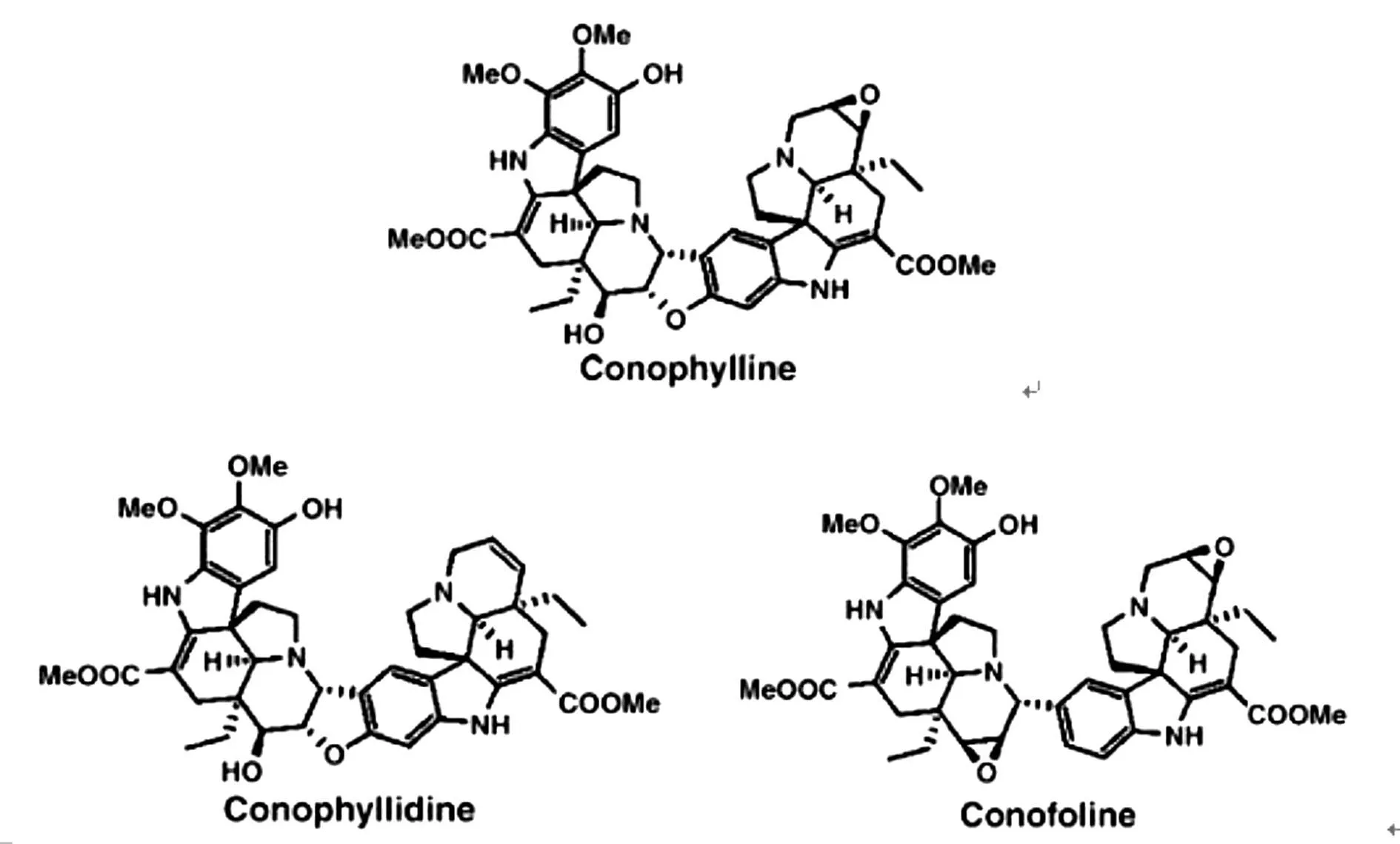
圖1 Conophylline、Conophyllidine和 Conofolline的結構
2008 年的內分泌學雜志報道使用 Conophylline和betacellulin-delta4體外成功誘導骨髓間充質干細胞定向分化成胰島素分泌細胞的實驗。該實驗將小鼠骨髓來源的間充質干細胞放在含有 10%胎牛血清和25mM葡萄糖的培養基中,當加入 activin A和 batacelluin作為誘導劑,14天后有胰島素產生;而換用 Conophylline和 betacellulin-delta4作為誘導劑,5~7天之后胰島素的mRNA就能被探測到,并且這些細胞對高濃度的葡萄糖起反應而分泌成熟的胰島素[8]。當這些細胞被移植到經鏈脲酶素誘導的小鼠糖尿病模型上,小鼠的血糖濃度大幅度降低,且這種效應至少持續 4周[8]。這個實驗證明 Conophylline確實具有誘導骨髓間充質干細胞體外分化成胰島素分泌細胞的能力。
關于 Conophylline究竟通過怎樣的途徑誘導胰島素分泌細胞的分化的,至今仍沒有一個完全明確的答案。研究表明,TAK 1-MKK 3-p38MAPK途徑的信號轉導可能在 activin A誘導胰腺前體細胞產生 Neurogenin3(ngn3)基因的表達中起重要作用[9]。ngn3不僅是胰腺內分泌前體細胞的標志,當將小鼠體內的 ngn3靶向斷裂后,這些小鼠就不能產生胰腺內分泌細胞,也不能產生大多數內分泌細胞分化所需的基本轉錄因子[10];相反,胰芽細胞中 ngn3的過度表達則會促進其向內分泌細胞分化[11,12]。說明 ngn3是胰腺內分泌細胞分化中起決定性作用的一個轉錄因子。實驗證明,轉化生長因子 β相關激酶 1(TAK 1)或絲裂原活化蛋白激酶激酶 3(MKK3)的顯性負性突變的過度表達,或者是 p38 MAPK抑制劑SB203580的使用都會抑制 activin A和肝細胞生長因子(HGF)誘導的 ngn3的表達[9]。另外,該實驗還表明,activin A和HGF通過TAK1-MKK 3-p38MAPK信號轉導途徑作用于ngn3基因的啟動因子-402~-327堿基對上,從而減輕其對轉錄的抑制,并最終激活了 ngn3的表達和內分泌細胞的分化[9]。而 Conophylline具有和 activin A類似的激活 p38絲裂原活化蛋白激酶(MAPK)的特性,并且p38MAPK特異性的抑制劑 SB203580會完全抑制 Conophylline誘導的類似神經細胞的形態學改變和胰島素的產生[8]。所以,p 38MAKP的激活是 Conophylline誘導胰島素分泌細胞產生的關鍵步驟。其它研究也表明,Conophylline可能是通過和 activin A類似的作用方式誘導胰島素分泌細胞的分化的[5]。因此,推測Conophylline可能也是主要通過TAK 1-MKK 3-p38MAPK這個信號轉導途徑,作用于 ngn3基因的啟動因子上,從而激活ngn3的表達和內分泌細胞的分化的。
3 Conophylline應用前景
目前,除了誘導分化胰島素分泌細胞外,關于Conophylline的一些其它方面的研究也正在進行之中,尤其在腫瘤方面它也顯示出相當的優勢。已有實驗表明,Conophylline具有抑制子宮內膜癌細胞的黏附和侵襲的作用[13],也有研究顯示,Conophylline具有抑制表達K-ras基因腫瘤的生長的功能[14],另外,它還具有下調人類T細胞白血病細胞的腫瘤壞死因子 α受體的作用[15]。總之,Conophylline是一種具有廣闊應用前景的長春花堿類的小分子物質,其誘導骨髓干細胞體外分化成胰島素分泌細胞的能力為糖尿病的治療開辟了新的天地。關于 Conophylline的作用機制以及實際臨床應用等方面的問題還需要廣大科研和醫學工作者繼續努力解決。希望不久的將來,能將從患者自體骨髓提取出的干細胞用于糖尿病的治療,從而為廣大糖尿病患者帶來福音。
[1] Shapiro AM,Lakey JR,Ryan EA,et al.Islet transplantation in seven patientswith type 1diabetesmellitus using a glucocorticoid-.free immunosuppressiveregimen[J].The New England journalofmedcine,2000,343(4):230-238.
[2] Chen Li Bo,Jiang Xiao Bing,Yang Lian.Differentiation of rat marrow mesenchymal cells into pancreatic islet beta cells[J].World Journal of Gastroenterology,2004,10(20):3016-3020.
[3] Lee RH,Seo MJ,Reger RL,etal.Multipotent stromal cells from humanmarrow home toand promote repair of pancreatic islets and renalglomeruli in diabetic NOD/SCIDmice[J].Proceedings of the national academy of sciences of the United States of America,2006,103(46):17438-17443.
[4] Ianus A,Holz GG,Theise ND,et al.In vivo derivation of glucose-.competent pancreatic endocrine cells from bone marrow withoutevidenceof cell fusion[J].Journal of clinical investigation,2003,111(6):843-850.
[5] Takeki Ogata,Lei Li,Satoko Yamada,et al.Promotion of beta cell differentiation by conophylline in fetal and neonatal rat pancreas[J].Diabetes,2004,53(10):2596-2602.
[6] Kojima I,Umezawa K.Conophylline:A novel differentiation inducer for pancreaticβcells[J].International journal of biochem istry&cell biology,2006,38(5-6):923-930.
[7] Umezawa K,HirokiA,KawakamiM,etal.Induction of insulin production in rat pancreatic acinar carcinoma cells by conophylline[J].Biomedicine&Pharmacotherapy,2003,57(8):341-350.
[8] Hisanaga E,Park KY,Yamada S,et al.A simp le method to induce differentiation ofmurine bonemarrow mesenchymal cells to insulin-.producing cells using conophylline and betacellulin-delta4[J].Endocrine Journal,2008,55(3):535-543.
[9] Ogihara T,Watada H,Kanno R,et al.P38MAPK Is Involved in Activin A-.and Hepatocyte Grow th Factor-.mediated Expression of Pro-.endocrine Gene Neurogenin 3 in AR 42J-B13 Cells[J].Journal of biological chem istry,2003,278(24):21693-21700.
[10]GradwohlG,Dierich A,LeMeur M,et al.Neurogenin3 is required for the development of the four endocrine cell lineages of the pancreas[J].Proceedings of the national academy of sciences of the United States of America,2000,97(4):1607-1611.
[11]ApelqvistA,Li H,Sommer L,et al.Notch signalling controls pancreatic cell differentiation[J].Nature,1999,400(6747):877-881.
[12]Jensen J,Heller RS,Funder Nielsen T,et al.Independent developmentof pancreatic alpha-and beta-cells from neurogenin3-expressing precursors:a role for the notch pathway in repression of p remature differentiation[J].Diabetes,2000,49(2):163-176.
[13]Irie T,Kubushiro K,Suzuki K,et al.Inhibition of attachment and chemotactic invasion of uterine endometrial cancer cells by a new vinca alkaloid,conophylline[J].Anticancer Research,1999,19(4B):3061-3066.
[14]Umezawa K,Taniguchi T,Toi M,etal.Growth inhibition of K-.ras-.expressing tumours by anew vinca alkaloid,conophylline,in nudem ice[J].Drugs under experimental and clinical research,1996,22(2):35-40.
[15]Gohda J,Inoue J,Umezawa K.Down-.regulation of TNF-alpha receptors by conophylline in human T-cell leukemia cells[J].International Journal of Oncology,2003,23(5):1373-1379.

