自體干細胞移植治療糖尿病足胰島功能變化研究
姚秀宇,姚秀松,王 巍,劉艷杰
糖尿病的發病率達10%以上,由此引發的糖尿病并發癥高達30% ~40%[1],給患者及社會帶來巨大的經濟負擔。骨髓干細胞在一定條件下可以定向分化為機體內的功能細胞,形成多種類型的組織和器官以代替損傷和壞死的組織,從而達到治療疾病的目的[2-3]。目前骨髓間充質干細胞已在體外成功誘導分化為胰島β細胞[4],許多學者已經找到了體內胰島β細胞分化的相關因素[5]。本研究采用骨髓間充質干細胞治療糖尿病足,同時發現胰島β細胞的功能得到恢復,通過觀察在不同體內環境下,骨髓間充質干細胞向胰島β細胞轉化的程度是否不同,來尋找體內促使骨髓間充質干細胞向胰島β細胞轉化的相關因素,為徹底治愈糖尿病開辟一條新的途徑。
1 資料與方法
1.1 一般資料 選取2005年5月—2010年11月選擇采用骨髓干細胞移植治療的糖尿病足患者125例為研究對象,診斷均符合1999年世界衛生組織 (WHO)制定的糖尿病診斷標準。患者均有足部和 (或)下肢發涼、麻木、疼痛、間歇性跛行;Fontaine分期Ⅱ期80例、Ⅲ期32例、Ⅳ期13例。需要用止痛劑治療13例。以神經病變為主50例,血管病變為主30例,混合型45例。心肌缺血125例均存在,血脂異常100例,腦血栓12例。彩色多普勒檢查顯示各段動脈不同程度的狹窄或閉塞。術前采用胰島素控制血糖,根據血糖控制情況分為兩組;1組為全天血糖完全達標 (三餐前血糖<5.6 mmol/L,餐后2 h血糖<7.8 mmol/L)63例,其中男40例,女23例;年齡50~70歲,平均年齡62歲。2組為全天血糖均高于正常(三餐前血糖<9~10 mmol/L,餐后2 h血糖<12~16 mmol/L)62例,其中男39例,女23例;年齡50~69歲,平均年齡61歲。
1.2 方法 術前3 d用重組人粒細胞集落刺激因子 (GCSF)300 U/d肌肉注射,作骨髓干細胞動員,當外周血白細胞達 (25~30) ×109/L時,采集骨髓180~200 ml。在手術室絕對無菌的條件下,采用硬膜外麻醉,麻醉生效后,取雙髂后上棘后為穿刺點,常規無菌消毒,鋪無菌手術孔巾,用16號骨穿針多部位抽取骨髓液200 ml。送入我科干細胞分離實驗室。分離后配成一定的濃度,雙下肢多點深部肌肉注射、一部分股動脈內回輸。骨髓單個細胞分離方法:先將骨髓抗凝血用低溫離心機,溫度22℃、1 500 r/min,離心5 min,吸取少許上浮血漿,將單個核細胞層緩慢加入0.077的淋巴細胞分離液中,放入離心機中,1 200 r/min,離心20 min,取出后分為5層,吸取中間層,用0.9%氯化鈉溶液洗滌2次,配成一定濃度的懸液,回輸。留2 ml干細胞懸液,送學院中心實驗室,用流式細胞儀檢測CD34含量,以推算骨髓干細胞的數量。
1.3 評定方法 觀察患肢的麻木、疼痛感、冷感、間歇性跛行是否好轉,同時檢測術后3 d、1周、2周、1個月、3個月的餐前及餐后2 h血糖、C-肽值,同時觀察外用胰島素用量的變化。觀察有無不良反應發生。
1.4 統計學方法 采用SPSS統計軟件進行數據分析,計量資料采用 (x-±s)表示,兩組間比較采用t檢驗,以P<0.05為差異有統計學意義。
2 結果
2.1 125例患者均自訴下肢麻木、疼痛感、冷感、間歇性跛行癥狀明顯好轉。
2.2 手術前后兩組血糖變化比較 術前1組患者餐前和餐后2 h血糖較2組均明顯降低,差異有統計學意義 (P<0.05);術后3 d、1周、2周、1個月、3個月1組與2組患者餐前及餐后2 h血糖比較,差異均無統計學意義 (P>0.05,見表1)。
2.3 手術前后兩組胰島素用量變化比較 術后3 d兩組患者胰島素用量較術前均明顯降低,差異有統計學意義 (P<0.05)。術前1組患者胰島素用量較2組無明顯降低,差異無統計學意義 (P>0.05);術后3 d、1周、2周、1個月、3個月2組患者胰島素用量較1組均明顯降低,差異有統計學意義(P<0.05,見表2)。
2.4 手術前后兩組血C-肽水平變化比較 兩組患者術前、術后3 d、1周、2周、1個月、3個月餐前和餐后2 h血C-肽水平比較,差異均無統計學意義 (P>0.05,見表3)。2.5不良反應 兩組患者均無嚴重不良反應發生。
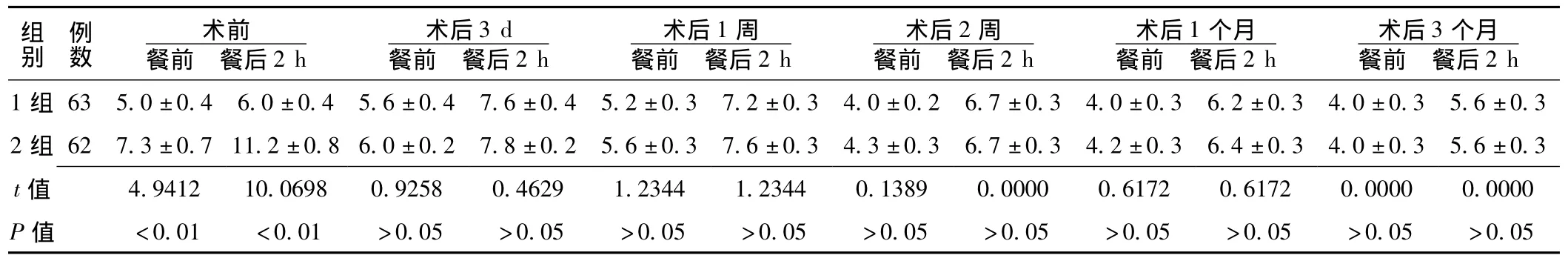
表1 手術前后兩組血糖變化比較 (x-±s,mmol/L)Table1 Comparison of change contrast of blood sugar before and after operation in two groups

表3 手術前后兩組血C-肽水平變化比較 (x-±s,μg/L)Table 3 Comparison of change contrast of blood C-peptide levels in two groups before and after surgery

表2 手術前后兩組胰島素用量變化比較 (x-±s,U/d)Table 2 Comparison of change contrast of the insulin dose in two groups before and after surgery
3 討論
目前在損傷的內分泌胰腺的治療研究中,骨髓來源的干細胞、胚胎干細胞、器官來源的干細胞均有作用[6]。最重要的是如何誘導出具有完全功能的胰島樣細胞,即具有雙相胰島素釋放功能,可以動態模擬生理狀態下的胰島素分泌。目前相關的研究證實,葡萄糖對胰島β細胞的再生有雙重作用[7],血糖略高于正常時可以促進干細胞分化為胰島β細胞,血糖極高時促使胰島本身的β細胞凋亡[8]。活化的絲-蘇氨酸激酶(PBK)使葡萄糖轉運子定位于β細胞表面,葡萄糖通過轉運子進入細胞內,經酵解使ATP/ADP及磷酸鹽濃度升高,進而ATP依賴的K通道關閉,質膜去極化,電壓依賴式L型鈣通道激活,胞內Ca2+濃度升高促進胰島素分泌。但較長時間的高濃度葡萄糖,又可通過調整不同的基因程序使β細胞產生關鍵表型的改變而致β細胞功能缺陷、去分化及最終致β細胞死亡。對于未分化細胞,葡萄糖可充當有絲分裂劑,有實驗證實,β細胞加入5%~25%葡萄糖,隨濃度上升分裂增殖加快。文獻分析可能由于正常的葡萄糖濃度可使葡萄糖調節基因正常化,恢復葡萄糖調節敏感性,有利于β細胞表型正常化的維持,高血糖在原始細胞階段可誘導干細胞向胰島β細胞分化及胰島素分泌[9]。本研究結果顯示,血糖略高于正常的患者,術后胰島素用量明顯減少,血糖完全正常組胰島素用量減少不明顯,兩組有顯著性差異。兩組術后血糖變化不大,考慮與兩組術前血糖控制差別很小有關,術后兩組血糖均控制在正常范圍,但胰島素用量明顯不同。高糖毒性解除后,胰島β細胞的功能都應有所恢復,術前血糖略高組胰島素用量明顯減少,說明干細胞部分轉化為胰島β細胞。血C-肽值術后兩組均有上升,但無顯著性差異,可能是由于本研究選擇的兩組患者術前均有部份殘存的胰島β細胞。術后兩組餐前、餐后血糖均在參考范圍,是造成術后血C-肽沒有顯著性差異的主要原因。但胰島素用量不同,說明了胰島β細胞恢復的程度不同。高葡萄糖可以誘導干細胞定向分化為胰島β細胞,但對自身的胰島β細胞又有促凋亡的作用,本研究認為最好將血糖控制在略高于正常的水平,有利于干細胞的分化,同時也有利于自身胰島β細胞的修復,對自身干細胞的作用可能是自體干細胞移植時,有部分造血干細胞及相關細胞因子對殘存β細胞有修復作用。研究顯示除葡萄糖外還有許多相關的因素可以促進β細胞分化,文獻報道有尼可酰胺、維甲酸、丁酸鹽類、shh抑制劑、活化素 (Activin)、胰高血糖素樣肽 (GLP)及其類似物等,均可誘導干細胞分化為胰島β細胞[10],這些因素是否能夠成為干細胞移植后體內轉化的相關因素,有待進一步研究。
綜上所述,干細胞來源廣泛,取材方便,在不同的理化環境下及細胞因子的誘導下具有多向分化的潛能,是組織工程、細胞移植及基因治療領域的理想靶細胞,但體外培養再回輸變數太大,如果可以找到體內誘導的方法,安全系數將明顯提高。
1 Docherty K.Growth and developmentof theisletsof Langerhans:implications for the treatment of diabetesmellitus[R].Cur Opin pharmacol,2001,1(2):641-650.
2 Shapiro J,Lakey JRT,Ryan EA,et al.Islet transplantation in seven patientswith type Idiabetesmellitus using a glucocorticoid-free immunosuppressive regimen [J].N Enegl JMed,2000,343(9):230-238.
3 Soria B,Roche E,Berana G,et al.Insulin-secreting cells derived from embryonic stem cells normalize glycemia in streptozotocin-induced diabeticmice[J].Diabetes,2000,49(7):1-6.
4 Han TL,Chiou SH,Chung LK,et al.Characterization of pancreatic stem cells derived from adulthuman pancreas duts by fluore-scence activated cell sorting,world [J].J Gastroenterol,2006,28(6):4529-4535.
5 Tang DQ,Li ZC,Brant R,etal.In vivo and in vitro characterization of insulin-priducing cell obtained from murine bonemarrow [J].Diabetes,2004,53(4):1721 -1732.
6 Voltarelli JC,CouriCE,Stracieri AB,etal.Autologous nonmyeloablative hematopoietic stem cell transplantation in newly diagnosed type Idiabetesmeliitus[J].JAMA,2007,297(14):1568-1576.
7 賈延頡,鐘樂,寧建輝,等.體外誘導大鼠骨髓間充質干細胞分化為胰島素分泌細胞[J].中國當代兒科雜,2003,5(3):393-397.
8 付漢東,張愛華,魯艷,等.自體骨髓干細胞移植治療糖尿病足患者血管內皮生長因子的表達及意義[J].中國全科醫學,2010,13(8):2554.
9 李艷華,白慈賢,謝超,等.成人骨髓間充質干細胞體外定向誘導分化為胰島樣細胞團的研究[J].自然科學進展,2003,13(6):593-597.
10 Moriscot C,Fraipont F,Richard MJ,et al.Human bonemarrow mesenchymal stem cells can express insulin and key transcription factors of the endocrine pancreas developmental pathway upon genetic and/ormicroenvironmental manipulation in vitro [J].Stem cells,2005,23(4):594-603.

