異基因造血干細胞移植治療重型再生障礙性貧血的療效研究
朱 玲,薛 梅,王志東,閆洪敏,劉 靜,丁 麗,王恒湘
重型再生障礙性貧血 (severe aplastic anemia,SAA)起病急,病情重,死亡率高,目前以免疫抑制劑及異基因造血干細胞治療為主。近十余年來,隨著新型免疫抑制劑問世及異基因造血干細胞移植 (allo-HSCT)包括單倍型HSCT的深入研究和廣泛開展,SAA的療效得到很大改觀。目前,對于年輕的SAA患者,人類白細胞抗原 (HLA)配型相合的allo-HSCT是優先選擇,但對于無全相合供者且藥物治療無效的嚴重患者,非親緣全相合、單倍型相合移植亦不失為選擇之一。我院2009年4月—2010年9月分別采用親緣HLA配型全相合、非親緣全相合、單倍型相合allo-HSCT方法,共治療8例SAA,取得較好療效,現報道如下。
1 資料與方法
1.1 一般資料 8例SAA患者中男5例,女3例,年齡3~52歲,中位年齡13.4歲;SAA-Ⅰ型5例,SAA-Ⅱ型3例;除1例 (例4)外,其余患者均接受過包括環孢素A(CSA)在內的多種免疫抑制劑治療;診斷至進行移植的時間為2~12個月,中位時間為5.1個月。8例中4例為父母提供的單倍型相合未去T細胞造血干細胞移植,1例為胞弟提供的全相合造血干細胞移植,3例為中華骨髓庫提供的非親緣全相合移植 (見表1)。SAA診斷及分型采用國際再生障礙性貧血研究組標準。
1.2 預處理方案 單倍型相合預處理方案:氟達拉濱 (FLU)30 mg·m-2·d-1(-10~ -7);環磷酰胺 (CTX)50 mg·kg-1·d-1(-6 ~ -3);馬利蘭 (BU)4 mg·kg-1·d-1(-10~ -9);抗 T淋巴細胞球蛋白 (ATG)20 mg·kg-1·d-1(-4~-1)或者抗胸腺細胞球蛋白5 mg·kg-1·d-1(-4~-1)。非親緣及親緣全相合移植預處理方案:FLU 30 mg·m-2·d-1(-10 ~ -5),CTX 60 mg·kg-1·d-1(-4 ~ -3),ATG 5 mg·kg-1·d-1(-4 ~ -1)。
1.3 造血干細胞移植類型 親緣及非親緣全相合采用外周血造血干細胞移植,供者經 rhG-CSF 5~10μg·kg-1·d-1動員,用藥5~6 d經血細胞分離機SC-3000PLUS分離外周血干細胞。單倍型相合移植采用外周血及骨髓造血干細胞混合移植。rhG -CSF(惠爾血)5 μg·kg-1·d-1動員,第 4 天采集骨髓干細胞,第5天采集外周血干細胞。8例患者輸注有核細胞數為 (7.57~17.38) ×108/kg,中位數為12.22×108/kg;CD34細胞數為 (1.64~12.49) ×106/kg,中位數為5.65×106/kg(見表2)。
1.4 移植物抗宿主病 (GVHD)預防 GVHD預防采用聯合免疫抑制劑方法。親緣全相合移植采用CSA+短程氨甲蝶呤(MTX),單倍型相合及非親緣全相合GVHD預防方案采用免疫抑制劑CSA、MTX、CD25單克隆抗體和霉酚酸酯 (MMF)。
1.5 支持治療 患者移植期間住空氣層流無菌病房,嚴格消毒隔離,進無菌飲食,適當腸外營養,回輸干細胞后第2天開始使用粒細胞集落刺激因子 (G-CSF),250μg/d,促進造血功能恢復,至中性粒細胞>2.0×109/L止。血紅蛋白低于80 g/L及血小板 (PLT)低于15×109/L時輸注已經濾白或20 GY照射過的紅細胞及PLT。常規應用腸道消毒藥物,使用無環鳥苷預防皰疹病毒感染,氟康唑預防真菌感染,靜脈滴注丙種球蛋白。體溫超過38℃者給予廣譜抗菌藥,3~5 d體溫不降,加用抗真菌藥物,每1~2周監測巨細胞病毒 (CMV),陽性者給予更昔洛韋或可耐治療。注意保護肝臟、心臟、腎臟功能,利尿,使24 h尿液保持在3 000 ml,5%碳酸氫鈉堿化尿液,使尿液pH值保持在7.5~8.0,使用美司鈉預防出血性膀胱炎。
1.6 療效評價 以外周血中性粒細胞絕對值 (ANC)≥0.5×109/L、PLT≥20×109/L為造血功能重建標準,以DNA短串聯重復序列多肽性分析 (STR-PCR)、性染色體分析、血型變化檢測等為植入依據,移植后1年內每3個月全面體檢1次,次年起每6個月體檢1次。隨訪至2011年3月。

表1 8例患者的臨床資料Table 1 The clinical data of 8 patients
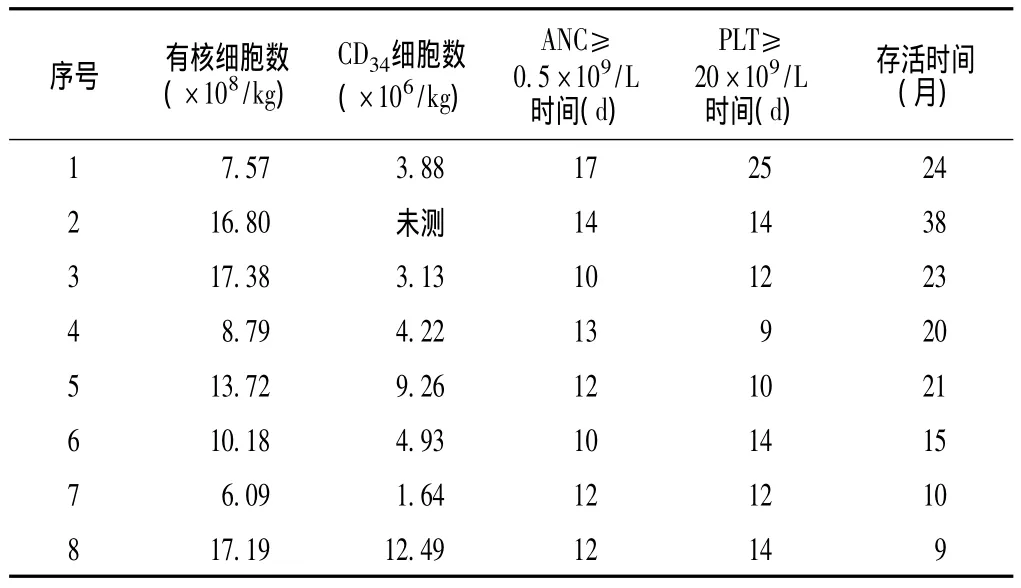
表2 8例患者的移植資料Table 2 Transplantation data of 8 patients
2 結果
2.1 造血重建 8例患者均獲造血重建,ANC恢復至≥0.5×109/L的時間為10~17 d,中位時間為12.5 d;PLT≥20×109/L的時間為9~25 d,中位時間為13.8 d。移植后靜脈輸注懸浮紅細胞3~45 U,平均12 U;靜脈輸注單采血小板2~39 U,平均9 U;移植后+30 d 7例患者血常規及骨髓恢復正常或接近正常,DNA STR-PCR、性染色體分析及血型鑒定等均證明為供者型。表2顯示,單倍型相合移植、全相合移植、非親緣全相合移植之間的造血重建時間無明顯差異。
2.2 GVHD 2例同時合并急性和慢性GVHD,例3于+30 d出現皮膚Ⅱ度GVHD,甲強龍治療25 d痊愈,+120 d出現皮膚及肝臟Ⅱ~Ⅲ度GVHD,甲強龍治療3周后痊愈。例6于+36 d出現腸道I度GVHD,經輸注甲強龍后控制,+79 d出現腸道Ⅱ~Ⅲ度GVHD,CSA改為靜脈滴注,靜脈輸注甲強龍后2周痊愈,其余患者未發生GVHD。
2.3 其他并發癥 8例患者中有5例 (例1、3、4、6、8)合并CMV血癥,前3例分別于+38 d、+30 d、+21 d合并CMV血癥,例6分別于+44 d、+85 d 2次合并CMV血癥,例8分別于+34 d、+53 d、+114 d 3次合并CMV血癥,均經膦甲酸鈉或更昔洛韋治療1~5周后轉陰;1例 (例6)+102 d合并卡氏肺孢子蟲感染,復方新諾明治療4周痊愈;1例 (例8)+9 d發生感染性休克,血培養為銅綠假單胞菌生長,抗感染治療后痊愈,+48 d再次出現中樞神經系統感染,血培養及腦脊液培養為銅綠假單胞菌生長,經多種抗菌藥物聯合治療,感染控制,+101 d發生純紅再障,經美羅華治療后骨髓紅系恢復;3例 (例1、6、8)合并出血性膀胱炎,經堿化、水化等治療,2~5周后痊愈。
2.4 隨訪 隨訪9~38個月,中位隨訪時間為20個月,8例均存活,無移植相關死亡,除1例血象恢復慢仍需要定期輸血外,其余7例血象完全恢復正常。
3 討論
再生障礙性貧血 (AA)是由理化因素、生物因素、藥物及不明原因引起的骨髓干細胞及造血微循環損傷,導致紅髓脂肪化、全血細胞減少的疾病。SAA病情較重,威脅患者生命。目前,主要治療方法是免疫抑制療法和HLA相合allo-HSCT。免疫抑制劑治療可使20%~40%的患者血象完全恢復正常,但起效慢,通常需3~6個月,期間患者仍需輸血、預防和治療感染等,風險較大。allo-HSCT治療AA始于20世紀70年代,隨著移植技術改良和新型免疫抑制劑的問世,移植相關并發癥明顯降低、造血重建迅速,存活率明顯提高。新近的文獻報道,SAA患者 allo-HSCT后其長期生存率可達70% ~90%[1-3],兒童療效更佳,Bai等[4]報道 SAA 患者移植后 3年、5年生存率分別為76%和74%,兒童患者長期生存率達90%[5]。國內翟衛華等[6]報道16例 AA患者在allo-HSCT治療后14例 (87.5%)獲得造血重建,移植排斥2例(12.5%)。雖然植入失敗和GVHD是影響患者生存率和生活質量的主要原因[7],但具有較強免疫抑制作用的FLU作為預處理方案有更高的植入率。而對HLA相合非親緣供者造血干細胞移植采用FLU為主的預處理方案也有較好的效果,Locatelli等[8]應用FLU/ATG/CTX預處理的HLA相合非親緣HSCT治療了13例AA患者,其總生存率達到74.6%。
目前,異基因骨髓移植 (allo-BMT)已經成為年齡<50歲、有HLA匹配供者的SAA患者的治療選擇之一;對于年齡<20歲的SAA患者,allo-BMT成為首選治療措施;對于免疫治療無效的SAA患者,其allo-BMT年齡可放寬至50~65歲[9]。
但由于HLA相合供者只解決了近30%患者的造血干細胞來源,而我國獨生子女政策進一步限制了allo-HSCT臨床應用。因此,單倍型相合HSCT為所有患者解決了干細胞來源,其主要障礙是移植排斥率和GVHD發生率更高。隨著HLA高分辨配型的完善,預處理方案的改進,GVHD的預防和支持治療的完善,移植患者的生存質量明顯提高。但用于治療SAA的文獻較少,多為個案或例數有限的報道[10-11]。
本研究結果顯示,單倍型相合移植、親緣全相合移植、非親緣全相合移植的造血重建時間無明顯差異。8例患者中4例SAA患者接受單倍型相合移植,1例接受親緣HLA全相合移植、3例接受非親緣全相合移植,均采用含有FLU的預處理方案,其中4例單倍型相合移植患者采用FLU+CTX+BU+ATG預處理方案、增加預處理免疫清除強度以及植入較全相合移植患者細胞量更高的有核細胞數量以及CD34細胞量的方法,保證了干細胞的植活,獲得了滿意效果,4例患者均成功植活。8例患者全部成功植入,ANC恢復至≥0.5×109/L的中位時間為12.5 d,PLT≥20×109/L的中位時間為13.8 d。8例全部存活。另外,本研究有2例發生急性Ⅰ~Ⅲ度GVHD,1例發生局限慢性GVHD,均為單倍型相合移植,但經激素等治療后很快控制,預后良好。我們還觀察到,5例移植后發生CMV感染,1例2次發生CMV感染,1例3次發生CMV感染,這2例均為單倍型相合移植,與患者免疫功能低下有關,提示單倍型相合移植治療SAA,尤其要注意防治感染特別是CMV病毒感染。
我們的體會是,采用FLU為基礎的預處理方案的allo-HSCT治療SAA,移植后要重視感染尤其CMV感染的預防和治療,但無論是親緣全相合、非親緣全相合或是單倍型相合的allo-HSCT,均是有效的治療方法,能夠成功植入,且GVHD發生率低,安全可行,為適合移植的患者提供了治愈的機會。
1 Inamoto Y,Suzuki R,Kuwatsuka Y,et al.Long-term outcome after bone marrow transplantation for aplasticanemia using cyclophosphamide and total lymphoid irradiation as conditioning regimen[J].Biol Blood Marrow Transplant,2008,14(1):43 -49.
2 Bacigalupo A.Treatment strategies for patients with severe aplastic anemia [J].Bone Marrow Transplant,2008,42(Suppl 1):S42 -S44.
3 Armand P,Antin JH.Allogeneic stem cell transplantation for aplastic anemia [J].Biol Blood Marrow Transplant,2007,13(5):505 -516.
4 Bai LY,Chiou TJ,Liu JH,et al.Hematopoietic stem cell transplantation for severe aplastic anemia experience of an institute in Taiwan[J].Ann Hematol,2004,83:38 -43.
5 Stary J,Locatelli F,Niemeyer CM,et al.Stem cell transplantation for aplastic anemia an dmyelodysplastic syndrome[J].Bone Marrow Transplant,2005,1:S13 -S16.
6 翟衛華,王玫,周征,等.異基因造血干細胞移植治療再生障礙性貧血16例臨床觀察[J].中華血液學雜志,2007,28(2):78-82.
7 Armand P,Antin JH.Allogeneic stem cell transplantation for aplastic anemia [J].Biol Blood Marrow Transplant,2007,13(5):505 -516.
8 Locatelli F,Bruno B,Zecca M,et al.Cyclosporin A and short-term methotrexate versus cyclosporinAas graft versushost disease prophylaxis in patients with severe aplastic anemia given allogeneic bone marrow transplantation from an HLA-identical sibling:results of a GITMO/EBMT randomized trial[J].Blood,2000,96(5):1690 -1697.
9 Hengxiang W,Zhidong W,Mei X,et al.Co-transfusion of haploidentical hematopoietic and mesenchymal stem cells to treat a patient with severe aplastic[J].Cytotherapy,2010,12(4):563-565.
10 Georges GE,Storb R.Stem cell transplantation for aplastic anemia[J].Int J Hematol,2002,75:141 -146.
11 Rihani R,Lataifeh I,Halalsheh H,et al.Haploidentical stem cell transplantation as a salvage therapy for cord blood engraftment failure in a patient with Fanconi anemia [J].Pediatr Blood Cancer,2010,55(3):580-582.

