熱處理對黑色巖系鎳鉬礦富集的影響
孫 偉,劉建東,胡岳華,耿志強
(中南大學 資源加工與生物工程學院,湖南 長沙,410083)
鉬是一種重要的戰略金屬,在地殼中其豐度約為1×10-6。我國的鉬礦資源具有品位低、規模大、多金屬伴生等特點[1]。鉬的來源主要來自輝鉬礦的提取,輝鉬礦大多存在于鎳鉬礦中。在我國湘、渝、黔三省市交接處蘊藏非常豐富的黑色巖系鎳鉬礦,初步探明貯量達937萬t[2]。黑色巖系鎳鉬礦含有多種金屬元素,具有很高的經濟價值,但由于其成分復雜,礦物形態特殊,因而采用傳統的物理及化學選礦技術較難將其中的有用組分有效富集,鎳鉬礦物資源的綜合回收選礦效果不理想。現階段主要采用焙燒-氧堿浸法[3]來提取鉬,再從浸出渣中提取鎳。采用此種處理方法會嚴重污染環境和浪費資源。熱性質分析技術可以從根本上了解鎳鉬礦焙燒過程中發生的各種變化,為綜合利用黑色巖系鎳鉬礦和減小環境污染提供理論依據。目前,國內外對黑色巖系鎳鉬礦熱性質研究較少。有一些研究人員對鎳鉬礦火法進行處理工藝研究,如伍宏培等[4]報道了一種處理鉬鎳礦的濃酸熟化浸出一氨水解聚一溶劑萃取工藝。該工藝將原礦磨細至粒徑小于74 μm 的礦粒含量占56%,再在530~570 ℃下氧化焙燒2.5 h,用濃硫酸在加熱條件下熟化2~3 h;隨后加水,并在85 ℃下攪拌浸出1.5 h,用氨水解聚分離(控制pH值為0.5~0.8),即可得到大部分鉬。皮關華等[5]對難選鎳鉬礦提取鉬提出了一種焙燒脫硫-氧化浸出工藝,該工藝在600 ℃時將鎳鉬礦直接焙燒脫硫,得到MoO3,MoO2,Mo和Mo2S3等混合物,然后,以NaOH(質量分數為 30%)或 Na2CO3(質量分數為 50%)作浸出劑,并向溶液中通入活性氧(臭氧)進行氧化浸出,當浸出溫度為90~100 ℃、活性氧氣通氣時間為3 h、液固比為 3:1時,鉬的浸出率為 100%。秦純[6]研究了一種采用碳酸鈉轉化處理黑色頁巖來分離鉬鎳的工藝,該工藝將黑色頁巖焙燒脫硫并粉碎后,加入50%的碳酸鈉及30%的水進行調漿。礦漿經高溫轉化后加水溶浸,再用清水洗滌得到浸液,尾渣即為鎳精礦。將浸液除磷凈化、過濾,所得到的濾液經沉鉬處理即得鉬酸鈣鹽產品。該工藝的鉬回收率可達到90%以上,鎳回收率則高達98%。以上幾種方法均涉及鎳鉬礦的高溫焙燒工藝,而對于鎳鉬礦焙燒過程中發生的各種變化有待進一步研究。為此,本文作者在對黑色巖系鎳鉬礦多元素分析與 XRD分析的基礎上,采用綜合熱分析儀對空氣氣氛和氬氣氣氛下鎳鉬礦熱性質進行比較,分析加熱過程中鎳鉬礦發生的具體變化,從而為鎳鉬礦選擇合適的選冶流程提供理論依據。
1 礦石的性質
試樣中主要的金屬礦物是黃鐵礦、菱鐵礦、磁鐵礦、鎳黃鐵礦、輝砷鎳礦、輝鉬礦、閃鋅礦、黃銅礦、方鉛礦、毒砂等;脈石礦物主要是石英、白云石、方解石、碳質物、云母、磷灰石等。鎳鉬礦原礦化學多元素分析結果(質量分數)見表1。

表1 鎳鉬礦原礦化學多元素分析Table1 Chemical multielement analysis of Ni-Mo raw ores%
2 實驗部分
(1) 利用綜合熱分析儀(NETZSCH STA 449C) 對鎳鉬礦在空氣氣氛和氬氣氣氛中進行熱重(TG)及差熱(DTA)分析。加熱速度為10 ℃/min, 加熱終溫為1 400℃。采用X線衍射分析儀分析原礦及800 ℃焙燒燒后鎳鉬礦的礦物組成, 焙燒具體方法是:取少量鎳鉬礦在800 ℃時于馬弗爐中灼燒1.5 h, 待其冷卻后研成粒徑為74 μm細粉進行XRD分析。
(2) 通過具體條件實驗確定最佳藥劑方案和浮選流程,對鎳鉬礦原礦和焙燒預處理礦進行浮選試驗。
3 試驗結果討論
3.1 焙燒鎳鉬礦晶形的轉變
孫小白[7]利用反射爐分段升溫焙燒工藝制備了試劑鉬酸鈉。將鉬精礦加入到反射爐膛右邊先預熱,然后將部分預熱好的礦粉移至火墻邊鋪開(厚度≤2 cm),控制焙燒溫度在 500 ℃左右;待爐料燒至黃色時,升溫到550~660 ℃繼續焙燒一段時間,當焙砂呈金黃色顆粒狀時出料。得到的焙砂采用純堿浸出,浸出液經除雜、凈化(硫化物除重金屬、鋇鹽除硫酸根、鎂鹽除磷)、重結晶,得到鉬酸鈉產品。William[8]采用閃速焙燒的方法處理鉬精礦。以上實例說明礦物經焙燒可以產生晶形和形貌的變化,焙燒過程中會發生大量的物理、化學反應。本研究對鎳鉬礦進行焙燒處理,且對原礦和焙燒礦進行XRD檢測,通過兩礦樣XRD圖譜對比分析焙燒過程發生的反應。鎳鉬礦原礦的XRD圖譜如圖1所示。由圖1可知:鎳鉬礦原礦主要礦物成分是 SiO2,CaCO3,FeS2,CaSO4·2H2O,云母,NiAsS,Ca5(PO4)3F和CaS。鎳鉬礦焙燒礦XRD圖譜如圖2所示。將鎳鉬礦在800 ℃中性焙燒1.5 h后緩慢降至室溫,取樣磨至粒徑74 μm,進行XRD檢測(在700,750,800和850 ℃時進行焙燒礦的XRD檢測,800 ℃時效果最佳)。由圖2可知:焙燒后鎳鉬礦中的主要成分是 SiO2,CaCO3,Ca5(PO4)3F,CaS,Fe7S8和NiS。與鎳鉬礦原礦XRD圖譜進行對比,其變化在于:CaCO3在 2θ為 29.31°處的衍射峰強度下降,說明此時部分 CaCO3發生了分解反應;FeS2在 2θ為32.83°,36.92°,40.73°,47.35°,56.08°和 64.24°處的衍射峰消失,同時在2θ為30.01°,44.08°和53.27°出現 Fe7S8衍射峰,表明 FeS2發生了脫硫反應生成了Fe7S8(Fe7S8為 FeS的一種特殊形態);CaSO4·2H2O在2θ 為 11.39°,20.58°,43.25°和 48.47°處的衍射峰消失,說明CaSO4·2H2O發生了脫水、分解反應;云母在2θ為30.85°處的衍射峰消失,表明云母已經分解;NiAsS在 2θ 為 35.80°,39.03°和 53.39°處的衍射峰消失,同時在2θ為45.36°和54.96°處產生了NiS衍射峰,表明在此溫度范圍內NiAsS分解產生了NiS;CaS在2θ為44.79°,50.16°和54.51°處發生了變化,說明此過程產生了CaS。
圖2所示輝鉬礦(MoS2)在2θ為12.68°處產生了很小的衍射峰,而原礦的 XRD圖譜上并未存在 MoS2的衍射峰。因為鎳鉬礦原礦中鉬、鎳以非晶質的硫化物形式存在,礦物的 XRD圖譜上完全沒有含鉬礦物的衍射峰。說明中性焙燒使原礦中的非晶質硫化鉬轉化為晶質硫化鉬。
利用鎳鉬礦原礦與 800 ℃中性焙燒鎳鉬礦 XRD圖譜分析,可以對鎳鉬礦在空氣氣氛和氬氣氣氛下的差熱與熱重分析圖譜進行準確、詳細解析,清楚地了解焙燒過程中鎳鉬礦具體發生了怎樣的物理、化學反應,為鎳鉬礦的選-冶聯合提供理論依據。

圖1 鎳鉬礦原礦XRD圖譜Fig.1 XRD spectrum of Ni-Mo raw ore
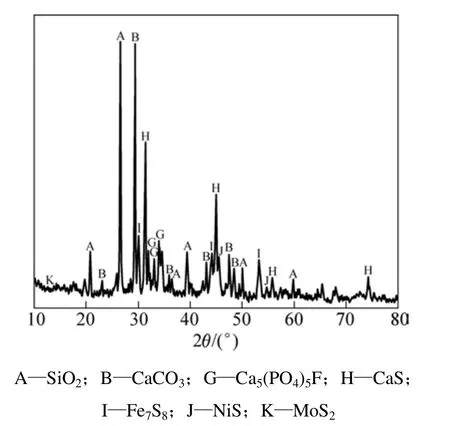
圖2 焙燒預處理鎳鉬礦XRD圖譜Fig.2 XRD spectrum of roasting pretreatment Ni-Mo ore

圖3 鎳鉬礦在空氣氣氛下的DTA曲線Fig.3 DTA curve of Ni-Mo ores in air atmosphere
3.2 不同氣氛下黑色巖系鎳鉬礦差熱和熱重分析
3.2.1 鎳鉬礦在空氣氣氛下的差熱和熱重分析
鎳鉬礦在空氣氣氛下差熱曲線如圖3所示。由圖3可以看出:DTA曲線上存在室溫~231 ℃,778~855 ℃和 907~1 400 ℃ 3個吸熱峰,以及 231~778 ℃和855~907 ℃ 2個放熱峰。室溫~231 ℃之間的吸熱峰是鎳鉬礦脫去物理吸附水及其結晶水所致,做差熱的礦樣為天然原礦,其中含有吸附水和結晶水;778~855 ℃處的吸熱峰主要是云母分解所致。由于天然云母含羥基(—OH),從200 ℃就開始有質量損失的趨勢,當溫度高于450 ℃時就開始分解,高于600 ℃時質量損失加劇,到900 ℃時幾乎完全分解;907~1 400 ℃處的吸熱過程是Ca5(PO4)3F,CaCO3和CaSO4等逐級熱分解所致;當溫度達到1 400 ℃時,礦樣還在吸熱,說明分解還未完全,分解反應仍在進行,還存在一定物質有待分解。在231~778 ℃之間有一個非常大的放熱峰, 它是有機質燃燒和黃鐵礦氧化形成的,放熱峰大說明鎳鉬礦中有機質和黃鐵礦含量比較高。從表1所示的多元素分析結果可以看出:原礦含碳量大于10%,黃鐵礦含量為20%左右。在855~907 ℃有1個很小的放熱峰,這是鎳鉬礦中黃鐵礦氧化產生的SO2與部分CaCO3分解產生的CaO化合生成CaSO4所致;當溫度升高到1 400 ℃時,分解反應還沒有達到最高峰,據此推測鎳鉬礦完全完成分解反應的溫度應當超過1 500 ℃。
鎳鉬礦在空氣氣氛下的熱重曲線如圖4所示。從圖4可以看出:室溫~280 ℃之間鎳鉬礦產生的質量損失率為 1.99%,這是鎳鉬礦脫去物理吸附水及結晶水造成的,如原礦 X線衍射(圖 1)中顯示原礦樣中含有CaSO4·2H2O,可脫去結晶水變為無水CaSO4,反應式為式(1);在280~668 ℃,鎳鉬礦中有機質迅速燃燒,引起質量快速下降,產生大量的CO2,此溫度區間黃鐵礦焙燒可發生如式(2)和(3)的反應[9],生成赤鐵礦[10]和磁鐵礦,此過程也會產生一定質量損失,此區間質量損失率大于16%;在668~1 008 ℃,質量損失率為8.62%,在此過程中Ca5(PO4)3F和CaCO3完全分解,CaCO3產生的CaO部分與黃鐵礦氧化產生的SO2反應生成CaSO4,反應式為式(4)~(6)。1 008~1 400 ℃處的吸熱過程是CaSO4熱分解所致,此過程質量損失率為5.75%,分解反應為式(7)。超過1 400 ℃質量仍有微弱的下降趨勢,表明還有很微弱的分解反應在進行。

圖4 鎳鉬礦在空氣氣氛下的TG曲線Fig.4 TG curve of Ni-Mo ores in air atmosphere

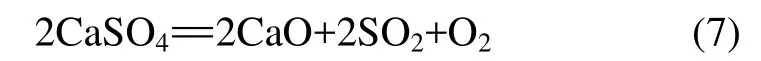
3.2.2 鎳鉬礦在氬氣氣氛下差熱和熱重分析
鎳鉬礦在氬氣氣氛下差熱曲線如圖5所示。由圖5可以看出:DTA曲線存在常溫~231 ℃,600~655 ℃和740~1 320 ℃ 3個吸熱峰與231~600 ℃和655~740℃ 2個放熱峰。常溫~231 ℃之間吸熱峰是鎳鉬礦脫去物理吸附水及其結晶水造成的;600~633 ℃處有1個小的吸熱峰,是磁鐵礦轉變為磁黃鐵礦及部分CaCO3分解吸熱所致;740~1 320 ℃處的吸熱峰是Ca5(PO4)3F,CaCO3和CaSO4等逐級熱分解以及CaSO4被還原為CaS所致;當溫度超過1 320 ℃時,分解反應結束,DTA曲線顯示礦樣開始放出大量的熱,表明鎳鉬礦開始出現大量的化合反應。在231~600 ℃之間有1個小的放熱峰, 主要是鎳鉬礦中的黃鐵礦與其表面附著的氧氣發生氧化反應所致;在633~740 ℃之間有1個曲折的放熱峰,因黃鐵礦與表面附著的氧發生氧化反應及一些化合反應所致。
考慮到氬氣氣氛下無氧參與,鎳鉬礦中的化學反應比較復雜,所以,對800 ℃中性焙燒鎳鉬礦進行了X線衍射分析(見圖 2),以便更清晰地分析此熱重曲線。
從圖6所示的TG曲線可以看出:在常溫~285 ℃之間,由于鎳鉬礦脫去物理吸附水及其結晶水,造成質量損失率為 1.73%,脫去結晶水(圖 2中顯示為CaSO4·2H2O衍射峰消失),脫水反應與空氣氣氛下相同,反應式為式(1);在 285~706 ℃,質量損失率為8.47%,主要是其中的有機質揮發及黃鐵礦受熱分解最終生成磁黃鐵礦[11],黃鐵礦通過2種可能途徑轉變為磁黃鐵礦[12]:一種是黃鐵礦顆粒首先經表面吸附氧的氧化轉變為磁鐵礦,隨溫度升高,新生成的磁鐵礦與黃鐵礦晶格中揮發出的硫進一步反應轉變為磁黃鐵礦,反應式為式(8)和(9);另一可能途徑是黃鐵礦直接脫硫轉變為磁黃鐵礦[11,13],反應式為式(10),由于氬氣環境下缺氧,此反應為磁黃鐵礦的主要來源。對比圖1與圖2可以看出:焙燒后,FeS2衍射峰消失而產生FeS衍射峰。在此溫度區間NiAsS分解產生了NiS,反應式為式(11);NiAsS衍射峰消失,產生了 NiS衍射峰;在706~945 ℃,由于云母及部分CaCO3分解導致質量損失率為11.74%,天然云母含—OH,從200 ℃就開始有質量損失趨勢,當溫度高于450 ℃時開始分解,在600 ℃以上時質量損失迅速增大,到900 ℃時云母幾乎完全分解。在此溫度區間,圖2顯示為云母衍射峰消失。在此溫度區間,部分CaCO3也開始分解。圖2中還顯示產生了CaS的衍射峰,而且沒有CaSO4衍射峰,說明CaSO4被還原而產生CaS,CaSO4被還原而產生 CaS的反應較復雜,具體反應式為式(12)~(16);在945~1 400 ℃,Ca5(PO4)3F、剩余CaCO3以及少量的 CaSO4逐級熱分解造成質量損失率為15.44%,Ca5(PO4)3F,CaCO3及 CaSO4的分解反應式為式(4)~(5)和(7)。
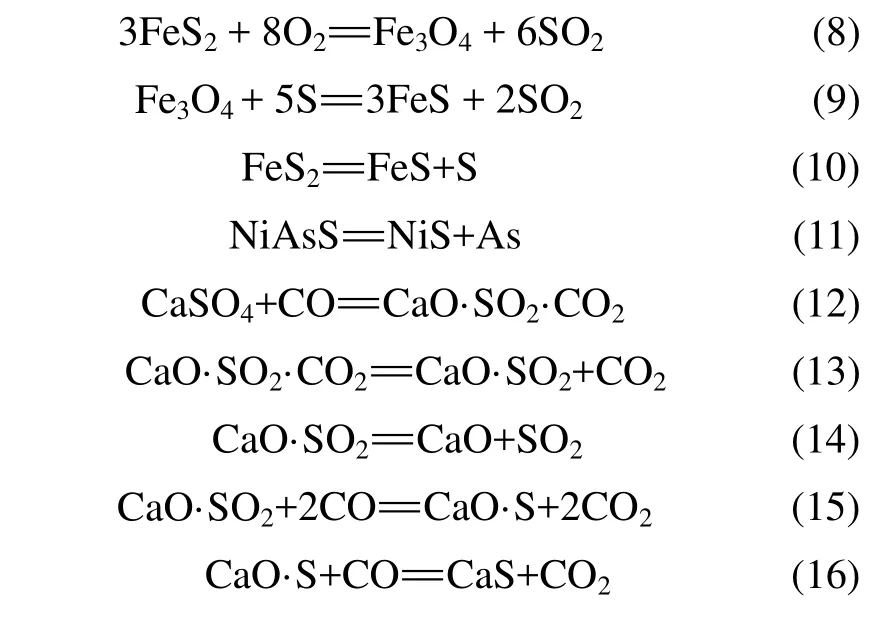
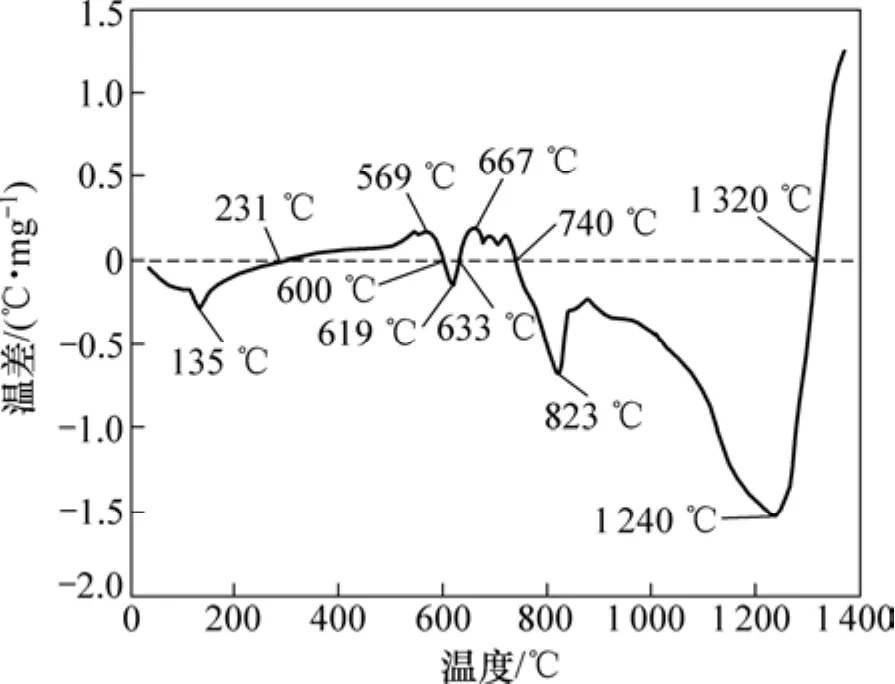
圖5 鎳鉬礦在氬氣氣氛下的DTA曲線Fig.5 DTA curve of Ni-Mo ores in argon atmosphere
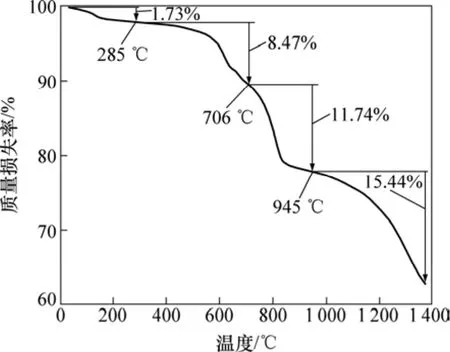
圖6 鎳鉬礦在氬氣氣氛下的TG曲線Fig.6 TG curve of Ni-Mo ores in argon atmosphere
4 鎳鉬礦晶形轉變對浮選的影響
在中性焙燒過程中,鎳鉬礦里的非晶質硫化鉬轉化為晶質硫化鉬,且其中含有的MoO3也可與黃鐵礦脫掉的硫發生反應生成MoS2,反應式如下:

由于輝鉬礦具有天然疏水性[14],可浮性好,從而可以提高鎳鉬的浮選回收率。下面通過對原礦和焙燒預處理礦浮選結果對比加以說明。
浮選法[15]采用泡沫浮選,浮選流程見圖 7。經過具體條件實驗確定最佳藥劑用量,最終確定了最佳磨礦時間、各藥劑的用量和浮選時間。

圖7 鎳鉬礦浮選流程圖Fig.7 Flotation flowchart of Ni-Mo ores
通過圖7所示浮選流程對原礦和焙燒預處理礦進行浮選試驗,結果如表2所示。從表2可以看出:經焙燒預處理的鎳鉬礦一次浮選回收率就達到73.25%,品位為 7.66%,與原礦的浮選回收率和品位相比均有很大提高。
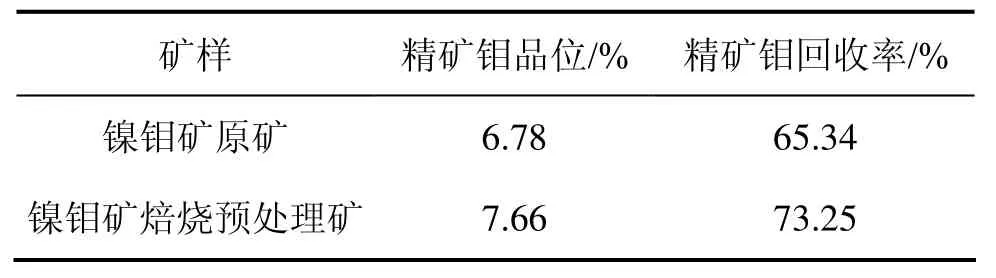
表2 鎳鉬礦原礦與焙燒預處理礦浮選結果Table2 Floatation results of Ni-Mo raw ores and roasting pretreatment ores
5 結論
(1) 鎳鉬礦中含碳量比較高,在焙燒過程中可以除去大部分有機碳,增加了礦物的可浮性,在浮選過程中減少藥劑用量。
(2) 焙燒可以提高鎳鉬礦浮選精礦中鉬的品位和回收率,說明熱處理可以改變黑色巖系鎳鉬礦的性質和形態,有利于其有效富集。
[1] 劉炯天, 李小兵, 王永田, 等. 旋流-靜態微泡浮選柱浮選某難選鉬礦的試驗研究[J]. 中南大學學報: 自然科學版, 2008,39(2): 300-306.
LIU Jiong-tian, LI Xiao-bing, WANG Yong-tian, et al.Experimental study on separating some molybdenum ore by using cyclonic-static micro-bubble flotation column[J]. Journal of Central South University: Science and Technology, 2008,39(2): 300-306.
[2] 陳代雄, 唐美蓮, 薛偉, 等. 高碳鉬鎳礦可選性試驗研究[J].湖南有色金屬, 2006, 22(6): 9-11.
CHEN Dai-xiong, TANG Mei-lian, XUE Wei, et al. Study on dressing concentrate of high carbon nickel-molybdenum ore[J].Hunan Nonferrous Metals, 2006, 22(6): 9-11.
[3] Park K H. Hydrometallurgical processing and recovery of molybdenum trioxide from spent catalyst[J]. International Journal of Mineral Processing, 2006, 80(18):261-265.
[4] 伍宏培, 馮光芬. 鉬鎳礦的濃酸熟化浸出解聚溶劑萃取工藝:中國, 1033784A[P]. 1989-07-12.
WU Hong-pei, FENG Guang-fen. The acid curing depolymerization solvent extraction process of Mo-Ni ores:China, 1033784A[P]. 1989-07-12.
[5] 皮關華, 徐徽, 陳白珍, 等. 從難選鎳鉬礦中回收鉬的研究[J].湖南有色金屬, 2007, 23(1): 9-12.
PI Guan-hua, XU Hui, CHEN Bai-zhen, et al. Study on recovering molybdenum from rocky-select Ni-Mo ores[J].Hunan Nonferrous Metals, 2007, 23(1): 9-12.
[6] 秦純. 用碳酸鈉轉化處理黑色頁巖分離鉬鎳的工藝: 中國,1177012[P]. 1998-03-25.
QIN Chun. The process of separation Mo-Ni with sodium carbonate conversion treatment black shale: China, 1177012[P].1998-03-25.
[7] 孫小白. 試劑鉬酸鈉的制備[J]. 甘肅化工, 1990(4): 6-8.
SUN Xiao-bai. Preparation of ammonium molybdate reagent[J].Gansu Chemical, 1990(4): 6-8.
[8] William A. Process for converting molybdenite to molybdenum oxide: US, 4551312[P]. 1985-11-05.
[9] Robert B C. 黃金提取技術[M]. 中國科學院化工冶金研究所譯. 北京: 北京大學出版社, 1991: 25.
Robert B C. Gold extraction technology[M]. Institute of Chemical Metallurgy, Chinese Academy of Sciences, transl.Beijing: Beijing University Press, 1991: 25.
[10] Tarling D H. Paleomagnetism[M]. London: Champman and Hall,1983: 50.
[11] Lambert J M, Simkovich G, Walker P L. The kinetics and mechanism of the pyrite to pyrrhotite transformation[J].Metallurgical and Materials Transactions, 1998, 29(2): 385-396.
[12] 李海燕, 張世紅. 黃鐵礦加熱過程中的礦相變化研究—基于磁化率隨溫度變化特征分析[J]. 地球物理學報, 2005, 48(6):1384-1391.
LI Hai-yan, ZHANG Shi-hong. Detection of mineralogical changes in pyrite using measurements of temperaturedependence susceptibilities[J]. Chinese Journal of Geophysics,2005, 48(6): 1384-1391.
[13] Bina M, Daly L. Mineralogical change and self reversed magnetizations in pyrrhotite resulting from partial oxidation geophysical implications[J]. Physics of the Earth and Planetary Interiors, 1994, 85: 83-99.
[14] 王暉, 陳立, 符劍剛, 等. 輝鉬礦浮選體系中的界面熱力學[J].中南大學學報: 自然科學版, 2007, 38(5): 893-899.
WANG Hui, CHEN Li, FU Jian-gang, et al. Interface thermodynamics of molybdenite floatation system[J]. Journal of Central South University: Science and Technology, 2007, 38(5):893-899.
[15] 王淀佐. 浮選劑作用原理及應用[M]. 北京: 冶金工業出版社,1982: 28-31.
WANG Dian-zuo. Flotation reagents: Fundamentals and application[M]. Beijing: Metallurgical Industry Press, 1982:28-31.

