pH值對水熱合成黃鐵礦型CoS2微晶的影響
謝玲玲 吳 榮 李 錦 孫言飛 簡基康
(新疆大學物理科學與技術學院,烏魯木齊 830046)
pH值對水熱合成黃鐵礦型CoS2微晶的影響
謝玲玲 吳 榮 李 錦 孫言飛 簡基康*
(新疆大學物理科學與技術學院,烏魯木齊 830046)
本文以EDTA-2Na為輔助劑,Na2S2O3·5H2O為硫源,運用水熱法制備了黃鐵礦型CoS2微晶,研究了溶液pH值對產物結構和形貌的影響。采用X射線粉末衍射儀(XRD),掃描電子顯微鏡(SEM)對產物的結構和形貌進行了表征。實驗結果表明,溶液為酸性環境時(pH=1、3)可得到純相的黃鐵礦型CoS2微晶,形貌為微米尺寸的空心球殼。溶液為中性和堿性環境時(pH=7、11),產物出現少量雜相,形貌變為規則的八面體晶粒。討論了這些CoS2微晶的形成機制。
CoS2;水熱合成;pH值;形貌
黃鐵礦型的CoS2半導體材料具有優異的光學、電學、磁學等性質[1],如半金屬鐵磁性[2-3]、高的自旋極化[3],在催化、光伏、電子等領域擁有重要的應用前景[4]。近年來,制備CoS2的研究取得較大進展,尤其是在液相中制備具有特殊形貌和尺寸的CoS2納米及微米晶的研究工作取得了一些重要的成果[5-13]。Qian等[5]以乙二胺為溶劑,Na2S3為硫源在130℃下合成立方體形貌的CoS2納米晶,粒徑為20 nm;Bi等[6]用聚合物為模板合成了針狀和棒狀非晶CoS2納米粒子;張玲等[7]以NiSe作為晶種在堿性條件下水熱合成CoS2晶體,并對產物進行結構精修,證實產物為黃鐵礦型CoS2。王敏等[8]報道了無模板、無表面活性劑,水熱合成立方相的CoS2空心微球。段鶴等[13]采用溶劑熱法,以甲苯為溶劑,多硫化納為硫源,制備了CoS2納米晶。
在溶液相中生長晶體,體系的pH值對產物的物相和形貌有較大影響[14]。本文以EDTA-2Na為輔助劑,以Na2S2O3·5H2O為硫源,水熱合成了CoS2微晶。討論了溶液pH值對產物物相和形貌的影響。通過調整溶液的pH值,使產物CoS2的形貌從空心微球轉變為規則的八面體晶粒。
1 實驗部分
1.1 樣品的制備
原料為氯化鈷(CoCl2·6H2O,分析純);EDTA-2Na(C10H14N2O8Na2·2H2O,分析純);硫代硫酸鈉(Na2S2O3·5H2O,分析純);氫氧化鈉(NaOH,分析純);無水乙醇(CH3CH2OH,分析純);去離子水。將35 mL去離子水注入容積為45 mL的反應釜中并投入4 mmol EDTA-2Na,待充分溶解后,按反應物比為nCoCl2·6H2O/nNa2S2O3·5H2O=1/2加入反應物并用磁子攪拌器攪拌15 min,充分混合后,滴入pH=12的氫氧化鈉溶液調節混合溶液的pH值。反應釜密閉后置于恒溫箱中,180℃下反應24 h后取出,自然冷卻至室溫。濾出釜底沉淀物,用無水乙醇和去離子水清洗數次,在60℃下真空干燥6 h,收集樣品并進行測試。
1.2 樣品的表征
采用MAC SCIENCE 18 kW轉靶X射線衍射儀(XRD,Cu靶 Kα 射線,λ=0.154 05 nm,40 kV,200 mA)對樣品進行物相分析。用掃描電子顯微鏡(SEM,Leo 1430VP 20 kV)對樣品表面形貌進行觀察。
2 結果與討論
不同pH值的溶液水熱生長后所得樣品的XRD圖如圖1所示。XRD圖顯示,所有樣品主晶相均為黃鐵礦型CoS2(空間群為Pa3,ICDD PDF No.65-3322)。其中,pH=5時,樣品中存在少量S(空間群為 Fddd,ICDD PDF No.42-1278)雜質,其衍射峰以“*”區分;pH=11時,樣品的XRD圖顯示低角處存在 S8(空間群為 P2/c,ICDD PDF No.53-1109)衍射峰,如圖中“○”所示。XRD表明,pH=5、11時產物中存在硫雜質,說明反應物未完全反應。仔細對比XRD圖發現,pH=7,11時所得樣品的XRD圖中(311)、(220)等衍射峰相對強度增大,如pH=11時,圖中(311)峰相對于(200)峰的衍射強度為68%,而在圖1標準CoS2衍射譜中僅為32%,顯示產物的形貌有可能發生變化。
圖2為生長溫度180℃,溶液的pH值為1,3時所得樣品的SEM圖像。圖2(a)顯示,pH=1時,樣品由空心微球組成,微球的球形規則,直徑達2~6 μm;從圖2(b)中可看出,CoS2球殼厚約幾百納米,球殼表面凹凸不平,表明空心微球是由尺寸更小的顆粒組成的。圖2(c),(d)顯示,pH=3時,樣品仍為空心微球,與pH=1時所得樣品形貌類似,但球殼表面比較粗糙。王敏等[8]制備的CoS2空心球直徑約為2 μm,球殼厚約100 nm。
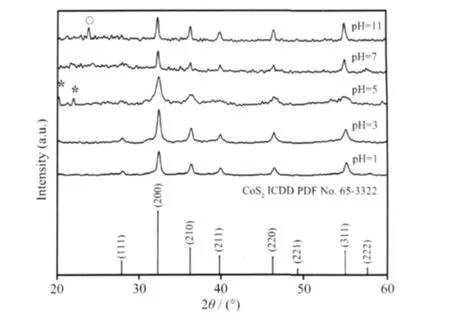
圖1 反應溫度為180℃,不同溶液pH值,(a)1;(b)3;(c)5;(c)7;(d)11所得樣品的XRD圖Fig.1 XRD patterns of samples synthesized under different pH values of solution at 180℃

圖2 反應溫度為180℃所得樣品的SEM圖像Fig.2 SEM images of samples synthesized at 180 ℃when(a),(b):pH=1,(c),(d):pH=3
為了研究空心微球的形成機制,調節EDTA-2Na用量為5 mmol,溶液pH值為1,溫度160℃,其他試驗條件相同的情況下水熱反應得到對比組樣品。對比組樣品的XRD及SEM如圖3所示。XRD圖顯示,所得樣品的主相為S(空間群為Fddd,ICDD PDF No.42-1278),圖中標出了衍射強度較大的3個S 的衍射峰(222),(026),(206),其余未標注各峰也為S衍射峰。從其SEM圖像中可看出,樣品由大量S空心微球組成,微球的球形規則,直徑達2~6 μm。右上角的插圖顯示,球殼由S納米顆粒排列堆積而成的。
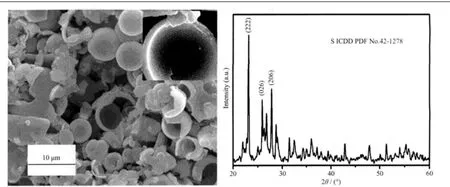
圖3 EDTA-2Na用量為5 mmol,pH=1時所得樣品的SEM圖像及XRD圖Fig.3 SEM image and XRD pattern of sample synthesized under pH=1 with the addition of 5 mmol EDTA-2Na
基于以上實驗事實推測反應過程如下:起初,EDTA-2Na在水中電解出EDTA2-,并與Co2+形成穩定的螯合物Co(EDTA),與文獻[15]報道的EDTA輔助生長FeS2納米晶類似,這有效地抑制了游離的鈷離子之間的聚合。接著,S2O32-不穩定而易分解出S和SO2,厭水的S聚集在SO2氣泡表面形成了S空心微球。螯合物Co(EDTA)中未配位的羧基上存在著氫原子,因此容易吸附在電負性較大的S空心微球表面[16]。最終,Co2+從螯合物Co(EDTA)中緩慢釋放與硫源反應生成黃鐵礦型CoS2晶粒,這些晶粒在三維空間堆積形成了CoS2空心微球。王敏等[8]指出,在反應過程中,S2O32-分解出S單質,S形成球形微粒,Co2+與S反應生成CoS2,最終S被耗盡而形成空心結構的CoS2微球。由于本實驗中使用了EDTA-2Na作為輔助劑,因此,雖然與王敏等[8]所得產物形貌類似,但反應過程是不同的。EDTA-2Na不僅作為一種常用的螯合劑,穩定了溶液中的Co2+濃度,并且作為一種酸提供了酸性環境,保障了足夠多的SO2產生。在對比組實驗中,EDTA-2Na的用量過大,Co2+難以從螯合物中逸出而無法與S空心微球反應生成CoS2。此外,本實驗結果顯示,S直接形成了空心微球結構,不是實心結構。
由上述生長實驗結果,提出CoS2空心微球可能的生長機制兩步模板法:第一步,S以分解出的SO2氣泡為模板形成S空心微球[17-19];第二步,后繼Co2+與S空心球模板反應生成CoS2空心微球。圖4描述了CoS2空心微球的合成過程:氣泡模板的形成、S空心球模板的形成、Co(EDTA)在S表面的吸附、CoS2空心微球的形成。
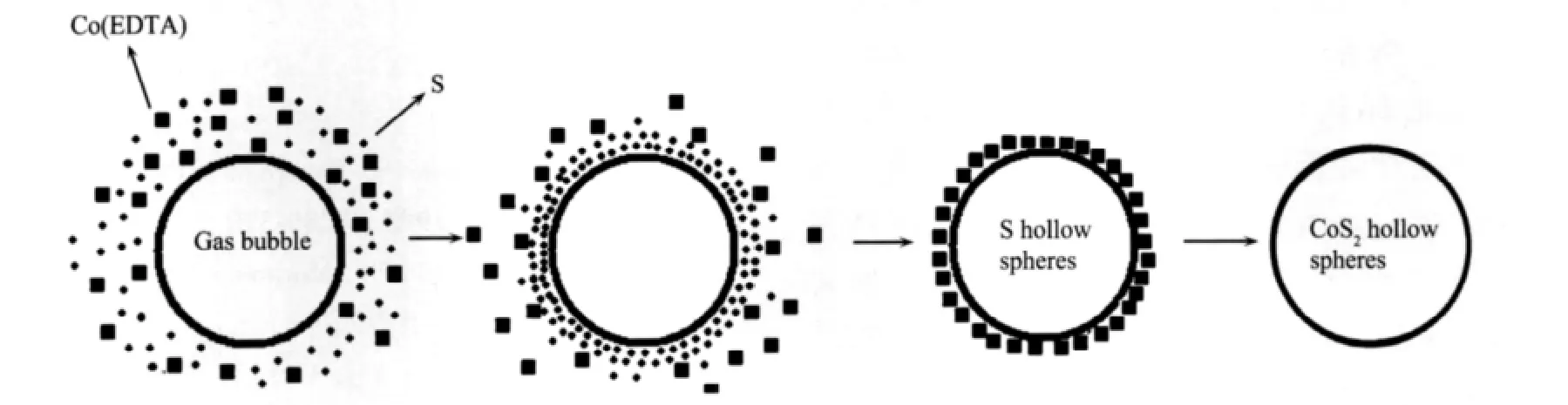
圖4 CoS2空心微球形成過程演示圖Fig.4 Schematic illustration of the possible formation process of CoS2hollow spheres
溶液的pH值為5、7、11所得樣品已經XRD圖證實主相為黃鐵礦型CoS2,相應的形貌如圖5所示。從圖5中可看出,樣品的形貌隨著pH值的增加而改變。pH=5時,樣品由類球形微粒組成,在這些微粒表面存在許多納米量級的須狀物,多個微粒間由須狀物互相連接,團聚。pH=7、11時,樣品形貌變為規則的八面體微粒,尺度約為1 μm。微粒之間互相團聚,同時還有一些外形不規則的納米級顆粒吸附在微粒表面上。

圖5 反應溫度為 180 ℃,溶液 pH 值為(a)、(b):5;(c)、(d):7;(e)、(f):11 所得樣品的 SEM 圖像Fig.5 SEM images of samples synthesized under pH values of(a),(b):5;(c),(d):7;(e),(f):11 at 180℃
須狀微粒形成的原因可能是吸附在S空心微球表面上的螯合物Co(EDTA)中未配位的羧基被OH-激活,不同微粒表面的活性羧基可與溶液中未配位的金屬陽離子進一步螯合形成結構復雜的多元螯合物,微粒之間通過多元螯合物的作用而相互吸引、鏈接[20]。溶液pH值增大,導致產物的空心球殼形貌消失,可以用上述兩步模板機制說明。在酸性環境中,S2O32-才能有效分解出SO2和S,保證氣泡模板的供應。增大溶液的pH值,溶液中的S2O32-逐漸趨于穩定,體系缺失了軟模板SO2氣泡因而得不到具有空心結構的產物。此外,酸性環境中Co(EDTA)穩定性降低,Co2+的氧化能力增強,便于S球殼模板向CoS2球殼的完全轉化。這也可以解釋在pH值增大到5時,產物中出現了少量S雜質。據文獻報道[21-22],在晶體生長過程中,那些表面能高的晶面由于具有較快的生長速率而在生長過程中慢慢消失。本體系中得到了八面體產物的原因可能是:在高pH值條件下EDTA2-會繼續電離得到EDTA4-,其與Co2+形成水溶性配合物[Co(EDTA)]2-。[Co(EDTA)]2-在CoS2各晶面吸附量不同,那些吸附量大的晶面因生長較快而逐漸消失。pH=7、11時產物XRD圖中峰強的變化間接證明了CoS2各晶面不同的生長速率。
3 結 論
本文以Na2S2O3·5H2O為硫源,在EDTA-2Na為輔助劑的條件下水熱合成CoS2微晶。XRD與SEM分析表明,pH=1,3時合成樣品為單一相的黃鐵礦型CoS2空心微球。pH=5、7、11時,合成樣品中存在硫雜質,產物的形貌由空心微球過渡到八面體微粒。結果表明在本體系中,pH值可以調節產物形貌,而空心微球結構的形成可以用兩步模板的機制解釋。
[1]Ennaoui A,Fiechter S,Pettenkofer C,et al.Sol.Energy Mater.Sol.Cells,1993,29:289-370
[2]Yamamoto R,Machida A,Moritomo Y,et al.Phys.Rev.B,1999,59(12):R7793-R7796
[3]Shishidou T,Freeman A J,Asahi R.Phys.Rev.B,2001,64:R180401-4
[4]Qian X F,Xie Y,Qian Y T,et al.J.Alloys Compd.,1998,278:110-112
[5]Qian X F,Li Y D,Xie Y,et al.Mater.Chem.Phys.,2000,66:97-99
[6]Hing B,Jiang X Q,Yang C Z,et al.Mater.Lett.,2003,57:2606-2611
[7]ZHANG Ling(張玲),ZHENG Yu-Feng(鄭毓峰),SUN Yan-Fei(孫言飛),et al.J.Xinjiang Univ.(Xinjiang Daxue Xuebao),2006,1:47-52
[8]WANG Min(王敏),MIN Yu-Ling(閔宇霖),ZHANG Yuan-Guang(張元廣),et al.Chem.World(Huaxue Shijie),2009,10:577-589
[9]Hu Q R,Wang S L,Zhang Y,et al.J.Alloys Compd.,2010,491:707-711
[10]Chen X H,Fan R.Chem.Mater.,2001,13:802-805
[11]Chakraborty I,Malik P,Moulik S.J.Nanopart.Res.,2006,8:889-897
[12]Dong J Q,Li D C,Peng Z H,et al.J.Solid State Electrochem.,2008,12:171-174
[13]DUAN He(段鶴),ZHENG Yu-Feng(鄭毓鋒),ZHANG Xiao-Gang(張校剛),et al.Mater.Mechan.Eng.(Jixie Gongcheng Cailiao),2004,28(5):49-51
[14]CHEN Yan-Hua(陳艷華),ZHENG Yu-Feng(鄭毓鋒),ZHANG Xiao-Gang(張校剛),et al.Sci.China G(Zhongguo Kexue G),2005,35(1):20-30
[15]WU Rong(吳榮),ZHENG Yu-Feng(鄭毓鋒),ZHANG Xiao-Gang(張校剛),et al.Acta Phys.Sin.(Wuli Xuebao),2004,53(10):3493-3497
[16]Kondo S(近藤精一),Ishikawa T(石川達雄),Abe I(安部郁夫),Translated by LI Guo-Xi(李國希).Science of Absorp
tion(吸附科學).Beijing:Chemical Industry Press,2005:25-26
[17]Liu X,Cui J,Zhang L,et al.Mater.Lett.,2006,60:2465-2469
[18]Wang J,Song B,Wang W J,et al.Powder Diffr.,2009,24(1):24-28
[19]Liu X D,Ma J M,Peng P,et al.Mater.Sci.Eng.B,2008,150:89-94
[20]ZHANG Hui(章慧).Coordination Chemistry:Principles and Applications(配位化學原理與應用).Beijing:Chemical Industry Press,2008:2-4
[21]Zhang L,He R,Gu H C.Mater.Res.Bull.,2006,41:260-267
[22]Wang Z L.J.Phys.Chem.B,2000,104(6):1153-1175
Effects of pH Value on Hydrothermal Synthesis of Pyrite CoS2Micro-Crystals
XIE Ling-Ling WU Rong LI Jin SUN Yan-FeiJIAN Ji-Kang*
(Department of Physics,Xinjiang University,Urumqi 830046,China)
Pyrite CoS2micro-crytals were synthesized under hydrothermal conditions employing sodium thiosulfate pentahydrate (Na2S2O3·5H2O)as sulfur source and ethylenediaminetetraacetic acid disodium (EDTA-2Na)as assistant.The effects of pH value of solution on the structures and morphologies of the products were investigated.X-ray diffraction(XRD)and scanning electron microscopy(SEM)were used to characterize the structural features and the morphology of the samples.The results show that the morphologies of the products could be tuned by the pH values of solutions.The pure-phase pyrite CoS2micro-crystals with regular hollow sphere-like morphology can be obtained in acid environment (pH=1,3),while well-faceted octahedron-shaped CoS2micro-crystals were synthesized in neutral and alkaline environment(pH=7,11).The mechanisms for the formations of the CoS2micro-crystals were discussed.
CoS2;hydrothermal synthesis;pH value;morphology
O614.81+2;O782+1;TB34
A
1001-4861(2011)01-0095-05
2010-08-03。收修改稿日期:2010-09-08。
新疆大學博士科研啟動基金(No.BS080109);新疆自治區教育廳高校教師科研項目(No.XJEDU2008I05)資助。
*通訊聯系人。E-mail:jianjikang@sina.com;會員登記號:S410800120M。

