E1A激活基因阻遏子促進人血管內皮細胞VEGF分泌和單層通透性增加*
王占勝, 韓雅玲, 康 建, 張效林, 陶 杰, 田孝祥, 閆承慧
(1沈陽軍區總醫院全軍心血管病研究所心內科, 遼寧 沈陽 110016;2大連醫科大學,遼寧 大連 116044)
E1A激活基因阻遏子促進人血管內皮細胞VEGF分泌和單層通透性增加*
王占勝2, 韓雅玲1△, 康 建1, 張效林1, 陶 杰1, 田孝祥1, 閆承慧1
(1沈陽軍區總醫院全軍心血管病研究所心內科, 遼寧 沈陽 110016;2大連醫科大學,遼寧 大連 116044)
目的探討E1A激活基因阻遏子(CREG)誘導的人血管內皮細胞(ECs)單層通透性改變中的作用及機制。方法用CREG過表達及CREG表達下調的ECs為模型,Transwell chamber彌散模型觀察ECs單層通透性的改變; 熒光倒置顯微鏡觀察細胞骨架肌動蛋白F-actin及黏附連接蛋白VE-cadherin在ECs中的分布和形態學改變;酶聯免疫吸附實驗(ELISA)檢測ECs血管內皮生長因子(VEGF)分泌。結果CREG過表達的ECs (EO組) 較EN組單層通透性明顯增高 (P<0.05);CREG表達下調的ECs(ES組)較EN組單層通透性有所下降(P<0.05)。與EN組相比較,EO組細胞中F-actin排列紊亂,形成大量應力纖維; ES組F-actin則主要呈細絲狀分布于細胞周邊,中央分布較少。同時,EO組VE-cadherin在細胞周邊的正常拉鏈狀結構減少或缺失,細胞間隙增寬;而ES組VE-cadherin在細胞周邊呈正常拉鏈狀分布,細胞之間連接緊密。ELISA檢測顯示EO組細胞上清中VEGF分泌較EN組明顯增加(P<0.05);ES組VEGF分泌較EN組減少(P<0.05)。應用VEGF中和抗體阻斷后,CREG過表達引起的EO通透性增加的現象明顯受到抑制。結論CREG過表達可能通過VEGF介導的信號途徑引起F-actin重構及VE-cadherin減少,使血管內皮細胞單層通透性增加。
E1A激活基因阻遏子; 血管內皮細胞; VE-cadherin; 細胞骨架; 通透性; 血管內皮生長因子
人類心肌血管新生治療為冠心病的治療提供了一種新的方法,通過調節血管的生成及增加心肌血管的密度,可以提高心肌的灌注,改善患者的癥狀和提高勞動能力[1]。血管內皮細胞骨架蛋白改變,內皮細胞收縮或回縮,血管內皮細胞黏附連接蛋白VE-cadherin破壞,細胞間隙增大,引起血管通透性增加則是血管新生序列事件中重要的始動環節。因此,闡明血管內皮通透性改變的機制,尋找促進血管新生調控的活性分子,對缺血性疾病的防治具有重要意義。
本室先前研究已證實[2-4],E1A激活基因阻遏子(cellular repressor of E1A-stimulated genes, CREG)在胚胎血管發育早期即開始表達,參與了血管發生的調控。并且,進一步研究證實,CREG是血管平滑肌細胞成熟分化的重要調控因子,參與了血管成熟穩態的調控。但目前關于CREG在血管內皮細胞中表達的生物學作用尚未見報道。本研究以體外培養的人血管ECs系(VE)為研究對象,應用逆轉錄病毒載體分別介導CREG在VE細胞中過表達及表達下調,觀察CREG表達對動脈ECs單層通透性的影響并探討其調控血管內皮細胞通透性的機制及其與內皮細胞血管新生的作用。
材 料 和 方 法
1材料
1.1主要試劑 抗CD31單克隆抗體購于Sigma;抗CREG多克隆抗體購于R&D;Biotin-BSA購于Sigma;異硫氰酸四甲基羅丹明-鬼筆環肽(TRITC-phalloidin)購于Sigma;抗VE-cadherin多克隆抗體購于Sigma;抗血管內皮生長因子(vascular endothe-lial growth factor,VEGF)中和抗體購于R&D。
1.2細胞來源 人血管ECs 細胞系VE購自ATCC,我室已建立感染pLNCX-CREG 逆轉錄病毒的過表達(over expressing)CREG 蛋白VE細胞株命名為EO、感染pLNCX-shRNA-CREG 病毒CREG表達沉默(suppression)的VE細胞株命名為ES;轉染的空載體對照組的VE細胞株命名為EN。上述細胞株均在含10%胎牛血清的DMEM培養液中培養,2-3 d傳代1次。
2方法
2.1Western blotting檢測CREG蛋白的表達 采用BCA法測定細胞裂解液中蛋白濃度,并進行SDS-PAGE、轉膜、抗體結合及顯色。Ⅰ抗為CREG多克隆抗體(1∶1 000),Ⅱ抗為HRP標記IgG(1∶2 000),按ECL試劑盒(Amersham)說明書進行檢測顯影。
2.2ECs單層通透性檢測 參照Essler等[5]建立的方法,用示蹤劑Biotin-BSA檢測ECs單層通透性變化。將ECs接種在12孔Transwell chamber (0.4 μm pore size,12 mm diameter)多聚碳脂濾膜的彌散模型中,每個小室鋪3×105個細胞,各設置2個復孔,置37 ℃、5%CO2的細胞培養箱培養,4 h后棄去未貼壁細胞,生長4 d細胞融合成單層后用于實驗。在上室中加入Biotin-BSA使其為終濃度為100 mg/L,作用30 min后,分別從下室取60 μL培養基置于96孔板,加入鏈霉親和素-過氧化物酶,TMB顯色10 min,然后加入2 mol/L H2SO450 μL終止反應,Bio-Rad 550型酶標儀在波長470 nm處檢測吸光度變化,實驗重復5次,取平均值。
2.3免疫熒光法檢測ECs的F-actin肌動蛋白的分布 將3組ECs接種于清潔滅菌的蓋玻片上,待生長融合至細胞單層后,用37 ℃的PBS洗3次,4%多聚甲醛磷酸緩沖液固定15 min,0.2% Triton X-100 通透15 min,加入1%BSA磷酸緩沖液封閉1 h,用100 μg/L的TRITC-phalloidin[TRITC最大吸收波長為(540±25) nm,最大發射波長為(608±32) nm]進行F-actin肌動蛋白染色,置暗處反應60 min,30%甘油-PBS封片,在熒光倒置顯微鏡下觀察肌動蛋白細胞骨架F-actin的分布變化。
2.4免疫熒光法檢測ECs黏附連接蛋白VE-cadherin改變 將3組ECs培養在清潔滅菌的蓋玻片上,待生長融合至細胞單層后,用37 ℃的PBS洗3次,4%多聚甲醛室溫固定20 min,0.2% Triton X-100室溫通透15 min,PBS洗滌3次后,5%山羊血清封閉30 min,加入抗人VE-cadherin抗體(1∶100)4 ℃孵育過夜,PBS洗滌3次,加入熒光標記Ⅱ抗(1∶100)室溫孵育2 h,PBS洗滌3次,甘油封片,在熒光倒置顯微鏡下觀察VE-cadherin表達的變化。
2.5酶聯免疫吸附實驗(ELISA)測ECs的VEGF分泌 將3組ECs在60 mm培養皿中融合至80%左右,棄去培養基,無菌PBS洗滌10 mL×3次,盡量吸盡殘留液體,加無血清的DMEM 4 mL(以盡量少的液體覆蓋細胞表面),置37 ℃、5% CO2的細胞培養箱繼續培養24 h后收集上清,進行VEGF的ELISA檢測,根據ELISA試劑盒說明書進行。實驗前以細胞計數結果校對上樣量,使上樣量保持一致。紫外透射儀讀取結果,每次實驗讀數取3個,重復5次。
2.6抗VEGF中和抗體阻斷實驗 同時應用抗VEGF中和抗體(0.5 mg/L)對3組內皮細胞預處理12 h,用Transwell chamber嵌套裝置按前述方法測定ECs單層的通透性。應用抗VEGF中和抗體(0.5 mg/L)對3組ECs預處理12 h后,按前述方法進行ECs肌動蛋白骨架F-actin及黏附連接蛋白VE-cadherin的免疫熒光染色及觀察。
3統計學處理

結 果
1Westernblotting檢測CREG蛋白的表達
結果顯示,ES組CREG表達量明顯減少,經計算CREG表達量為正常組的48.9%(對β-actin比值比為0.42±0.01,P<0.05)。EO組CREG表達量與對照組EN相比表達量明顯增高(1.20±0.03,P<0.05),增加了38.2%,見圖1。

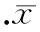
圖1Westernblotting檢測分析3組ECs的CREG表達量
2CREG過表達增加ECs單層的通透性
在Western blotting檢測上述各轉染組細胞中CREG的表達基礎上,應用示蹤劑Biotin-BSA檢測發現,CREG過表達的EO細胞單層通透性明顯增加(0.0490±0.0016),與EN對照組(0.0376±0.0061)比較差異顯著(P<0.05)。同時,CREG表達沉默的ES組單層通透性下降(0.0324±0.0114),與EN對照組(0.0376±0.0061)比較差異顯著(P<0.05),見圖2,結果提示CREG過表達引起內皮細胞通透性增加。
3CREG過表達引起ECs肌動蛋白骨架F-actin重排和VE-cadherin表達減少
應用激光共聚焦顯微鏡觀察,可見EN組細胞連接緊密,F-actin主要分布于細胞周邊,呈“花環”樣排列,少量呈細絲狀無序地分布于胞漿,核周偶有應力纖維形成。而CREG過表達的EO組細胞中的F-actin則明顯呈向心性回縮, F-actin邊聚現象消失,胞漿內的F-actin明顯增多,出現大量應力纖維,并呈典型的竹排樣結構。CREG表達沉默的ES組細胞中F-actin分布與EN組相似,主要分布于細胞周邊,中心也有少量分布。進一步應用免疫組化檢測細胞中黏附連接蛋白VE-cadherin,發現EN組和ES細胞中VE-cadherin在單層融合血管內皮細胞的周邊呈正常拉鏈狀排列,細胞之間連接緊密。EO組細胞中VE-cadherin分布明顯減少,同時細胞間隙增寬,見圖3。上述實驗結果提示,CREG過表達引起內皮細胞骨架蛋白重排和細胞間隙連接蛋白表達下降。

圖2Transwell測量3組ECs通透性的結果

Figure 3. Immunocytochemical staining of F-actin and VE-cadherin in different groups.
圖3免疫熒光染色觀察3組ECs的F-actin及VE-cadherin的變化
4VEGF介導CREG誘導的血管內皮通透性改變
ELISA檢測3組細胞上清中VEGF的結果顯示,與EN組(577.20±10.43) ng/L相比,CREG過表達的EO組細胞中VEGF分泌最高(1 392.00±5.83) ng/L,而CREG沉默的ES中VEGF最低(391.40±4.04),三者(EO組、EN組、ES組)間差異顯著(P<0.05),見圖4。加入VEGF中和抗體后,EO組細胞單層通透性下降至(0.0388±0.0013)與處理前(0.0490±0.0017)比較差異顯著(P<0.05),見圖5A;同時細胞F-actin應力纖維解聚,見圖5B,VE-cadherin回復為細胞周邊拉鏈狀分布,見圖5C。


圖4ELISA方法檢測培養基中VEGF的分泌

圖5VEGF中和抗體對CREG誘導ECs通透性改變及F-actin、VE-cadherin表達的影響
討 論
CREG是1998年Gill等首次從HeLa細胞系克隆出來的,研究證實CREG是一種分泌型糖蛋白,其在多種細胞中發揮抑制增殖和促進分化的作用。我室前期研究表明CREG過表達可通過PI3K-Akt途徑促進體外培養的人動脈ECs的遷移;可通過PI3K途徑促進動脈ECs的增殖[6]。由此我們可以推測CREG可能是正常血管維持穩態的重要調控蛋白,對于血管正常生理功能起重要作用。
本實驗研究表明,CREG過表達可誘導ECs通透性增加,促進ECs的VEGF分泌。CREG引起ECs通透性增高時,一方面,ECs的肌動蛋白細胞骨架解聚,出現大量的應力纖維,加入VEGF中和抗體后,F-actin分布向細胞膜處轉移,細胞內應力纖維形成有所減少;另一方面,EO組ECs的VE-cadherin在ECs周邊的正常鏈狀染色減少或脫失,加入VEGF中和抗體后,VE-cadherin在血管內皮細胞周邊的正常染色增多,提示CREG引起F-actin重新分布、VE-cadherin在ECs周邊的正常鏈狀染色減少或脫失及增加血管內皮細胞通透性的作用可能是通過VEGF介導來實現的。CREG表達下調可減低ECs通透性,減少ECs的VEGF分泌,使F-actin主要分布在ECs周邊,VE-cadherin在ECs周邊呈正常鏈狀染色,連接緊密,與EO組加入VEGF中和抗體后的表現相似,進一步證實VEGF在CREG引起ECs單層通透性增高中介導的作用。促進心肌缺血區血管新生的能力,進而限制損傷區域,是缺血性心臟病治療的一個重要方法。ECs通透性增高是血管新生的一個重要環節,可使血漿蛋白溢出血管外,導致纖維蛋白在血管外凝結,形成血管生成的臨時基質。這些基質一方面促進血管的生成,另一方面促使一些間質細胞進一步形成成熟的血管基質,從而有利于血管的生成。 因此探討ECs通透性改變及其機制研究尤為重要,目前認為ECs單層通透性變化與F-actin的重新分布及VE-cadherin表達的減少和脫失有關。F-actin的變化可通過VE-cadherin的鏈狀結構影響黏附連接,使ECs間裂隙和內皮通透性發生改變[7,8]。
總之,CREG作為一種新的具有維持血管穩態的重要調控蛋白,其大量表達可以增加ECs的VEGF表達,而VEGF是一種特異性作用于血管ECs表面受體的生長因子,能夠維持血管正常狀態和完整性,增加血管通透性,誘導血管發生并促進血管生成[9]。目前的研究表明CREG能夠促進ECs的增殖和遷移[6],而ECs穿過周圍細胞外基質增殖和遷移是血管新生事件中的一個重要環節[10]。因此,CREG可以用于缺血性心肌梗死的促血管新生的治療。基于VEGF表達時程,在心肌梗死中血管生成活動可能是一個延遲反應,那么,VEGF在亞急性及慢性階段是否可以應用CREG調控VEGF的表達從而充分利用內源性VEGF并獲得長期且最佳效果有待進一步探討。隨著醫學科學發展,CREG有望成為缺血性心臟病治療的又一可靠、有效的手段。
[1] Stegmann TJ, Hoppert T, Schneider A, et al.Induction of myocardial neoangiogenesis by human growth factors. A new therapeutic approach in coronary heart disease[J].Herz,2000,25(6):589-599.
[2] 韓雅玲,閆承慧,劉海偉,等. E1A激活基因阻遏子過表達誘導體外培養大鼠平滑肌細胞分化[J]. 生物化學與生物物理進展, 2004, 31(12):1099-1105.
[3] 韓雅玲,鄧 捷,梁 明,等. 逆轉錄病毒介導的E1A激活基因阻遏子抑制大鼠頸動脈球囊損傷后新生內膜形成[J]. 中國病理生理雜志, 2007, 23(10):1873-1877.
[4] Han Y, Guo L, Yan C, et al. Adenovirus-mediated intra-arterial delivery of cellular repressor of E1A-stimulated genes inhibits neointima formation in rabbits after balloon injury[J]. J Vasc Surg, 2008, 48(1):201-209.
[5] Essler M,Retzer M,Bauer M,et al.Mildly oxidized low density lipoprotein induced contraction of human endothelial cells through activation of Rho/Rho kinase and inhibition of myosin light chain phosatase[J].J Biol Chem,1999,274(43):30361-30364.
[6] 陶 杰.CREG基因調控人動脈內皮細胞遷移和增殖的作用及其機制研究[D].西安:第四軍醫大學,2009,49-60.
[7] Mackay DJ, Hall A. Rho GTPases[J].J Biol Chem,1998,273(33):20685-20688.
[8] Thurston G,Turner D.Thrombin-induced increase of F-actin in human umbilical vein endothelial cells[J].Microvasc Res,1994,47(1):1-20.
[9] 陳 勇,周正炎,季振威,等.組織修復中血管內皮生長因子作用及應用的研究進展[J].同濟大學學報,2003,24(4):285-288.
[10]李樹巖,李淑梅,董明慧,等.VEGF基因轉染同種異體骨髓間充質干細胞治療心肌梗死的實驗研究[J].中國老年學雜志,2007,27(7):622-625.
EffectsofcellularrepressorofE1A-stimulatedgenesonVEGFreleaseandmonolayerpermeabilityofhumanvascularendothelialcells
WANG Zhan-sheng2, HAN Ya-ling1, KANG Jian1, ZHANG Xiao-lin1, TAO Jie1, TIAN Xiao-xiang1, YAN Cheng-hui1
(1DepartmentofCardiology,GeneralHospitalofShenyangCommandofPLA,Shenyang110016,China;2DalianMedicalUniversity,Dalian116044,China.E-mail:wzs20700079@163.com)
AIM: To study the effects and mechanism of cellular repressor of E1A-stimulated genes (CREG) on VEGF release and monolayer permeability of human vascular endothelial cells (ECs).METHODSThe monolayer permeability of ECs was measured by transwell chamber model. The expression and localization of F-actin and VE-cadherin were examined by immunofluroscence using Olympus IX-70 fluorescent microscope. Enzyme-linked immunosorbent assay (ELISA) were performed to determine the concentration of vascular endothelial growth factors(VEGF) in the culture medium. VEGF neutrilization antibody was used to block the expression of VEGF in the cells.RESULTSThe monolayer permeability of CREG over-expressing ECs (EO group) was significantly higher than that of the normal control ECs (EN group,P<0.05). The monolayer permeability of CREG suppressing ECs (ES group) was lower than that in EN group (P<0.05). F-actin cytoskeleton in EO group showed disorganized, polymerized and bundled obviously to form large quantity of stress fibers in the central portion of the cells, whereas F-actin in EO group was mainly observed in the peripheral portion of the cells and only small amounts in the central portion of the cells. A widespread gap formation and a loss of VE-cadherin staining at the periphery were found in the cells of EO group. Inversely, the cells in ES group showed the localization of VE-cadherin at the cell-cell contacts tightly and the formation of zipper-like structures. Compared with EN group, the secretion of VEGF in the cell culture supernatants increased in EO group, but decreased in ES group (P<0.05). Furthermore, the changes of ECs permeability, cytoskeleton reorganization and loss of VE-cadherin induced by CREG were abolished by the addition of anti-VEGF neutralizing antibody.CONCLUSIONCREG over-expression increases the monolayer permeability of ECs, induces the cytoskeleton reorganization and reduces VE-cadherin expression by enhancing the secretion of VEGFinvitro.
Cellular repressor of E1A-stimulated genese; Vascular endothelial cells; VE-cadherin; Cytoskeleton; Permeability; Vascular endothelial growth factor
R363
A
10.3969/j.issn.1000-4718.2011.01.007
1000-4718(2011)01-0037-05
2010-04-13
2010-09-03
國家自然科學基金資助項目(No.30770793; No.30971218; No.30800465)
△通訊作者Tel:024-23056183; E-mail: wzs20700079@163.com

