二氫生物喋呤還原酶參與調控HEK293T細胞自噬作用的初步研究
古艷婷,趙婷婷,李 平,張浩軍,朱 斌,韓文兵,董 晞,費 敏,孫斯凡
(1.北京協和醫學院,北京 100021;2.衛生部中日友好醫院臨床醫學研究所,北京 100029)
糖尿病腎病的發病機制復雜,至今仍未完全闡明。許多研究認為糖尿病腎病時存在著自噬活性的下調,自噬途徑受到抑制可導致細胞內受損的細胞器或蛋白大量積聚,足細胞完整性受到破壞、腎小管上皮細胞損傷及腎肥大等病理進程,參與了DN的發生發展[1],而自噬激活對腎損傷有保護作用并可維持足細胞完整性。課題組在前期差異蛋白質組學中發現,二氫生物喋呤還原酶(dihydropteridine reductase,QDPR)在自發性II型糖尿病模型OLETF大鼠腎臟損害時的氨基酸發生突變,但該基因產物是否參與糖尿病腎病的發生發展還未有報道。本研究構建了野生型和突變型的QDPR重組質粒初步探討了二氫生物喋呤還原酶對自噬作用的影響,以期為深入研究其在糖尿病腎病發病機制中的作用奠定基礎。
1 材料和方法
1.1 材料
HEK 293T細胞、綠色熒光蛋白(GFP)為中日友好醫院臨床醫學研究所藥物藥理室保存;真核表達載體pcDNA3.1/V5-His(美國Invitrogen公司);新型pUM-T快速克隆試劑盒(北京百泰克生物技術有限公司)、大腸桿菌DH5α感受態細胞(北京鼎國昌盛生物技術有限公司);高保真PCR擴增試劑盒(德國Roche公司),T4 DNA連接酶、限制性內切酶EcoR V、Pst I、Xba I(美國NewEngland Biolabs公司);限制性內切酶Xba I、逆轉錄試劑盒(加拿大Fermentas公司);凝膠回收純化試劑盒、質粒中提試劑盒(德國QIAGEN公司);DNA Maker DM5000(北京康為世紀生物技術有限公司);鼠單抗V5抗體(美國Invitrogen公司);兔多抗LC3(美國Sigma公司),兔多抗Beclin1抗體(美國Sigma-Aldrich公司),山羊抗小鼠IgG抗體(美國Abcam公司);羊抗兔IgG抗體(美國Abcam公司);Western Lightening ECL(美國Perkin Elmer公司);胎牛血清(美國GIBCO公司);高糖DMEM培養基干粉(美國GICBO-BRL公司)。
1.2 野生型和突變型QDPR重組質粒的構建
1.2.1 引物設計與RT-PCR擴增 根據 G eneBank中大鼠QDPR mRNA序列設計引物,上游引物引入EcoR V酶切位點,下游引物引入 X ba I酶切位點,由北京擎科生物技術有限公司合成。引物序列如下:上游5'-AGATATCTGGCGGCTTCGGGCGAGGC-3';下游5'-ATCTAGAGAAATAGGCTGGAGTAAGCT-3',分別以正常LETO大鼠與OLETF糖尿病大鼠腎臟皮質cDNA為模板,采用高保真PCR試劑盒擴增正常QDPR以及突變QDPR cDNA片段,PCR反應體系(50μL)中上、下游引物各1μL,cDNA 2μL。反應條件為:94℃預變性2 m in;94℃變性30 s;54℃退火30 s;72℃延伸1 m in;共循環32次后72℃延伸10 m in。對PCR產物用1.2%瓊脂糖凝膠電泳進行分離,之后進行回收純化,-20℃保存。
1.2.2 pUM-T克隆 PCR產物回收純化后克隆至pUM-T載體,轉化到 D H5α感受態細胞,挑選陽性單克隆進行酶切鑒定及測序。
1.2.3 重組質粒的構建 用EcoR V、Xba I雙酶切QDPR/pUM-T獲得QDPR目的片段;用EcoR V、Xba I雙酶切 p cDNA3.1/V5-His作為載體。用 T 4DNA連接酶連接目的片段與載體,構建野生型 r QDPR/ pcDNA3.1/V5-His重組質粒(rQDPRwt)和突變型rQDPR/pcDNA3.1/V5-His重組質粒(rQDPRmut)。
1.3 HEK293T細胞轉染及分組
HEK 293T細胞常規培養于含10%胎牛血清的DMEM培養基中,于轉染前24 h傳代,以2x106/孔的細胞密度接種于 1 0 cm培養皿中,在37℃、5%CO2條件下培養24 h,細胞貼壁后利用磷酸鈣共沉淀法轉染,共轉染3次。實驗分組:野生型重組質粒組(rQDPRw t組),突變型重組質粒組(rQDPRmut組),pcDNA3.1/V5-His載 體組(control vector組)。綠色熒光蛋白(GFP)作為轉染效率的參照物,轉染72 h后倒置熒光顯微鏡下觀察轉染效率。
1.4 RT-PCR檢測LC3,Beclin1轉錄水平表達
轉染72 h后收集細胞,Trizol法提取細胞總RNA。取2μg RNA進行反轉錄,按Fermentas cDNA反轉錄試盒的步驟進行。PCR采用立陶宛MBl公司試劑盒PCR反應擴增,以CyclophilinB作為內參照。各引物序列見表1。PCR反應體系(12.5μL)中上、下游引物各0.5μL,cDNA 2μL。反應條件為:94℃預變性2 min;94℃變性30 s;退火30 s(LC3為52℃,Beclin1為56℃);72℃延伸45 s;共循環35次后72℃延伸10 min。PCR產物在2%瓊脂糖凝膠上電泳,用凝膠成像系統觀察條帶,以目的條帶吸光度值與CyclophilinB吸光度值比值作為目的產物的半定量值,Image J軟件進行分析。
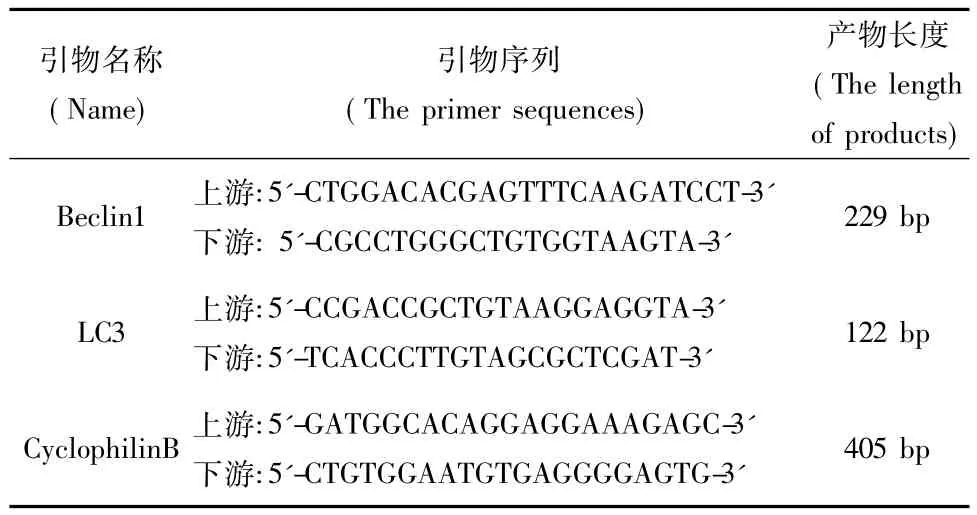
表1 PCR引物序列及產物長度Tab.1 The primer sequences and the length of products
1.5 WesternBlot檢測測LC3I,II,Beclin1蛋白水平表達
轉染72 h后收集細胞,吸棄培養液,PBS輕洗,加入預冷的細胞裂解液,冰浴10 min后移至離心管,超聲離心,分光光度計進行蛋白定量。分別取60μg蛋白樣品進行SDS-PAGE電泳并電轉移至PVDF膜,5 g/L脫脂奶粉封閉2 h,TBST洗膜,用鼠單抗V5抗體(1∶5000),LC3抗體(1:2000),Beclin1抗體(1∶2000)及抗β-actin抗體(1∶2000),4℃過夜。山羊抗鼠IgG(1∶10000),山羊抗兔IgG (1∶3000)孵育1 h,TBST洗膜3次后ECL化學發光顯色后顯影。ImageJ軟件進行分析吸光度(A)值,并計算LC3I,II和Beclin1的A值與β-actin A值的比值,分析各組LC3 I,II和Beclin1蛋白的相對表達水平。
1.6 統計學方法 數據資料用(±SD)
表示,采用SPSS 16.0統計軟件對數據進行處理。組間差異采用One-way ANOVA,P<0.05有統計學意義。
2 結果
2.1 重組質粒鑒定結果
重組質粒構建后經酶切鑒定,結果顯示酶切條帶與預期一致,野生型重組質粒測序結果與GeneBank BLAST比較后證實為QDPR cDNA序列,突變型重組質粒測序結果也顯示突變位置正確,說明野生型和突變型重組質粒構建成功(數據未顯示)。
2.2 WesternBlot檢測融合蛋白水平表達
轉染72 h后收集細胞蛋白,用鼠單抗V5抗體檢測到rQDPRwt組和rQDPRmut組融合蛋白的表達,對照組未見目的蛋白表達,見圖1。結果表明野生型和突變型重組質粒能夠在HEK 293T細胞中正確表達。
2.3 QDPR高表達以及QDPR突變高表達后對LC3,Beclin1mRNA水平的影響

圖1 Western blot檢測轉染后融合蛋白表達Fig.1 The detection of fusion protein after transfection
野生型QDPR重組質粒和突變型QDPR重組質粒轉染細胞72 h后,RT-PCR檢測結果顯示,與對照組相比,rQDPRwt組LC3 mRNA表達水平顯著上調(P<0.05),Beclin1表達水平無統計學意義,rQDPRmut組與對照組相比LC3和Beclin1表達水平差異均無統計學意義(P>0.05)。(圖2,3)。
2.4 QDPR高表達以及QDPR突變高表達后對LC3,Beclin1蛋白水平的影響
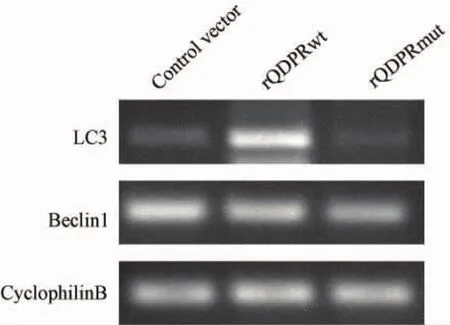
圖2 QDPR對LC3和Beclin1 mRNA表達的影響Fig.2 The effect of QDPR on the mRNAlevel of LC3 and Beclin1
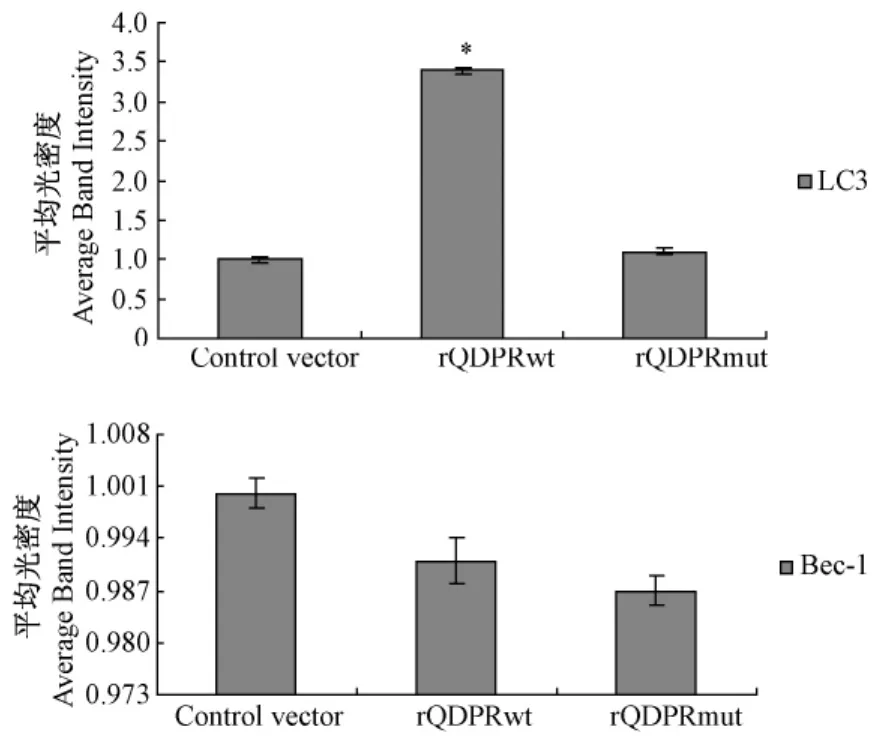
圖3 QDPR對LC3和Beclin1 mRNA表達影響的半定量分析(*P<0.05 vs.control)Fig.3 The semiquantitative analysis of QDPR on the mRNA level of LC3 and Beclin1(*P<0.05 vs.control)
野生型QDPR重組質粒和突變型QDPR重組質粒轉染細胞72 h后,Western blot檢測結果顯示,與對照組相比,rQDPRwt組LC3和Beclin1蛋白表達量顯著上調(P<0.05),rQDPRmut組LC3和Beclin1表達差異無統計學意義(P>0.05)。(圖4,5)。
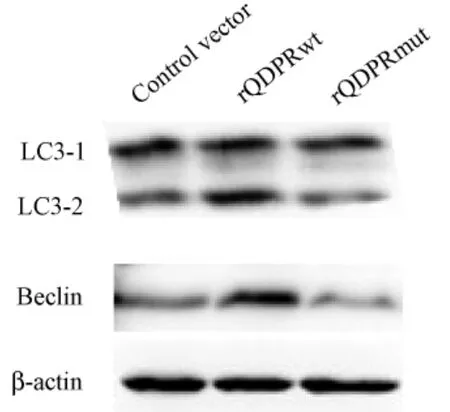
圖4 QDPR對LC3和Beclin1蛋白表達的影響Fig.4 The effect of QDPR on proteinlevel of LC3 and Beclin1
3 討論
二氫生物喋呤還原酶蛋白以二聚體形式在動物體內廣泛分布[2],該酶在四氫生物喋呤(tetrahydrobiopterin,BH4)再生過程中起到重要作用,其主要功能是催化醌型二氫生物喋呤(quinonoid dihydrobiopterin,qBH2)還原成BH4,對維持體內BH4含量穩定有著重要意義[3]。BH4生理功能廣泛,而這些生理功能和DN的發生關系密切。BH4是3種一氧化氮合酶(nitric oxide syhthase,NOS)激活所必需的輔助因子,而NOS是體內NO產量的主要來源[4]。有研究表明NO和自噬有密切關系[5]。課題組在前期差異蛋白質組學研究中發現,與正常LETO大鼠相比,自發性II型糖尿病模型OLETF大鼠QDPR基因發生突變,但該基因是否參與糖尿病及其并發癥的發生發展有待進一步研究。
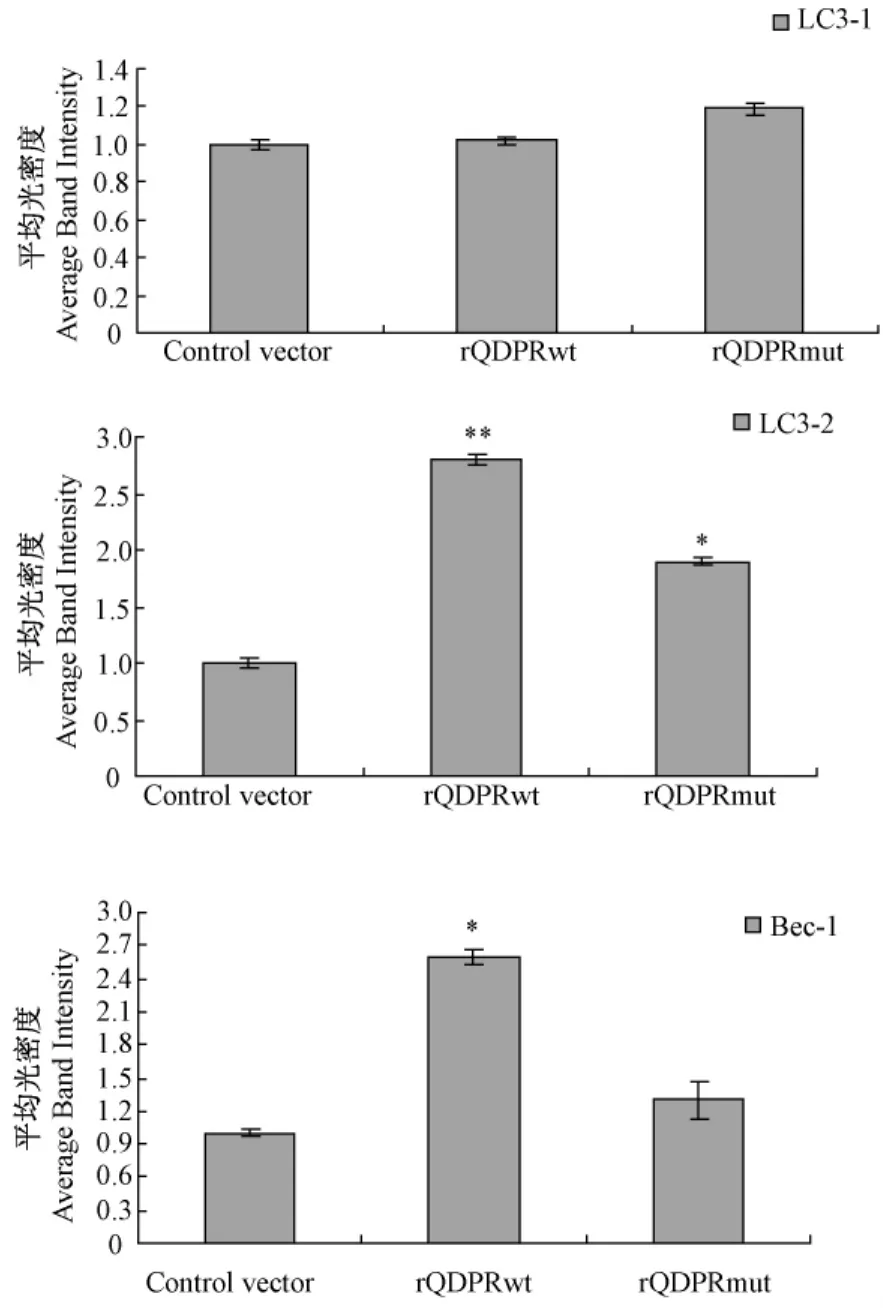
圖5 QDPR對LC3和Beclin1蛋白表達影響的半定量分析(*P<0.05 vs.control,**P<0.01 vs.control)Fig.5 The semiquantitative analysis of QDPR on proteinlevel of LC3 and Beclin1(*P<0.05 vs.control,**P<0.01 vs.control)
自噬是細胞通過溶酶體對自身結構的吞噬降解過程,主要是清除、降解細胞內受損傷的細胞結構、不需要的生物大分子以及衰老的細胞器等,同時也為細胞器的構建提供原料[6]。然而,過度的自噬也會引起細胞的損傷或死亡。因此,自噬對細胞的作用具有兩面性[7]。近年來有研究顯示在STZ誘導的1型DN大鼠腎組織自噬標志分子LC3-2明顯降低,糖尿病腎病存在著自噬活性的下調,而自噬激活在腎損傷中可能發揮著細胞保護作用[8]。自噬作用可通過Western blotting檢測自噬蛋白LC3和的Beclin-1表達量等方法來反映。LC3前體(proLC3)在蛋白水解酶的作用下剪切C末端形成LC3I,最后經泛素樣加工修飾過程成為與磷脂酰乙醇胺(PE)結合的LC3II,能靶向定位于自噬體膜,參與自噬的形成[9]。目前認為LC3II是自噬體的標志分子,是代表自噬作用的主要指標。Beclin-l基因是哺乳動物最早發現的一個自噬基因,其表達強度與自噬活性密切相關[10]。本研究通過構建QDPR野生型和突變型重組質粒,觀察了QDPR對HEK293T細胞自噬作用的影響,結果顯示野生型QDPR重組質粒組LC3II水平和Beclin-l水平顯著高于對照組和突變組,提示QDPR可能誘導自噬活性或者使發生自噬的潛能增加,當其93位氨基酸突變后對自噬的這一調控作用下降。由此我們推測QDPR可能和糖尿病腎病的發生發展有關,并且課題組發現的QDPR突變位點可能是其調控自噬作用的關鍵位點。但是它是如何調控自噬并參與疾病的具體分子機制還不清楚,有可能是通過影響NO的生成和氧化應激的一些變化或某些信號轉導機制來完成,但在疾病中究竟發揮了何種作用,目前仍在探索,也是我們下一步研究的方向。
[1]Barbosa JA,Zhou H,Hultenschmidt D,et al.Inhibition of cellular autophagy in proximal tubular cells of the kidney in streptozotocin-diabetic and uninephrectomized rats[J].Virchows Arch B Cell Pathol Incl Mol Pathol,1992,61(6):359-366.
[2]Thony B,Auerbach G,and Blau N.Tetrahydrobiopterin biosynthesis,regeneration and functions[J].Biochem J,2000, 347(Pt1):1-16.
[3]Rakovich T,Boland C,Bernstein I,et al.Queuosine deficiency in eukaryotes compromises tyrosine production through increased tetrahydrobiopterin oxidation[J].J Biol Chem.,2011 286 (14):doi:10.1074/jbc.M111.219576.
[4]Katusic ZS,Duscio LV,and Nath KA.Vascular protection by tetrahydrobiopterin:progress and therapeutic prospects[J].Trends Pharmacol Sci,2009,30(1):48-54.
[5]Sovan S,Viktor IK,Maurizio R,et al.Complex Inhibitory Effects of Nitric Oxide on Autophagy.Molecular Cell,2011,43:19-32.
[6]Klionsky DJ,Abeliovich H,Agostinis P,et al.Guidelines for the use and int erpret at ion of assays formonitoring aut ophagy in higher eukaryotes[J].Autophagy,2008,4(2):151-175.
[7]Mathew R,Kongara S,Beaudoin B,et al.Autophage suppresses tumor progression by limiting chromosomal instablity[J].Genes Dev,2007,21(11):1367-1381.
[8]Wu WH,Zhang MP,Zhang F,et al.The role of programmed cell death in streptozotocin-induced early diabetic nephropathy[J].JEndocrinol Invest,2011,34(9):e296-301.
[9]Mizushima N.Methods for monitoring autophagy[J].Int.J Biochem CeIIBiol,2004,36(12):2491-2502.
[10]Kabeya Y,Mizushima N,Ueno T,et al.LC3,a mammaIian homologue of yeast Apg8p,is localized in autophagosome membranes after processing[J].EMBO J,2000,19(21):5720 -5728.

