缺血再灌注損傷大鼠腦組織細胞因子VEGF mRNA的變化及通心絡對其的影響1)
盧昌均,鹿俊磊,安紅偉,劉國成,周哲屹,韋冰心,陸兵勛,尹瑞雪,王立新
血管內皮生長因子(VEGF)是一種內皮細胞特異的強效有絲分裂原[1]。缺血性腦損傷后,盡早恢復缺血半暗帶的血供有助于神經功能的恢復。腦缺血再灌注損傷時,VEGF可通過與其受體結合發揮促進血管內皮細胞的增殖作用,加速新生血管的形成。因此,制作大鼠缺血再灌注損傷(MCAO)模型,采用反轉錄集合酶鏈式反應(RT-PCR)檢測缺血再灌注損傷后不同時間點神經干細胞增殖分化相關細胞因子VEGF mRNA的變化,并研究通心絡膠囊對其表達的影響,探討通心絡膠囊在缺血性腦損傷中的神經保護作用。
1 材料與方法
1.1 栓線制備 采用3-0號尼龍線,線頭一端用酒精燈將其燙成球形,在需要長度處折彎作標記,將此線浸泡消毒后,栓線頭端浸入0.1%多聚賴氨酸溶液中過夜,60℃烤箱中1h后取出,然后浸入1.25×104U肝素鹽水中備用。
1.2 動物模型制作 選用健康雄性SD大鼠180只,體重250 g±20g,南方醫科大學實驗動物中心提供。隨機分為缺血再灌注3d、5d、14d、30d共四批次進行,每批次隨機分為通心絡劑量組、缺血再灌注模型對照組(等量的生理鹽水)和假手術組,每組12只。參考改良的線栓法大鼠缺血性及缺血再灌注模型改進。放入栓線后用消毒鋼尺量自頸總動脈分叉處的血管外線長度,計算栓線實際的進入長度。在穿刺點外5mm剪斷殘留的栓線,埋于胸鎖乳突肌下。手術后縫皮,消毒切口,在缺血后90 min拔出線栓形成缺血再灌注動物模型。根據經典的Zea Longa神經功能評分法評分(5級4分法)[2]。除假手術組外,各組選取造模后6h神經功能缺損評分在2分以上的大鼠納人試驗研究,癥狀輕微(0分及1分)的大鼠剔除。假手術組也插入栓線,但深度為10mm左右,不阻塞大腦中動脈。術后大鼠自由進食、進水,在約20℃的空調環境下單籠飼養。
1.3 給藥方法 先將通心絡膠囊內容物溶于蒸餾水中配成溶液,通心絡組按每只1g/(kg·d)給藥,MCAO模型對照組、假手術組用等量蒸餾水分別灌胃,每組大鼠在再灌注清醒后即灌胃給藥,每日2次,給藥時間分別為3d、5d、14d、30d。
1.4 腦組織制備 將每組大鼠于末次腹腔注射BrdU后24h,在10%水合氯醛麻醉下,迅速斷頭取出腦組織,放入特制的小盒內,緩緩平放入盛有液氮的小杯中,當盒底接觸液氮時即開始氣化沸騰,10s~20s后腦組織迅速冰結成塊,取出腦組織冰塊立即置入-70℃冰箱中備用。
1.5 腦組織總RNA提純分離 大鼠缺血再灌注后3d、5d、7 d和14d、21d、30d各組腦缺血側、缺血對側區腦組織,以及通心絡治療后缺血側腦組織,提取總RNA。進行RT-PCR及半定量分析,以2% 瓊脂糖-TBE凝膠電泳,凝膠成像系統成像;采用gel pro軟件分析,以目的片段與β-actin的光密度比值(D)作為目的片段mRNA的相對含量,分離PCR產物,以DL-2000Marker為參照物。
引物設計:參考Genbank核普酸序列資料,應用Oligo5.0軟件程序設計有意義引物,由北京賽百盛基因技術有限公司合成純化。其具體設計如下:
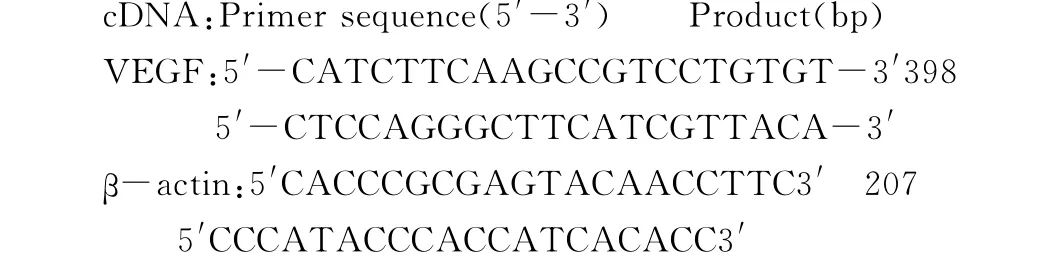
2 結 果
2.1 腦組織總RNA的提取結果 二條分別代表RNA的18 s,28s清晰條帶,電泳圖譜28s和18s酶比值約為2∶1,說明實驗中的RNA完整無降解。
2.2 缺血再灌注模型組與通心絡組VEGF mRNA表達 假手術組幾乎檢測不到VEGF mRNA的表達;大鼠腦缺血再灌注后在病灶對側僅見少量VEGF mRNA表達;缺血再灌注模型組及通心絡組病灶側VEGF mRNA在不同時間段均有表達,并隨時間延長其表達增加,第5、7天最高,第14天時表達開始下降,但通心絡組同一時間點VEGF mRNA的表達均較模型組增強。
3 討 論
缺血性腦損傷后,動脈血管閉塞而致局部腦血流減少,腦組織缺血、缺氧,產生神經組織損傷。缺血半暗帶的理論是由Astrup等1981年根據動物實驗首次提出的,此區域存在側支循環,部分血流可供應此區域,尚有大量神經元存活,如果血液迅速恢復,腦代謝得以改善,損傷仍然可逆,神經細胞仍可存活并恢復功能,這種可逆性取決于血管的新生和側支循環的形成。腦缺血再灌注損傷時,VEGF可通過與其受體結合而促進血管內皮細胞的增殖,加速新生血管的形成,提高血管通透性,并以自分泌、旁分泌和胞內分泌的方式特異地作用于血管內皮細胞受體,促進內皮細胞生長、增殖、遷移、細胞外基質降解、血管管型結構形成[3]。
缺血半暗帶在缺血性腦損傷后雖然有神經功能的缺失,但仍有潛在的存活能力,神經細胞仍可存活并恢復功能,因此,急性腦梗死治療的關鍵是保護這些可逆性的神經元。有研究發現[4],VEGF促進梗死區周圍血管側支循環的建立,改善了血流動力學狀況和疾病預后。在新生血管生成方面VEGF及其受體具有特異性,因此在缺血性腦損傷中,研究VEGF及其受體對神經細胞保護作用已成為目前國內外研究的熱點。VEGF參與許多中樞神經系統疾病,包括中風、腦缺血的神經保護。最近的研究表明,VEGF增強缺血后的神經再生[5]。缺血或缺氧可促使VEGF及其受體的mRNA和蛋白表達、生物活性均增加[6]。本實驗提示,缺血損傷組在術后第3天即可檢測到VEGF的表達,第5天達到高峰,第14天VEGF的表達開始下降,第30天恢復到基線水平;而假手術組幾乎檢測不到VEGF的表達,從而證實了缺血性腦損傷誘導了VEGF的表達。
祖國傳統醫學將本病歸屬于缺血性中風的范疇,國家中醫藥管理局腦病急癥協作組將中風病定位在腦和腦脈,指出缺血性中風的病機是腦脈痹阻,與致病因素瘀最為緊密,因此治療此病的方法為活血化瘀藥,通過活血、疏通血脈、祛痰通絡從而達到治療目的。通心絡膠囊是目前臨床上治療缺血性腦血管病的常用藥物,在治療缺血性腦血管疾病中己經取得了顯著療效;但其作用機制及作用靶點尚不完全清楚。本研究以通心絡為干預因素,觀察VEGF在通心絡組及缺血對照組中變化,結果顯示:通心絡能夠促進神經功能的恢復,降低缺血后神經功能的評分,使VEGF mRNA表達明顯增加,從而推斷通心絡膠囊能夠激活神經干細胞的增殖或者分化,促進VEGF基因的表達,這可能是通心絡膠囊治療缺血性腦血管疾病的機制之一。
VEGF表達的調控可能涉及多種機制,包括受一系列激素、生長因子和細胞因子的調節,受一些癌基因、抑癌基因的表達產物調節,特別是缺血、缺氧的刺激作用[7],缺血性腦損傷通過誘導VEGF的表達而發揮血管生成和神經保護的作用。本實驗提示,通心絡可能通過促進VEGF大量表達,使新生血管的形成增加及側支循環的建立,降低了神經功能的缺失,這為臨床運用通心絡治療缺血性腦血管病提供了有利的證據。本實驗還觀察到,在各時間點缺血對照組VEGF基因表達水平均低于通心絡組,通心絡組5d后VEGF mRNA開始增加,晚于缺血對照組,在以后的各時間點觀察值均高于缺血對照組,一直持續到第30天;而對照組VEGF mRNA表達已回歸至基線水平。因此,推斷通心絡中的某種成分可能促進了細胞表達VEGF或者表達該基因的細胞增加,但其具體機制還不清楚。本實驗僅研究了通心絡在基因水平對VEGF mRNA表達的影響,對于其在蛋白水平的表達尚未涉及;具體通心絡中何種成分發揮作用,以及其作用機制如何尚有待進一步的探討。
[1] Ferrara N.History of discovery:Vascular endothelial growth factor[J].Arterioscler Thromb Vasc Boil,2009,29(1):22-24.
[2] Longa EZ,Weinstein PR,Carlson S,et al.Reversible middle cerebral artery occlusion without craniectomy in rats[J].Stroke,1989,20(1):84-91.
[3] Cook KM,Figg WD.Angiogenesis inhibitions:Current strategies and future prospects[J].Ca Cancer J Clin,2010,60(4):222-243.
[4] Lanfranconi S,Locatelli F,Corti S,et al.Growth factors in ischemic stroke[J].J Cell Mol Med,2011,15(8):1645-1687.
[5] Ma Yihui,Qu Yan,Fei Zhou.Vascular endothelial growth factor in cerebral ischemia[J].J Neu Res,2011,89(7):969-978.
[6] 周榮峰,鄧茜.芪棱湯對腦缺血再灌注損傷大鼠VEGF、CD34的影響[J].中國中醫急癥,2011,6(20):922-923.
[7] 謝婧,魏有東.阿托伐他汀抑制急性腦梗死患者炎癥反應與增強血管修復[J].醫學研究雜志,2010,39(6):82-84.

