消融前靜息心率對房顫導管消融復發的影響
張麗利,李學文,王 群,劉向東,郝大潔
心房顫動是臨床最常見且嚴重的快速性心律失常,據報道歐洲患病人數約有(5.5~7)百萬人[1,2],我國的患病人數約8百萬人,高患病率已促使人們探尋更好的方法來治療及預測房顫發生。目前治療房顫的有效手段為導管消融技術,為提高手術的成功率,有眾多研究探討了影響房顫導管消融復發的預測因素。近年來,心率在房顫發病機制中的重要作用越來越受到重視,但消融前靜息心率對心房顫動導管消融復發的影響還少有報道。本研究探討了消融前靜息心率對房顫導管消融復發的預測價值。
1 資料與方法
1.1 研究對象及消融前靜息心率測定 入選2010年1月—2011年12月入院后在三維電解剖標測系統(CARTO,Biosense Webster)指導下首次行環肺靜脈線性消融的陣發性房顫患者。排除標準:經食道超聲發現左心房血栓;有風濕性心臟病或先天性心臟病;既往行房顫射頻消融治療。共入選40例,其中男23例,女17例,年齡56.8歲±11.2歲(37歲~78歲),伴高血壓7例。所有患者在術前做12導聯動態心電圖測消融前平均靜息心率。
1.2 電生理檢查和消融過程 已用華法林者術前至少停用3 d,并改用低分子肝素代替至術前12h;術前停用抗心律失常藥物至少5個半衰期以上;所有患者簽署術前知情同意書;在空腹狀態下實施手術。穿刺右側頸內靜脈放置冠狀靜脈竇電極,穿刺右側股靜脈2次,行房間隔穿刺入左房后首劑給予普通肝素5 000U,然后每小時追加1 000U,并用肝素鹽水持續沖洗鞘管。行左、右肺靜脈造影后,在三維電解剖標測系統指導下,通過專用標測消融導管在左房取點行左房及肺靜脈三維解剖重建,在Carto2Merge指導下行環肺靜脈線性消融。消融參數設定:功率(35~40)W,預設溫度40℃~45℃,放電時生理鹽水灌注速度17mL/min。消融時給予患者異丙酚鎮痛,消融終點為實現肺靜脈電隔離,陣發性房顫消融結束后房顫不能誘發。
1.3 術后處理與隨訪 消融術后流食一周;口服抗心律失常藥物及華法林抗凝至少3個月;維持國際標準化比值在1.8~2.5;術后3個月行12導聯心電圖及24h動態心電圖檢查。
1.4 房顫復發判定標準 消融術后100d~120d為本試驗評估房顫復發的時期。內容包括:行24h動態心電圖檢查;癥狀發作時行心電圖檢查。心電圖和24h動態心電圖等客觀檢查發現的持續時間超過30s的快速型房性心律失常。
1.5 統計學處理 采用SPSS13.0統計軟件分析,計量資料以均數±標準差(±s)表示,組間計數資料行卡方檢驗,計量資料比較采用t檢驗分析,以雙側檢驗P<0.05為有統計學意義。
2 結 果
所有患者均完成射頻消融術,術后100d~120d隨訪期內,40例中有4例(10%)房顫復發。將40例分為復發組和未復發組,復發組與未復發兩組資料比較詳見表1。配對t檢驗分析,消融前靜息心率在復發與未復發組間差異無統計學意義(P=0.16)。消融前靜息心率與消融后靜息心率差別也無統計學意義。兩組間年齡、性別、高血壓比例差異無統計學意義。
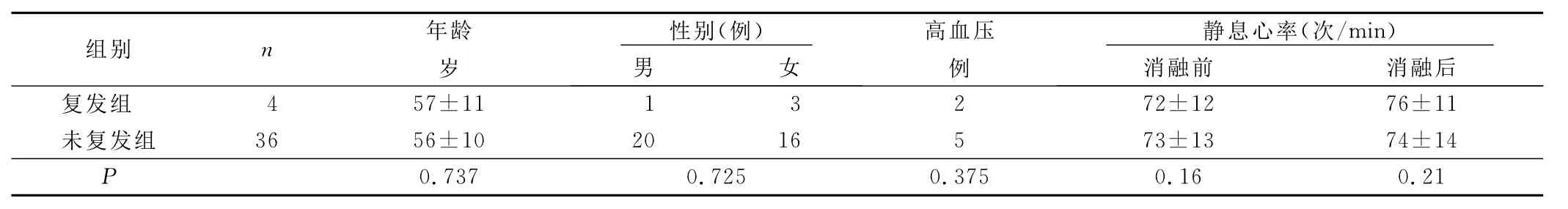
表1 復發組與未復發組資料比較
3 討 論
房顫患者心率過快時可使心臟每搏輸出量減少,射血分數下降,心肌做功增加,耗氧增加甚至出現心力衰竭。目前認為適當地降低房顫患者的心率,可有效減少房顫的發生率,同時還減緩了心房肌電重構的發生和隨之產生的心房肌纖維化程度。根據多數RCT的研究,心室率控制已成為多項臨床指南推薦的一線治療方案,AHA~ACC/ESC2006指南推薦目標心率為靜息時心率控制在<80次/min,中等活動量時心率應控制在<110次/min[3],此推薦目標就是建立在竇性心律時心率較慢的患者臨床癥狀較少的推論上[4]。
本研究中,心房顫動患者均接受環肺靜脈線性消融電學隔離肺靜脈手術治療成功率高,并發癥如肺靜脈狹窄發生率低[5-7],應用心電圖和動態心電圖作為房顫復發的隨訪手段,防止遺漏無癥狀房顫的存在,低估了房顫的復發率[8]。另外,由于陣發性房顫與持續性房顫的病理生理基礎不同,故導管消融治療的方法、成功率存在差異。對于陣發性房顫,肺靜脈為最常見的觸發灶,因此隔離肺靜脈成為主要消融方法[9]。鑒于持續性房顫手術更為復雜,受影響因素多等原因,本研究在選取資料時已將其排除。心率可以影響房顫的發生,但尚未影響房顫導管消融的成功率。本研究顯示消融前靜息心率不影響肺靜脈隔離后房顫的復發,提示肺靜脈的異常電活動仍是觸發房顫最重要的機制。本研究根據24h動態心電圖測心房顫動患者術后3個月后平均心率差異無統計學意義,考慮與樣本選取量較少有關。
本研究還存在許多不足,如排除了持續性房顫患者,而這些患者可能受益更多等。因此,探討消融前靜息心率的研究仍需繼續。
[1]Benjamin EJ,Wolf PA,D’Agostino RB,etal.Impact of atrial fibrillation Oil the risk of death:The Framingham Heart Study[J].Circulation,1998,98:946-952.
[2]Stewart S,Hart CL,Hole DJ,etal.A population based study of the long term risks associated with atrial fibriilation:20year follow-up of the Renfrew/Paisley study[J].Am J Med,2002,113:359-364.
[3]Fuster V,Rydem LE,Cannom DS,etal.ACC/AHA/ESC 2006 guidelines for the management of patients with atrial fibrillation:A report of the American College of Cardiology/American Heart Association task force on practice guidelines and the European Society of cardiology committee for practice guidelines(writing committee to revise the 2001guidelines for the management of patients with atrial fibrillation):Developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society[J].Circulation,2006,114(7):e257-e354.
[4]Dorian P.Rate control in atrial fibrillation[J].N Engl J Med,2010,362(15):1439-1441.
[5]Pappone C,Rosanio S,Oreto G,etal.Circumferential radio frequency ablation of pulmonary vein ostia a new an atomic approach for curing atrial fibrillation[J].Circulation,2000,102:2619-2628.
[6]Khaykin Y,Marrouche NF,Saliba W,etal.Pulmonary vein antrumisolation for treatment of atrial fibrillation in patients with valvular heart disease or prior open heart surgery[J].Heart Rhythm,2004,1:33-39.
[7]Ouyang F,Bnsch D,Ernst S,etal.Complete isolation of left atrium surrounding the pulmonary veins:New in sights from the double Lasso technique in paroxysmal atrial fibrillation[J].Circulation,2004,110:2090-2096.
[8]Senatore G,Stabile G,Bertaglia E,etal.Role of trans telephonicelectro cardiographic monitoring in detecting short term arrhythmia recurrences after radio frequency ablation in patients with atrial fibrillation[J].J Am Coll Cardiol,2005,45:873.
[9]Ouyang F,Antz M,Ernst S,etal.Recovered pulmonary vein conduction as a dominant fact or for recurrent atrial tachyarrhythmia as after complete circular isolation of the pulmonary veins:Lessons from double Lasso technique[J].Circulation,2005,111:127-135.

