鉻鐵礦酸溶生產三價鉻化合物
紀 柱
(中海油天津化工研究設計院,天津 300131)
鉻鐵礦是制取各種鉻化合物的唯一天然原料,其含鉻成分稱為鉻尖晶石 (Mg,Fe)[Cr,Fe,Al]2O4,晶胞中Fe2+可被氧化,導致晶格畸變,穩定性下降,有利于鉻尖晶石參與化學反應。從鉻鐵礦生產鉻化合物的基本路線有下面3種。
第一種為堿性氧化路線,即鉻鐵礦同堿在空氣或純氧中反應,三價鉻氧化為六價鉻(鉻酸鈉),鉻酸鈉易制取重鉻酸鈉及其他價態的鉻化合物。其中焙燒法由于具有良好的選擇性,即礦石中僅鉻以陰離子形式生成水溶性的鉻酸鈉,占鉻鐵礦質量1/2以上的雜質均以水不溶物殘留在浸取渣中,致后續工藝變得簡捷易行。此工藝路線已工業化200 a。目前堿性氧化路線所產鉻化合物超過鉻化合物總產量的95%。
第二種為高溫還原路線,即鉻鐵礦在電爐內用焦炭還原制成碳素鉻鐵。全球工業開采的鉻鐵礦92%用于冶金,其中絕大部分消費在冶煉碳素鉻鐵。盡管目前碳素鉻鐵主要用于生產不銹鋼,但由碳素鉻鐵硫酸溶解后制某些三價鉻鹽以及進而電解生產金屬鉻早已工業化;碳素鉻鐵經堿性氧化(無鈣焙燒法、水熱法)生產鉻酸鈉已完成工業試驗。冶煉碳素鉻鐵無疑是鉻鐵礦的高效富集法,除鐵外礦中雜質基本清除,故用碳素鉻鐵加工制鉻化合物正引起學者的重視。
鉻在鉻尖晶石中處于三價態,占鉻化合物消費量1/2以上的氧化鉻、堿式硫酸鉻,用作中間體的醋酸鉻、氯化鉻,以及正在醫藥、保健品和飼料添加劑、油氣田開采等領域快速發展的氨基酸鉻、有機酸鉻均處于三價狀態。故若由第一或第二種路線制取三價鉻化合物,必須先對鉻鐵礦分別進行氧化制得鉻酸鈉或還原成碳素鉻鐵之后,再反過來將鉻酸鈉還原為三價鉻或將碳素鉻鐵氧化為三價鉻,這種價態的反復改變造成了資源、能源和人力的浪費。
第三種路線簡稱酸溶法,即鉻鐵礦直接同硫酸反應制得硫酸鉻溶液,經分離雜質和復分解制成其他三價鉻化合物,鉻的價態不變。此法理論上最為合理,只需酸溶,無需氧化或還原等反應激烈工序。但因鉻尖晶石極耐化學侵蝕,即使用過量沸騰濃硫酸長時間反應亦難以全溶;而且礦中雜質除硅不溶外,鐵、鋁、鎂等亦同時酸溶,而溶液中三價的鉻、鐵、鋁離子由于離子半徑和電負性近似,許多化學性質相差無幾,難以廉價高效分離,致使得到的硫酸鉻無論在品質上還是在成本上均無法與第一種路線競爭,故迄今此工藝尚未工業化。但隨著科學的發展和節能降耗的要求越來越高,酸溶法重新得到重視,并出現了一些新技術。
1 鉻鐵礦酸溶
鉻尖晶石耐化學侵蝕,常用的強酸如硫酸、鹽酸、硝酸在常壓和沸點難以將其全溶,磷酸、磷酸加硫酸的混酸在沸點雖可使鉻鐵礦全溶,但磷酸根難以分離,且不免生成難溶的磷酸鹽或焦磷酸鹽,不利于制取純凈的鉻化合物。
E.Vardar 等[1]曾引述 W.J.Biermann 等[2]研究了硫酸對鉻鐵礦的侵蝕作用,反應機理為質子H+攻擊鉻鐵礦晶格,使金屬成分依它們在晶格中占據的同樣比例進入溶液;隨著硫酸濃度的增加形成水及酸均不溶解的多核產物(包括硫酸鉻沉淀)。A.M.Amer[3]研究了硫酸加壓浸取鉻鐵礦,得到的最佳條件為:鉻鐵礦粒度小于64 μm,用質量分數為50%的硫酸于250℃浸取30 min。
如果在強酸中加入具有氧化作用的催化劑,則鉻鐵礦得以較快、較完全地溶解。其原因之一是鉻尖晶石中的Fe2+首先被氧化為Fe3+,致晶格畸變而穩定性下降,易被酸侵蝕。文獻所用催化劑均為常用氧化劑,其催化首先表現在氧化作用,但氧化的效果常大于作為單純氧化劑的效果,故本文采用催化-氧化劑連用的寫法。
高氯酸就是這種催化-氧化劑的一例。高氯酸既是最強無機酸,又是極強的氧化劑,故常作為鉻礦石化驗用的溶劑之一,例如鉻礦石分析的國際標準ISO 6130—1985《鉻礦石總鐵含量的測定——還原滴定法》就是用硝酸、硫酸和高氯酸的混酸溶解鉻鐵礦后測定礦中總鐵。但是高氯酸易揮發,高氯酸同鉻生成劇毒的氣體氯化鉻酰CrO2Cl2導致鉻揮發損失。另外高氯酸價格高昂,少量用作催化劑尚可,大量用作溶劑不適于工業生產。
E.Vardar等[1]使用表1組成的南非鉻鐵礦同硫酸、高氯酸于140~210℃進行反應,研究了硫酸鉻生成動力學,查明反應的控制步驟為界面化學反應,使用質量分數為82%的硫酸于140~210℃的反應活化能為77 kJ/mol,得出鉻溶浸的最佳條件:1)僅使用硫酸時,在硫酸質量分數為77%、固液質量比為1∶25、210℃浸取 6 h條件下,鉻的浸出率為 66%;2)加高氯酸(HClO4質量分數為70%)時,在硫酸質量分數為82%、固液質量比為1∶25、高氯酸體積(mL)與鉻鐵礦質量(g)的比值取0.5、210℃浸取6 h條件下,鉻可全溶。
A.Geveci等[4]也用硫酸、高氯酸對表 1 組成的土耳其鉻精礦進行了溶解研究,得出以下結論:1)無高氯酸時,在硫酸體積分數為70%、于175℃浸取2 h條件下得到最大鉻收率約58%;2)加高氯酸時,當高氯酸體積(mL)與鉻鐵礦質量(g)之比為0.5,在相同硫酸濃度和溫度浸取2 h,得到最大鉻收率約83%;3)無論有無高氯酸,鉻收率均低于E.Vardar等[1]得到的收率;4)高氯酸能使部分三價鉻氧化,既使是最大收率時,溶液中六價鉻濃度依然很低;5)加高氯酸條件下,鉻收率最大的固體渣經X射線衍射分析證明存在明顯量的固體硫酸鉻Cr2(SO4)3。

表1 南非鉻鐵礦和土耳其鉻精礦組成%
同樣使用硫酸和高氯酸溶解鉻鐵礦,A.Geveci等[4]的鉻收率低于E.Vardar等[1],其原因 A.Geveci等[4]認為是所用土耳其鉻精礦的組成與南非鉻鐵礦不同,土耳其礦MgO和SiO2含量高于南非礦。但根據后面第3節介紹可推定更主要的原因是南非礦的亞鐵(FeO)含量是土耳其礦的3.2倍,在高氯酸作用下,亞鐵氧化引起南非礦鉻尖晶石晶格畸變更大,更不穩定,更易溶解。
John C.Stauter 等[5]研究了用海錳核(深海底發現的球核狀錳礦)或天然錳礦為催化-氧化劑,對鉻鐵礦進行硫酸溶解試驗。10 g鉻礦與海錳核(MnO2質量分數為28.3%)混磨至粒徑小于220 μm,海錳核與鉻礦的質量比取(0.1~1)∶1。與不同量濃硫酸在燒杯中混勻,然后置于罐爐于350~400℃加熱10 min至水分蒸發剛冒出硫酸煙霧時停止加熱。冷至60℃并在此溫度浸取攪拌3 h。海錳核與鉻礦的質量比為1∶1時隨硫酸量及溫度不同鉻浸出率為81.9%~100%。經核算,海錳核中二氧化錳同時發揮了催化劑及氧化劑作用,致被氧化的三價鉻高達(二氧化錳僅為氧化劑)理論量的2倍。
前引文獻中提到在高濃度硫酸中無水硫酸鉻溶解性低,A.Geveci等[4]在溶解后的渣中證實存在固體 Cr2(SO4)3,這些不溶物必然不同程度地滯留在反應界面(待反應的鉻尖晶石表面),不利于鉻鐵礦進一步溶解。與鉻鐵礦酸溶性類似的碳素鉻鐵,在硫酸中溶解時亦有硫酸鉻沉淀,為防止沉積,Bruno München Wenzel等[6]在高碳鉻鐵生產鞣革劑硫酸鐵和硫酸鉻的研究中,使用了硫酸銨同硫酸鉻形成易水溶的鉻銨礬,當碳素鉻鐵用質量分數為75%的硫酸于170℃溶解2 h,若加入生成鉻銨礬理論量100%的硫酸銨時,鉻溶出率由不用硫酸銨時的87.5%增大到接近100%;鐵溶出率亦有增加。預計在鉻鐵礦酸溶時,硫酸銨理應有同樣的催化作用。
2 鉻酸酐在鉻鐵礦酸溶時的催化-氧化作用
鉻鐵礦酸溶使用最多的催化劑是價格廉宜又不帶入雜質的鉻酸酐。實際上不用硫酸只用鉻酸水溶液亦可溶解鉻鐵礦,如:1974年美國專利(US, 3787555),將鉻鐵礦在空氣中預氧化,使90%的Fe2+氧化為Fe3+,然后同質量分數為50%的CrO3水溶液于沸點反應24 h,鉻鐵礦分解率為76%。
波格達洛夫[7]引述,早在1940年前蘇聯應用化學雜志就報道,將粒度為2.0 mm的鉻精礦1 t,用質量分數為60%的硫酸3.78 m3和催化劑鉻酸酐11.72 kg于140~150℃溶浸,濾液進行陽極氧化、蒸發析出晶體鉻酸酐,離心過濾得到0.4825 t鉻酸酐,鉻收率為68.3%。
E.Vardar等[1]引述了 R.R.Lloyd 等[8]制電解鉻的半工業試驗,即鉻鐵礦用質量分數為40%的硫酸溶液于130~160℃的熱壓釜內溶浸,加2.5%~3.0%(質量分數)的鉻酸(H2CrO4)作催化劑。
史培陽等[9]用質量分數為60%~95%的硫酸于110~170℃同鉻鐵礦反應,鉻鐵礦粒度為0.05~0.09 mm,硫酸質量為鉻鐵礦質量的的1~4倍,用重鉻酸鈉為催化劑,其量為鉻鐵礦質量的4%~20%,反應時間為1~8 h,經過濾、除鐵、調堿度、干燥得到堿式硫酸鉻,鉻收率為79%~82%。
劉承軍等[10]研究了硫酸加入量對鉻鐵礦硫酸浸出行為的影響,使用Cr2O3質量分數為40.0%、總Fe質量分數為7.7%的巴基斯坦鉻鐵礦,鉻鐵礦與硫酸的質量比取1.5~3.0,加入鉻鐵礦質量5%的鉻酸酐作催化劑,于160℃反應60 min。其結論:隨著硫酸用量的增加鉻浸出率逐漸增大,鉻鐵礦與硫酸的質量比為3.0時鉻浸出率為98.5%[11];但鐵的浸出率隨著硫酸用量的增加先增加后減小,在鉻鐵礦與硫酸的質量比 2.5時呈現極大值 70.1%[10]或71.9%[11]。
劉承軍等[12]采用水熱法溶解鉻鐵礦。例如:粒度為100 μm的鉻鐵礦(Cr2O3質量分數為40.0%、Fe2O3質量分數為11%),加入質量分數為68%的硫酸,其量為鉻礦質量的1.0倍,加入鉻礦質量3.2%的鉻酸酐作催化劑,于155℃、0.7 MPa壓力下反應60 min,攪拌速度為250 r/min。反應完成后用板框壓濾機于1.6 MPa過濾,濾渣中鉻的質量分數低于0.3%。
以上使用鉻酸酐作催化劑的文獻既未說明鉻酸酐用量的依據,亦未說明鉻酸酐加入量與鉻收率之間的關系,且各文獻用量極不一致。波格達洛夫[7]認為,前引鉻精礦用硫酸和鉻酸酐溶浸的鉻收率過低(68.3%)的原因是鉻酸酐用量太少,只占鉻精礦質量的1.17%,或者對于鉻精礦中FeO質量來說,僅為后者的8.64%,而按照下面所示的反應式:
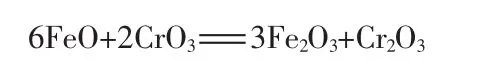
要將1 g FeO氧化為Fe2O3,需用0.464 g鉻酸酐,因此,波格達洛夫提出鉻酸酐的用量必需為鉻礦中FeO質量的70%~100%,才能將鉻鐵礦充分溶解得到高收率。
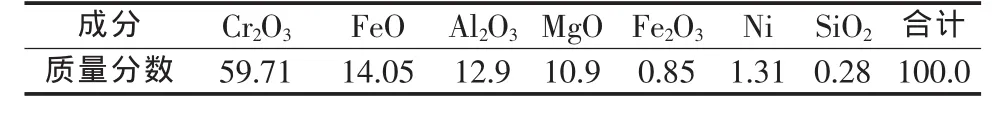
表2 重選得到的鉻精礦 %
波格達洛夫[7]利用重選得到的鉻精礦1000 g(組成見表 2)進行了一批試驗,鉻精礦粒度為2.0 mm,用3.7 L質量分數為60%的硫酸和不同量鉻酸酐組成的溶液于140~150℃溶浸,然后離心分離、洗滌。當鉻酸酐加入量相對于鉻精礦中FeO質量分數分別為9.11%、66.2%、70.0%、99.64%、100.8%、106.8%時,鉻收率分別為65.8%、75.0%、78.4%、86.48%、86.58%、86.67%。數據說明,催化劑鉻酸酐用量如果與鉻礦中FeO質量相同,鉻浸出率超過86%。
3 從浸出液中分離鉻
3.1 脫硅
將硫酸浸取后的懸浮液過濾、洗滌可以濾除不溶物,包括未溶解的鉻鐵礦、石英SiO2,以及酸溶過程中副產的不溶物,如某些硅酸鹽類脈石酸溶后生成的水合硅酸及其鹽,可以阻止硅進入浸出液。
3.2 除鐵
濾除不溶物后的濾液主要成分為鉻、鋁、鎂、鐵的硫酸鹽,若能除去鐵,調整堿度后經蒸發濃縮、噴霧干燥可制得鉻鞣革劑,這樣得到的鉻鞣革劑除含堿式硫酸鉻外,尚含鋁和鎂,鋁也有鞣革作用,鎂對鞣革無害。史培陽等[9]在溶解鉻鐵礦后的濾液中加碳酸鈉調游離堿至2.3%(質量分數),加氧化鈣加熱反應,過濾除去含鐵渣,濾液加碳酸鈉調堿度,干燥得到堿式硫酸鉻,產品的組成未交待。史培陽等[13]在7 a后公開的另一專利改用萃取分離法,即向Cr、Fe質量分數分別為7%、4%的硫酸鉻和硫酸鐵混合液中加入混合液體積30%的萃取劑十八烷基二甲基叔胺進行萃取,分層后硫酸鉻進入水相,硫酸鐵進入有機相。水相直接結晶得到硫酸鉻產品,含Cr2O3質量分數≥30%,含水不溶物、氯化物質量分數均≤0.01%,含Fe質量分數≤0.005%。有機相用氫氧化鈉反萃后制成氧化鐵紅顏料,顏料含Fe2O3質量分數≥96%。
3.3 鹽析法分離紫色硫酸鉻
溶液中的硫酸鉻因水合形式不同而有多種形態,10~30℃有利于生成紫色的六水合硫酸鉻[Cr(H2O)6]2(SO4)3。 紫色鹽在水中溶解度大,而在鹽析劑與水的混合溶劑中溶解度小。硫酸鐵恰好相反,故加入鹽析劑并熟化后,硫酸鉻可同硫酸鐵鹽析分離。例如,硫酸鉻與硫酸鐵的混合溶液含Cr質量濃度為40.6 g/L、Fe質量濃度為15.0 g/L,pH約為1,在15℃振動熟化24 h,硫酸鉻幾乎100%轉化為紫色鹽。加入鹽析劑即99.5%乙醇 (約為溶液質量的50%),于20℃振動4 h,紫色鹽便鹽析出來。分離后鐵及其他金屬雜質的硫酸鹽留在母液中,濾餅即紫色鹽析物于150℃干燥24 h,產品含Cr質量分數為25.77%、Fe質量分數為 0.36%,以 Cr2(SO4)3計的純度為97.13%,鉻收率為96.41%。反復多次鹽析及分離,硫酸鉻純度還可進一步提高[14]。
3.4 以六價鉻形式分離
脫硅后的含 Cr、Fe、Al、Mg 等陽離子的濾液,若能將鉻轉變為陰離子,則其他陽離子的分離便易于完成。 John C.Stauter等[5]以二氧化錳作催化-氧化劑,用硫酸溶解鉻鐵礦后的浸出液中的鉻為六價鉻(可補加二氧化錳將浸出液中殘存的三價鉻離子繼續氧化),溶液用萃取劑(體積組成為5%三辛叔胺溶液、5%起乳化作用的磷酸三丁酯、90%的煤油)萃取,六價鉻進入有機相,分離后的有機相用水洗滌殘留錳和鐵。有機層用氫氧化銨水溶液將鉻洗脫,得到鉻酸銨。波格達洛夫[7]將鉻精礦用硫酸、鉻酸酐溶液溶浸,濾洗后溶液用裝有隔膜和鉛陽極的電解槽于30~50℃電解。電解完成液于140~150℃蒸發至硫酸質量濃度為1100 g/L,鉻酸酐即結晶析出,離心分離,濾餅于140~150℃用硫酸(質量濃度為1140 g/L)洗滌。晶體鉻酸酐于150℃干燥即為產品,其CrO3質量分數為99.73%,SO42-質量分數為0.15%,不溶物質量分數為0.10%,鐵、鋁、鎂、鎳等氧化物雜質質量分數為0.02%,符合俄羅斯標準。
3.5 參考碳素鉻鐵酸溶后的鉻鐵分離經驗
碳素鉻鐵硫酸溶解時,生成硫酸鉻與硫酸亞鐵的溶液,一般采用莫爾鹽法將硫酸鉻與硫酸亞鐵分離。例如,鄔建輝等[15]在溶液pH為0.5、硫酸銨過量系數為3.0、Cr3+質量濃度為70 g/L左右、Fe2+質量濃度為5~20 g/L以及溫度為70℃的條件下反應6 h,然后快速冷卻結晶24 h,將析出的晶體硫酸亞鐵銨[Fe(NH4)2(SO4)2·6H2O]過濾,除鐵率達到 96.52%,鉻損失只有1.85%。
北京有色金屬研究總院提出用萃取法從碳素鉻鐵硫酸浸出液中回收鉻。例如,含Cr3+質量濃度為60~80 g/L、Fe2+質量濃度為25 g/L的硫酸鹽溶液,用伯胺 R,R′-CH-NH2作萃取劑 (R、R′代表 C8至 C12的烷基,平均相對分子質量為372),煤油作稀釋劑并加5%(體積分數)的混合醇,萃取劑體積分數為25%~30%。于最佳pH(2~3)萃取,硫酸亞鐵不被萃取,分離因子>200。進入有機相的 Cr3+用 2.5~3.0 mol/L的H2SO4反萃取,反萃率>98%,得到含Cr3+質量濃度為50 g/L、Fe質量濃度<0.05 g/L的硫酸鉻溶液。
胡國華[16]利用草酸作亞鐵的沉淀劑,可與三價鉻高效分離。將高碳鉻鐵硫酸溶解后的溶出液先用氨水調pH至3,加入草酸,使鐵以草酸亞鐵沉淀同硫酸鉻溶液分離;濾液再用氨水調pH至9,得到氫氧化鉻沉淀,經過濾、洗滌、干燥后煅燒得到氧化鉻,其含Fe質量分數為0.2%,鉻收率為98%。
韓登侖等[17]用無鈣焙燒渣制得的碳素鉻鐵硫酸溶出液生產草酸亞鐵,實現鉻鐵分離。將含有硫酸鉻和硫酸亞鐵的溶出液加到飽和的熱草酸溶液中,得到含草酸亞鐵99.0%(質量分數)的產品。往含少量Fe3+和Fe2+的硫酸鉻濾液中加適量金屬鉻細粉,將Fe3+還原為Fe2+,加入氫氧化鈉溶液至pH為7,生成氫氧化鉻沉淀,加絮凝劑后濾洗,得到的氫氧化鉻含Cr2O3質量分數為53.7%,含鐵(以Fe2O3計)質量分數<0.1%。
鉻鐵礦酸溶后,溶液中的鐵為三價,要利用上述技術以亞鐵形式同鉻分離,只需在鉻鐵礦直接酸溶后仍含過量硫酸的溶液中加入適量粉狀碳素鉻鐵或金屬鉻,反應析出的原子氫足以將溶液中的Fe3+還原為 Fe2+。
4 討論
綜上所述,提高鉻收率及鉻鐵分離已取得新進展,若能進一步深入研究,可望不久的將來實現酸溶法工業化。所引文獻中以下各項更為可取:1)選用品位(Cr2O3)高,亞鐵含量多,鋁、鎂、硅少的鉻精礦進行酸溶;2)使用硫酸、鉻酸酐混合溶液作浸取劑,嘗試用硫酸銨防止無水硫酸鉻沉積在反應界面;3)向懸浮液中加入粉狀高碳鉻鐵,借助高碳鉻鐵酸溶生成的原子氫將Fe3+還原為Fe2+,分離不溶物后的濾液以草酸為沉淀劑,使亞鐵生成FeC2O4沉淀;4)濾除FeC2O4后的濾液同堿反應,生成鉻和鋁的氫氧化物沉淀,沉淀同氫氧化鈉反應,將氫氧化鋁以鋁酸鈉形式溶解分離后,經晶種分解制得氫氧化鋁產品;5)濾洗后的氫氧化鉻經煅燒制成氧化鉻,或酸溶制成相應酸的三價鉻鹽。
[1]Vardar E,Eric R,Letowski F.Acid leaching of chromite[J].Miner.Eng.,1994,7(5/6):605-617.
[2]Biermann W J,Heinrichs M.The attack of chromite by sulphuric acid[J].Can.J.Chem.,1960,38(9):1449-1454.
[3]Amer A M.Processing of Ras-Shait chromite deposits[J].Hydrometallurgy,1992,28(1):29-43.
[4]Geveci A,Topkaya Y,Ayhan E.Sulfuric acid leaching of turkish chromite concentrate[J].Miner.Eng.,2002,15(11):885-888.
[5]Stauter John C,Um Richard T.Recovery of chromium values:US, 4029734[P].1977-06-14.
[6]Bruno München Wenzel,Nilson Romeu Marcilio,Marcelo Godinho,et al.Iron and chromium sulfates from ferrochromium alloy for tanning[J].Chem.Eng.J.(Amsterdam,Netherlands),2010,165(1):17-25.
[7]波格達洛夫.鉻酸酐制法:RU, 2349551[P].2009-03-20.
[8]LloydRR,Rosembaum JB,Homme VB,etal.Pilo-plamt production of electrolytic chromium[J].Trans.Electrochemical Soc.,1948,94(3):122-138.
[9]史培陽,姜茂發,劉承軍.一種堿式硫酸鉻的制備方法:中國, 1526646A[P].2004-09-08.
[10]劉承軍,史培陽.硫酸加入量對鉻鐵礦硫酸浸出行為的影響[J].工業加熱,2011,40(3):59-60,76.
[11]Liu Chengjun,Qi Jie,Jiang Maofa.Experimental study on sulfuric acid leaching behavior of chromite with different temperature[J].Advanced Materials Research(Durnten-Zurich,Switzerland),2012,361-363 (Pt.1,Natural Resources and Sustainable Development):628-631.
[12]劉承軍,史培陽,姜茂發.一種硫酸浸出處理鉻鐵礦的方法:中國, 101979679A[P].2011-02-23.
[13]史培陽,劉承軍,姜茂發.由多組分溶液中分離鉻離子和鐵離子的方法:中國, 101974688A[P].2011-02-16.
[14]悅周,熊谷幹郎,高島洋一.鉻的分離回收方法:日本公開,平 8157219[P].1996-06-18.
[15]鄔建輝,陽倫莊,湛菁,等.鉻鐵合金中鉻、鐵分離研究[J].濕法冶金,2011,30(1):51-56.
[16]胡國華.一種從碳素鉻鐵中生產三氧化二鉻和草酸亞鐵的方法:中國, 101041466A [P].2007-09-26.
[17]韓登侖,張忠元,何喜善,等.用無鈣鉻渣生產草酸亞鐵副產金屬鉻和鉻酸的方法:中國, 101445446B[P].2011-05-25.

