硫酸介質中天冬氨酸及天冬酰胺對N80碳鋼的緩蝕性能
錫林春, 張 弢, 劉 柳, 曹 賀, 劉 瑕
(沈陽化工大學應用化學學院,遼寧沈陽 110142)
在工業生產中,很多酸性介質對鋼鐵腐蝕非常嚴重,常引起設備的嚴重蝕損,給企業帶來巨大的經濟損失[1-5].添加緩蝕劑可有效地減緩酸性介質造成的腐蝕問題,因此加快緩蝕劑的開發與應用對建立節約型社會具有重大意義.近年來,酸性介質中鋼鐵有機緩蝕劑的研究已取得了重大進展,逐步從功能單一、緩蝕效率低、毒性大向多功能、緩蝕效率高、低毒性方面發展[6-11].氨基酸具有可生物降解性,對環境友好,是一種較有前途的綠色緩蝕劑[12-14].近年來,對氨基酸的研究也有報道,大多是天然的氨基酸[7-8].本文篩選2種價格相對廉價,含有多個吸電子基團的氨基酸:天冬氨酸和天冬酰胺為研究對象(結構式如圖1所示),研究其做為緩蝕劑在0.1 mol·L-1硫酸介質中對低碳鋼N80的緩蝕性能,并初步探討了緩蝕機理.
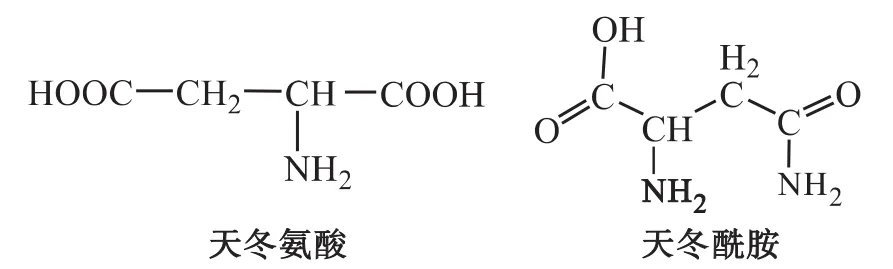
圖1 天冬氨酸及天冬酰胺的結構式Fig.1 Structural formula of D-Aspartic Acid and L-Asparagine
1 實驗部分
實驗材料為N80碳鋼,其化學成分見表1.除工作表面(1 cm2)外,其余部分均用聚四氟乙烯密封,工作表面經金相砂紙逐級打磨,再拋光成鏡面,依次用水、丙酮、無水乙醇擦拭,干燥備用.電化學測量采用三電極體系,輔助電極為硅碳棒,參比電極為飽和甘汞電極.
電化學儀器是上海辰華儀器公司生產的CHI604C.其中線性掃描速率為0.166 mV·s-1,掃描范圍為自腐蝕電位±10 mV.電化學阻抗譜測試頻率范圍為10 mHz~20 kHz,交流激勵信號幅值為5 mV.天冬氨酸和天冬酰胺兩種氨基酸均為A.R,實驗介質為 0.1 mol·L-1的 H2SO4.
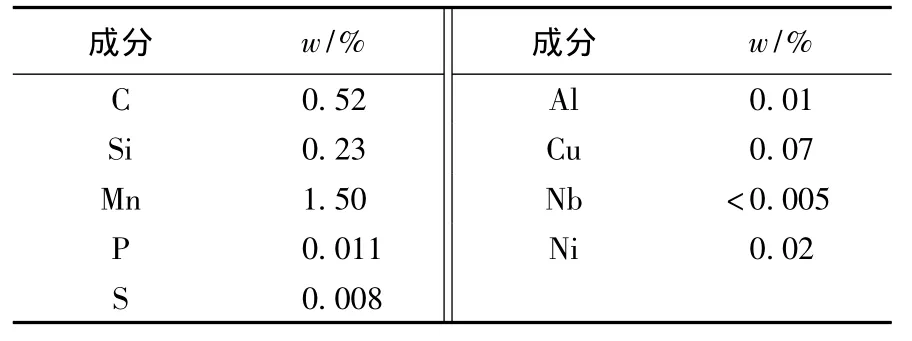
表1 N80的化學成分Table 1 N80 chemical composition
2 結果與討論
2.1 極化曲線
測試在0.1 mol·L-1硫酸空白溶液及加入不同濃度的2種氨基酸緩蝕劑的N80碳鋼的極化曲線,結果見圖2和表2.從圖2可以看出:對空白溶液,在陽極低極化電位下,鋼片的溶解主要受電荷傳遞過程控制.而在含有緩蝕劑的硫酸介質中,電極的腐蝕電位相對于空白體系中的明顯負移,陽極溶解反應和陰極氫的反應在不同程度上都受到了抑制,但比較而言陰極過程的抑制作用更大,這說明它們為陰極型緩蝕劑.
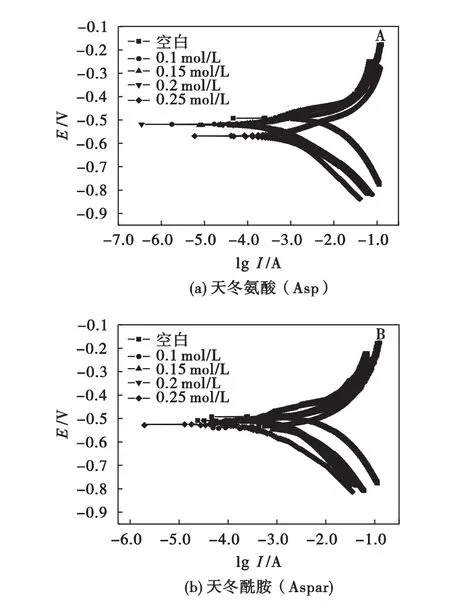
圖2 緩蝕劑對N80低碳鋼電極在0.1 mol·L-1H2SO4溶液中的極化曲線Fig.2 Polarization curves of N80 mild steel exposed in 0.1 mol·L-1H2SO4solution without or with different concentration inhibitor
Tafel直線外推法常用于測定酸性溶液中金屬腐蝕速度及緩蝕劑的影響,由此方法得到相關的腐蝕電化學參數,腐蝕電位(Ecorr)、腐蝕電流密度(Icorr),腐蝕電流密度應用切線法得取,緩蝕劑的緩蝕效率I可按公式
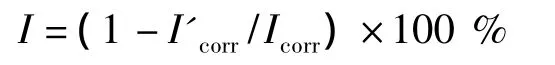
求出.式中Icorr和I'corr分別為金屬在不含緩蝕劑的溶液(也稱為空白溶液)中和添加了緩蝕劑的腐蝕介質中的腐蝕電流密度.擬合計算結果列于表2.
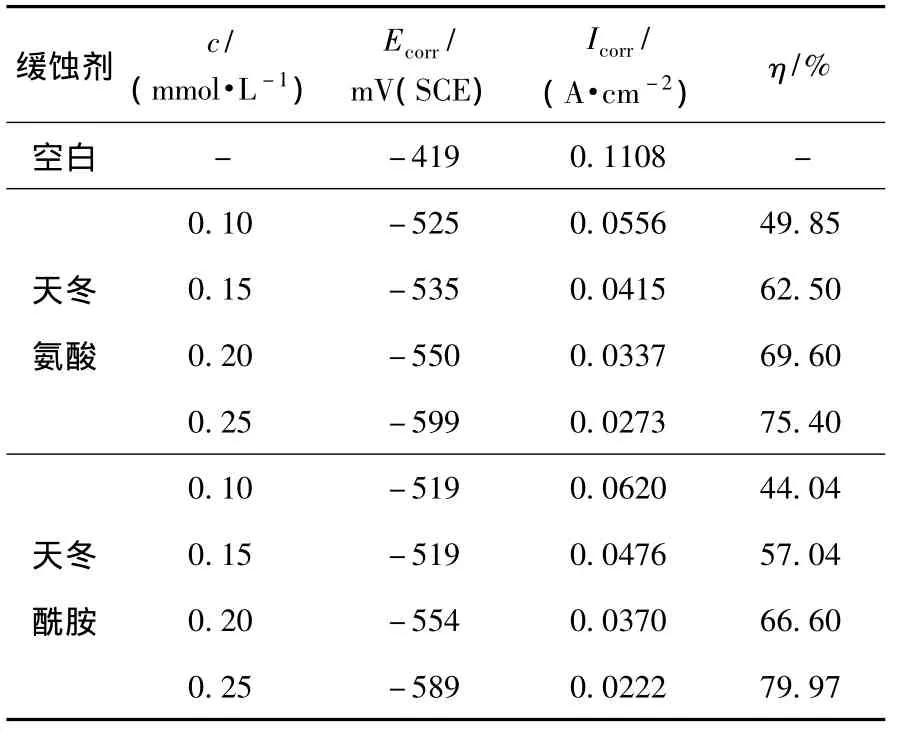
表2 N80低碳鋼在0.1 mol·L-1H2SO4溶液中電化學參數擬合結果Table 2 Fitting results of the electrochemical parameters of N80 mild steel exposed in 0.1 mol·L-1 H2SO4solution without and with inhibitor
由圖2和表2可知,緩蝕劑的加入使體系的自腐蝕電位負移,腐蝕電流密度大大減少 ,2種緩蝕劑都隨緩蝕劑濃度的增大而緩蝕效率增大,且天冬酰胺的緩蝕效率高于天冬氨酸.
2.2 交流阻抗
N80碳鋼在含有2種緩蝕劑的0.1 mol·L-1硫酸溶液中的Nyquist圖如圖3所示.
圖4是阻抗譜的等效模擬電路圖,其中Cd是電極溶液界面電容,Rs為溶液電阻,Rt為N80碳鋼腐蝕反應傳遞電阻,Rf和Cf是由吸附過程所引起的吸附電阻和吸附電容,用來表征由于吸附引起的電極表面狀態變化而產生的第2個容抗弧,L是電感 .擬合數據列于表3.緩蝕效率計算公式為:
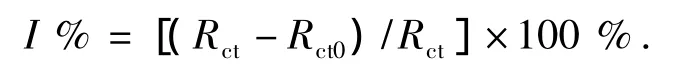
式中Rct和Rct0分別為在有和無緩蝕劑的溶液中測得的極化電阻.
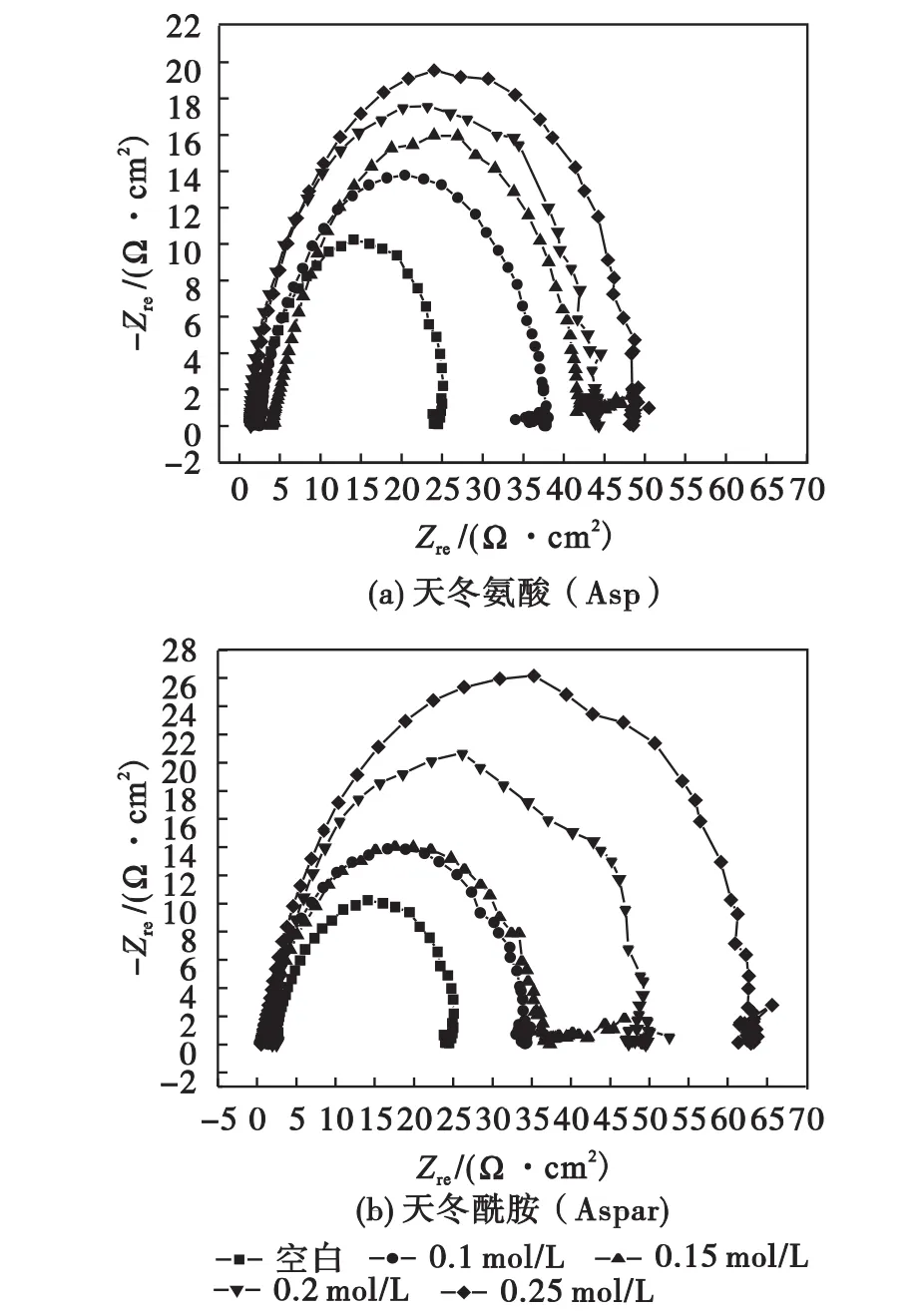
圖3 N80低碳鋼在包含不同濃度緩蝕劑的0.1mol·L-1H2SO4中的 Nyquist阻抗圖Fig.3 Nyquist impedance plot for N80 mild steel in 0.1 mol·L-1H2SO4containing different concentrations
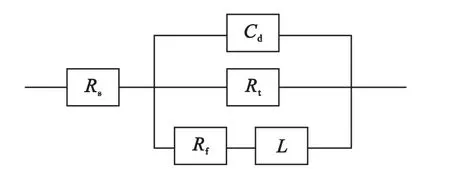
圖4 阻抗譜的等效模擬電圖Fig.4 Equivalent circuit model used to represent the impedance results
從圖3可以看出:阻抗譜中出現一個容抗弧,隨著緩蝕劑濃度的增加容抗弧半徑呈現增大趨勢,其半圓的直徑對應于電極界面的電荷轉移電阻(Rt),說明緩蝕劑的存在使緩蝕反應的傳遞電阻(Rt)大大增加,緩蝕效果增大.同濃度的天冬氨酸和天冬酰胺比較,天冬酰胺的容抗弧半徑大于天冬氨酸的容抗弧,說明在相同濃度時天冬酰胺比天冬氨酸具有更好的緩蝕效果.這與極化曲線測試結果一致.
從表3可以看出:交流阻抗數據與極化曲線數據結果一致,隨著緩蝕劑濃度的增加,Rct和緩蝕效率都增加,說明這2種緩蝕劑的加入都對碳鋼在0.1 mol·L-1H2SO4溶液的腐蝕具有緩蝕作用.并且天冬酰胺的緩蝕效果要優于天冬氨酸.這是由于分子中的N有孤對電子,鋼在酸性環境中表面帶正電荷,天冬氨酸和天冬酰胺依靠靜電引力,擠掉鋼表面水分子,吸附到鋼表面,使H+無法靠近鋼表面,析氫腐蝕難以進行.另一方面由于鐵離子有d空軌道,N上的孤對電子可與其形成表面配合物,使吸附更加緊密,腐蝕速度降低,單分子層更加牢固.同時,天冬酰胺的分子結構上含有酰基,酰基是極性基團,氨基酸的酰基吸附在碳鋼表面上后非極性基團一端在金屬表面定向排列形成疏水薄膜,阻止碳鋼與酸溶液接觸,使天冬酰胺在緩蝕上具有優勢,且在水溶液中天冬氨酸以酸性形式出現,這都可能影響緩蝕效率.
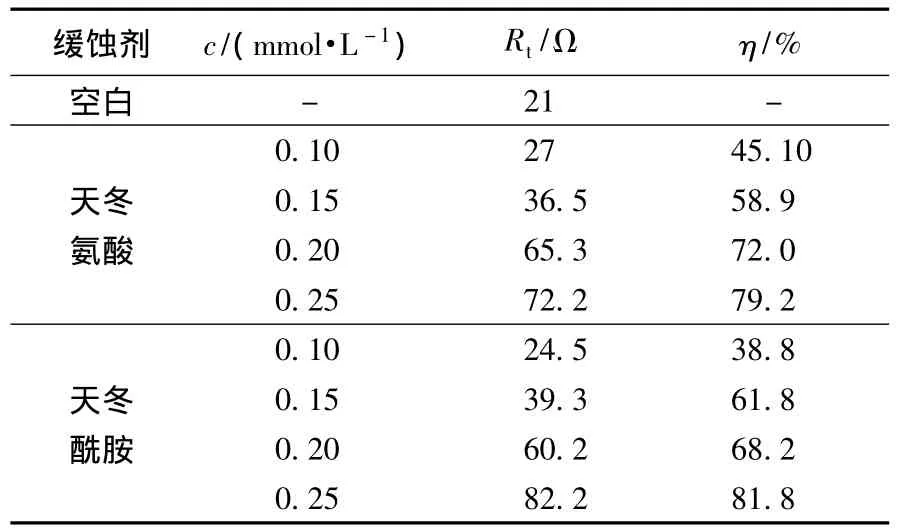
表3 N80低碳鋼在包含不同濃度緩蝕劑在0.1 mol·L-1 H2SO4的電荷傳遞電阻和緩蝕效率Table 3 Charge transfer resistance Rtand inhibition efficiency η%for N80 mild steel in 0.1 mol·L-1H2SO4 solution containing Asp and Aspar
3 結論
(1)天冬氨酸及天冬酰胺在0.1 mol·L-1硫酸中對N80碳鋼都具有不同程度的緩蝕作用,并且后者緩蝕性大于前者,天冬酰胺的緩蝕效率達到81.8%,而天冬氨酸的緩蝕效率達到79.2%,兩者緩蝕作用為陰極型緩蝕劑.
(2)兩種氨基酸的緩蝕性能都隨著緩蝕劑濃度的增加而增大.
(3)天冬酰胺結構上的酰基能夠提供極性基團,吸附中心原子N或O上均具有未共用的電子對,而金屬表面存在空的d軌道時,極性基團中心原子的孤對電子就與空的d軌道形成配位鍵,與金屬表面的鐵離子配位從而形成吸附膜,而天冬酰胺有更多的N原子吸附在碳鋼表面.
[1] 周曉湘,劉建平.酸洗緩蝕劑的應用研究現狀及發展趨勢[J].工業水處理,2002,22(1):16-19.
[2] 杜天保.硫酸中環己基炔氧甲基胺乙酸鹽對鐵的緩蝕及與Cl-的協同緩蝕作用[J].材料保護,1997,30(8):1-4.
[3] 劉天晴,鄒愛華,郭榮.表面活性劑對鎳的緩蝕作用[J].材料保護,2000,33(5):35-40.
[4] 張健,陳棟華.吡咯在鐵表面的吸附行為及其緩蝕作用[J].材料保護,2000,33(6):28-31.
[5] 袁朗白,劉曉軒,李向紅,等.銅離子和聚乙二醇辛基苯基醚(OP)對鋼的緩蝕作協同效應[J].云南大學學報:自然科學版,2003,25(4):361-363.
[6] 劉曉軒,朗白.氨基酸類有機物在硫酸介質中對鋼的緩蝕作用[J].云南大學學報:自然科學版,2003,25(4):355-360.
[7] 孫海梅,郭崇潔,曾昭輝.一種天然阻垢劑阻垢及緩蝕性能的研究[J].工業水處理,2000,20(5):42-43.
[8] 許海波.硫酸溶液中硫脲對鐵緩蝕作用的電化學[J].中國腐蝕與防護,1998,19(1):66-68.
[9] 宋彥梅.綠色阻垢劑的研究現狀及應用進展[J].工業水處理,2005(9):75-76.
[10]吳偉明,楊萍,杜海燕,等.綠色緩蝕劑氨基酸在抑制金屬腐蝕方面的應用[J].表面技術,2006,35(6):51-56.
[11]曹楚南.鐵在鹽酸中的緩蝕劑的兩種作用類型的研究[J].腐蝕科學與防護技術,1992,4(1):1-8.
[12]蔡奇睿.氨基酸及其衍生物對銅的緩蝕機理的研究[D].上海:上海大學,2009:20-21.
[13]曹楚南.關于緩蝕劑研究的電化學方法[J].腐蝕科學與防護技術,1990,2(1):237-245.
[14]杜海燕,彭小紅,張燕芬,等.豆渣中氨基酸類緩蝕劑的制備和緩蝕性能評價[J].安徽化工,2008,34(3):35-37.

