改性柿子粉吸附劑對Cd2+的吸附性能
郭學益,肖彩梅,梁莎,田慶華
(中南大學 冶金科學與工程學院,湖南 長沙,410083)
據報道,國內連續發生了重金屬污染事件。隨著現代工業的迅猛發展,重金屬污染日趨嚴重。重金屬離子主要是通過含有大量污染金屬的工業廢水(主要來源于冶煉、醫藥、電鍍、紡織印染、造紙等)、城市生活廢水以及各種礦山廢水向自然環境中排放,并進一步通過食物鏈的傳遞對動植物造成嚴重的影響。生物吸附法是一種新興的重金屬廢水處理技術,它利用廉價的生物材料對重金屬離子進行吸附,尤其適宜低濃度重金屬廢水的處理,并且具有吸附量高、吸附速率快等優點[1]。生物吸附劑的來源并不局限于微生物和藻類,豐富的農林業副產物如橘子皮[2?3]、甜菜渣[4]、榛子殼[5]、玉米芯[6]、谷殼[7]、樹皮[8]、廢棄的茶葉[9?10]、馬鈴薯渣[11]、鋸末[12]等亦被認為是有相當潛力的生物吸附劑。我國是柿子主產國,每年的柿子總產量在500萬t左右,但由于其味澀未廣泛用于食品行業,大部分柿子未得到有效利用而自然腐壞[13]。柿子中的主要有效成分為單寧,又稱單寧酸、鞣質,是多酚中高度聚合的化合物,其結構中含有大量的活性官能團酚羥基,可與金屬離子通過離子交換、螯合等方式結合,從而用于水溶液中重金屬離子的凈化[14?16]。但直接采用柿子粉吸附水溶液中的重金屬離子,存在單寧等可溶性物質溶解而導致吸附能力降低、水中化學耗氧量增加等問題。近年來,有研究者利用甲醛或濃硫酸交聯改性的柿子皮吸附重金屬離子[17?19]。在此,本文作者以柿子粉為基體,經丙酮和硫酸改性處理得到柿子生物吸附劑AP并研究其對Cd2+的吸附,包括初始pH、溫度等對吸附過程的影響、生物吸附動力學、等溫平衡研究以及生物吸附劑的循環再生。
1 實驗材料與方法
1.1 儀器與試劑
儀器為:WFX?130B原子吸收分光光度計(北京市瑞利分析儀器公司制造);SHA?C水浴恒溫振蕩器(江蘇省金壇市榮華儀器制造有限公司制造);PHS?3C酸度計(上海雷磁制造);TDL?40B低速臺式離心機(上海安亭科學儀器廠制造);LS908型激光粒度分析儀(廣東珠海歐美克公司制造)、電子分析天平(上海天平儀器公司制造);FD?1B?50冷凍干燥機(北京博醫康實驗儀器有限公司制造)。
試劑為:CdCl2·2H2O,CH3COCH3,H2SO4,緩沖劑HEPES等,均為分析純。
1.2 改性柿子吸附劑的制備
柿子的主要有效成分單寧的分子結構中存在大量的酚羥基,易溶于水,因此,本實驗研究通過化學改性的方法使柿子中的有效成分單寧發生縮合沉淀,從而獲得柿子生物吸附劑。在45 ℃時,取100 g柿子粉末(PP)加入300 mL丙酮和200 mL 3mol/L H2SO4浸泡攪拌反應24 h,然后離心分離,用蒸餾水洗至中性,冷凍干燥8 h,所得改性柿子粉生物吸附劑簡稱為AP,采用激光粒度分析儀測其平均粒度為29.97 μm。
1.3 靜態吸附實驗
在50 mL錐形瓶中加入一定量的改性柿子粉生物吸附劑及Cd2+溶液,密閉瓶口以防實驗過程中體積發生變化。將其放入水浴恒溫振蕩器中振蕩反應,達到預定吸附時間后過濾。
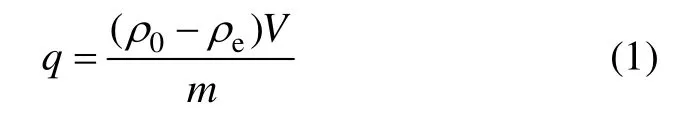
濾液中金屬離子濃度均用原子吸收分光光度計測定。用下式計算吸附量:式中:V為溶液體積,mL;ρ0和ρe分別為金屬離子的初始質量濃度和平衡質量濃度,mg/L;m為所用生物吸附劑的質量,mg。吸附率(R)由下式計算:

1.4 解吸附實驗
將達到吸附平衡的生物吸附劑過濾后,往濾渣中加入一定量的0.1 mol/L HCl溶液,恒溫振蕩解吸3 h,過濾,用蒸餾水洗至中性,烘干,再生后的吸附劑被反復使用。
2 結果與討論
2.1 吸附劑的表征
圖1所示為PP和AP的紅外光譜圖。由PP的紅外光譜圖可知柿子粉的成分很復雜,PP的主要成分有單寧、果膠、蛋白質、糖類等,其中在3 550~3 100 cm?1范圍內的寬峰表明 PP存在大量的羥基(—OH),在2 937 cm?1附近的峰主要緣于芳香環中C—H鍵的伸縮振動[20];1 730 cm?1附近的峰屬于官能團—COOH和—C=O的吸收峰;1 610~1 455 cm?1范圍的峰主要緣于芳香族中C=C鍵的伸縮振動;1379 cm?1附近的吸附峰是由多酚中的 O—H在面內形變振動形成的[21]。醚鍵 CH2—O—CH2的吸收峰出現在 1 150~1 085 cm-1范圍內。苯環上C—H鍵的變形振動產生的吸附波段為910~740 cm?1。
對比PP和AP的紅外光譜圖可知:經化學改性后,PP中3 299 cm?1附近的羥基峰移動到3 329 cm?1,并且 3 329 cm?1附近的波峰較寬,芳香環中 C—H 峰(2 937和931 cm?1)減弱或消失,很可能是其與丙酮發生縮合反應引起的。反應式為:
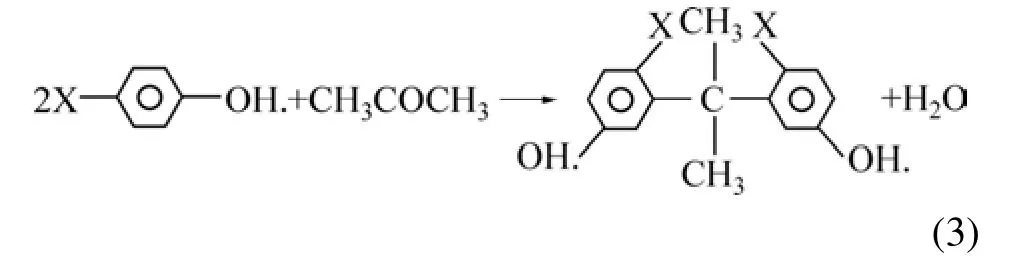
式中:X表示其他官能團。在1 730和1 610 cm?1附近的峰結合成1個峰,并在1 621 cm?1附近變寬,很可能是C=O官能團在AP上的環境發生改所致[22]。在1 213 cm?1附近的波峰得到加強,是由C—O—C鍵不對稱振動引起的。上述分析說明柿子粉在硫酸的催化作用下,與丙酮發生了有效的縮合反應,從而改變柿子粉的水溶性;同時,大量的羥基官能團可以通過離子交換或配合等方式吸附溶液中的重金屬離子,進而提高吸附性能。
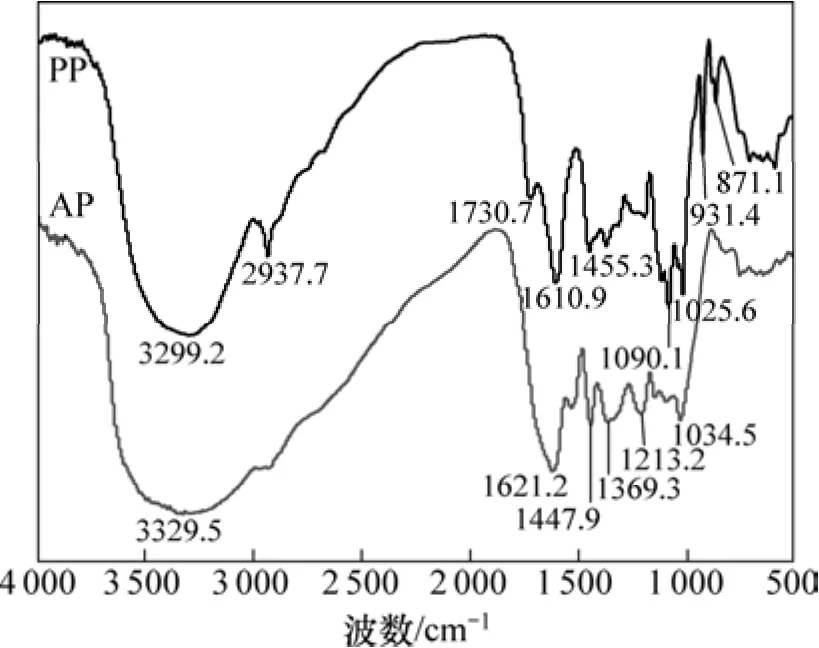
圖1 PP和AP的紅外光譜圖Fig.1 FIIR spectra of PP and AP
2.2 溶液初始pH的影響
圖2 所示為溶液初始pH對吸附過程的影響。顯然,溶液初始 pH對吸附過程的影響很大。當溶液初始pH<3.5時,AP對Cd2+的吸附量很小;而當溶液初始pH在4.0~6.0范圍內,吸附率迅速增大;在pH為6.8左右趨于平緩。在較低pH下,H+的濃度和活動性較高,與Cd2+形成了競爭吸附,從而吸附率較低[23];隨著pH的增大,H+的濃度降低,吸附劑表面暴露更多的負電荷基團,有利于Cd2+吸附在活性位點上。因此,本研究的所有實驗選取溶液初始pH為6.5~6.8。
2.3 反應溫度的影響
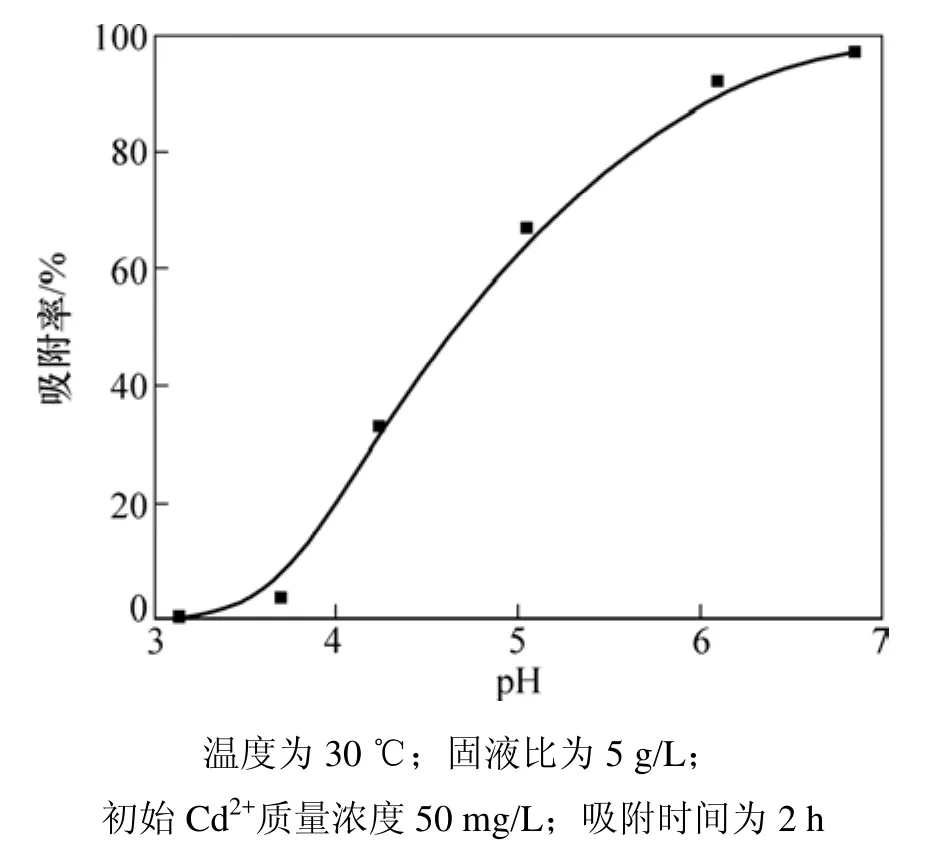
圖2 初始pH對吸附過程的影響Fig.2 Effect of initial pH on adsorption
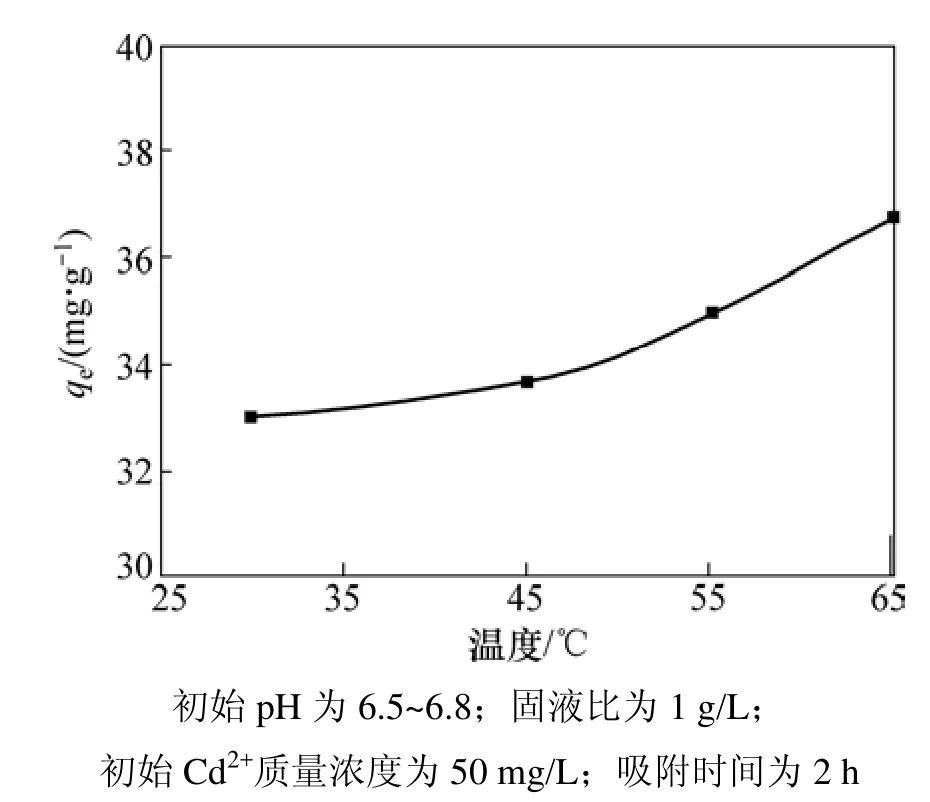
圖3 反應溫度對吸附量qe的影響Fig.3 Effect of temperature on adsorption

圖3所示為反應溫度對吸附過程的影響。由圖3可知:AP對 Cd2+的吸附過程受溫度影響較小,Cd2+的吸附量隨溫度升高而緩慢增大。吸附熱(ΔH0)可根據下式計算:式中:ΔG0為標準吉布斯自由能,kJ/mol;R為熱力學氣體常數,8.314 J/(mol?K);T為熱力學溫度,K;ΔH0為反應的焓變量,kJ/mol;ΔS0為反應的熵變量,J/(mol?K);KC為熱力學平衡常數;ρ?為吸附到吸附劑上的金屬離子的質量濃度,mg/L。以lnKC對1/T作圖并進行線性擬合,計算熱力學參數,所得結果見表1。
由表1所示熱力學參數可知ΔH0>0,說明AP吸附Cd2+的反應為吸熱反應。吸附吉布斯自由能ΔG0是吸附驅動力和吸附優先性的體現,ΔG0在試驗溫度范圍內均為負值,這說明AP對Cd2+的吸附過程是自發進行的。
2.4 動力學研究
在生物吸附動力學的研究中,通常用準二級動力學方程對實驗數據進行模擬以分析金屬離子濃度隨吸附時間的變化關系(如圖4所示)。準二級動力學方程的線性表達式為:
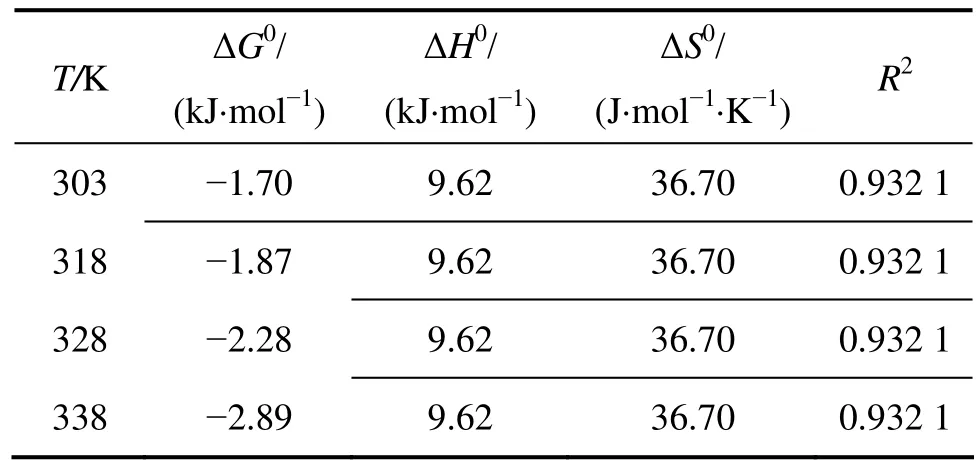
表1 AP吸附Cd2+的熱力學參數Table 1 Thermodynamics parameters of adsorption
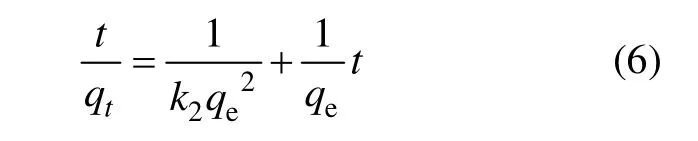
式中:qt為t時間時生物吸附劑對金屬離子的吸附量,mg/g;qe為吸附平衡時的吸附容量,mg/g;k2為準二級動力學方程速率常數,g/(mg·min)。利用上述方程對圖4所示實驗結果進行模擬,以t/qt對t作圖,所得結果見表2。從表2可以看出:試驗結果可以很好地用準二級動力學方程進行模擬,相關系數均接近于 1,且qe的實驗值與理論值相差很小。這表示吸附過程遵循準二級反應機理,吸附過程被化學吸附所控制[24]。

圖4 初始離子質量濃度對吸附的影響Fig.4 Effect of initial mass concentration on adsorption
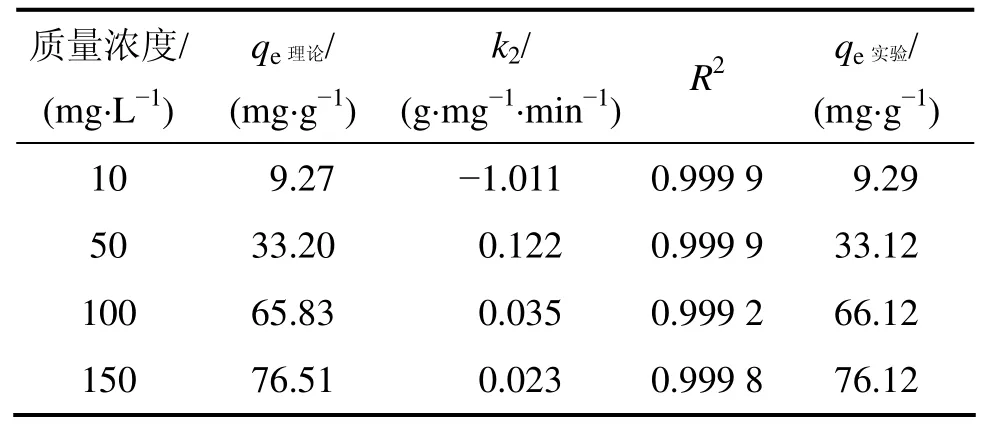
表2 AP吸附Cd2+的準二級反應動力學參數Table 2 Kinetic parameters of pseudo-second-order equation for adsorption
2.5 等溫平衡研究
圖5所示為AP和PP吸附Cd2+的等溫吸附曲線。可以直觀看出柿子粉吸附劑AP對Cd2+的吸附量明顯大于原始柿子粉 PP的吸附量。采用 Langmuir和Freundlich吸附等溫模型對圖5中的數據進行模擬。Langmuir模型的表達式為:

式中:qm為生物吸附劑吸附金屬離子飽和容量,mg/g;b為Langmuir常數,L/mg。qm和 b可分別由 ρe/qe對 ρe作直線方程的斜率和截距求出。Freundlich 模型的表達式為:
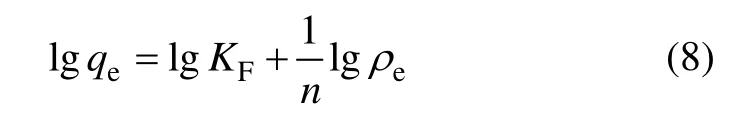
式中:KF和n為Freundlich吸附經驗常數,分別由lgqe對lgρe作直線方程的斜率和截距求出。模擬結果如表3所示。從表 3可以看出:AP對 Cd2+的吸附均符合Langmuir和 Freudlich模型,模擬所得的相關系數為0.972 3;AP和PP對Cd2+的最大吸附量分別為82.78 mg/g和3.50 mg/g,即通過化學改性制備的柿子粉吸附劑AP較原始柿子粉PP對Cd2+的吸附量有很大提高,進一步說明了改性處理使得柿子粉表面有效官能團增加,與金屬離子結合能力增強。
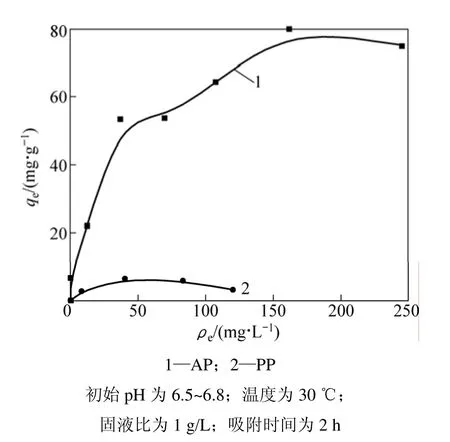
圖5 AP和PP吸附Cd2+的等溫線Fig.5 Adsorptions isotherms of adsorption
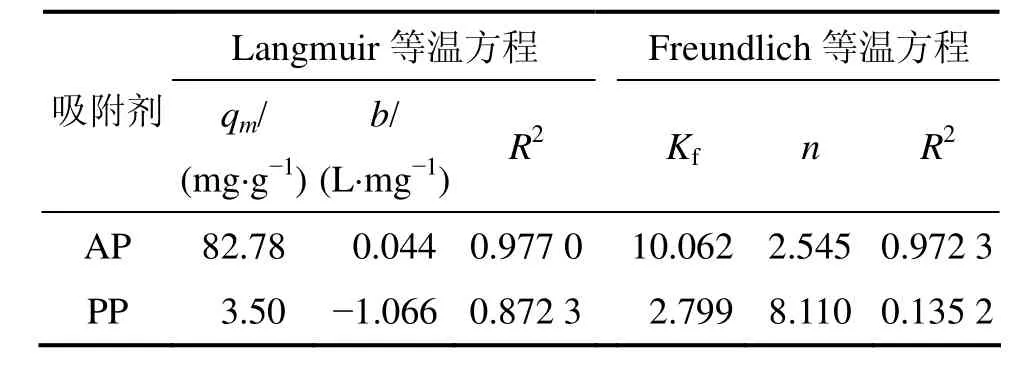
表3 AP吸附Cd2+的Langmuir和Freundlich模型參數Table 3 Parameters of Langmuir and Freundlich equations for adsorption
2.6 解吸再生
實驗考察了已吸附Cd2+的改性柿子生物吸附劑的解吸與再吸附性能,結果如圖6所示。由圖6可知:用再生后的生物吸附劑進行吸附試驗,吸附能力穩定,Cd2+的吸附率均在99%左右,并且吸附劑的質量略微減少,且每次解吸率均在97%左右,說明改性后柿子吸附劑至少可以循環使用5 次以上。
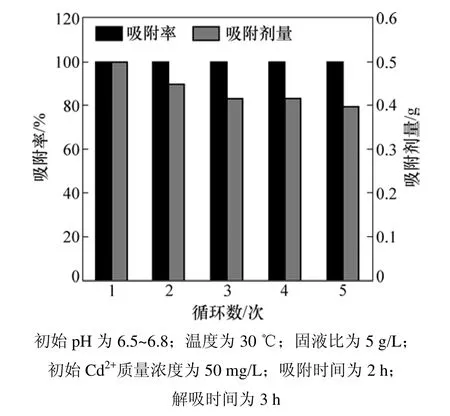
圖6 AP吸附Cd2+的循環吸附實驗Fig.6 Cd2+ adsorption cycles of AP
3 結論
(1) 將改性柿子粉生物吸附劑用于處理含 Cd2+的水溶液,吸附率顯著提高且可再生循環使用,是一種性能良好的生物吸附劑。
(2) 溶液初始pH是影響吸附效果的重要因素,最佳吸附pH為6.5~6.8。吸附動力學可以用準二級動力學方程很好地描述。AP對Cd2+的吸附均符合Langmuir和Freudlich模型。PP和AP對Cd2+的最大吸附量分別為82.78 mg/g和3.50 mg/g。
[1]WANG Xue-song, QIN Yong. Equilibrium sorption isotherm for Cu2+on rice bran[J]. Process Biothem, 2005, 40(2): 677?680.
[2]馮寧川, 郭學益, 梁莎, 等. 皂化交聯改性橘子皮生物吸附劑對 Cu2+的吸附[J]. 中南大學學報: 自然科學版, 2009, 40(4):857?862.FENG Ning-chuan, GUO Xue-yi, LIANG Sha, et al. Adsorption of Cu2+by saponified and cross-linked orange peel[J]. Journal of Central South University: Science and Technology, 2009, 40(4):857?862.
[3]LIANG Sha, GUO Xue-yi, FENG Ning-chuan, et al. Application of orange peel xanthate for the adsorption of Pb2+from aqueous solutions[J]. Journal of Hazardous Materials, 2009, 170(1):425?429.
[4]Reddad Z, Gerente C, Andres Y, et al. Ni (II) and Cu (II) binding properties of native and modified sugar beet pulp[J]. Carbohydr Polym, 2002, 49(1): 23?31.
[5]Cimino G, Passerini A, Toscano G. Removal of toxic cations and Cr(VI) from aqueous solution by hazelnut shell[J]. Water Research, 2000, 34(11): 2955?2962.
[6]王文華, 馮永梅, 常秀蓮, 等. 玉米芯對廢水中鉛的吸附研究[J]. 水處理技術, 2004, 30(2): 95?98.WANG Wen-hua, FENG Yong-mei, CHANG Xiu-lian, et al.Removal of lead from aqueous solution by corncobs[J].Technology of Water Treatment, 2004, 30(2): 95?98.
[7]Mohanty K, Jha M, Biswas M N, et al. Removal of chromium(VI) from dilute aqueous solutions by activated carbon developed from Terminalia arjuna nuts activated with zinc chloride[J]. Chem Eng Sci, 2005, 60(11): 3049?3059.
[8]Randall J M. Variations on effectiveness of barks as scavengers for heavy metal ions[J]. Forest Product Journal, 1977, 27(11):51?56.
[9]章明奎, 方利平. 利用非活體生物質去除廢水中重金屬的研究[J]. 生態環境, 2006, 15(5): 897?900.ZHANG Ming-kui, FANG Li-ping. Use of non-living biomass materials to remove selected heavy metals from wastewater[J].Ecology and Environment, 2006, 15(5): 897?900.
[10]Tee T W, Khan R M. Removal of lead, cadmium and zinc by waste tea leaves[J]. Environ Technol Lett, 1988, 9(11):1223?1232.
[11]呂金順, 姜春華, 王小芳, 等. 用PDF處理含Pb2+、Cu2+重金屬離子廢水的研究[J]. 甘肅科學學報, 2004, 16(3): 110?112.LU Jin-shun, JIANG Chun-hua, WANG Xiao-fang. The treatment of waste water containing heavy metal ions of Pb2+and Cu2+by PDF adsorption[J]. Journal of Gansu Sciences, 2004,16(3): 110?112.
[12]Shukla S S, Yu L J, Dorris K L, et al. Removal of nickel from aqueous solutions by sawdust[J]. Journal of Hazardous Materials,2005, 121(1/2/3): 243?246.
[13]張寶善, 伍曉紅, 陳錦屏. 柿單寧研究進展[J]. 陜西師范大學學報: 自然科學版, 2008(1): 99?105.ZHANG Bao-shan, WU Xiao-hong, CHEN Jin-ping. Research progress of Kaki tannin[J]. Journal of Shanxi Normal University:Natural Science, 2008(1): 99?105.
[14]Parajuli D, Adhikari C R, Kawakita H, et al. Reduction andaccumulation of Au(Ⅲ) by grape waste: A kinetic approach[J].Reactive & Functional Polymers, 2008, 6(8): 1194?1199.
[15]Mack C, Wilhelm B, Duncan J R, et al. Biosorption of precious metals[J]. Biotechnology Advances, 2007, 25(3): 264?271.
[16]?engil ?, ?zacar M. Biosorption of Cu(II) from aqueous solutions by mimosa tannin gel[J]Journal of Hazardous Materials, 2008, 157(2/3): 277?285.
[17]Parajuli D, Kawakita H, Inoue K, et al. Persimmon peel gel for the selective recovery of gold[J]. Hydrometallurgy, 2007,87(3/4): 133?139.
[18]Nakajima A, Baba Y. Mechanism of hexavalent chromium adsorption by persimmon tannin gel[J]. Water Research, 2004,38(12): 2859?2864.
[19]XIONG Ying, Adhikari C R, Kawakita H, et al. Selective recovery of precious metals by persimmon waste chemically modified with dimethylamine[J]. Bioresource Technology, 2009,100(18): 4083?4089.
[20]?zacar M, ?engil ?, Türkmenler H.Equilibrium and kinetic data,and adsorption mechanism for adsorption of lead onto valonia tannin resin[J]. Chemical Engineering Journal, 2008, 143(1/2/3):32?42.
[21]Yurtsever M, ?engil ?. Biosorption of Pb(II) ions by modified quebracho tannin resin[J]. Journal of Hazardous Materials, 2009,163(1): 58?64.
[22]Oo C W, Kassim M J, Pizzi A. Characterization and performance of Rhizophora apiculata mangrove polyflavonoid tannins in the adsorption of copper (II) and lead (II)[J]. Industrial Crops and Products, 2009, 30(1): 152?161.
[23]?engil ?, ?zacar M, Türkmenler H. Kinetic and isotherm studies of Cu(II) biosorption onto valonia tannin resin[J]. Journal of Hazardous Materials, 2009, 162(2/3): 1046?1052.
[24]Cruz C C, Costa A C, Henriques C A, et al. Kinetic modeling and equilibrium studies during cadmium biosorption by dead Sargassum sp.biomass[J]. Biores Technol, 2004, 9l(3): 249?257.

