雙藤巴布劑中青藤堿、雷公藤甲素的體外釋放與體外透皮機制研究Δ
鄧亞利,周莉玲(1.華南農業大學制藥工程系,廣州510642;2.廣州中醫藥大學,廣州510405)
青風藤、雷公藤抗炎抗風濕療效確切,臨床上應用廣泛。青風藤有效成分主要為青藤堿;雷公藤有效成分主要為雷公藤內酯醇(甲素)[1,2]。本研究擬通過合理組方,以青風藤、雷公藤配成藥對,組成復方,制成復方巴布劑,對其合用后藥物釋放及其透皮行為進行研究,并與青藤堿、雷公藤甲素單體組成的復方巴布劑進行比較,探討外用替代口服、復方替代單方的可行性與優越性。
筆者對2種巴布劑的體外釋藥和透皮吸收特征[3,4]進行數學模型擬合,探討制劑中藥物的釋放機制,同時考察經皮給藥后2種有效成分局部藥物濃度隨時間變化的規律,并預期合用后其治療特點,為其他復方中藥經皮給藥系統的研發提供借鑒。
1 儀器與材料
1.1 儀器
Summit P680型高效液相色譜儀,由PDA-100型二級管陣列檢測器、ASI-100型自動進樣器、Summit恒溫箱、Chromeceon色譜工作站組成(德國Dionex公司);ZRS-4型智能溶出試驗儀(天津大學無線電廠);TK-12A型透皮擴散試驗儀(上海鍇凱科技貿易有限公司);TGL-16型高速臺式離心機(上海醫療器械六廠)。
1.2 試藥
雙藤巴布劑(STEP)、青藤堿雷公藤甲素巴布劑(STP)由筆者自制(均含青藤堿 2.5 mg·cm-2、雷公藤甲素 25 μg·cm-2);青藤堿對照品(批號:0774-200105)、雷公藤甲素對照品(批號:111567-200502)均由中國食品藥品檢定研究院提供。
1.3 動物
4周齡BALB/C裸鼠,♂,體重(20±2)g,由廣州中醫藥大學實驗動物中心提供(動物生產合格證號:0028166)。
2 方法與結果
2.1 含量測定方法的建立
2.1.1 色譜條件與系統適用性試驗 色譜柱:Diamonsil-C18(250 mm×4.6 mm,5μm);流動相:甲醇-磷酸鹽緩沖液(0.005 mol·L-1磷酸氫二鈉溶液,以0.005 mol·L-1的磷酸二氫鈉調pH值至8.0,再以1%三乙胺調pH值至9.0)=55∶45;檢測波長:225 nm。理論板數按青藤堿峰計算應不低于1500。
2.1.2 標準曲線的制備 精密稱取青藤堿、雷公藤甲素對照品各適量,用甲醇配成每1 mL含青藤堿0.2352 mg、雷公藤甲素40.512 μg的對照品貯備溶液,貯藏,備用。精密吸取對照品貯備溶液1 mL,置25 mL量瓶中,甲醇定容,得青藤堿(9.41 μg·mL-1)與雷公藤甲素(1.62 μg·mL-1)對照品溶液,將此溶液分別進樣1、2、4、6、8、10 μL;精密吸取對照品貯備溶液5 mL,置10 mL量瓶中,甲醇定容,分別進樣1、2、4、8、12、16、20 μL。以青藤堿、雷公藤甲素進樣量(X)為橫坐標,相應峰面積積分值(Y)為縱坐標,進行線性回歸,得青藤堿的回歸方程為Y=0.0281X-0.0205(r=0.9998,n=6)與Y=35.142X-0.1393(r=0.9994,n=7)。結果表明,青藤堿進樣量在9.41~94.08 ng與0.12~2.35 μg之間與其峰面積積分值呈良好線性關系。雷公藤甲素的回歸方程為Y=0.0487X-0.0135(r=0.9995,n=6)與Y=0.0369X+0.0356(r=0.9999,n=7)。結果表明,雷公藤甲素進樣量在3.24~16.20 ng與20.26~405.12 ng之間與其峰面積積分值呈良好線性關系。
2.1.3 精密度試驗 取“2.1.2”項下對照品貯備液(含青藤堿0.2352 mg·mL-1、雷公藤甲素40.512 μg·mL-1)、對照品溶液(含青藤堿9.41 μg·mL-1、雷公藤甲素1.62 μg·mL-1),分別按“2.1.1”項下色譜條件測定。日內精密度(n=6)結果:青藤堿峰面積的RSD為1.04%與1.86%,雷公藤甲素峰面積的RSD為1.22%、1.88%;日間精密度(n=5)結果:青藤堿峰面積的的RSD為1.26%、1.93%,雷公藤甲素峰面積的RSD為1.72%、1.98%,表明該方法精密度良好。
2.1.4 穩定性試驗 取“2.1.2”項下對照品溶液適量,室溫條件下每隔2 h進樣1次,8 h內測定4次。結果,青藤堿峰面積的RSD為1.56%(n=4),雷公藤甲素峰面積的RSD為1.97%(n=4),表明在室溫條件下檢測成分8 h內穩定。
2.1.5 加樣回收率測定 精密吸取青藤堿(9.41 μg·mL-1)與雷公藤甲素(1.62 μg·mL-1)對照品溶液5.0 mL,氮氣吹干,甲醇定容至1 mL,過0.22 μm濾膜,取續濾液10 μL,按“2.1.1”項下色譜條件進樣測定。結果,青藤堿的平均回收率為99.86%(RSD=1.03%,n=6),雷公藤甲素的平均回收率為97.56%(RSD=1.02%,n=6),表明該方法準確度良好。
2.1.6 最低檢測限測定 按信噪比(S/N)=3作為最低檢測限,測得雷公藤甲素的最低檢測限為1.62 ng,青藤堿的最低檢測限為9.41 ng。
2.2 體外釋放度試驗
參照2005年版《中國藥典》釋放度測定第三法進行。釋放介質為30%乙醇-生理鹽水。量取經脫氣處理過的釋放介質250 mL注入溶出杯內,預溫至(32±0.5)℃。取經皮給藥制劑各1片(面積為25 cm2),分別固定于兩層不銹鋼碟片的中央,釋放面朝上,再將網碟置于溶出杯下部,使制劑與槳底旋轉面平行,兩者相距(25±2)mm。開始計時,轉速為100 r·min-1,分別于1、2、4、6、8、12、16、24 h取樣5 mL,取樣位置在介質液面與槳葉上端之間正中,離溶出杯壁距離1 cm。每次取樣后立即補充相同體積的空白釋放介質。
取上述溶出液1 mL,氮氣吹干,甲醇定容至1 mL,過0.22 μm濾膜,取續濾液5 μL,按“2.1.1”項下色譜條件進樣,測定青藤堿、雷公藤甲素的峰面積,根據對照品的峰面積計算其濃度。按以下公式計算單位面積累積釋放量(Q,μg·cm-2):
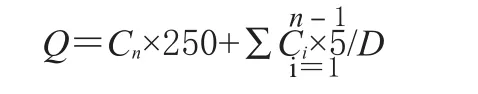
式中,Cn為第n個取樣點測得的藥物濃度(μg·mL-1);Ci為第i(i=n-1)個取樣點測得的藥物濃度(μg·mL-1);D為制劑中青藤堿、雷公藤甲素含量(μg)。
青藤堿與雷公藤甲素的累積釋放量見圖1。
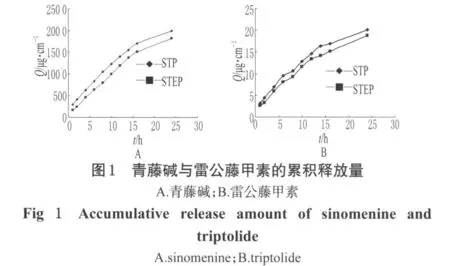
將STP與STEP經皮給藥制劑的單位面積的Q分別對時間(t,h)按零級、一級與Higuchi動力學方程進行線性回歸,解釋其釋藥機制[6]。結果均以Higuchi方程擬合度較優(STP中:r青=0.9955,r甲=0.9958;STEP中:r青=0.9920,r甲=0.9963),說明2種制劑均屬骨架型釋藥系統。藥物以微細的粒子混懸分散在基質中,每單位體積基質所含溶解與混懸藥物總量比藥物在基質中的飽和濃度大,藥物的釋放量與時間的平方根成正比。青藤堿、雷公藤甲素以單體入藥和以浸膏入藥,在相同基質中的釋藥速率(J)基本相同。青藤堿、雷公藤甲素的體外釋放動力學方程分別見表1、表2。
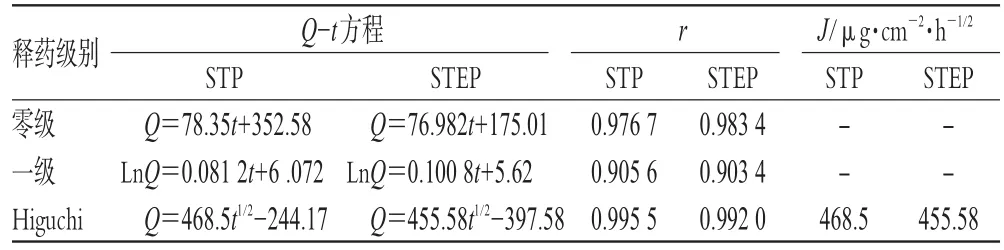
表1 青藤堿的體外釋放動力學方程Tab 1 In vitro release kinetics equation of sinomenine

表2 雷公藤甲素的體外釋放動力學方程Tab 2 In vitro release kinetics equation of triptolide
由表1、表2可知,2種經皮給藥制劑的體外釋藥隨時間為一個遞增過程。青藤堿在STP、STEP中,24 h的累積釋放百分率(Q%)分別為83.52%、78.09%;J分別為468.5、455.58 μg·cm-2·h-1/2。雷公藤甲素在STP、STEP中,24 h的Q%分別為80.32%、75.26%;J分別為4.6112、4.3879 μg·cm-2·h-1/2。
2.3 體外透皮試驗
采用透皮擴散試驗儀[5],先將磁攪拌子放在接收池內,再將制備的離體裸鼠背部皮膚平放在接收池上端,角質層面向上,然后將釋放池用夾子固定于接收池上。在接收室中注入接收液7 mL,保持(32±0.2)℃恒溫水浴,磁力攪拌轉速為(200±5)r·min-1,預平衡1 h。倒掉接收池中的溶液,加入空白接收液。釋放池中放上巴布劑,于預定的間隔時間(2、4、6、8、10、12、16 h)分別取樣5 mL,每次取樣后補加相同體積的新鮮接收液并排除接收室中的氣泡。
取上述溶出液5 mL,氮氣吹干,甲醇定容至1 mL,過0.22 μm濾膜,取續濾液10 μL,按“2.1.1”項下色譜條件進樣,測定峰面積,根據對照品的峰面積計算其濃度。按以下公式計算Q

式中,Cn、Ci、D的意義同“2.2”項下。
以STP、STEP中青藤堿和雷公藤的Q和Q%對t(h)分別按零級、一級與Higuchi動力學方程進行線性回歸,可知2種巴布劑的經皮滲透可較好地擬合零級動力學方程。青藤堿在STP、STEP中的r分別為0.9951、0.9926;透皮速率(J)分別為 21.729、20.063 μg·cm-2·h-1。雷公藤甲素在STP、STEP中的r分別為0.9942、0.9902;J分別為0.4783、0.4168 μg·cm-2·h-1。STP與STEP中青藤堿、雷公藤甲素的體外透皮動力學方程分別見表3、表4。和Q%。
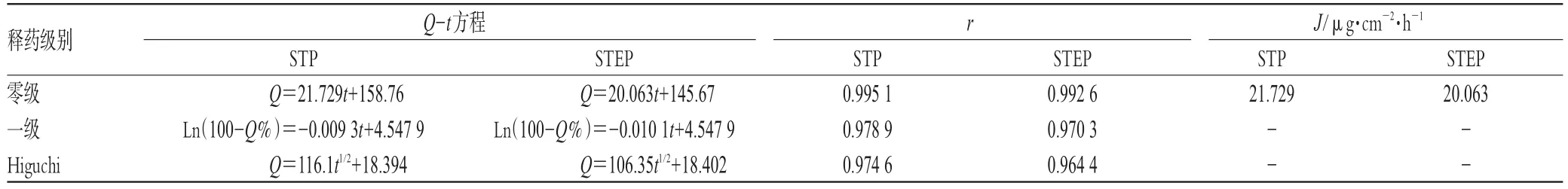
表3 STP與STEP中青藤堿的體外透皮動力學方程Tab 3 Transdermal rate parameters and equations of sinomenine in STPand STEP
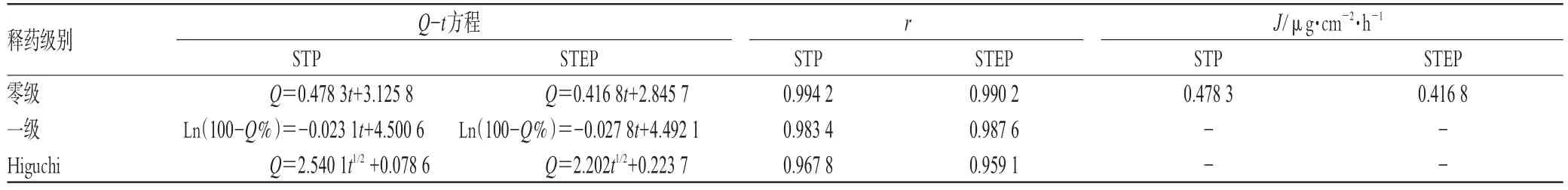
表4 STP與STEP中雷公藤甲素的體外透皮動力學方程Tab 4 Transdermal rate parameters and equations of triptolide in STPand STEP
2.4 藥物釋放機制探討
將STP、STEP中青藤堿、雷公藤甲素的體外釋放數據代入Ritger-Peppas:Q%=ktn模型進行擬合,判斷其從巴布劑中釋放的機制,并將兩者進行比較。結果,2種巴布劑中各組分體外釋放的擴散指數0.45<n<0.89,說明藥物的釋放機制是非Fick擴散(藥物的擴散和骨架溶蝕協同作用);2種巴布劑中各組分的體外透皮指數n<0.45,說明藥物的透皮機制是Fick擴散。STP與STEP中青藤堿、雷公藤甲素的體外Ritger-Peppas模型釋放參數見表5。

表5 STP與STEP中青藤堿、雷公藤甲素的體外Ritger-Peppas模型釋放參數Tab 5 Ritger-Peppas model release parameter of sinomenine and triptolide in STPand STEP
3 討論
釋放度是指藥物從該制劑在規定的溶劑中釋放的速度和程度。經皮給藥過程包括藥物在基質中擴散、在皮膚表面分配、通過皮膚滲透3個連續過程。故巴布劑的溶出度或釋放度測定在一定程度上可反映藥物在經皮給藥裝置中的傳遞性能,為評價給藥過程的限速步驟提供參考數據。
對于經皮給藥制劑釋放度研究,目前公認的試驗方法是采用藥典所規定的釋放度測定第三法(小杯法),故本研究采用小杯法。小杯法中制劑的狀態較為穩定,攪拌對基質的影響較小,溶出液澄明度好。本研究采用的溶出介質為30%乙醇生理鹽水溶液,在長時間的試驗中,應注意溶出過程中的介質蒸發量,這種損失量可能對釋放度測定結果的準確性產生較大影響。
2種巴布劑中的有效成分體外經皮滲透行為略有所不同。單體入藥的青藤堿、雷公藤甲素透皮速率均稍大于浸膏入藥的2種成分;但浸膏入藥的STEP時滯較小,推測與浸膏中其他成分存在有關。
藥物的經皮吸收過程包括擴散和代謝2個過程。許多藥物的藥理作用的強度和持續時間取決于在機體中的代謝失活情況。所有進入活性皮膚中的藥物分子及經皮全身性吸收的藥物分子都要經過皮膚中酶的代謝作用。體外通透試驗很少能獲得有關代謝、分布和血流對通透性影響的信息,所以在體的透皮實驗研究很有必要[6]。
因體外釋放與體外透皮濃度變化范圍較大,故采用2條標準曲線以滿足不同檢測濃度需要;體外釋放與體外透皮取樣后,經過氮氣吹干甲醇定容后按色譜條件進樣,對此過程造成的測量誤差進行了回收率試驗,結果表明該處理方法簡單、回收率良好。
在主要有效成分含量相同、基質相同的STP、STEP巴布劑中,體外釋放因為溶出介質量較大,與成分的飽和濃度相差較遠,故單體入藥與浸膏入藥釋放速率相近,無顯著性差異。而皮膚透過試驗中,因為單位面積皮膚對透過量有飽和性,在其他成分存在的情況下,可能會限制有效成分的透過速率,所得浸膏入藥的透皮速率低于單體入藥的透皮速率。
[1]劉春芳,林 娜.雷公藤甲素抗類風濕性關節炎機制研究進展[J].中國中藥雜志,2006,31(19):1575.
[2]王 巖,周莉玲.促滲劑對青藤堿脂質體透皮貼劑經皮滲透的影響[J].中藥材,2005,28(7):567.
[3]郝保華,王彥玲,李偉澤,等.青風藤電離巴布劑電致孔透皮給藥的藥動學研究[J].中草藥,2009,40(7):1060.
[4]高運軍,李 麗,李 文.癌痛寧巴布劑中烏頭堿的體外透皮吸收研究[J].中成藥,2008,30(11):1619.
[5]祁 艷,陳 軍,李 磊,等.不同促滲劑對馬錢子堿貼劑體外透皮吸收的影響[J].中國藥房,2011,22(3):195.
[6]鄭俊民.經皮給藥新劑型[M].北京:人民衛生出版社,2006:236、265.

