血漿一氧化氮水平與支氣管哮喘的相關性研究*
陳嘉馨 陸家政 黎惠貞 吳榮華 杜一凡 麥燕瑜 臧林泉
器官和細胞功能是在無數信號分子,包括脂質、肽、有機和無機分子、代謝中間物等作用下實現的,氣體信號分子作為其中的成員對器官和細胞功能的維持起重要作用。一氧化氮(nitric oxide,NO)既是一種信號分子,又是一種細胞毒性分子,調節體內一系列生理病理過程,包括血管舒張、抑制血小板在內皮細胞表面粘附與血小板凝集、神經傳遞、宿主防御和細胞毒作用等,并在一定條件下參與組織炎癥及損傷,參與多種疾病的病理生理過程[1]。研究發現,在哮喘患者氣道上皮細胞中NO的表達增加,其作為一種效應分子,能參與炎癥與組織損傷修復,過量的NO能擴張血管,促進炎癥細胞滲出及炎癥介質釋放,被認為是哮喘炎癥反應的前介質,NO在哮喘的發病機制中起著非常重要的作用[2]。本實驗觀察不同時期哮喘患者和健康人之間血漿NO水平的差異及其相關性,從新的角度探討哮喘的病因及防治。
1 資料與方法
1.1 一般資料 70例哮喘患者,診斷標準、急性發作期分級及緩解期的判斷符合2006年哮喘全球倡議(global initiative for asthma,GNA)標準[3]:氣道可逆試驗陽性系指吸入支氣管擴張劑第1秒用力呼氣容積(force expiration volume in one second,FEV1.0)增加15%以上且其絕對值增加200 ml以上;緩解期系指經過治療,患者癥狀、體征消失,肺功能恢復到急性發作前水平。其中哮喘急性發作期40例,男性21例,女性19例,平均年齡(43.1±5.1)歲;臨床緩解期30例,男性14例,女性16例,平均年齡(40.5±6.3)歲;健康對照組15例,男性8例,女性7例,平均年齡(30.5±4.6)歲,無呼吸道癥狀及心肺等疾患。性別情況各組的差異無統計學意義(P>0.05),年齡情況各組的差異有統計學意義(P<0.01)。所有研究對象均為非吸煙者,均獲知情同意并簽署知情同意書。NO測定試劑盒(Bioting-Tech公司),亞乙烯二胺(sigma 公司),其余試劑為國產,分析純。
1.2 方法
1.2.1 肺功能測定 所有對象入選時采用肺活量計法測定第1秒用力呼氣容積占預計值百分比(FEV1.0%百分比)、FEV1.0/FVC及呼氣峰流速(peak expiratory flow,PEF)。
1.2.2 血漿一氧化氮水平測定 血漿NO含量的間接測定,硝酸還原酶測定法。因NO化學性質活潑,半衰期極短,迅速與分子氧反應生成NO2-和NO3-,故以血漿NO2-和NO3-之和檢測NO的相對含量,應用Bioting-Tech公司提供的NO測定試劑盒,采用硝酸還原酶特異性地將NO3-還原為NO2-,NO2-與顯色劑亞乙烯二胺作用,生成粉紅色偶氮化合物,通過比色測出NO2-/NO3-含量[4]。
1.2.3 誘導痰細胞計數分類 參照文獻[5]報道的方法進行:受試者測試肺功能FEV1.0>FEV1.0pre的60%,可以進行痰液誘導,試驗前受試者漱口后,吸入沙丁胺醇(萬托林)400 μg,15 min后開始超聲霧化吸入4%(質量分數)的高滲鹽水40 ml,20~40 min后收集痰液,加入等量0.1%(質量分數)二硫蘇糖醇(DTT)溶液,振蕩至痰液完全均勻化開,取50 μl痰液注入細胞池作細胞計數,其余痰液在常溫下3500 r/min離心10 min,取上清液分裝,-80 ℃保存待測。離心沉渣涂片行瑞氏-吉姆薩染色作細胞分類計數。
1.3 統計學處理 采用SPSS 10.0統計軟件進行統計學分析,數據以()表示,兩組之間比較采用t檢驗,多組之間比較采用單因素方差分析(F檢驗),采用Pearson相關分析計算相關系數,以P<0.05為差異有統計學意義。
2 結果
2.1 一般情況 正常對照組FEV1.0%預計值為(89.7±6.5),FEV1.0/FVC 值為 (81.7±8.5),PEF%預計值 (95.7±13.5);哮喘緩解期組FEV1.0%預計值為(67.7±5.5),FEV1.0/FVC值為(65.7±3.5),PEF%預計值(69.8±19.5);輕度急性發作期組FEV1.0%預計值為 (58.7±7.2),FEV1.0/FVC 值為 (59.6±7.5),PEF%預計值(57.6±18.5);中度急性發作期組FEV1.0%預計 值 為 (50.7±4.9),FEV1.0/FVC 值 為 (52.8±5.3),PEF%預計值(49.8±20.5);重度急性發作期組FEV1.0%預計值為 (40.7±4.8),FEV1.0/FVC 值 為 (48.8±7.8),PEF% 預 計 值(40.3±21.6)。各組的FEV1.0%預計值、FEV1.0/FVC值及PEF%預計值比較差異均有統計學意義(F值分別為23.132、25.012、21.025,P<0.01)。
2.2 血漿NO比較 健康對照組的血漿NO水平為(43.28±4.06)μmol/L,哮喘臨床緩解組為(56.30±3.07)μmol/L,急性發作期輕度組為(65.57±2.38)μmol/L,中度組為(71.73±6.08)μmol/L,重度組為(87.36±7.15)μmol/L,各組比較差異均有統計學意義 (F=23.5,P<0.101)。
2.3 誘導痰細胞計數分類 誘導痰細胞總數、中性粒細胞百分比、巨噬細胞百分比及嗜酸性粒細胞百分比在各組之間的比較差異均有統計學意義(F值分別為8.753、21.856、32.526、19.827,P<0.01),誘導痰淋巴細胞百分比在各組之間差異無統計學意義(F=0.461,P>0.05)。見表1。
表1 各組誘導痰細胞總數及分類計數()
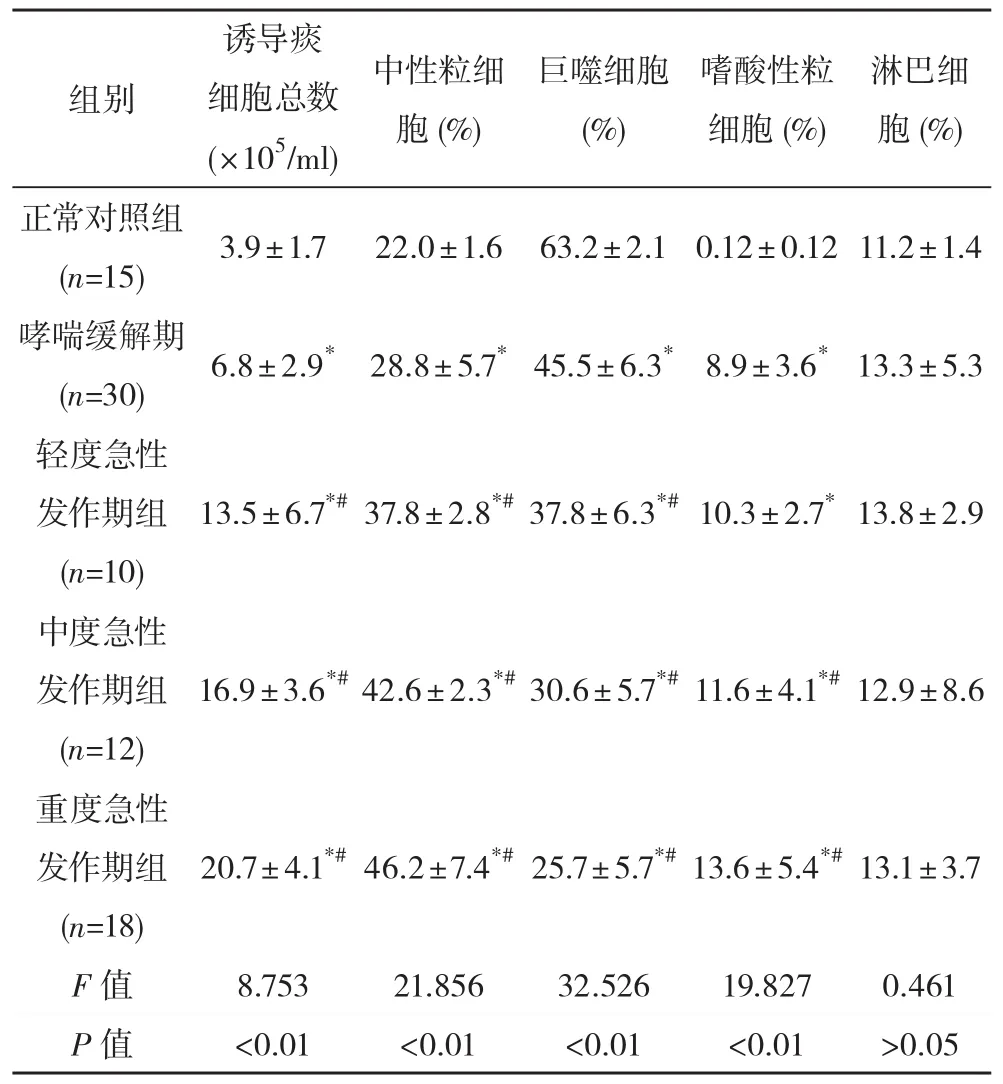
表1 各組誘導痰細胞總數及分類計數()
*與正常對照組相比,P<0.01;#與哮喘緩解期相比,P<0.01
正常對照組(n=15) 3.9±1.7 22.0±1.6 63.2±2.1 0.12±0.12 11.2±1.4哮喘緩解期(n=30) 6.8±2.9* 28.8±5.7*45.5±6.3* 8.9±3.6*13.3±5.3輕度急性發作期組(n=10)13.5±6.7*#37.8±2.8*#37.8±6.3*#10.3±2.7*13.8±2.9中度急性發作期組(n=12)16.9±3.6*#42.6±2.3*#30.6±5.7*#11.6±4.1*#12.9±8.6重度急性發作期組(n=18)20.7±4.1*#46.2±7.4*#25.7±5.7*#13.6±5.4*#13.1±3.7 F值 8.753 21.856 32.526 19.827 0.461 P值 <0.01 <0.01 <0.01 <0.01 >0.05
2.4 相關性分析 研究對象所處的狀態(健康、哮喘緩解期及哮喘發作期)與血漿一氧化氮水平明顯相關(r=0.786,P<0.01)。急性發作期患者血漿一氧化氮水平與FEV1.0%預計值呈負相關(r=-0.872,P<0.01),與誘導痰細胞總數、中性粒細胞百分比及誘導痰嗜酸細胞百分比呈正相關(r分別為0.857、0.816和0.825,P<0.01),與誘導痰巨噬細胞百分比呈負相關 (r=-0.820,P<0.01)。
3 討論
支氣管哮喘(簡稱哮喘)的發作是由于炎性細胞及某些結構性細胞釋放的多種細胞因子和趨化因子組成的復雜網絡,主要包括氣道炎癥、免疫與變態反應、氣道神經調節以及遺傳機制等,在內外因素的作用下,發生調控異常,導致炎癥-上皮細胞-氣道重塑-炎癥加重的惡性循環,牽涉多種炎癥介質及細胞因子。目前,合適的哮喘標志物及氣道炎癥介質的測定成為哮喘氣道炎癥研究新的熱點課題。
本研究表明,支氣管哮喘組的血漿一氧化氮水平顯著高于正常對照組,其中急性發作期組顯著高于緩解期組,急性發作期組中輕度、中度、重度三者之間比較差異均有統計學意義(P<0.01)。線性相關性分析顯示,一氧化氮水平與支氣管哮喘發作有相關性。與羅春玲[6]報道的一致。Ward等[7]通過實驗發現,NO供體可明顯抑制乙酰膽堿、組胺、白三烯D4所致的氣道收縮,NOS抑制劑L-NAME可以減弱由于干冷空氣、運動所引起的氣道收縮,但不影響乙酰膽堿釋放,提示NO有對抗乙酰膽堿收縮氣道平滑肌的作用,cNOS來源的NO可以松弛氣道平滑肌,對氣道平滑肌調節發揮作用;但哮喘發作時,cNOS來源的NO生成減少,氣道非腎上腺素能非膽堿能神經功能發揮不足,而iNOS活性大大增強導致局部NO大量產生,當體內持續大量合成NO,在發揮免疫效應的同時也造成局部組織損傷。NO造成氣道損傷的機理為,直接損傷氣道組織細胞的DNA、線粒體及含鐵酶類的活性,在氣道內的特殊化學環境中和O2-形成過氧化亞硝酸(ONOO-),與其他氮氧化物相互轉變,形成NO2等高毒性物質。血漿中大量的NO更多表現為細胞毒性作用,致毛細血管后微靜脈滲出增多,加重肺通氣/血流比例失調及加重支氣管痙攣。
哮喘時,嗜酸性粒細胞會顯著的升高已被公認,并與哮喘嚴重程度成正相關;它主要通過釋放胞質中的主要堿基蛋白(MBP)、嗜酸性粒細胞陽離子蛋白(ECP)、嗜酸性粒細胞衍生性神經毒素(EDN)等毒性顆粒蛋白損傷靶器官,這些顆粒蛋白是造成哮喘特征性表現的主要原因之一[8]。哮喘氣道炎癥時,嗜酸性粒細胞釋放NO的同時又促進嗜酸細胞的趨化,并抑制其凋亡,提示NO在哮喘嗜酸性粒細胞炎癥中起著放大作用[9]。
近年來的研究發現,在重度哮喘患者的氣道組織、支氣管肺泡灌洗液和痰液中中性粒細胞增多,它主要是其激活后釋放IL-8、氧自由基(O2-)、胰肽酶等介質,對肺組織造成損傷,從而在哮喘的發生發展中發揮重要的作用[10]。NO主要存在中心粒細胞的胞漿中,當中心粒細胞被激活時,分泌到細胞外并隨病情的嚴重程度而增加[11],它主要引起肺基底膜的降解、黏液腺過度增生、黏液過度分泌、上皮細胞損傷等,在哮喘患者大量的黏液栓形成中起著重要作用。另外,NO還能刺激IL-8的產生,促進中心粒細胞的聚集,加重氣道炎癥。
本研究結果表明,隨著哮喘的嚴重程度,誘導痰細胞總數及中性粒細胞百分比、嗜酸性粒細胞百分比升高,血漿一氧化氮水平明顯升高,提示NO可能通過上述途徑參與哮喘的慢性氣道炎癥過程,但仍需對此進行深入研究。
本研究作為支氣管哮喘發病機制的探究,尚有較多的局限性,認為一氧化氮的表達增高是導致哮喘炎癥改變的形成和進展的重要原因之一,將為下一步研究如何增加cNOS的活性和/或選擇性iNOS抑制劑的作用提供依據,可能為哮喘的治療提供一個新的突破點。
[1]Ricciardolo F L.Multiple roles of nitric oxide in the airways[J].Thorax,2003,58(2):175-182.
[2]Sapienza M A,Kharitonow S A,Horvath I,et al.Effect of Inhaled L-arginine on Exhaled Nitric Oxide in Normal and Asthmatic Subjects[J].Thorax,1998,53(3):172-175.
[3]中華醫學會呼吸病學分會哮喘學組.支氣管哮喘防治指南[J].中華結核和呼吸雜志,2008,31(3):177-189.
[4]張清友,杜軍保,石琳,等.內源性一氧化氮與硫化氫在大鼠低氧性肺動脈高壓中的相互作用[J].北京大學學報(醫學版),2004,36(1):53-56.
[5]Gibson P G,Wlodarczyk J W,Hensley M J,et al.Epidemiological association of airway inflammation with asthma symptoms and airway hyper responsiveness in childhood[J].Am J Rasp Crypt Care Med,1998,158(1):36-41.
[6]羅春玲,鄒晨容.哮喘患者血漿一氧化氮變化的臨床意義[J].中國醫學創新,2010,7(29):35-36.
[7]Philip E.ATS Workshop proceedings: exhaled nitric oxide and nitric oride oxidative metabolism in exhaled breath condensate[J].Proc Am Thorac Soc,2006,173(7):131-145.
[8]Park Y J,Oh E J,Park J W,et al.Plasma eosinophil cationic protein,interleukin-5,and ECP/Eo count ratio in patient with various eosinophilic diseases[J].Ann Clin Lab Sci,2006,36(3):262-266.
[9]Lex C,Ferreira F,Zacharasiewicz A,et al.Airway eosinophilia in children with severe asthma: predictive values of noninvasive test[J].Am J Respir Crit Care Med,2006,175(12):1286-1290.
[10]林劍.中心粒細胞在支氣管哮喘發病機制中的作用[J].國外醫學兒科學分冊,2001,28(1):22-24.
[11]Ramesh G,Jindal S K,Ganguly N K,et al.Increased nitric oxide production by neutrophils in bronchial asthma[J].Eur Respir J,2001,17(5):868-871.

