乳酸-EDTA雙配位劑體系化學鍍鎳的研究
劉定富, 崔 東
(貴州大學,貴州 貴陽550003)
0 前言
化學鍍鎳是通過可控的氧化還原反應在具有自催化作用的材料表面沉積鎳-磷合金的一種表面處理技術[1]。由于氧化劑與還原劑處于同一液相中,鍍液是熱力學上的不穩定體系。除了穩定劑外,還需加入適量的配位劑,以降低游離Ni2+的質量濃度,才能得到磷的質量分數高的耐蝕性鍍層。但如果配位劑與Ni2+形成的配合物的穩定性太高,則鍍速太慢,沒有實際價值;如果配位劑與Ni2+形成的配合物的穩定性太差,雖然鍍速很快,但所得鍍層中磷的質量分數不高,耐蝕性差。為兼顧鍍速與鍍層中磷的質量分數這對矛盾,通常采用復合配位劑[2]。本文將乳酸和EDTA進行復配,以鍍速與鍍層中磷的質量分數為評價指標,考察不同復配方式的結果,以期兼收兩者的優點,克服各自的缺點,得到鍍速適中、鍍層中磷的質量分數高且穩定的鍍層。
1 實驗
1.1 實驗材料
基體材料為45#碳鋼,試片尺寸為50mm×55 mm×1.5mm,表面積為56cm2。
1.2 工藝流程
1.3 鍍液組成及工藝條件
NiSO4·6H2O 23g/L,NaH2PO2·H2O 26g/L,NaAc·3H2O 15g/L,硫脲2mg/L,乳酸5~25g/L,EDTA 0~20g/L,pH值4.85,(88±1)℃,1h,裝載量1.1dm2/L。實驗規模為500 mL/次。
1.4 性能檢測
(1)鍍速
采用增重法測定鍍速,公式為:
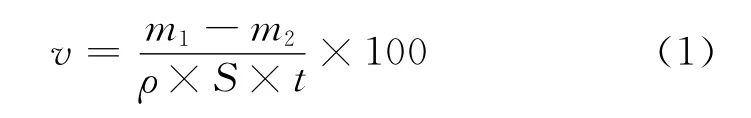
式中:v為鍍速,μm·h-1;m1為試片鍍前的質量,g;m2為試片鍍后的質量,g;ρ為鍍層密度,取7.85 g·cm-3;S為試片的表面積,dm2;t為時間,h。
(2)鍍層中磷的質量分數
根據GB/T 13913-92,采用磷鉬釩黃分光光度法測定鍍層中磷的質量分數。用濃硝酸將鍍層退鍍,然后加入高錳酸鉀將磷氧化成正磷酸鹽,再加入亞硝酸鈉還原多余的高錳酸鉀,將退鍍液轉入容量瓶中,用水定容,即得試液。在H+的濃度為0.2~1.6mol/L的硝酸介質中,正磷酸與鉬酸銨-釩酸銨溶液反應生成可溶性的磷鉬釩黃三元配位物,該配位物對波長為420nm的單色光有最大吸收,并且在質量濃度為2~20mg/L范圍內遵守比爾定律。
2 結果與討論
2.1 單獨用乳酸作配位劑
單獨用乳酸作配位劑,考察了乳酸的質量濃度對鍍速及鍍層中磷的質量分數的影響,實驗結果,如圖1和圖2所示。
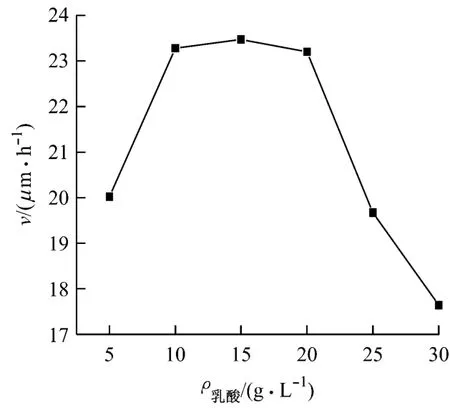
圖1 乳酸對鍍速的影響
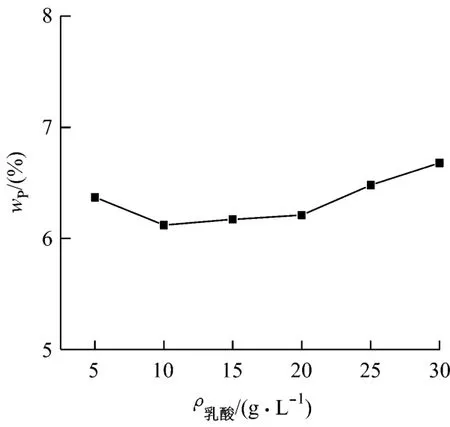
圖2 乳酸對鍍層中磷的質量分數的影響
由圖1可知:當乳酸的質量濃度小于10g/L時,鍍速隨乳酸的質量濃度的增加而增大;當乳酸的質量濃度大于20g/L時,鍍速隨乳酸的質量濃度的增加而減小;當乳酸的質量濃度為10~20g/L時,鍍速較大,最大約為23.6μm/h。由圖2可知:鍍層中磷的質量分數先隨乳酸的質量濃度的增加而略有減小;當乳酸的質量濃度大于10g/L時,鍍層中磷的質量分數隨乳酸的質量濃度的增加而緩慢增大;當乳酸的質量濃度為10~20g/L時,鍍層中磷的質量分數在6.2%~6.7%之間。由此可見,單獨用乳酸作配位劑,只能得到中磷鍍層。
2.2 固定乳酸時EDTA的影響
固定乳酸的質量濃度為20g/L,改變EDTA的質量濃度,考察其對鍍速及鍍層中磷的質量分數的影響,實驗結果,如圖3和圖4所示。
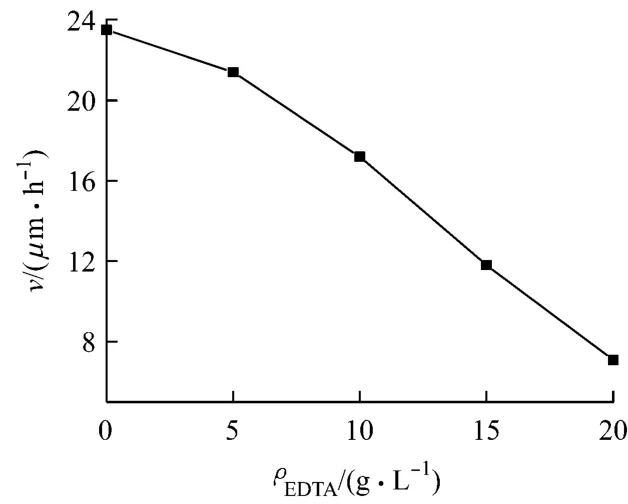
圖3 固定乳酸時EDTA對鍍速的影響
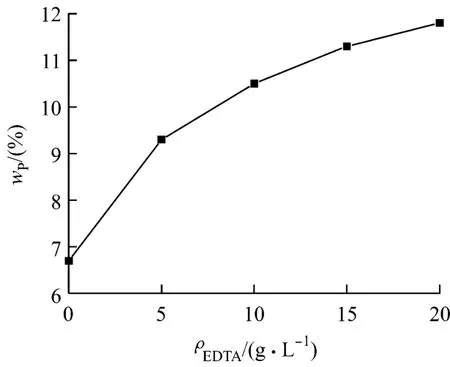
圖4 固定乳酸時EDTA對鍍層中磷的質量分數的影響
由圖3可知:固定乳酸的質量濃度為20g/L時,鍍速隨EDTA的質量濃度的增加而迅速下降。隨著EDTA的質量濃度從0g/L增加至20g/L,鍍速從23.5μm/h下降至7.1μm/h。由圖4可知:在乳酸的質量濃度固定不變的條件下,鍍層中磷的質量分數隨EDTA的質量濃度的增加而增大。開始時增幅較大,當EDTA的質量濃度增加至5g/L后,增幅減緩。單獨用乳酸作配位劑,即使其質量濃度高達20g/L,鍍層中磷的質量分數也僅為6.7%。而加入EDTA后,鍍層中磷的質量分數迅速增加,當EDTA的質量濃度增加至20g/L時,鍍層中磷的質量分數可達11.8%。采用乳酸+EDTA作復合配位劑,可得到高磷鍍層。
2.3 固定EDTA時乳酸的影響
固定EDTA的質量濃度為8g/L,改變乳酸的質量濃度,考察其對鍍速及鍍層中磷的質量分數的影響,實驗結果,如圖5和圖6所示。
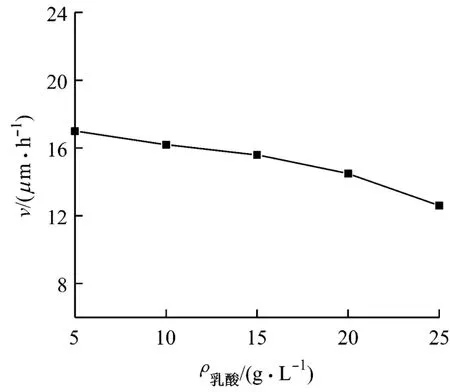
圖5 固定EDTA時乳酸對鍍速的影響
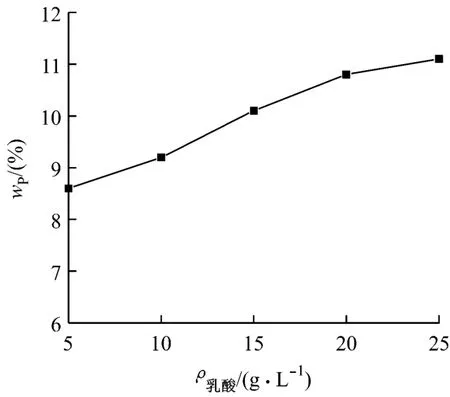
圖6 固定EDTA時乳酸對鍍層中磷的質量分數的影響
由圖5可知:在乳酸-EDTA雙配位劑體系中,固定EDTA的質量濃度為8g/L時,鍍速隨乳酸的質量濃度的增加而緩慢下降。隨著乳酸的質量濃度從5g/L增加到25g/L,鍍速從17.1μm/h下降至12.6μm/h。由圖6可知:在EDTA的質量濃度固定不變的條件下,鍍層中磷的質量分數隨乳酸的質量濃度的增加而緩慢增大。當乳酸的質量濃度為5~25g/L時,鍍層中磷的質量分數在8.7%~11.2%之間波動;當乳酸的質量濃度大于15g/L時,可獲得磷的質量分數大于10%的高磷鍍層。
在乳酸-EDTA雙配位劑體系中,乳酸主要起穩定鍍速的作用,而EDTA則主要起提高鍍層中磷的質量分數的作用。但兩者的質量濃度需控制在適當的范圍內,才能兼顧鍍速與鍍層中磷的質量分數這對矛盾。EDTA有兩個氨基和四個羧基,與Ni2+結合時會形成非常穩定的環狀螯合物,其配位穩定常數高達1018.6。隨著EDTA的質量濃度的增加,溶液中的游離Ni2+減少,沉積速率變慢。要使鍍速適中,EDTA的質量濃度應控制在5~10g/L之間。乳酸是一種兼配位劑、加速劑和緩沖劑于一體的有機酸,其與Ni2+的配位穩定常數適當,pK為2.2。單獨用乳酸作配位劑,當其質量濃度為10~20g/L時,鍍速較大,最大可達23.6μm/h,但所得鍍層中磷的質量分數較低(小于7%)。乳酸與EDTA復配時,既可以獲得較高的鍍速(17.1μm/h),又能得到高磷(10.5%)鍍層,彌補兩者單獨使用時的不足。
3 結論
單獨使用乳酸作配位劑時,只能得到中磷鍍層。乳酸與EDTA復配時,可兼顧鍍速與鍍層中磷的質量分數這對矛盾。在乳酸20g/L,EDTA 8g/L的條件下,鍍速為17.1μm/h,鍍層中磷的質量分數為10.5%。
[1]李寧,袁國偉,黎德育.化學鍍鎳基合金理論與技術[M].哈爾濱:哈爾濱工業大學出版社,2000.
[2]姜曉霞,沈偉.化學鍍理論及實踐[M].北京:國防工業出版社,2000.

