從制備血紅蛋白肽的血渣中提取血紅素
衛樂紅,時亞文,姜無邊,陳石良,*
(1.湖北奧彤生物制品科技有限公司,湖北孝感432600:2.湖北寶迪農業科技有限公司,湖北孝感432600)
我國有豐富的豬血資源,從豬血中可以得到超氧化物歧化酶(SOD)、凝血酶、血紅素鐵、蛋白粉等生化產品,如果能夠得到充分的開發利用,將是一筆極其巨大的財富[1]。血紅素的原料來源比較窄,一般是從動物的血液中提取,隨著動物血液的開發應用,其價格不斷上升。從制備超氧化物歧化酶或血紅蛋白肽的血渣中提取,如果技術得當,生產血紅素的成本可以大大降低。血紅素是人體中血紅蛋白的活性中心,其核心部位為鑲嵌在卟啉環中心的二價鐵離子,具有攜氧能力[2]。血紅素是暗紫色有光澤的細微針狀結晶或黑褐到棕色顆粒,顏色隨純化溶劑的不同而略有區別。在干燥的固體狀態下血紅素比較穩定,但在有光和氧化物的存在下容易被破壞,對熱比較穩定。能溶于酸性丙酮、堿性溶液、熱醇等溶劑中,不溶于水、稀酸、醚和氯仿[3]。主要存在于動物的血液中,具有重要的生理功能和很高的實用價值,在醫藥、保健品、食品、精細化工、化妝品等行業有廣泛的應用[4]。鐵是一種重要的微量元素,血紅素是一種重要的膳食鐵來源,在西方飲食中,有三分之二的鐵是由血紅素提的,主要來源于肌紅蛋白和血紅蛋白[5]。
1 材料與方法
1.1 材料與儀器
新鮮紅血球 寶迪農業科技有限公司恩彼事業部取來,通過水溶脹法溶血后用復合酶水解,上清液脫色噴霧干燥后即為血紅蛋白肽,下層沉淀作為提取血紅素的原料于4℃冰箱中儲存備用;NaHSO3、鹽酸、丙酮、無水乙醇、乙醚、醋酸鈉均為分析純 廣東金華科技股份有限公司;氯化血紅素標品為生化試劑 國藥集團化學試劑有限公司。
紫外可見分光光度計 UV-VIS 745,上海舜宇恒平科學儀器有限公司;離心機 D275M,長沙湘智離心機儀器有限公司;電子天平 DJ-6002,福州華志科學儀器有限公司;分析天平 BSA 224S-CW,賽多利斯科學儀器,北京有限公司;電熱鼓風干燥箱 DAG-9070A型,上海飛越實驗儀器有限公司;定時電動攪拌器 JJ-1,江蘇金壇市中大儀器廠。
1.2.1 酸性丙酮法提取血紅素的工藝流程

1.2.2 單因素實驗設計 取50g血渣,根據質量體積比加入不同體積的鹽酸丙酮混合溶液,充分攪拌,6000r/min離心10min,血紅素留在上清液中,取上清液。用2mol/L的NaOH調節上清液pH至5,并按體積比加入醋酸鈉溶液攪拌均勻靜置使血紅素沉降,6000r/min離心10min,沉淀即為血紅素。將沉淀分別用去離子水、無水乙醇以及乙醚洗滌兩次,60℃烘箱干燥即可。分別設置酸酮比(1∶100、2∶100、3∶100、4∶100、5∶100)、料液比(1∶2、1∶3、1∶4、1∶5、1∶6)和攪拌時間(5、10、15、20、25min)三個單因素實驗。
1.2.3 正交實驗設計 選定鹽酸丙酮體積比、料液比、攪拌時間進行單因素實驗,在單因素實驗的基礎上確定正交實驗的工藝條件,通過正交實驗確定優化的提取工藝條件,每個實驗重復3次,正交實驗設計如表1所示。

表1 血渣中提取氯化血紅素的正交實驗設計Table 1 Coded values and corresponding actual values of the optimization factors in the orthogonal array design
1.2.4 血紅素粗品的純化 采用劉任民[6]等的方法稍有改動,粗血紅素用0.1mol/L的NaOH充分溶解,6000r/min去掉沉淀,取上層溶液用1mol/L鹽酸溶液調節pH至5,加入1g/100mL的醋酸鈉,使血紅素沉淀下來,離心取沉淀,用去離子水反復清洗3次,95%的乙醇清洗兩次,乙醚清洗一次后60℃烘箱干燥即可。
1.2.5 血紅素各項指標檢測方法建立
1.2.5.1 血紅素鑒定
a.顯色反應:采用袁曦[7]等的方法,取血紅素鐵2mg,加0.1mol/L的氫氧化鈉溶液2mL于熱水中溶解,冷卻后加20%的硫酸溶液8mL,混合均勻,即生成棕色沉淀。過濾后取濾液1mL,加入硫酸氫銨試劑數滴,搖勻,溶液顯棕紅即為血紅素鐵。取標準樣品2mg,以同樣的操作方法作為對比。
b.血紅素的紫外掃描:分別取0.01g血紅素標準品和樣品血紅素,用0.1mol/L的氫氧化鈉溶解定容到100mL,用紫外可見分光光度計在200~800nm處掃描。
1.2.5.2 氯化血紅素含量的檢測
a.氯化血紅素標準曲線的繪制:取一定量的氯化血紅素標準品,105℃烘箱干燥4h以除去水分,精確稱取20mg干燥好的標準品,用0.1mol/L的NaOH溶解,定容至 100mL 分別吸取 1.0、2.0、3.0、4.0、5.0mL置于100mL的容量瓶中,用0.1mol/L的NaOH溶液定容至刻度,搖勻。以0.1mol/L的NaOH為空白,與385nm處測定吸光值,繪制標準曲線為y=0.0758x-0.0008,R2=0.9998。
b.氯化血紅素樣品含量的測定:取經過105℃干燥至恒重的氯化血紅素樣品,研成粉末;精密稱取適量樣品,置于100mL燒杯中,加0.1mol/L的氫氧化鈉溶液溶解,將溶液轉移到 100mL容量瓶中,加0.1mol/L的氫氧化鈉溶液至刻度,搖勻,過濾。取濾液10mL于100mL容量瓶中,用0.1mol/L氫氧化鈉溶液稀釋至刻度,搖勻,以0.1mol/L的氫氧化鈉溶液為空白。在385nm波長處測定其吸光度A。代入回歸方程即可求算氯化血紅素的含量,酶解血渣中的氯化血紅素含量為0.864g/100g,其血紅素提取率計算公式如式(1)。

1.2.5.3 氯化血紅素中鐵含量的測定
a.原子吸收分光光度法測氯化血紅素鐵含量
標準溶液:按國標GB/T 5009.90-2003的方法進行測定,準確稱量1g的精制鐵粉,用硝酸溶解,然后用0.5N的硝酸溶液定容到1000L,此溶液相當于1mg/mL,分別量取 0.5、1、2、3、4mL 標準使用液于100mL的容量瓶中,用0.5N的硝酸定容搖勻,用原子吸收分光光度計測定,繪制標準曲線。
樣品中鐵含量的測定:精確稱取均勻干燥的樣品1、2、3與標準樣品40mg,于100mL的燒杯中,加入混合酸消化液20mL,上蓋表皿,置于可調功率電爐中消化,直至無色透明為止,加入幾毫升去離子水,繼續加熱以除去多余的硝酸,待燒杯中溶液為2~3mL時,取下冷卻,用去離子水洗并移于10mL的刻度管中,用去離子水定容到10mL。空白用相同體積的混合酸消化液消化,步驟與上相同。
b.磺基水楊酸法測血紅素中鐵含量
標準溶液的配制:準確稱取0.7030g硫酸亞鐵銨于100mL的燒杯中,加入50mL 1mol/L鹽酸溶液,完全溶解后移入1L容量瓶中,再加入50mL 1mol/L,再用蒸餾水稀釋至刻度,混勻。取6支100mL的容量瓶編號,分別用移液槍取 0、1、2、3、4、5mL 鐵標準液于100mL容量瓶中,每份分別加入20%的磺基水楊酸7mL,然后加入1∶1的氨水2mL,使溶液由紅色變為穩定的黃色,再過量1mL,稀釋至刻度,搖勻。在分光光度計上選取最大吸收波長,λ=420nm,使用蒸餾水作為參比液,分別測定1~6號容量瓶吸光值,重復一次,然后取平均值,以測得的的吸光值為縱坐標,溶液濃度為橫坐標,繪制標準曲線。
樣品鐵含量的測定:配置樣品溶液,放入100mL的容量瓶中,按上述方法顯色并測其吸光值,求出樣品鐵含量。
2 結果與分析
2.1 單因素實驗
2.1.1 鹽酸丙酮添加量對氯化血紅素含量和提取率的影響 血紅蛋白是由4分子的血紅素和1分子的珠蛋白結合而成的,在酸性條件下,血紅蛋白中原先不帶電荷的埋藏在分子內部的組氨酸殘基(PI=7.0),由于帶有負電荷而暴露出來,此時血紅素和珠蛋白的結合較為疏松,蛋白質在丙酮的作用下沉淀后血紅素則留在溶液中[8]。料液比為5∶1,攪拌時間為20min,醋酸鈉添加量與提取液體積比為1∶100的條件下,由表2可知不同的酸酮比對氯化血紅素的含量有一定的影響,隨著鹽酸添加量的不斷增加,血紅素的含量和提取率持續上升,當酸酮比為3∶100時,得到的產品的含量和提取率都較高,分別達到了97.91%和63.50%。

表2 鹽酸丙酮比對氯化血紅素含量和提取率的影響Table 2 Effect of hydrochloric acid and acetone volume ratio on hemin purity and yield
2.1.2 料液比對氯化血紅素的含量以及提取率的影響 提取過程中加入丙酮是為了溶出血紅素并使蛋白質變性沉降下來,用量過少不能使蛋白質充分沉降,而用量過大料液比超過1∶6時,則產量不穩定,過濾困難[9]。在鹽酸丙酮體積比為3∶100,攪拌時間為20min,醋酸鈉添加量為1%的條件下,由表3可知:隨著酸性丙酮添加量的加大,提取的樣品的質量下降,這可能是因為丙酮的量增加,使珠蛋白沉降的更充分。當料液比為1∶5時,含量達到了最大值,再加大酸性丙酮的添加量時含量和提取率變化不大。

表3 料液比對氯化血紅素含量和提取率的影響Table 3 Effect of solid-liquid ratio on hemin purity and yield
2.1.3 攪拌時間對氯化血紅素的含量以及提取率的影響 在鹽酸丙酮體積比為3∶100,料液比為1∶5,醋酸鈉添加量為1%的條件下,由表4可以看出:攪拌時間在20min時所得的氯化血紅素的含量和提取率都較高,時間延長到25min時,則變化不明顯。
2.2 正交實驗
在單因素實驗的基礎上,選取鹽酸丙酮比、料液比、攪拌時間三個因素,采用正交設計表L9(34)進行三因素三水平的正交實驗,結果見表5,在分析過程中以氯化血紅素的含量與提取率為考察指標。

表4 攪拌時間對氯化血紅素含量和提取率的影響Table 4 Effect of stirring time on hemin purity and yield
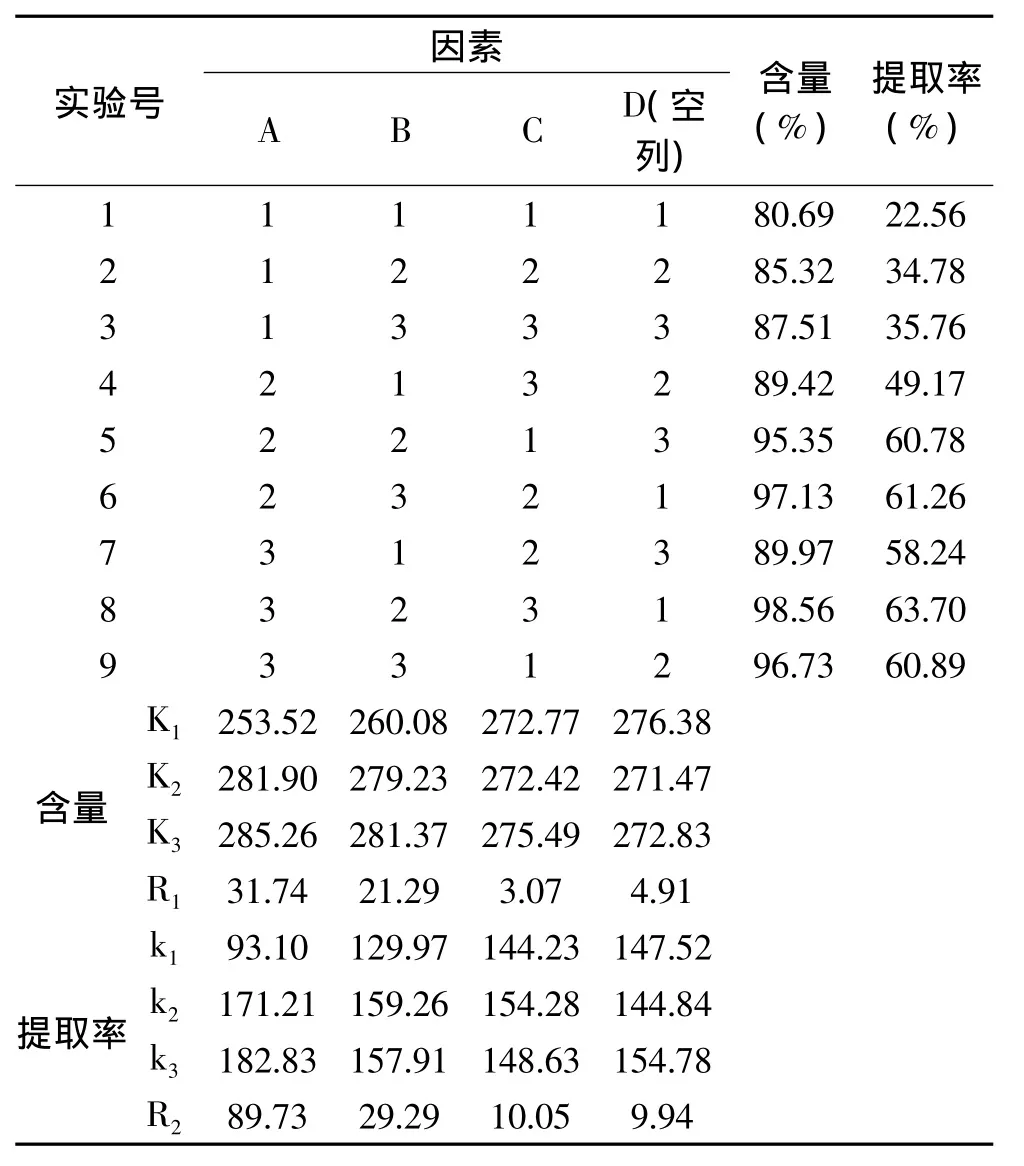
表5 工藝條件確定正交實驗設計及結果Table 5 Orthogonal array design matrix and corresponding experimental results
由正交表5可知,各因素對氯化血紅素的含量的影響次序是A>B>C,即鹽酸丙酮的體積比>料液比>攪拌時間,其最優水平為A3B3C3。各因素對氯化血紅素提取提取率的影響次序是A>B>C,即鹽酸丙酮的體積比>料液比>攪拌時間,最優水平為A3B2C2。由于兩個考察指標獨立分析后得出的最佳工藝條件不同,需要對它們影響的主次順序進行綜合考慮以確定最后的最佳工藝,考慮到氯化血紅素的提取率與其含量和樣品的質量相關,且呈正比關系,故以氯化血紅素的提取率為主要考慮因素。根據正交實驗結果,對于因素B,即為料液比(v/v)為1∶5和1∶6時,2水平和3水平相差不大,考慮到有機試劑成本問題,選擇B2比較合適。綜合考慮,優化的工藝條件是 A3B2C2,即鹽酸丙酮體積比為4∶100,酸性丙酮添加量為血渣體積的5倍,攪拌時間為20min。通過極差分析可得到因素C的R值小于空白列的R值,說明此因素對氯化血紅素含量這一指標沒有顯著意義。
2.3 氯化血紅素的鑒定
2.3.1 產品性狀 所得產品肉眼觀察為黑褐色,反射光下為鋼藍色的粉末狀晶體,與參考文獻[10]報道的氯化血紅素性狀一致;不溶于水、稀酸、醚、氯仿、及丙酮,溶于氫氧化鈉水溶液、熱醇或氨水中,在水中穩定,在有氧與光照條件下容易被破壞,與參考文獻[11]的報道一致。
2.3.2 顯色反應 見圖1,左邊試管為血紅素標準樣品,右邊為樣品,可以看出兩個試管中溶液顏色都是淺棕色,外觀性質一致,可以確定樣品為氯化血紅素。

圖1 氯化血紅素的顯色反應Fig.1 Color yield properties of hemin
2.3.3 氯化血紅素的紫外掃描圖譜 從圖2可以看出,對照品和供試品紫外可見光譜基本一致,最大吸收峰為410nm,與文獻報道一致[12],可以判定所提取的樣品為氯化血紅素。
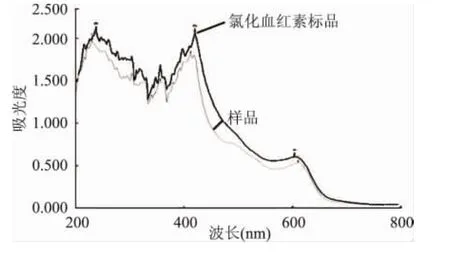
圖2 氯化血紅素的紫外光譜圖Fig.2 The UV spectrum of hemin
2.4 氯化血紅素制備收率及含量
用優化的工藝重復3次,純化后制備氯化血紅素,結果見表6。

表6 氯化血紅素提取率和收率Table 6 The purity and yield of hemin
2.5 氯化血紅素鐵含量檢測
分別采用國標GB/T 5009.90-2003中原子吸收分光光度法以及磺基水楊酸顯色法對血紅素中鐵含量進行檢測,其標準曲線見圖3。
所提樣品中鐵含量檢測及分析結果見表7。

圖3 原子吸收分光光度法測氯化血紅素中的鐵含量Fig.3 The detection of hemin’s iron content by atomic absorption spectrophotometric

圖4 氯化血紅素鐵含量檢測的標準曲線Fig.4 The standard curve of hemin iron content

表7 氯化血紅素成品鐵含量檢測Table 7 The detection of hemin’s iron content
從表7可見用原子吸收法所測得的鐵含量指標比用分光光度法測得的數值偏高,考慮到原子吸收分光光度法法的精密度比分光光度法的高,并且省時,選擇原子吸收分光光度法為這一指標的檢測方法。
3 結論與討論
3.1 血渣中提取血紅素的最佳工藝條件是A3B2C2,即鹽酸丙酮比為4∶100、料液比為1∶5、攪拌時間為20min,提取的血紅素含量可以達到98%以上,鐵含量7.8%以上,提取率達到60%以上,達到市場要求。此工藝方法易于操作、重復性好、所得產品含量高,適合工業化生產。
3.2 血紅素很不穩定,容易被氧化成氯化血紅素,所以提取之前在血渣中添加少量的還原劑,可以防止血紅素在提取過程中被氧化,另外還可以將已經被氧化的血紅素還原成亞鐵血紅素。血紅素在光照下不穩定,因此整個提取過程應盡量避免光照。
3.3 動物血球酶解制備血紅蛋白肽之后剩下的血渣富含血紅素,可以用來提取血紅素,且在提取工藝過程中丙酮使用率量較其他工藝大大減少,提取后剩下的雜蛋白經過脫除有機溶劑處理又可以作為飼料銷售,增加了豬血附加值。
[1]宋照軍,張延生,劉璽,等.豬血中血紅素提取純化新技術研究[J].肉類工業,2004,8(8):23-25.
[2]吳立芳.利用豬血制備氯化血紅素技術的研究[D].湖南農業大學,2006.
[3]李志釗,葉春華.血紅素的應用與生產技術研究進展[J].食品研究與開發,2000,10(20):12-14.
[4]張婷,莊紅,薛培宇.血紅素鐵功能及其二價鐵保護探索[J].肉類研究,2008,3:18-20.
[5]Adrian R West,Phillip S Oates.Mechanisms of heme iron absorption:Current questions and controversies[J].World J Gastroenterol,2008,14(26):4101-4110.
[6]劉任民,范萬東,王搖風,等.豬血中高純度血紅素的提取工藝[J].現代醫學衛生,2007,23(18):2687-2689.
[7]鐘耀廣.豬血中卟啉鐵的提取方法及血紅素修飾技術的研究[D].北京:中國農業大學,2002.
[8]袁曦,洪清.氯化血紅素提取工藝及質量標準研究[J].藥品檢驗,1997,32(6):360-362.
[9]王穎明,莫寶慶,徐濟達,等.豬血中血紅素提取條件的比較[J].食品科技,2007,32(10):246-254.
[10]汪長國,戴亞,劉少民,等.超聲波酸性丙酮法制備氯化血紅素[J].食品科學,2010,31(6):109-113.
[11]羅章,鄭立紅.血紅素色素制取及在肉品加工中的應用[J].中國農業科技導報,2006,8(1):40-42.
[12]楊娟.利用豬血制備氯化血紅素及分析[D].重慶:重慶大學,2008.

