復方硫磺洗劑微生物限度檢查方法的建立
王海華(南寧食品藥品檢驗所,南寧 530001)
復方硫磺洗劑處方由升華硫、硫酸鋅、樟腦醑、甘油、甲基纖維素等組成,制劑中硫磺與皮膚分泌物作用生成硫化物,能使表皮軟化,并有脫脂、殺菌、止癢以及抑制角質形成作用;硫酸鋅具有輕度殺菌以及收斂作用;樟腦具有局部止痛、止癢的效果。該洗劑可用于治療疥瘡、體癬、手足癬、腳氣等,為外用藥。
在對具有抗菌活性的藥品進行微生物限度檢查時,應首先消除其抗菌活性,并通過試驗驗證是否徹底去除抗菌活性,以保證檢驗結果的有效性。薄膜過濾法是消除藥品中抗菌活性的最有效方法,但由于復方硫磺洗劑處方中升華硫不溶于水,使得無法簡單地采用水溶液作為沖洗劑去除抗菌活性。筆者在試驗中發現,在薄膜過濾法中以聚山梨酯80作為增溶劑,可有效去除復方硫磺洗劑的抑菌作用。據此,筆者建立了通過薄膜過濾結合在沖洗液中加入聚山梨酯80的方法,對復方硫磺洗劑進行了微生物限度檢查;并按2010年版《中國藥典》(二部)規定的方法[1]對復方硫磺洗劑微生物限度檢查方法進行了驗證,以確定該制劑所用微生物限度檢查方法的有效可行。
1 材料
1.1 儀器
LRH-250-G型光照培養箱、LRH-250-A型生化培養箱(廣東省醫療器械廠);HR-8753GM微波爐(青島海爾微波制品有限公司);Ⅱ級生物安全柜(上海振梓創空氣凈化設備有限公司)。
1.2 藥品
復方硫磺洗劑(廣西中醫學院瑞康醫院制劑室,批號:090218、090303、090316,規格:每瓶 200ml,含硫磺 0.03g/ml)。
1.3 菌種
枯草芽孢桿菌(Bacillus subtilis)[CMCC(B)63501]、金黃色葡萄球菌(Staphlococcus aureus)[CMCC(B)26003]、大腸埃希菌(Escherichia coli)[CMCC(B)44102]、銅綠假單胞菌(Pseudomonas aeruginosa)[CMCC(B)10104]、白色念珠菌(Candida albicans)[CMCC(F)98001]、黑曲霉(Aspergillus niger)[CMCC(F)98003]均來自中國醫學細菌保藏管理中心。
1.4 培養基及稀釋劑、增溶劑
營養瓊脂培養基(批號:090226)、玫瑰紅鈉瓊脂培養基(批號:090318)、膽鹽乳糖培養基(BL,批號:090529)、蛋白胨(批號:090617)均來源于廣西食品藥品檢驗所;營養肉湯培養基(批號:090518)、溴化十六烷基三甲銨瓊脂培養基(批號:090601)均來源于北京三藥科技開發公司;改良馬丁培養基(批號:090302)、甘露醇氯化鈉瓊脂培養基(批號:090311)均來源于北京陸橋技術有限責任公司;適用性檢查符合2010年版《中國藥典》的相關規定。pH7.0無菌氯化鈉-蛋白胨緩沖液、0.1%蛋白胨水溶液、含0.1%聚山梨酯80的0.1%蛋白胨水溶液、0.9%無菌氯化鈉溶液等為自制。
2 方法與結果
參照2010年版《中國藥典》(二部)微生物限度檢查法[1]進行試驗,簡述如下:
2.1 菌液的制備
接種金黃色葡萄球菌、枯草芽孢桿菌、大腸埃希菌和銅綠假單胞菌的新鮮培養物至營養肉湯培養基中,30~35℃培養18~24h;接種白色念珠菌的新鮮培養物至改良馬丁培養基中,23~28℃培養24~48h。上述培養物用0.9%無菌氯化鈉溶液制成每1ml含菌數為50~100CFU的菌懸液。接種黑曲霉的新鮮培養物至改良馬丁瓊脂培養基中,23~28℃培養5~7d,加入3~5ml 0.9%無菌氯化鈉溶液,將孢子洗脫。吸出孢子懸液至無菌試管內,用0.9%無菌氯化鈉溶液制成每1ml含孢子數為50~100CFU的孢子懸液。
2.2 供試液制備
取供試品10ml,加pH 7.0無菌氯化鈉-蛋白胨緩沖液稀釋至100ml,制備成均勻的1∶10的供試液,靜置5min,取上清液備用。
2.3 微生物限度檢查方法
2.3.1 平皿法:取1∶10的供試液1ml注入平皿。
2.3.2 培養基稀釋法:取1∶10的供試液1ml,注入5個平皿,每個平皿0.2ml。
2.3.3 薄膜過濾法:取1∶10的供試液10ml,采用薄膜過濾法,分別以0.1%蛋白胨水溶液(A)及含0.1%聚山梨酯80的0.1%蛋白胨水溶液(B)為沖洗液。沖洗量:A 100、200、300、400、500、600、700、800ml,B 100、200ml。
2.4 細菌、霉菌和酵母菌檢查方法學驗證試驗
2.4.1 試驗組:按“2.3”項下方法操作后,分別將50~100CFU/ml的試驗菌1ml,注入同一平皿中(n=3),立即傾注瓊脂培養基,待凝固后置于規定溫度,細菌培養24~48h,白色念珠菌和黑曲霉培養48~72h,測定其菌數;薄膜過濾法時,取供試液過濾、沖洗,在最后一次沖洗液中加入試驗菌1ml,過濾,按薄膜過濾法測定其菌數。
2.4.2 菌液組:取試驗菌1ml注入平皿中(n=3),立即傾注瓊脂培養基,待凝固后置于規定溫度,細菌培養24~48h,白色念珠菌和黑曲霉培養48~72h,測定所加入的試驗菌數;薄膜過濾法時,取供試液過濾,沖洗,在最后一次沖洗液中加入試驗菌1ml,過濾,按薄膜過濾法測定其菌數。
2.4.3 供試品對照組:按“2.3”項下相應方法操作后,立即傾注瓊脂培養基,待凝固后置于規定溫度,細菌培養24~48h,白色念珠菌和黑曲霉培養48~72h,測定供試品本底菌數;薄膜過濾法時,取供試液過濾,沖洗,按薄膜過濾法測定其菌數。
2.4.4 回收率的計算:試驗組的加菌回收率=(試驗組平均菌落數-供試品對照組平均菌落數)/(菌液組的平均菌落數)×100%。
試驗結果表明,本品采用平皿法、培養基稀釋法、薄膜過濾法[A,即以0.1%蛋白胨水溶液為沖洗液(沖洗量100、200、300、400、500、600、700、800ml)進行檢驗,枯草芽孢桿菌的回收率均小于70.0%];采用薄膜過濾法[B,即以含0.1%聚山梨酯80的0.1%蛋白胨水溶液為沖洗液(沖洗量為每膜200ml)]進行檢驗,枯草芽孢桿菌的回收率均>85.0%。而大腸埃希菌、金黃色葡萄球菌、白色念珠菌、黑曲霉采用培養基稀釋法(每皿0.2ml)測定,回收率均>80.0%,結果詳見表1。3批樣品5種試驗菌采用薄膜過濾法(B),回收率均>85.0%,結果見表2。
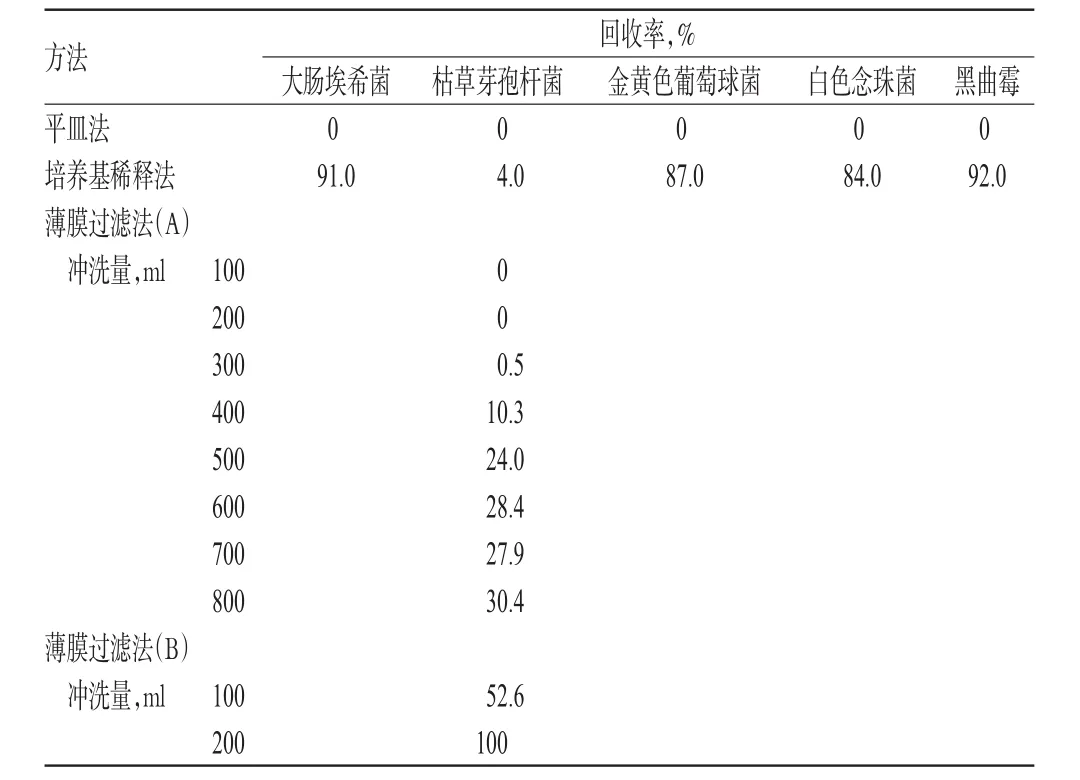
表1 不同方法回收率結果(n=3)Tab 1Recovery rate by different methods(n=3)
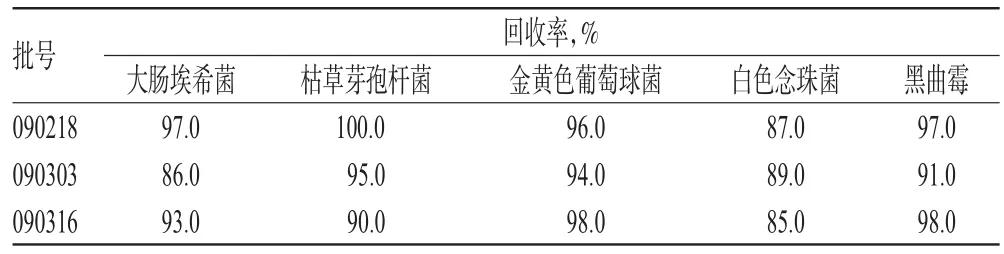
表2 3批樣品薄膜過濾法(B)回收率結果(n=3)Tab 2 Recovery rate of membrane filtration method(B)for 3batches of samples(n=3)
2.5 控制菌檢查驗證試驗
2.5.1 金黃色葡萄球菌:取上述1∶10的供試液10ml加入至相應100、200、300ml的營養肉湯培養基中(共2組),同時一組接種金黃色葡萄球菌10~100CFU作為試驗組,另一組接種大腸埃希菌10~100CFU作為陰性菌對照組,35℃培養24h。結果,試驗組、陰性菌對照組的營養肉湯均呈現渾濁。分別取培養物劃線接種于甘露醇氯化鈉瓊脂培養基平板上,35℃培養24~72h,結果陰性菌對照組100、200、300ml及試驗組100、200ml在平板上均未見菌落生長,試驗組300ml在平板上有金黃色葡萄球菌典型菌落生長,結果見表3。

表3 金黃色葡萄球菌驗證試驗結果Tab 3 Results of validation tests for Staphlococcus aureus
從表3可得出,采用培養基稀釋法(培養基300ml),陰性菌對照組未檢出陰性對照菌,試驗組檢出試驗菌。表明金黃色葡萄球菌可采用此法進行控制。
2.5.2 銅綠假單胞菌:取上述1∶10的供試液10ml加入至100ml BL培養基中(共2組),同時一組接種銅綠假單胞菌10~100CFU作為試驗組,另一組接種大腸埃希菌10~100CFU作為陰性菌對照組,35℃培養18~24h。結果,試驗組、陰性菌對照組的BL均呈現渾濁。分別取培養物劃線接種于溴化十六烷基三甲銨瓊脂培養基平板上,35℃培養18~24h,結果陰性菌對照組在平板上未見菌落生長,試驗組在平板上有銅綠假單胞菌典型菌落生長,結果表明銅綠假單胞菌可采用常規法進行控制,詳見表4。

表4 銅綠假單胞菌驗證試驗結果Tab 4 Results of validation tests for Pseudomonas aeruginosa
2.6 驗證試驗結果
按上述建立的復方硫磺洗劑微生物限度檢查法,細菌數采用薄膜過濾法(B),即以含0.1%聚山梨酯80的0.1%蛋白胨水溶液為沖洗液(沖洗量為每膜200ml)進行測定,霉菌、酵母菌數采用培養基稀釋法(每皿0.2ml)測定,對控制菌金黃色葡萄球菌采用培養基稀釋法(培養基300ml),銅綠假單胞菌采用常規法。對3批樣品進行檢驗,結果可確定上述方法為本品的微生物限度檢查方法,詳見表5。

表5 3批樣品微生物限度檢查方法驗證試驗結果Tab 5 Results of validation tests of microbial limit test for 3batches of samples
3 討論
(1)增溶劑對試驗結果的影響:復方硫磺洗劑處方中主要抑菌成分為升華硫,不溶于水,微溶于乙醇、醚,易溶于二硫化碳。最直接、有效的去除抑菌活性的方法當屬薄膜過濾法。試驗中,薄膜過濾采用以0.1%蛋白胨水溶液為沖洗液從100ml至800ml進行沖洗,但枯草芽孢桿菌的回收率仍無法達到《中國藥典》70.0%的要求;且試驗菌生長緩慢、弱小,往往需要延長2d培養時間。聚山梨酯80是非離子型的表面活性劑,具有乳化、擴散、增溶和穩定的作用,還可作為中和劑(滅活劑),即其使用不但增加藥品的溶解性,還對藥品抑菌性具有中和作用[2],故選擇聚山梨酯80作為增溶劑。其增溶機制是表面活性劑在水中形成“膠束”的結果,由于膠束的內部與周圍溶劑的介電常數不同,難溶性藥物根據自身的化學性質,以不同方式與膠束相互作用,使藥物分子分散在膠束中。對增溶劑的加入量進行選擇,結果顯示,加入量過小,不能完全分散藥物;加入量過大,會出現過量的泡沫,影響沖洗效果。故最后以0.1%的聚山梨酯80作為增溶劑,可滿足試驗需要。
(2)不同醫院生產的復方硫磺洗劑在微生物限度檢查方法有所不同,有使用薄膜過濾法[3],也有采用離心沉淀法結合薄膜過濾法[4]。原因有可能是不同醫院同一制劑在處方原料和制備方法上有所不同,由于制劑穩定性的問題,有的醫院可能對該制劑作一些改進;也可能有的醫院用升華硫,有的用沉降硫;還有可能硫磺的質量不同等。因此,在藥品監督檢驗工作中,經常遇到同一制劑不同生產廠家提供的微生物限度檢查資料所采用的方法不同的情況,比如有常規法、培養基稀釋法、離心沉淀法、薄膜過濾法等。
微生物限度檢查目前在國外越來越受到重視,每版藥典收載的品種也越來越多,如《美國藥典》(USP)24版收載微生物限度品種(217個)較23版(150個)增加67個[5]。從發展趨勢來看,國家藥品標準對不同單位生產的同一劑型同一品種的藥品應制訂統一的檢驗方法,以促進我國由以劑型制訂微生物限度標準向以品種制訂微生物限度標準過渡工作的進行。從本試驗結果得出,為了制訂科學合理的復方硫磺洗劑微生物限度檢查方法,建議統一采用在沖洗液中加入0.1%聚山梨酯80的薄膜過濾法較為穩妥。該方法具有簡便、實用的特點。
(3)《中國藥典》規定[1],若藥品的組分或原檢驗條件發生改變可能影響檢驗結果時,對檢查方法應重新驗證。由于進行再驗證時,藥品中的活性成分未發生改變,故其抗菌譜也未改變,因此筆者認為再驗證工作僅需針對《中國藥典》規定的全部驗證菌株中的最敏感菌株即可,而不必對全部菌株進行再驗證。即對復方硫磺洗劑進行再驗證時,僅需證明試驗中最敏感菌株(枯草芽孢桿菌)的回收率大于70.0%,即可說明檢查方法有效,無需再逐一驗證大腸埃希菌、金黃色葡萄球菌、白色念珠菌和黑曲霉的回收率。采用這種方法,既可保證檢驗方法的有效性,又節省了大量人力、物力,使得驗證工作有可能成為日常檢驗的一部分。建議《中國藥典》逐步收載各抗菌藥物的最敏感驗證菌株作為質控菌株,以方便日常檢驗工作。
[1] 國家藥典委員會.中華人民共和國藥典:二部[S].2010年版.北京:中國醫藥科技出版社,2010:附錄107-116.
[2] 張光華,余立.聚山梨酯80和卵磷脂在化學藥微生物限度檢查時的中和作用[J].藥物分析雜志,2008,28(7):1127.
[3] 夏巧鳳,王曉梅.復方硫磺洗劑微生物限度檢查方法研究[J].臨床合理用藥,2012,5(2B):32.
[4] 馬曉璇,李汶,溫玉瑩.2種含硫磺制劑的微生物限度檢查方法驗證[J].今日藥學,2009,19(2):50.
[5] 周劍,李霞.藥品微生物限度檢查法中幾種樣品前處理方法的可行性研究[J].中國藥房,2012,23(33):3136.

