鋰電池負極材料復合鈦酸鋰的制備及電化學性能研究
張 勇,王興蔚,馬 勇,侯春平,龔波林
(寧夏共享新能源材料有限公司,寧夏銀川 750021)
目前,商品化動力鋰離子電池負極材料以嵌鋰碳材料為主。這類嵌鋰碳材料容易與電解液表面形成SEI鈍化膜,會減小極片與電解液發生副反應的機會,但卻消耗了電解液,降低了庫侖效率,并導致明顯的電壓滯后現象。在充放電過程中,容易產生鋰枝晶現象,造成短路等安全問題。鈦酸鋰(Li4Ti5O12)作為最有希望實現產業化的非碳類負極材料,具有結構穩定、循環性能好、使用壽命長和高安全性的特點。鈦酸鋰的理論比容量為175 mAh/g,實際可達165 mAh/g。其電位電壓為1.55 V,可以與鈷酸鋰、磷酸亞鐵鋰、錳酸鋰等組成電池電壓在3.7~4.2 V的鋰離子電池。鈦酸鋰(Li4Ti5O12)材料電子導電率較低,僅為10-9S/cm,不利于電池容量及循環性能的發揮。本文采用液相混合分散-霧化干燥和一次煅燒法,對鈦酸鋰制備工藝及改性方法進行探究。
1 實驗部分
1.1 藥品和儀器
藥品:碳酸鋰(Li2CO3),純度97.0%;二氧化鈦(TiO2),純度99.5%,粒徑≤500 nm;導電炭黑,SSA 800 m2/g;羧甲基纖維素鈉(CMC),純度 97%,粘度 140 mPa·s,pH7.5;無水乙醇(A.R)。
制備及檢測設備:選用砂磨分散機、行星式球磨機、噴霧干燥機、管式燒結爐等合成設備及萬分之一天平、真空烘箱、鼓風干燥箱、手套箱、電性能測試儀等檢測設備。
1.2 實驗過程
1.2.1 鈦酸鋰(Li4Ti5O12)的合成 按照 n(Li):n(Ti)=0.75的配比,稱取化學藥品Li2CO3和TiO2以及3 wt%的CMC作為粘結劑。首先量取一定量的CMC藥品于容器內,加入適量的無水乙醇作為分散劑,使CMC充分溶解。然后,按比例加入鋰源與鈦源,并加入合適的去離子水。在攪拌作用下,使物料充分溶解并混合均勻。對物料進行濕法球磨處理24 h,通過噴霧干燥制備出前驅體。將前驅體在N2氣氛保護下,進行高溫煅燒,得到尖晶石型鈦酸鋰(Li4Ti5O12)目標產物。該反應方程式如下:
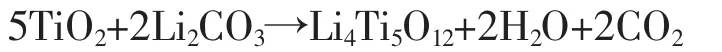
1.2.2 電池的裝配與測試 電極制備:將活性物過200目標準篩處理后,放置于烘箱中,在115℃下干燥2 h。同時,將處理過的導電炭黑和聚四氟乙烯/N-甲基吡咯烷酮溶液按計量比混合均勻。加入活性物,并經過間歇攪拌,制成均勻漿料。涂覆在銅箔上,制成電極片,并作標號處理。將該極片置于100℃以上的真空干燥箱中干燥約8~12 h后,進行碾壓和干燥,待機裝配。
電池組裝與測試:該測試為半電池測試。電解液為以DMC/EMC/EC為溶劑的LiPF6溶液,隔膜為PP/PE/PP多孔聚合物膜材料,鋰片為對電極,在充滿氫-氬混合氣的手套箱中進行組裝。通過恒流充放電循環測試,測試電壓為1.0~2.5 V。
1.3 結構及形貌表征
對鈦酸鋰前驅體進行熱失重(TG-DSC)分析,可以得出較為準確的合成溫度范圍。測試條件如下:溫度:室溫~1 000℃,N2氣氣氛,升溫速率 10℃/min。
用X射線衍射對產物進行結構分析。條件:管壓4.0 kV,管流 20 mA,Cu Kα 射線,λ=0.154 05 nm,掃描范圍 10~70℃。
通過掃描電鏡觀察樣品的粒徑和形貌(200 kV)。
2 結果與討論
2.1 鈦酸鋰樣品分析
2.1.1 TG-DSC分析
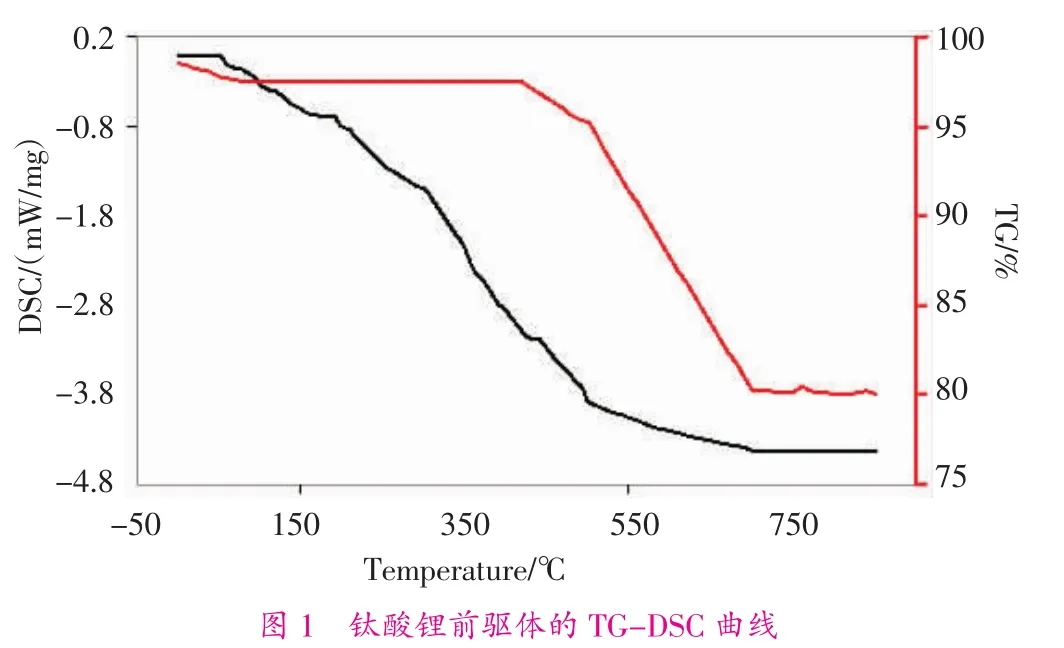
圖1為鈦酸鋰前驅體熱重曲線。由圖可知:TG曲線上有3個吸熱峰對應熱重曲線上的3段失重。經分析,可以看出:在450℃以下為第一段,有3%的失重。在該階段,由于混合粉末中的少量有機物和結晶水或表面吸附水的損失,或者是未揮發溶劑損失造成。溫度在45~680℃為第二失重階段,開始表現出主要的損失,約有15%的失重。該階段,原料高溫燃燒,發生熔融分解,活性自由基團逐步擴散,相互接觸反應,最終生成目標產物鈦酸鋰。但在該階段,仍有少量中間相或其它副產物。到680℃時,為第三失重階段。曲線沒有明顯的失重,表明反應基本完全。因此,鈦酸鋰的合成溫度應控制在700~1 000℃,本文選取700℃、800℃、900℃煅燒前驅體合成樣品,并進行結果分析。
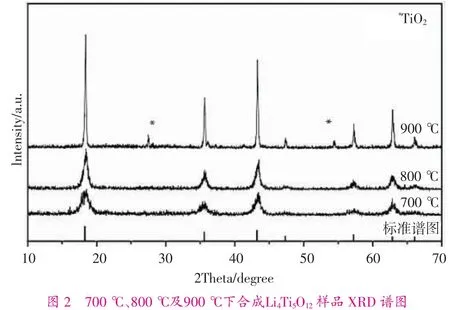
2.1.2 樣品XRD衍射分析 圖2為前驅體在不同溫度(700℃、800℃、900℃)下燒結得到的樣品XRD譜圖,發現衍射峰與標準卡片JCPDS(26-1198)衍射峰吻合,表明制備的樣品具有尖晶石型結構的鈦酸鋰。圖中的衍射峰比較尖銳,說明樣品的晶型較為完整。由圖可看出,在700℃下燒結得到的產物各衍射峰尖銳,說明該條件下Li4Ti5O12已基本生成。當燒結溫度為800℃時,衍射峰強度更強,且與標準卡JCPDS(26-1198)衍射峰完全相符,無雜質衍射峰,表明800℃下生成了唯一物相Li4Ti5O12。當燒結溫度達到900℃時,譜圖中出現了金紅石型TiO2特征峰,分析認為:Li4Ti5O12在此溫度下發生分解。
2.1.3 樣品SEM表征分析 圖3為不同燒結曲線下,樣品Li4Ti5O12的SEM圖。由圖看出:隨著燒結溫度升高,顆粒逐漸增大且團聚現象也越加明顯。其中,燒結溫度為800℃時,分散較好,團聚適中。溫度為900℃時,粒徑最大。總體來看,在800℃燒結制備出的樣品Li4Ti5O12顆粒徑較小,團聚較少,很大程度上能夠增大反應接觸面積,有利于Li+的嵌入和脫出,從而利于提高材料的實際比容量,降低極化程度,增強導電性能。
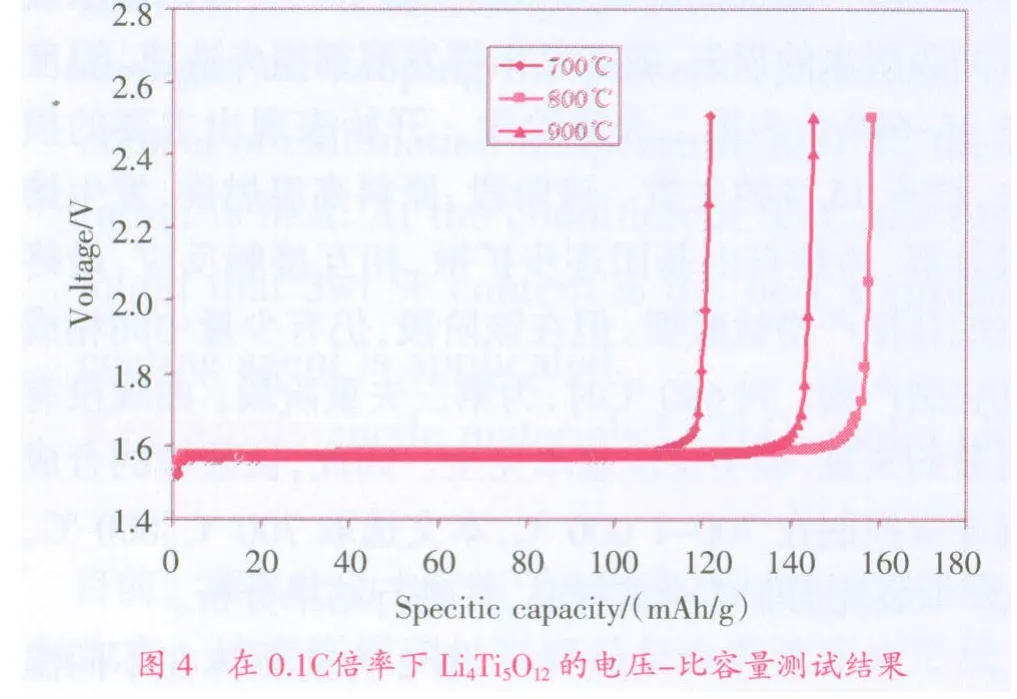
2.1.4 樣品電化學性能 圖4反映了前驅體經過700℃、800℃、900℃高溫燒結后的電性能測試結果。
由圖4能夠看出:固定物料配比和其它條件,控制焙燒溫度為700℃、800℃、900℃時,隨著溫度的升高,比容量呈先增大后減小的趨勢。同時看到:比容量的變化幅度在逐漸下降,即(Δ比容量/Δ溫度)的量值在不斷減小。由電壓分布規律,可明顯觀察到:在充電深度(COD)不到70%時,不同燒結溫度下的放電電壓平臺幾乎重合。電位電壓穩定在1.55 V左右,該測量值與理論值較為接近,被認為具有較好的穩定性。

2.2 碳包覆鈦酸鋰樣品分析
經過高溫煅燒制備的鈦酸鋰樣品,雖然首次放電比容量能夠達到160 mAh/g,但容量衰減較快,且效率較低。需要經過包覆改性,來提高容量保持率和充放電效率。
2.2.1 XRD衍射分析
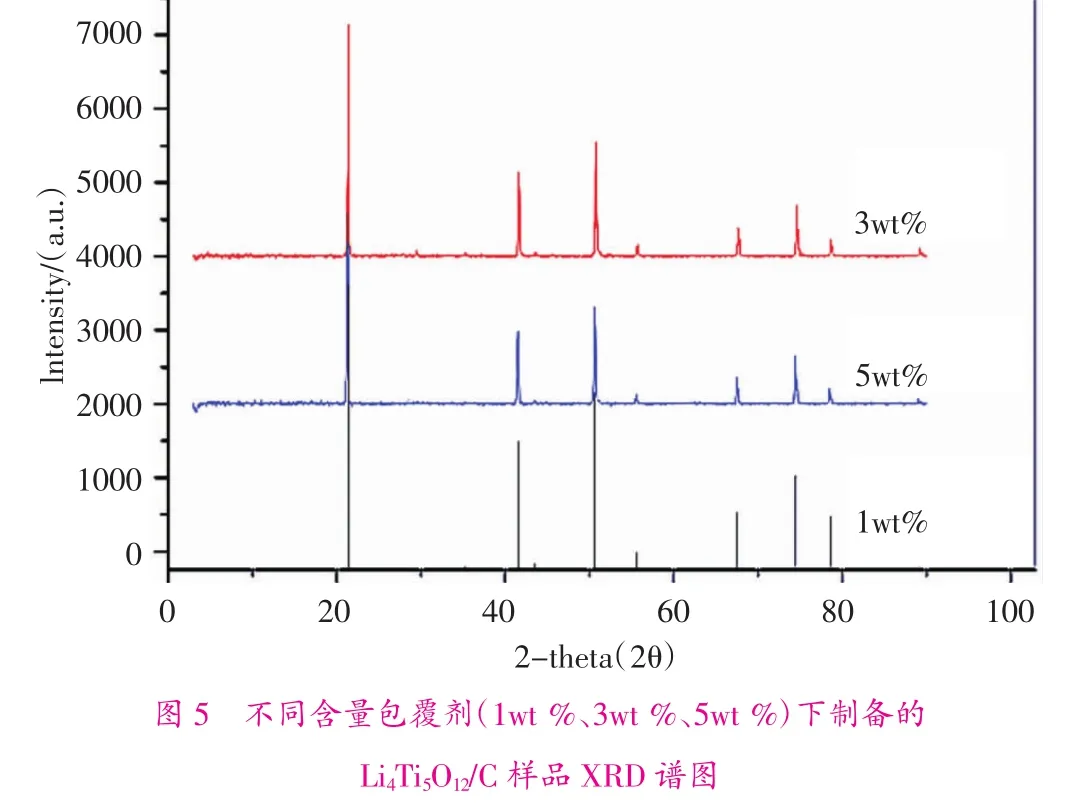
圖5 為 n(Li)/n(Ti)=0.75 的配比下,摻入 1wt%、3wt%、5wt%的碳材料,在溫度為800℃燒結得到的Li4Ti5O12/C樣品XRD譜圖。可以看出:各峰之間峰位基本一致,沒有出現雜峰,由此推斷出沒有雜相出現,說明各產物之間結構基本保持一致。通過添加不同含量的碳包覆劑,對Li4Ti5O12/C結構影響不大。同時,明顯觀察到:各峰值強度不盡相同。隨著燒結溫度升高,2θ對應強度在20°范圍內峰值逐步升高,隨2θ逐漸增大,峰值卻呈現降低趨勢。說明包覆劑含量對結晶發育完整度影響較大,含量過低,效果不明顯;當包覆劑含量過多,會使鈦酸鋰發生團聚。
2.2.2 SEM分析 圖6為 n(Li)/n(Ti)=0.75的配比下,摻入1wt%、3wt%、5wt%的碳材料在800℃煅燒得到碳包覆鈦酸鋰負極材料。經過SEM測試,可以看到:在該工藝條件下制備出的復合電極材料,顆粒形狀規整,呈球狀分布,且分布均勻,基本無雜質出現。包覆含量為1wt%時,晶體顆粒已經基本形成,與未包覆相比,差別不大;且缺陷較少,無團聚現象。含量為3wt%時,晶體在包覆劑作用下,顆粒粒徑被控制在合理范圍內;當為5wt%時,晶體結構成型完整,顆粒發生團聚,擴散通道被嚴重阻礙。經分析:3wt%為最優化包覆含量。
2.2.3 電化學性能 圖7分別反映了在n(Li)/n(Ti)=0.75時,摻入1wt%、3wt%、5wt%的碳材料在800℃煅燒得到Li4Ti5O12/C樣品0.1C倍率下充放電曲線。
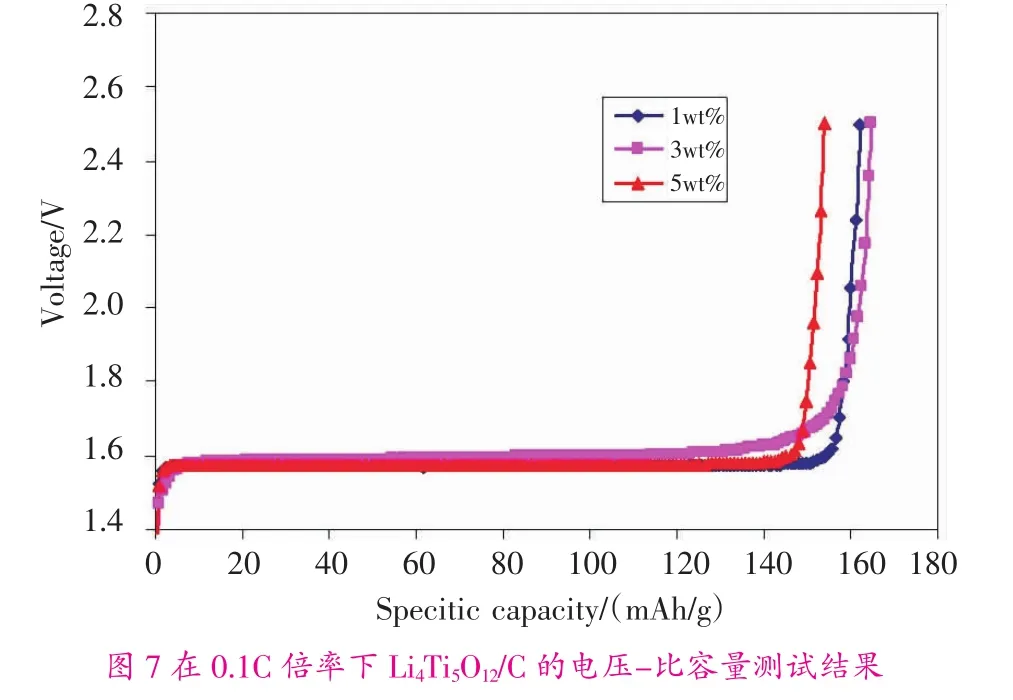
通過圖7能夠看出:當包覆劑含量為1wt%和3wt%時,比容量均達到165 mAh/g。但同時,電位電壓出現較大差異。其中,包覆劑含量為3wt%時,隨充電深度(COD)不斷升高,電壓平臺也呈現出微升趨勢,當比容量達到140 mAh/g時,電位電壓陡升;相比較之下,包覆劑含量為5wt%時,在整個充電過程中,電位平臺幾乎穩定在1.55 V,充電深度為82.5%(理論比容量為175 mAh/g),充電比容量可達到155 mAh/g。同時,比較包覆劑含量為1wt%和5wt%可發現,二者電位平臺幾乎重合,但充電深度不同,前者為85.7%,后者只有82.5%。
可以得出結論:通過碳包覆改性,能夠有效解決鈦酸鋰試樣的容量衰減問題,提高了容量保持率。同時,充放電效率得到提高。但包覆劑量不同,對比容量和平臺電位的影響不盡相同。
3 結論
本文經過優化配比,重點探究了煅燒溫度、碳包覆材料的含量對鈦酸鋰材料放電性能的影響,并借助電化學工作站實現了在不同倍率下的放電比容量測試。通過對比及重復性實驗,得到如下結論。
(1)在低于鈦酸鋰分解溫度范圍進行反應,隨煅燒溫度升高,晶體發育逐漸完全,但顆粒分布也隨之更加均勻,放電比容量也逐漸增大。但當溫度達到900℃后,逐漸發生團聚現象,并產生缺陷,晶體規整度下降,顆粒變得不均勻,對電性能影響較大。
(2)通過包覆碳材料進行鈦酸鋰的改性。減少反應缺陷,抑制了晶體不斷膨脹的過程。同時,提升了充放電比容量(增加5~10 mAh/g)、庫侖效率和循環性能等電化學性能。
(3)以噴霧干燥法為制備工藝,以 n(Li):n(Ti)=0.75為實驗配比,得出在800℃下煅燒、包覆碳含量為3wt%為最佳條件。
[1]高劍,姜長印,應皆榮,萬春榮,等.Li4Ti5O12的合成及性能研究[J].電源技術,2006,30(5):362-365.
[2]劉東強,賴瓊鈺,郝艷靜,盧集政,吉曉洋,等.Li4Ti5O12溶膠-凝膠法合成及其機理研究[J].無機化學學報,2004,20(7):829-832.
[3]唐致遠,高飛,韓彬,等.鋰離子電池負極材料Li4Ti5O12的研究進展[J].化工進展,2006,25(2):159-162.
[4]于海英,謝海明,楊桂玲,顏雪冬,王榮順,等.鋰離子電池新型快充負極材料Li4Ti5O12的改性研究[J].高等學校化學學報,2007,28(8):1556-1560.
[5]高劍,姜長印,應皆榮,萬春榮,等.鋰離子電池負極材料鈦酸鋰的研究進展[J].電池,2005,35(5):390-392.
[6]郭志紅,張治安,賴延清,等.二步煅燒法制備高振實密度鈦酸鋰負極材料[J].中國有色金屬學報,2012,22(8):2387-2392.
[7]Daisuke Yoshikawa,Yoshihiro Kadoma,Jung-Min Kim,Koichi Ui,Naoaki Kumagai,Naoto Kitamura,Yasushi Idemoto,et al.Spray-drying synthesized Lithium-excess Li4+xTi5-xO12-δ and its electrochemical property as negative electrode material for Li-ion batteries[J].Electrochimica Acta,2010,55:1872-1879.
[8]Ting-Feng Yi,Li-Juan Jiang,J.Shu,Cai-Bo Yue,Rong-Sun Zhu,Hong-Bin Qiao,et al.Recent development and application of Li4Ti5O12as anode material of lithium-ion battery[J].Journal of Physics and Chemical of Solids,2010,71:1236-1242.
[9]H.F.Xiang,Q.Y.Jin,R.Wang,C.H.Chen,X.W.Ge,et al.Nonflammable electrolyte for 3-V lithium-ion battery with spinel materials LiNi0.5Mn1.5O4and Li4Ti5O12[J].Journal of Power Source,2008,179:351-356.
[10]Seo Hee Ju,Yun Chan Kang,et al.Effects of drying control chemical additive on properties of Li4Ti5O12negative powders prepared by spray pyrolysis [J].Journal of Power Sources,2010,195:4327-4331.

