苦參堿對肝癌細胞增殖及其細胞自噬的影響
范 悅 王世明 石青青
山西醫科大學第一醫院普通外科,山西太原 030001
在中國傳統醫藥中,苦參堿是一種從苦參、山豆根中提取的生物堿,其分子式為C15H24N2O。而苦參堿早被廣泛用于治療病毒性肝炎、肝纖維化、心律失常等疾病[1]。國內外研究表明[2]:無論是在體內還是體外,苦參堿具有較高的抗腫瘤活性。它可以抑制腫瘤增殖、誘導分化、誘導凋亡、抗轉移等作用,同時又具有免疫調節、升高白細胞、緩解癌痛等許多常規化療藥物所不具備的優勢。此外,研究發現苦參堿誘導了大鼠C6膠質瘤細胞的自噬[3]。而自噬與腫瘤關系密切,同樣在抑制腫瘤中起著非常重要的作用[4-5]。細胞自噬在輔助化療藥物治療惡性腫瘤方面起著非常重要的作用。本實驗通過研究不同濃度的苦參堿作用于肝癌HepG2細胞,探討苦參堿對肝癌HepG2細胞細胞周期以及細胞自噬的影響,為臨床化療藥物治療肝癌提供理論基礎。
1 資料與方法
1.1 一般資料
肝癌HepG2細胞由北京協和醫學院提供。苦參堿(Matrine,廣州白云山明興制藥有限公司)、DMEM 4.5 g/L Glu(Gibco公司)、PBS 液、胎牛血清(美國 Sigma公司)、單丹磺酞戊二胺(MDC)(美國Sigma公司)、二甲基亞砜(DMSO)、熒光顯微鏡(日本 OlympuS公司)、CO2培養箱、離心機(北京醫用離心機廠)、流式細胞儀(美國BD公司,型號:FACSCalibur)、電熱恒溫培養箱 (河北省黃石市醫療器件廠)等。
1.2 方法
1.2.1 細胞培養及處理 將肝癌HepG2細胞培養在含10%胎牛血清的DMEM培養液的培養瓶中,在37℃、5%CO2、飽和濕度下常規培養。顯微鏡下觀察細胞貼壁達80%時,用胰酶消化處理,取對數期細胞進行實驗。
1.2.2 MTT法 肝癌HepG2細胞用0.25%胰酶處理制成單細胞懸液,以每孔約104個細胞接種于96孔板(每孔100μL)。分別加入不同濃度的苦參堿溶液,使其終濃度為0.5、1.0、2.0 mg/mL,每個濃度設三個孔。然后在加培養液100 μL,每孔總體積為200 μL,同時設定空白孔及對照孔。然后放回CO2箱中培養24、36、48 h。分別在各個時間段結束前4 h加入 MTT(5 mg/mL)溶液 10 μL,反應 4 h離心棄上清液。每孔加入DMSO 150 μL振蕩蕩5~10 min。用酶標儀測定波長為490 nm的吸光值。根據公式計算:腫瘤細胞增值抑制率=(1-實驗組OD值/對照組OD值)×100%。
1.2.3 流式細胞術分析細胞周期 肝癌HepG2細胞以5×104/mL接種至6孔板中,細胞貼壁后,分別加入0.5 mg/mL、1.0 mg/mL、2.0 mg/mL的苦參堿,培養36 h后,收集細胞,并用流式細胞儀行細胞周期分析。
1.2.4 單磺酰戊二胺 (monodansylcadaverine,MDC)熒光染色 將DMEM液培養的肝癌HepG2細胞以1×104/mL接種至12孔板中,待細胞貼壁后,分別加入0.5、1.0、2.0 mg/mL的苦參堿,培養36 h棄培養液,用PBS液洗2遍,加入50 μmol/L MDC,37℃孵育10 min染色。 再用 PBS漂洗細胞3次,在熒光顯微鏡下觀察。
1.3 統計學方法
2 結果
2.1 苦參堿顯著抑制肝癌HepG2細胞的增殖
MTT測定結果見圖1,苦參堿顯著抑制肝癌HepG2細胞的增殖,并呈現時間-劑量依賴性。見表1。苦參堿0.5、1.0、2.0mg/mL作用于肝癌HepG2細胞36 h后的抑制率分別:(17.21±2.02)%、(28.25±3.20)%、(38.77±5.58)%。

表1 不同濃度苦參堿作用于肝癌HepG2細胞不同時間的抑制率(±s,%)
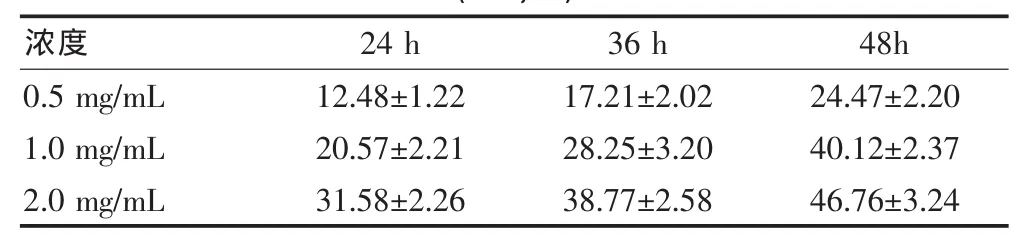
表1 不同濃度苦參堿作用于肝癌HepG2細胞不同時間的抑制率(±s,%)
注:同一濃度不同時間比較,P<0.05;同一時間不同濃度比較,P<0.05
濃度 24 h 36 h 48h 0.5 mg/mL 1.0 mg/mL 2.0 mg/mL 12.48±1.22 20.57±2.21 31.58±2.26 17.21±2.02 28.25±3.20 38.77±2.58 24.47±2.20 40.12±2.37 46.76±3.24
2.2 流式細胞儀檢測結果
不同濃度苦參堿作用于肝癌HepG2細胞36 h后,流式細胞儀分析細胞周期見表2。結果所示:不同濃度苦參堿作用于肝癌HepG2細胞中36 h后,G1期細胞增多,S期細胞減少,呈現劑量依賴性。結果表明苦參堿將肝癌HepG2細胞阻滯在細胞周期的G1期。
表2 不同濃度的苦參堿作用于肝癌HepG2細胞36 h后細胞周期(±s)

表2 不同濃度的苦參堿作用于肝癌HepG2細胞36 h后細胞周期(±s)
注:同一時間不同濃度組之間,分別比較G1期和S期P<0.05,而G2/M期P>0.05
濃度 G1期 S期 G2/M期0.5 mg/mL 1.0 mg/mL 2.0 mg/mL 37.23±1.72 39.42±1.74 42.66±1.35 35.34±2.16 35.26±0.87 34.75±1.27 15.02±1.35 15.36±1.47 14.92±2.03
2.3 MDC染色顯示苦參堿誘導肝癌HepG2細胞自噬的產生
為了研究苦參堿是否誘導了肝癌HepG2細胞自噬的產生,本文用熒光鏡觀察MDC染色的肝癌HepG2細胞,細胞顯著的形態學變化如圖2所示。MDC是自噬泡的特異性標記物熒光顯微鏡下觀察細胞時,胞質內可見到清晰的點泡狀結構,表明苦參堿誘導了自噬 的產生。

3 討論
原發性肝癌是惡性程度最高的腫瘤之一。全球男性發病率位于惡性腫瘤的第5位,死亡率居惡性腫瘤的第2位;全球女性發病率位于第7位,死亡率位于第6位。全球每年新發肝癌約75萬人,而我國占半數以上[6]。由于肝癌具有惡性程度高、病情發展快、預后差、死亡率高等特點,多數就診時已屬晚期。目前手術治療依然是肝癌的首選,但是肝癌發病隱匿,確診時能手術者僅占l0%~15%,因此必須聯合其他非手術措施(如化療、生物治療等)進行綜合治療,才能有望提高肝癌患者的長期生存率[7]。近年來,苦參堿作為一種新型化療藥物,具有療效顯著、副作用小、毒性低等特點應用于臨床。
苦參堿(Matrine)是中藥苦參、山豆根、苦豆子的主要活性成分,具有保護肝細胞、抗病毒、抗過敏等多種藥理作用[8]。此外苦參堿具有廣泛的抗腫瘤作用。研究發現:在體外實驗中苦參堿可明顯地誘導人乳腺癌[9]、骨肉瘤[10]及肝癌細胞[11]等的凋亡。苦參堿的抗腫瘤的作用機制很多,主要包括誘導腫瘤細胞凋亡、誘導腫瘤細胞分化、誘導細胞自噬以及細胞毒等多種作用[3,12-13]。本實驗結果表明:苦參堿對人肝癌HepG2細胞有明顯的抑制作用,不同濃度的苦參堿作用不同時間后,肝癌細胞的存活率降低,這種抑制作用呈時間和劑量依賴性。流式細胞儀分析細胞周期結果:苦參堿作用于人肝癌HepG2細胞后,G1期細胞數目明顯增多,S期細胞數目減少(P<0.05),這表明苦參堿作用肝癌細胞后將細胞周期阻滯在G1期,使細胞不能進入S期進行DNA合成,并最終抑制了肝癌HepG2細胞的抑制,本文實驗結果與以往郭丹等[14]、夏寶妹等[15]、楊道科等[16]在肝癌、子宮內膜癌以及結腸癌細胞中的研究結果一致。同時熒光顯微鏡檢測:苦參堿誘導肝癌HepG2細胞自噬泡的產生,這表明自噬參與了苦參堿抑制肝癌HepG2細胞的增殖,可能提示苦參堿作用于肝癌HepG2細胞后,自噬多發生在細胞周期的G1期。而自噬作為一把雙刃劍,它與腫瘤之間的關系錯綜復雜,既可以促進腫瘤的生長,也可以誘導腫瘤的生長,在本實驗研究中認為它參與了苦參堿抑制肝癌細胞的增殖。本文在既往研究的基礎上,探討了苦參堿對人肝癌HepG2增殖及其細胞自噬的影響,而其發生的信號通路及其作用機制仍需作進一步的研究。希望本實驗研究能為細胞周期與腫瘤的增值、分化等之間的關系提供研究基礎,為臨床進一步更好的治療肝癌提供理論基礎。
[1]李正蓉.苦參素的藥理與臨床研究進展[J].華西藥學雜志,2003,18(6):435-437.
[2]Han Y,Zhang S,Wu J,et al.Matrine induces apoptosis of human multiple myeloma cells via activation of the mitochondrial pathway[J].Leuk Lymphoma,2010,51(7):1337-1346.
[3]Zhang S,Qi J,Sun L,et al.Matrine induces programmed cell death and regulates expression of relevant genes based on PCR array analysis in C6 glioma cells[J].Mol Biol Rep,2009,36(4):791-799.
[4]Morselli E,Galluzzi L, Kepp O, et al.Anti-and pro-tumor functions of autophagy[J].Biochim Biophys Acta,2009,1793(9):1524-1532.
[5]Biederbick A,Kern HF,Elsasser HP.Monodansylcadaverine(MDC)is a specific in vivo marker for autophagic vacuoles[J].Eur J Cell Biol,1995,66(1):3-14.
[6]Jemal A,Bray F,Center M M,et al.Global cancer statistics[J].CA Cancer J Clin, 2011,61(2):69-90.
[7]Marin JJ,Romero MR, Martinez-Becerra P, et al.Overview of the molecular bases of resistance to chemotherapy in liver and gastrointestinal tumours[J].Curr Mol Med,2009,9(9):1108-1129.
[8]廖春燕,梁健,楊燕,等.苦豆子的藥理及應用概述[J].中國民族民間醫藥,2009,18(5):6-8.
[9]周炳剛,孫靖中,蘇剛,等.苦參堿誘導人乳腺癌細胞MCF27/ADR的凋亡研究[J].中華實驗外科雜志, 2003, 20(6):515-516.
[10]鄭安祥,陳杰,陶惠民.苦參堿抑制人骨肉瘤MG-63細胞增值和誘導凋亡的體外實驗研究[J].實用腫瘤雜志,2005,20(6):516-519.
[11]張立明,鄭傳莉.苦參堿誘導人肝癌細胞SMMC-7721凋亡的實驗研究[J].西北藥學雜志,2006,22(3):128-129.
[12]查勇,寸英麗,黃云超,等.苦參堿對肝癌細胞株SMMC-7721凋亡和自噬相關基因表達的影響[J].世界華人消化雜志,2010,18(29):3078-3083.
[13]薛凈,李瑜元,聶玉強,等.苦參堿對人肝癌細胞株HepG2基因表達譜的影響[J].胃腸病學和肝病學雜志,2007,16(4):341-343.
[14]郭丹,陳娜娜,周萍,等.苦參堿抑制肝癌Hep3B細胞生長及β-catenin的轉錄活性[J].中藥材,2010,33(5):778-781,
[15]夏寶妹,周懷君,胡婭莉,等.氧化苦參堿抑制子宮內膜癌細胞株Ishikawa 的實驗研究[J].現代婦產科進展,2009,18(4):278-281.
[16]楊道科,王英俊,朱洪海.氧化苦參堿誘導結腸癌細胞株SWI116凋亡的實驗研究[J].中國醫藥導報,2008,5(27):26-27.

