虎皮楠內生真菌Aspergillus sp.DCS31化學成分研究
孟欣欣,葛 鋒,曾 英,趙沛基*
1昆明理工大學生命科學與技術學院,昆明 650500;2中國科學院昆明植物研究所植物化學與西部植物資源持續利用國家重點實驗室,昆明 650204
長序虎皮楠(Daphniphyllum longeracemosum)為虎皮楠科(Daphniphyllaceae)虎皮楠屬(Daphniphyllum)植物,在我國主要分布于云南東南部和廣西,是一種生于海拔1000~1800 m密林中的常綠喬木[1,2]。虎皮楠科植物在傳統中藥中具有一定的藥用價值,具有愈合、消炎等作用[3]。其代謝產物中含有大量的虎皮楠生物堿,該類生物堿多變的結構和復雜的多環骨架,成為化學和生物合成的熱點之一。
植物內生真菌是指在某一時期生活在植物體內,但對寄主植物組織并不引起明顯病害癥狀的真菌[4]。內生真菌長期與藥用植物共同相互共生,有可能產生與宿主相同或相似生理活性的化學成分[5]。為了進一步尋找新型的天然產物及活性物質,我們對一株分離自長序虎皮楠韌皮部的內生真菌的化學成分進行研究,從內生真菌Aspergillus sp.DCS31的固體發酵培養基中分離得到五個化合物,分別為 asperpyrone D(1)、asperpyrone A(2)、flavasperone(3)、1,2-benzene dicarboxylic acid bis(2αmethyl heptyl)ester(4)、2,5-dihydroxyphenylacetic acid methyl ester(5)。化合物1~4為首次從虎皮楠內生真菌中分離得到。
1 實驗部分
1.1 儀器與材料
Bruker AM-400型核磁共振儀;DRX-500型核磁共振儀;Avance III 600型核磁共振儀;Finnigan LCQ-Advantage型質譜儀;薄層層析用硅膠板和柱層析硅膠G,200~300目(青島海洋化工廠),柱層析硅膠H(Merck公司);Sephadex LH-20葡聚糖凝膠(Amersham Pharmacia公司)。
Aspergillus sp.DCS31分離來自長序虎皮楠(Daphniphyllum longeracemosum)的樹皮韌皮部。長序虎皮楠采自2009年移栽于昆明植物園的植物。
1.2 內生菌的鑒定
Aspergillus sp.DCS31的總DNA根據文獻采用肌氨酸鈉法提取[6]。實驗中所用的ITS 4與ITS 5引物是真菌系統學研究中設計的通用引物ITS 4(5'>TCC TCC GCT TAT TGA TAT GC<3')和ITS 5(5'>GGA AGT AAA AGT CGT AAC AAG G <3')。PCR程序為95℃預變性15 min(加酶);95℃變性40 s,55 ℃退火 40 s,72 ℃ 延伸 90 s,30 個循環;72℃延伸10 min,PCR后回收到大約700 bp的核酸片段,測序后通過與GenBank數據庫比對來鑒定菌株。
1.3 培養基及培養條件
PDA培養基:馬鈴薯200 g,葡萄糖20 g,瓊脂20 g,定容至1 L,pH 自然,121 ℃滅菌20 min。
培養條件:Aspergillus sp.DCS31經PDA固體培養基發酵10 L,28℃培養14 d。
1.4 發酵產物的分離純化
將長滿菌絲的固體培養基劃成小塊放于錐形瓶中,用乙酸乙酯:甲醇:冰醋酸 =(80∶15∶5,V/V/V)混合溶劑提取3次,所得提取液經45℃減壓濃縮得到浸膏,將浸膏懸浮于蒸餾水后加入等體積的乙酸乙酯萃取至無色,最后得到提取物37 g。粗提物經正相柱層析(200~300目),分別用石油醚:丙酮(10∶1、9∶1、8∶2、7∶3),氯仿:甲醇(20∶1、10∶1、9∶1、8∶2、7∶3)進行梯度洗脫,得到7個組分。組分2(215.5 mg)經過反復的正相柱層析得到化合物3(6.0 mg),組分4(4.0 g)經過反復的正相柱層析和Sephadex LH-20柱分離得到化合物1(26.5 mg)、2(5.2 mg)、5(8.2 mg),組分5(2.0 g)經過反復的正相柱層析和Sephadex LH-20柱分離得到化合物4(31 mg)。
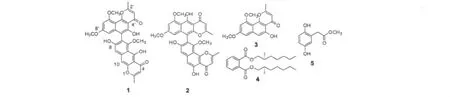
圖1 化合物1~5的結構式Fig.1 Structures of compounds 1-5
2 結果與討論
2.1 內生真菌的鑒定
Aspergillus sp.DCS31 的 5.8S rDNA 序列(Gen-Bank:JX025097)通過與GenBank數據庫序列比對,Aspergillus sp.DCS31與曲霉屬(Aspergillus)的同源性達99%,因此Aspergillus sp.DCS31鑒定為曲霉屬真菌。
2.2 結構鑒定
化合物1 C31H24O10,黃色無定形粉末;ESI-MS m/z:557[M+H]+;1H NMR(C5D5N,600 MHz)δ:1.93(3H,s,CH3-2),2.13(3H,s,CH3-2'),3.58(3H,s,OCH3-8'),3.78(3H,s,OCH3-6),3.91(3H,s,OCH3-10'),6.05(1H,s,H-3),6.12(1H,s,H-3'),6.64(1H,d,J=2.3 Hz,H-7'),6.90(1H,d,J=2.4 Hz,H-9'),7.26(1H,s,H-10),7.61(1H,s,H-9);13C NMR(C5D5N,150 MHz)δ:185.0(s,C-4'),184.8(s,C-4),168.4(s,C-2'/2),163.8(s,C-5'),162.8(s,C-5),162.3(s,C-8'),161.9(s,C-10'),160.6(s,C-6),159.8(s,C-8),153.5(s,C-10a),151.8(s,C-10a'),141.7(s,C-9a),141.6(s,C-9a'),118.4(s,C-7/6'),111.3(s,C-5a/4a'),109.2(d,C-5a'),107.5(s,C-3),107.3(d,C-3'),106.5(s,C-9),104.5(d,C-4a),100.9(s,C-10),97.5(d,C-7'/9'),62.3(q,OCH3-6),56.1(q,OCH3-10'),55.1(q,OCH3-8'),20.2(q,CH3-2'),22.1(q,CH3-2)。以上數據與文獻報道一致[7],由于化合物1與相類似化合物NMR的數據差別很小,通過2D NMR進一步確定化合物1為asperpyrone D。
化合物2 C31H24O10,黃色無定形粉末;ESI-MS m/z:557[M+H]+;1H NMR(C5D5N,600 MHz)δ:1.96(3H,s,CH3-2'),2.24(3H,s,CH3-2),3.62(3H,s,OCH3-6'),3.67(3H,s,OCH3-10),3.92(3H,s,OCH3-8'),6.06(1H,s,H-3'),6.40(1H,s,H-3),6.66(1H,d,J=2.2 Hz,H-7'),6.92(1H,d,J=2.2 Hz,H-9'),7.29(1H,s,H-6),7.60(1H,s,H-7);13C NMR(C5D5N,150 MHz)δ:187.0(s,C-4'),185.2(s,C-4),170.4(s,C-2'),169.4(s,C-2),165.8(s,C-5'),164.4(s,C-6'),163.9(s,C-8'),162.5(s,C-8),160.1(s,C-10),159.1(s,C-5),157.6(s,C-10b),153.8(s,C-10a'),143.6(s,C-6a),143.6(s,C-9a'),119.8(s,C-9),112.7(d,C-3),111.3(s,C-4a),111.3(s,C-5a'),109.8(d,C-3'),109.5(s,10a),108.5(d,C-7),108.5(s,C-10a'),107.6(d,C-6),106.7(s,C-4a'),99.4(d,C-9'),99.4(d,C-7'),63.4(q,OCH3-10),58.1(q,OCH3-8'),57.1(q,OCH3-6'),22.2(q,CH3-2'),22.0(q,CH3-2)。以上數據與文獻報道一致[8]。通過2D NMR進一步確定化合物2為asperpyrone A。
化合物3 C16H14O5,黃色無定形粉末;ESI-MS m/z:287 [M+Na]+;1H NMR(CDCl3,500 MHz)δ:7.28(1H,s,OH-6),6.98(1H,s H-7),6.60(1H,d,J=3.2 Hz,H-9),6.41(1H,d,J=3.1 Hz,H-11),6.02(1H,s,H-3),4.02(3H,s,OCH3-10),3.94(3H,s,OCH3-12),2.39(3H,s,CH3-2);13C NMR(CDCl3,125 MHz)δ:184.2(s,C-4),167.4(s,C-2),162.6(s,C-10),161.5(s,C-6),160.6(s,C-12),153.3(s,C-14),141.1(s,C-8),108.4(s,C-13),107.3(d,C-7),104.3(s,C-5),101.0(d,C-3),97.8(d,C-9),97.2(d,C-11),56.1(q,OCH3-12),55.4(q,OCH3-10),20.7(q,CH3-2)。以上數據與文獻報道一致[9]。
化合物4 C24H38O4,淡黃色油狀;ESI-MS m/z:391[M+H]+;1H NMR(CDCl3,400 MHz)δ:7.71(2H,m,H-4,5),7.54(2H,m,H-3,6),4.26(4H,m,H-1',1″),1.70(2H,m,H-2',2″),1.25-1.45(16H,m,H-3',3″,4',4″,5',5″,6',6″),0.93(6H,d,J=7.5 Hz,CH3-2',2″),0.90(6H,t,J=6.6 Hz,H-7',7″);13C NMR(CD3Cl3,100 MHz)δ:167.63(s,C=O),132.39(s,C-1,2),130.76(d,C-3,6),128.70(d,C-4,5),68.07(t,C-1',1″),38.67(d,C-2',2″),30.29(t,C-4',4″),29.84(t,C-5',5″),23.68(t,C-6',6″),22.88(t,C-3',3″),13.91(t,C-7',7″),10.86(q,CH3-2',2″)。以上數據與文獻報道一致[10]。
化合物5 C9H10O4,無色油狀;ESI-MS m/z:183[M+H]+;1H NMR(CD3OD,600 MHz)δ:8.72(1H,s,OH-5),8.64(1H,s,OH-2),6.62(1H,d,8.6 Hz,H-3),6.59(1H,d,2.9 Hz,H-6),6.55(1H,dd,8.6,3.0 Hz,H-5),3.67(3H,s,OCH3-8),3.54(2H,s,H-7);13C NMR(CD3OD,150 MHz)δ:174.7(s,C-8),151.2(s,C-4),149.7(s,C-2),123.3(s,C-1),118.7(d,C-6),116.7(d,C-3),115.8(d,C-5),52.5(q,OCH3-9),36.6(t,C-7)。以上數據與文獻報道一致[11]。
1 Zheng M(鄭勉),Min TL(閔天祿).Flora of China(中國植物志),Beijing:Science Press,1980,45:1.
2 Yang TQ(楊廷全),Di YT(邸迎彤),He HP(何紅平),et al.A new alkaloid from the fruits of daphniphyllum longeracemosum(Daphniphyllaceae).Acta Botanica Yunnanica(云南植物研究),2010,32:561-563.
3 Xu MF(許明峰),Shen LQ(沈蓮清).NMR characterization of two flavonyl glycosides isolated from Daphniphyllum angustifolium Hutch.Chin J Magn Reson(波譜學雜志),2010,27:260-264.
4 Huang WY,Cai YZ,Xing J,et al.A potential antioxidant resource:Endophytic fungi from medicinal plants.Econ Bot,2007,60:14-30.
5 Li LQ(李良群),Yang YG(楊艷光),Zeng Y(曾英),et al.Chemical constituents of endophyte Talaromyces sp.T1BF from Taxus yunnanensis.Guihaia(廣西植物),2011,31:699-701.
6 Sambrook J,Russell DW.Molecular cloning:A laboratory manual.3rd ed,NewYork:Cold Spring Harbor Laboratory Press,2001.
7 Zhan J,Gunaherath GM,Wijeratne EM,et al.Asperpyrone D and other metabolites of the plant-associated fungal strain Aspergillus tubingensis.Phytochemistry,2007,68:368-372.
8 Akiyama K,Teraguchi S,Hamasaki Y,et al.New dimeric naphthopyrones from Aspergillus niger.J Nat Prod,2003,66:136-139.
9 Sakurai M,Kohno J,Yamamoto K,et al.TMC-256A1 and C1,New inhibitors of IL-4 signal transduction produced by Aspergillus niger var niger TC 1629.J Antibiot,2002,55:685-692.
10 Singh N,Mahmood U,Kaul VK,et al.A new phthalic acid ester from Ajuga bracteosa.Nat Prod Res,2006,20:593-597.
11 Lebouvier N,Jullian V,Desvignes I,et al.Antiplasmodial activities of homogentisic acid derivative protein kinase inhibitors isolated from a vanuatu marine sponge Pseudoceratina sp.Mar Drugs,2009,7:640-653.

