汽爆玉米秸稈糖化及發酵丁醇工藝的優化研究
劉利平,申利英,常 春
(鄭州大學化工與能源學院,河南鄭州450001)
0 引言
能源短缺與環境污染,使新型生物能源的開發勢在必行.丁醇因其具有能量密度高、易與汽油混合等特點,而成為替代石油的重要選擇[1].秸稈是地球上最豐富廉價的資源,以秸稈為原料制備生物丁醇在解決糧食、能源、環境污染等問題中具有重要的作用.
微生物無法直接利用秸稈為底物進行丁醇發酵,需將其水解產生葡萄糖、木糖等單糖后再用于丁醇發酵[2].而水解后還原糖含量直接影響到丁醇的產量.但目前,對經蒸汽爆破預處理的玉米秸稈為原料,進行糖化和丁醇發酵工藝研究的報道較少.李冬敏等[3]用汽爆玉米秸稈進行丁醇發酵,丁醇濃度達到了6.52 g/L.其丁醇含量較低,難以滿足規模化應用的條件.因此,本研究嘗試首先通過對汽爆玉米秸稈的糖化工藝進行考察,篩選出較佳的糖化工藝,并在此基礎上,分別對溫度、pH值、底物濃度、纖維素酶用量、菌種種齡及接種量、培養基的組成和發酵時間8個方面進行丁醇發酵工藝條件的試驗研究,得出汽爆玉米秸稈發酵丁醇的優化工藝,為進一步的放大試驗研究提供參考依據.
1 材料與方法
1.1 試驗材料
丙酮丁醇梭菌(Clostridium acetbutylicum ZZU-01):鄭州大學生化中心保藏;種子培養基:5%玉米醪;種子液活化:取一玉米醪儲存的試管菌種,沸水浴中處理90 s.然后在厭氧操作臺上(YQX-Ⅱ厭氧培養箱,上海躍進醫療器械廠)接種于5%玉米醪培養基,活化至對數期;纖維素酶:濾紙酶活力110 IU/mL;汽爆玉米秸稈:將玉米秸稈切至3~4 cm長,于1.5 MPa,205℃條件下汽爆處理8 min,汽爆處理后秸稈經水洗脫毒并于80℃干燥恒重后,保藏待用;酶解液的制備:取一定量烘干的秸稈于錐形瓶中,加自來水,使底物質量分數為15%.然后按照糖化工藝設計的條件加入纖維素酶(30 IU/g),木聚糖酶(200 IU/g),Tween-20(質量分數為0.15%),調pH為4.8,于50℃,150 r/min下反應一定時間后,離心取上清液.
1.2 糖化工藝設計
以蒸汽爆破預處理的玉米秸稈為原料,共進行了6種不同的秸稈糖化發酵丁醇工藝研究(稱為糖化工藝Ⅰ~Ⅵ).分別對比了汽爆玉米秸稈經6種糖化工藝后的丁醇發酵結果.不同糖化方法的具體工藝為
糖化工藝Ⅰ:將纖維素酶一次性加入,糖化48 h;
糖化工藝Ⅱ:首先加入纖維素酶量的1/2,反應24 h后再加入1/2纖維素酶,共糖化48 h;
糖化工藝Ⅲ:將纖維素酶分成3等份,首先加入纖維素酶量的1/3,每隔6 h加一次纖維素酶,共糖化24 h;
糖化工藝Ⅳ:纖維素酶加入法與糖化工藝Ⅲ相同,但糖化時間延至48 h;
糖化工藝Ⅴ:首先加入纖維素酶量的1/3,反應24 h后,再加入1/3纖維素酶,剩下的纖維素酶再隔12 h加入,共糖化48 h;
糖化工藝Ⅵ:初始底物體質量分數為15%,加入相應量的纖維素酶,反應24 h,每隔12 h,補一次原料,并且加入相應量的纖維素酶,共糖化48 h.
1.3 發酵培養基與培養方法
發酵培養基:秸稈酶解上清液1 L,酵母抽提物 1 g,KH2PO40.5 g,MgSO4·7H2O 0.3 g,(NH4)2SO45 g,FeSO4·7H2O 0.01 g,尿素 2 g,CaCO35 g[3-4].pH7.0,121 ℃,滅菌 20 min.除了考察培養基的影響因素外,其他試驗中的發酵培養基均采用以上基礎培養基.
發酵方法:將活化24 h的種子液,按體積分數為5%接種量進行接種,首先采用35℃,厭氧發酵72 h的條件,考察不同糖化工藝對丁醇發酵的影響.在此基礎上,對丁醇發酵的溫度、底物濃度、纖維素酶的用量、接種量和發酵時間進行了單因素試驗;對培養基酵母抽提物,KH2PO4,MgSO4·7H2O,(NH4)2SO4,FeSO4·7H2O,尿素和CaCO3進行了L32(74)正交試驗.在優化的基礎上,對發酵后的丁醇產量進行了考察.
1.4 分析方法
(1)秸稈成分測定:采用質量減重法[5].
測得汽爆玉米秸稈主要成分為:纖維素的質量分數為33.68%;半纖維素的質量分數為7.29%;木質素的質量分數為22.31%.
(2)還原糖的測定:DNS 法[6].
(3)溶劑的測定:氣相色譜法[7].
2 試驗結果與分析
2.1 糖化工藝對丁醇發酵的影響
根據1.2節的試驗設計,以還原糖含量和發酵丁醇濃度為考察目標,試驗結果如表1所示.
表1結果表明,糖化工藝Ⅵ的還原糖含量最高,為48.77 g/L,但丁醇含量僅有4.01 g/L,這可能是因為分批補料糖化使底物濃度增加的同時,也增加了抑制劑的濃度,嚴重抑制了丁醇發酵.糖化工藝Ⅰ與Ⅱ相比較,可知分步酶解要比一步酶解得到的還原糖含量高,還原糖含量的增加,也使得后續的丁醇發酵的濃度升高.以上結果表明,多步糖化和適當的糖化時間能夠更充分地酶解纖維素,提高還原糖的含量,從而提高后續的丁醇發酵濃度.糖化工藝Ⅴ的丁醇產量達到了7.44 g/L,高于其它5種糖化發酵的丁醇產量,因此糖化工藝Ⅴ是汽爆玉米秸稈糖化發酵丁醇工藝中較優的工藝路線.下面在糖化工藝Ⅴ的基礎上,進一步優化丁醇發酵的工藝條件.

表1 不同糖化發酵試驗結果Tab.1 Fermentative results of different saccharification
2.2 丁醇發酵工藝條件的優化
2.2.1 溫度對發酵的影響
本研究以得到最高的丁醇濃度為考察目標,首先對溫度的影響進行考察.試驗條件為:底物濃度15%(質量分數),纖維素酶用量30 IU/g,接種量7%,基礎培養基,發酵時間72 h.不同溫度對丁醇發酵的影響如圖1所示.由圖可知,本試驗中發酵溫度為37℃時,丁醇產量最高.

圖1 溫度對發酵的影響Fig.1 Effect of temperature on fermentation
2.2.2 底物濃度對發酵的影響
通常采用增加底物的方法,獲得較高的丁醇產量,提高丁醇生產的經濟性.但隨著底物的增加,會造成有害抑制物的積累等一系列問題[8].因此尋找適宜的底物濃度顯得尤為必要.試驗對底物濃度研究條件如下:溫度37℃,纖維素酶用量30 IU/g,接種量7%,基礎培養基,發酵時間72 h.考察不同底物濃度對發酵的影響,結果如圖2所示.由圖可知,當底物質量分數為15%時,丁醇濃度最高.
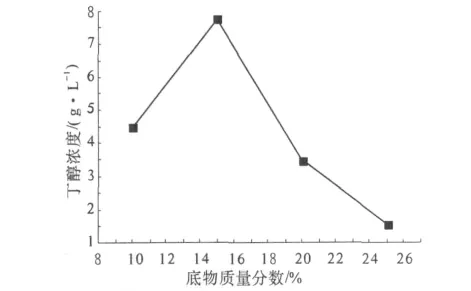
圖2 底物濃度對發酵的影響Fig.2 Effect of substrate concentration on fermentiaon
2.2.3 纖維素酶用量對發酵的影響
在丁醇發酵過程中,酶的水解對丁醇的生成有決定性的作用.在溫度37℃,底物濃度15%,接種量7%,基礎培養基,發酵時間72 h的試驗條件下,不同纖維素酶用量對發酵的影響如圖3所示.圖中結果表明,在纖維素酶用量25~40 IU/g的范圍內,丁醇濃度隨酶用量的增加而增加.較低的纖維素酶用量,不能有效的將秸稈酶解轉化為還原糖,不利于后續的發酵;而較高的纖維素酶用量會增加生產成本.因此,選用30 IU/g為較優的纖維素酶用量.
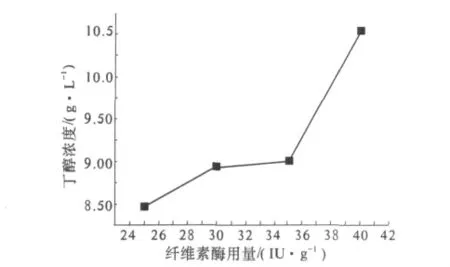
圖3 纖維素酶用量對發酵的影響Fig.3 Effect of loading of cellulose on fermentation
2.2.4 菌種接種量對發酵的影響
在發酵過程中,接種量與菌種的生長速度和丁醇的產量密切相關.因此,在溫度37℃、底物濃度15%、纖維素酶用量30 IU/g、基礎培養基、發酵時間72 h的試驗條件下,進一步考察接種量對發酵的影響,結果見圖4.接種量為7%時,丁醇產量最高.而接種量過高或過低,都會造成丁醇濃度明顯下降.所以確定7%為最佳接種量.
2.2.5 培養基組成對發酵的影響
發酵培養基的組成對菌體的生長代謝和溶劑的生成有重要的影響.因此筆者重點考察了酵母抽提物(A),KH2PO4(B),MgSO4·7H2O(C),(NH4)2SO4(D),FeSO4·7H2O(E),尿素(F)和CaCO3(G)7種營養物組成對丁醇濃度的影響.試驗條件為:溫度37℃、底物濃度15%、纖維素酶用量30 IU/g、接種量7%、發酵時間72 h.試驗采用L32(74)正交試驗進行培養基的優化,優化試驗及結果見表2.
由表2的數據可以得到,優化培養基組成為:KH2PO40.8 g/L,MgSO4· 7H2O 0.1 g/L,FeSO4·7H2O 0.01 g/L,尿素3 g/L,CaCO38 g/L.
進一步和丁醇濃度最高的28號試驗進行驗證試驗,結果如表3所示.
由表2和表3的結果,可得到較優的培養基組合為:酵母抽提物 1 g/L,KH2PO40.8 g/L,MgSO4·7H2O 0.1 g/L,(NH4)2SO42 g/L,FeSO4·7H2O 0.03 g/L,尿素2 g/L.在此條件下,發酵的丁醇濃度為9.37 g/L.
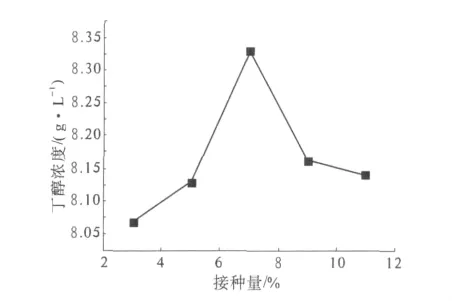
圖4 接種量對發酵的影響Fig.4 Effect of inoculums on fermentation
2.2.6 發酵時間對發酵的影響
發酵時間直接影響丁醇生產的效率.在溫度37℃,底物濃度15%,纖維素酶用量30 IU/g,接種量7%,優化的培養基的條件下,不同發酵時間對發酵的影響結果見圖5.
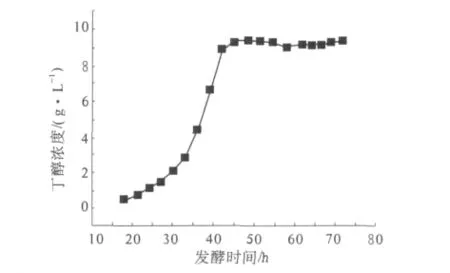
圖5 發酵時間對發酵的影響Fig.5 Effect of fermentation time on fermentation

表2 培養優化的正交試驗表Tab.2 Results of orthogonal experiment
試驗結果表明,當發酵時間達到48 h時,丁醇濃度已基本趨于平穩.因此,可以選擇48 h為較優的發酵時間,此時的丁醇含量為9.42 g/L.
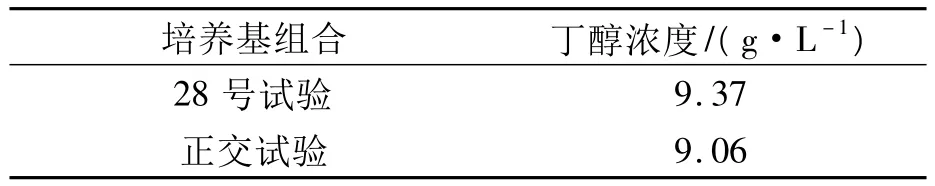
表3 兩種培養基對發酵的影響Tab.3 Effects of two kinds of medium on fermentation
3 結論
(1)筆者通過對不同糖化發酵丁醇試驗結果的比較,得到糖化工藝Ⅴ,即首先加入纖維素酶量的1/3,反應24 h后,再加入1/3纖維素酶,剩下的纖維素酶再隔12 h加入,共糖化48 h是一條較佳的工藝路線.
(2)在糖化工藝Ⅴ的基礎上,通過對丁醇發酵工藝中8個影響因素的考察研究,得到了在溫度37℃,底物濃度15%,纖維素酶用量30 IU/g,接種量7%,優化的培養基組成:酵母抽提物1 g/L、KH2PO40.8 g/L,MgSO4·7H2O 0.1 g/L,(NH4)2SO42 g/L,FeSO4·7H2O 0.03 g/L,尿素2 g/L,發酵周期為48h的條件下,丁醇濃度達到9.42 g/L.
(3)試驗表明汽爆玉米秸稈糖化發酵丁醇,取得了較好的發酵效果,為進一步的放大試驗提供參考.
[1]WU M,WANG M,LIU J,et al.Assessment of potential life-cycle energy and greenhouse gas emission effects from using corn-based butanol as a transportation fuel[J].Biotechnology Progress,2008,24(6):1204-1214.
[2]QURESHI N,SAHA B C,DIEN B,et al.Production of butanol(a biofuel)from agricultural residues:Part I-Use of barley straw hydrolysate[J].Biomass and Bioenergy,2010,34(4):559-565.
[3]李冬敏,陳洪章.汽爆秸稈膜循環酶解耦合丙酮丁醇發酵[J].過程工程學報,2007,7(6):1212-1216.
[4]陳守文,馬昕,汪履綏,等.稻草酶法水解液的丙酮丁醇發酵[J].工業微生物,1998,28(4):30-34.
[5]常春.生物質制備新型平臺化合物乙酰丙酸的研究[D].杭州:浙江大學材料與化學工程學院,2006.
[6]中國食品發酵工業研究院,北京寧馨兒生物科技開發有限公司,諾維信(中國)生物技術有限公司,等.QB 2583—2003附錄A(規范性附錄)濾紙酶活力(FPA)的測定方法[S].北京:中國輕工業出版社,2003.
[7]劉廣慧,朱文眾,胡鐵功.毛細管氣相色譜法分析丙酮和丁醇發酵產物[J].食品與發酵工業,2007,33(11):115-117.
[8]EZEJI T,QURESHI N,BLASCHEK H P.Butanol production from agricultural residues:Impact of degradation products on Clostridium beijerinckii growth and butanol fermentation[J].Biotechnology and Bioengineering,2007,97(6):1460-1469.

