補腎益氣活血中藥對大鼠缺血再灌注腦組織血管內皮生長因子表達和血腦屏障通透性的影響
趙鳳玲 孫佳紅 張寶蘭 張秀梅
內蒙古醫學院第四附屬醫院,內蒙古包頭 014030
尋求腦梗死的治療方法一直是世界醫學的焦點。血管內皮生長因子(VEGF)是一類普遍存在于中樞神經系統的生長因子,又稱為血管通透性因子,具有刺激血管內皮細胞增生、遷移,促進血管生成和增加血管通透性的作用[1]。VEGF直接作用于血管內皮細胞的有絲分裂原及內皮細胞上的受體,發揮其促血管再生的作用[2]。目前認為VEGF是最重要的成血管因子[3]。研究表明,VEGF是強效血管再生因子,VEGF可使血腦屏障(BBB)內皮細胞間緊密聯接蛋白復合物的完整性破壞,從而引起BBB通透性增高,誘發腦水腫[4]。VEGF是主要的血管生成的調節介質和一個強血管通透性因子。VEGF能夠開放BBB和介導腦水腫[5]。Davisa等[6]發現在VEGF表達后BBB有著明顯的開放,并得出了VEGF是通過提高表達VEGFR-2而實現開放血腦屏障的結論。本實驗研究旨在深入探討腦缺血再灌注后VEGF表達的動態變化與BBB破壞的關系,為VEGF臨床應用前景提供實驗依據。
1 儀器與試藥
1.1 試驗動物
健康雄性Wistar大鼠80只,體重350~420 g,包頭醫學院實驗動物部提供(符合國家清潔級動物標準)。
1.2 試藥
血塞通注射液(昆明制藥集團股份有限公司,批號:12FB17),脈絡寧注射液(金陵藥業股份有限公司南京金陵制藥廠,批號:20111023),10%水合氯醛,生理鹽水,4%多聚甲醛(PBS,0.1 mol,pH 7.4),甲酰胺,伊文思藍(Evans blue,EB),試劑盒(武漢博士德公司提供)。
1.3 儀器
熒光分光光度儀(960型,上海光學儀三廠),單尼龍線,水浴箱,石蠟切片機,光學顯微鏡。
1.4 試驗動物分組及模型制備
大鼠隨機分為假手術組8只,生理鹽水對照組36只(分別為缺血90 min再灌注1,3,7 d各12只)和中藥組36只(分組同生理鹽水對照組)。每小組中6只用于BBB通透性的測定,6只用于VEGF的檢測。大腦中動脈閉塞再灌注模型制作參照koizumis線栓法[7]。10%水合氯醛(350 mg/kg)腹腔注射麻醉后,頸部切口,分離左側的頸總動脈、頸內動脈、頸外動脈及其分支,結扎頸外動脈及其分支,在頸內動脈近端放線,遠端放動脈夾,頸總動脈分叉處剪一小口,將直徑0.25 mm單尼龍線經小口插入頸內動脈(18±1)mm。尼龍線外留15~20 mm,線栓成功后移除遠端動脈夾;再灌注時只需將栓線抽出至頸內動脈起始部。模型成功的標準是:栓線即刻出現左側Horner征,麻醉清醒后出現右前肢運動功能障礙。假手術組除栓線只插入0.5 cm左右外,余均同動物模型制備。中藥組給藥劑量按成人用量10 mL/60 kg,2次/d的10倍換算應為1.67 mL/kg,2次/d,腹腔注射。生理鹽水組腹腔注射生理鹽水1.67 mL/kg,2次/d。
1.5 行為學檢查
參照Bederson等[8]的評分方法對大鼠進行神經癥狀評分。無神經病學征象為0分;提尾時右側前肢不能完全伸直為1分;向右側旋轉征象為2分;向右側跌倒為3分;無自發活動及意識障礙者為4分。均于術后每日觀察。
1.6 血腦屏障通透性的定量測定[9-10]
使用EB作為測量血腦屏障通透性的標蹤劑,各小組內隨機取6只動物在處死前2 h按20 mg/kg體重自尾靜脈注入2%EB液。幾秒鐘后,大鼠眼球結膜,四肢等顯示藍色,表示注射成功。在預定的時間內用250 mL生理鹽水進行心臟灌注,迅速取左半球稱重后機械性粉碎腦組織標本,按每100 mg濕腦組織加3 mL甲酰胺加蓋避光,在37℃水浴箱中提取72 h,提取液在熒光分光光度儀上測定熒光強度,激發波長624 nm,發射波長683 nm,波寬為10 nm。用倍比稀釋法制作EB標準曲線計算出線性回歸方程,再根據線性回歸方程計算出提取液中EB的濃度,最后求得腦組織EB的含量,以μg/g濕腦組織表示。
1.7 VEGF表達檢測
到達各再灌注時間點后迅速以10%水合氯醛麻醉各組大鼠(每組中剩余的6只),經左心室用生理鹽水沖洗,用 4%多聚甲醛(PBS,0.1 mol,pH 7.4)灌注固定腦組織,將腦組織浸于相同固定液中48 h。取視交叉平面作為觀察平面。石蠟包埋,以石蠟切片機切成4 μm厚的連續冠狀切片。每張切片分別計數高倍鏡下缺血區5個視野里陽性細胞數,取其均值為該張切片每高倍視野下陽性細胞數。VEGF免疫組織化學染色采用SABC法,按試劑盒操作說明書進行。
1.8 腦組織病理學檢查
從各組織中隨機選取與用于免疫組化的切片相鄰的4張連續切片進行常規HE染色,在光鏡下觀察其組織形態學變化特點。
1.9 統計學方法
采用統計軟件SPSS 13.0對實驗數據進行分析,計量資料數據以均數±標準差(±s)表示,采用方差分析,兩兩比較采用LSD-t檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 腦組織血腦屏障的變化
2.1.1 肉眼觀察 假手術組左側半球未見藍染;生理鹽水組和藥物組左側半球(MCAO側)均有以大腦中動脈為圓心的藍染,藥物組藍染區顏色較淡。見表1。
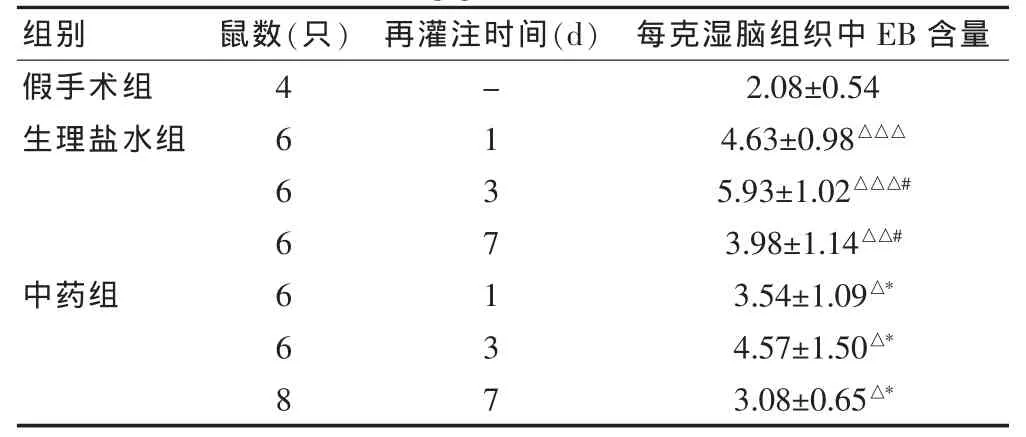
表1 大鼠腦組織不同再灌注時間腦組織EB含量分析結果(μg/g濕腦組織)
2.1.2 腦組織中EB含量的檢測分析 在各再灌注時間點生理鹽水組和中藥組均與假手術組比較,差異有統計學意義(P<0.05),二者均呈現在缺血90 min再灌注24 h迅速升高,72 h達到高峰,以后開始減少,至少持續到缺血再灌注7 d以上。中藥組在各時間點均明顯低于生理鹽水組(P<0.05)。
2.2 腦組織VEGF免疫組化染色結果分析
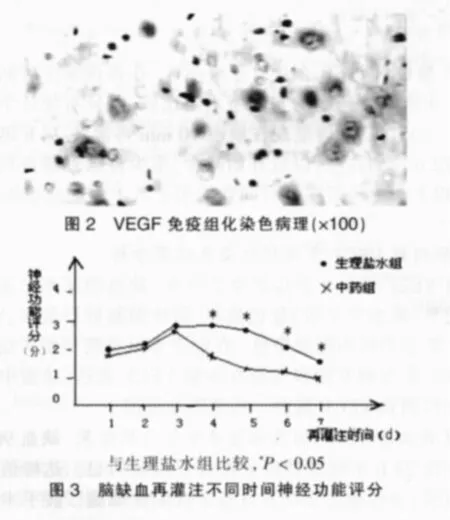
2.2.1 VEGF蛋白在腦組織中的分布 缺血側壞死與正常組織交界(缺血半暗帶)顯色最深,陽性細胞數目最多;VEGF陽性細胞為核周胞漿染色。在假手術組及模型組各組大鼠腦組織在雙側室管膜均存在少量VEGF表達,缺血中心區未能檢測到VEGF蛋白。病理圖片見圖1。
2.2.2 缺血區VEGF陽性細胞半定量分析結果 缺血90 min再灌注24 h半暗帶神經元陽性反應最明顯。達峰值后迅速減少,至再灌注3~7 d只有少數陽性細胞。假手術組皮層未能檢測到VEGF蛋白陽性細胞。見表2。
2.2.3 中藥對VEGF蛋白表達的影響 中藥在再灌注1~7 d對VEGF蛋白的表達沒有影響(P>0.05)。
2.3 病理學觀察
組織病理學研究顯示:MCA區呈典型的腦缺血后壞死改變,以尾殼核外側部分損害最重,其次是背外側皮層,神經元呈缺血性改變,胞體縮小胞核固縮,數量減少。膠質細胞反應性增生和少量白細胞滲出。毛細血管擴張明顯,內皮細胞腫脹。病理圖片見圖1。
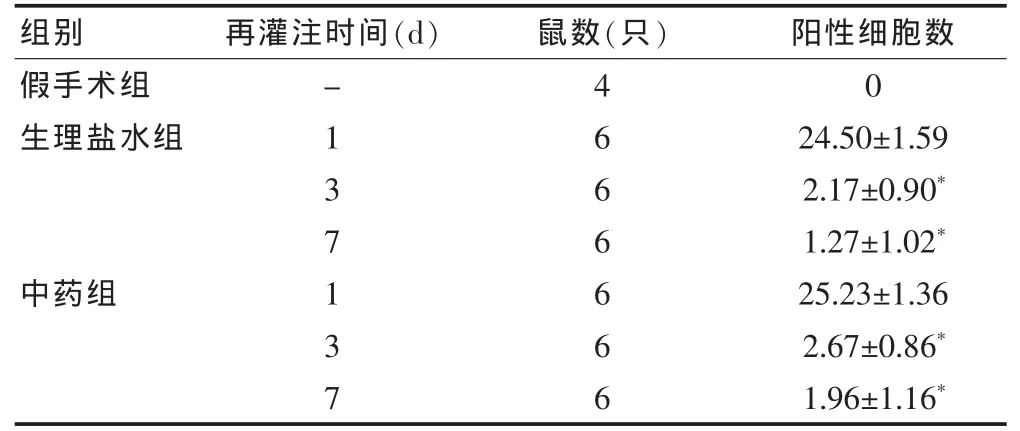
表2 大鼠腦組織不同再灌注時間缺血區免疫組化分析結果(個/高倍視野,×400)

2.4 癥狀變化
栓線即刻出現左側Horner綜合征,麻醉清醒后出現右前肢癱瘓。模型組動物偏癱癥狀評分均為在缺血再灌注3 d后趨于穩定,逐漸降低。中藥組在3 d后較生理鹽水組評分降低(P<0.005)。 見圖2。
3 討論
本實驗顯示腦缺血再灌注后血腦屏障破壞為一動態變化過程,在缺血再灌注1 d腦組織EB含量已明顯升高(P < 0.001),72 h達高峰(與 1 d比較,P < 0.05),這與臨床上大面積腦梗死病情多在3 d內惡化相一致。因為血腦屏障破壞導致血管源性腦水腫,腦水腫加重是缺血性腦損傷病情惡化最主要的危險因素。故對能引起血腦屏障破壞的因素進行深入討論進而實施有針對性的治療成為缺血性腦血管疾病研究的熱點。
近年有關VEGF在缺血性腦組織中的表達調節及作用機制的研究迅速增多。VEGF在缺血性損傷后腦組織功能的保護和修復中的作用逐漸引起了人們的注意并已取得積極的研究進展,許多實驗結果證實VEGF在抗腦缺血損傷中起著非常重要的作用。VEGF是一種內皮細胞特異的有絲分裂原,可以刺激體內尤其是缺血部位的血管形成[11]。目前認為,缺氧是VEGF/VEGFR表達的最主要的調節因素[12]。缺血、缺氧時,VEGF表達明顯增加,尤以腦組織中VEGF表達升高明顯。在腦缺血后的“缺血半暗帶”低氧區,低氧激活低氧誘導因子后促使VEGF及其受體VEGFR-1和VEGFR-2的表達,引起血管反應,以血管內皮細胞增殖和新血管形成為特征,刺激缺氧組織建立有效的側支循環并恢復內皮細胞的完整性,發揮搭橋作用,誘導新生血管形成,并使新生血管從正常組織向半暗帶及缺血中心區延伸,增加受累腦組織再灌注及供氧量,從而減輕腦缺血再灌注損傷[13]。但是VEGF可增加血管通透性,促使病變組織微血管內血漿外滲,尤其對皮膚微血管通透性影響最明顯。國外已有少數研究涉及VEGF在卒中后腦水腫形成中的作用,但結果不盡一致。本實驗動態觀察了MCA閉塞后再灌注不同時間點BBB破壞和VEGF表達的動態變化,顯示腦組織EB含量在24 h升高明顯,72 h達高峰,其后逐漸回落。而VEGF在24 h達高峰,其后迅速下降,72 h已回落接近正常。從二者動態變化的時程上看BBB破壞并不是VEGF表達的結果。另外實驗結果還顯示:補腎益氣活血中藥能夠降低各再灌注時間點大鼠腦組織EB含量,維護血腦屏障,減輕神經功能缺損癥狀,但對VEGF蛋白表達沒有影響,故從這兩方面實驗結果說明VEGF不是BBB結構和功能破壞的重要介質,VEGF未加重卒中后血管源性腦水腫。這為應用外源性VEGF蛋白或基因治療缺血性腦損傷提供了實驗依據。中藥組大鼠的肢體活動改善在3 d后較生理鹽水組進步,證明中藥正是通過改善BBB的功能,減輕血管源性腦水腫,進而使肢體功能改善成為可能。應用中醫中藥治療缺血性腦損傷是我國神經科學工作者探索的一個方向,中藥作用的多途徑性似乎與缺血性腦損傷病理變化的多樣性具有針對性效應,補腎益氣活血中藥在一定程度上能夠減輕BBB的破壞,臨床上可以安全使用,其BBB開放的機制及與其他促血管生成因子的關系仍需進一步探討。
[1]徐雙云,徐家麗.血管內皮細胞生長因子在缺氧缺血性腦損傷中的神經保護作用[J].國際兒科學雜志,2009,36(3):290-292.
[2]李雪梅,牛文澤,陳翔.芹菜素對大鼠腦缺血再灌注后VEGF表達的影響及意義[J].中國病理生理雜志,2010,26(12):2473-2477.
[3]孫國棟,岳永花,李先榮,等.芪蛭通絡膠囊輔助阿司匹林對腦缺血再灌注損傷大鼠的影響[J].中國實驗方劑學雜志,2010,16(17):202-210.
[4]鄧志寬,錢桂生,程賽宇,等.siRNA沉默腦組織血管內皮生長因子表達對高原大鼠血腦屏障通透性的影響[J].中華醫學雜志,2009,89(37):2640-2643.
[5]田子健,楊楠,楊蕾琪.缺血再灌注后血腦屏障通透性改變的研究進展[J].中國醫藥指南,2011,9(23):222-223.
[6]Davisa B,Tang J,Zhang L,et al.Ferriero Role of vasodilator stimulated phosphoprotein in VEGF induced blood-brainbarrier permeability in endothelial cell monolayers [J].Int J Devl Neurosci,2010,28(6):423-428.
[7]Nagasawa H,Kogure K.Correlation between cerebral blood and histologic changes in a new rat model of cerebral artery occlusion[J].Stroke,1989,20:1037.
[8]Bederson JB,Pitts LH,Tsuji M,et al.Rat middle cerebral artery occlusion:evaluation of the model and development of a neurologic examination[J].Stroke,1986,17:472.
[9]Drummond JC,Patel PM,Cole DT,et al.The effect of the reduction of colloid oncotic pressure,with and without reduction of osmolality,on post-traumatic cerebral edema[J].Auesthesiology,1998,88(4):993-1002.
[10]Kawai N,Kawanishi M,Okauchi M,et al.Effects of hypothermia on thronrbin-induced brain edema formation [J].Brain Res,2001,895(1-2):50-58.
[11]韓為,王穎,程紅亮,等.針刺涌泉、重灸百會對局灶性腦缺血大鼠VEGF 表達的影響[J].上海針灸雜志,2009,28(9):554-557.
[12]Kiselyov A,Balakin KV,Tkachenko SE.VEGF/VEGFR signaling as a target for inhibiting angiogenesis[J].Expert Opin Investing Drugs,2007,16(1):83-107.
[13]李逸塵,姜信誠,景玉宏,等.大鼠腦缺血再灌注后海馬CA1區血管內皮細胞生長因子與突觸素的關系[J].蘭州大學學報:醫學版,2010,36(1):9-12.

