α-丙二醇-水相中氯代二噁英的催化加氫脫氯降解
金士威,華 曄,李晨曦,鄒 彬,Daniel Dianchen Gang,3
(1.馬里蘭大學土木與環境工程系,美國馬里蘭州 大學公園20742;2.武漢工程大學化工與制藥學院,綠色化工過程教育部重點實驗室,湖北 武漢 430074;3.路易斯安那大學拉法葉分校土木工程系,美國路易斯安那州 拉法葉 70504)
0 引 言
多氯二苯并二噁英polychlorinated dibenzop-dioxin簡稱 PCDDs)和多氯二苯并呋喃polychlorinated dibenzofuran(簡稱 PCDFs)是一類典型的持久性有機污染物(POPs),主要來源于人類活動,如市政垃圾焚燒、化工、冶金、造紙、汽車尾氣排放等[1-4].PCDD/Fs的毒性隨氯原子的取代數量和取代位置不同而有所差異,其中2,3,7,8-四氯代二苯-并-對二噁英(2,3,7,8-TCDD)是迄今為止人類已知的毒性最強的污染物,不僅具有三致毒性,還具有生殖毒性、發育毒性、免疫毒性以及內分泌干擾效應[4-6],因此受到國際社會的普遍重視.杜絕或盡量避免人類接觸二噁英的最佳途徑是源頭控制,也就是說,嚴格控制工業過程,以盡可能減少二噁英的形成.但進入環境的二噁英,因其難生物降解,而可持久存在于環境中.近十年來,已經開發了許多降解二噁英的方法,如微生物降解法、光催化降解法、高溫熱解法等.近年來發展的催化加氫脫氯法,相比其他方法,具有簡單、高效、反應條件溫和、幾乎不產生二次污染等優點[1-2].許多金屬催化劑,包括 Pd/C,Pt/C,Rh/C等被用于氯代有機物的催化脫氯.
已開發的貴金屬催化劑對二噁英類物質的催化還原脫氯方法可歸為兩類:一類用H2作為氫源[7-8],而另一類用2-丙醇作為氫源[9-14],兩類催化系統都在水/有機溶劑中以多孔粉末為載體的貴金屬催化下進行.Ukisu等[14-15]對2-丙醇為溶劑的氯代二噁英的催化脫氯進行了卓有成效的研究.Mitoma等[15-16]用鈣催化劑降解醇溶液中的二噁英,取得了較好的結果.但二噁英的催化加氫脫氯研究,主要在低氯代方面,少數研究涉及高氯代二噁英,如 Zhang等[7,11]研究了乙醇-水溶液中八氯代二噁英以H2作為氫源的催化脫氯.
由于α-丙二醇是一種對人體無毒無害同時能夠與水和多種有機溶劑混溶的溶劑,本研究選擇以α-丙二醇與水按1∶1混合液作為溶劑,以實驗室自制的質量分數5%Pd/C為催化劑,以1,2,7,8-四氯代二噁英(1,2,7,8-TCDD)為模型化合物,在堿性條件下研究了反應溫度、反應物初始濃度和催化劑濃度等對二噁英催化加氫脫氯的影響.
1 實驗部分
1.1 儀器與試劑
Agilent GC 7890/MS 5975氣質聯用色譜儀,以及 DB-5MS毛細管柱 (60m × 250μm×0.25μm),均購自美國Agilent公司.
標準樣品:1,2,7,8-TCDD(質量分數98%)、內標物五氯苯(C6HCl5)(質量分數為98%)購自美國 Cambridge Isotope.Laboratories,Inc;1,2-丙二醇、氫氧化鈉為分析純;正己烷,二氯甲烷,甲苯,均為農殘級 (J.T.Baker,USA);催化劑:質量分數為5%的Pd/C,粉末狀(實驗室合成);H2、He為高純鋼瓶氣(四川天一科技股份有限公司武漢供氣分公司),純度大于99.999%.
1.2 方法與步驟
反應在裝有玻璃通氣管、溫度計和回流冷凝管的250mL四口燒瓶中進行.將反應儀器搭建好后,在加料口處加入催化劑Pd/C,塞上磨口塞,通入氮氣約5min,將燒瓶中空氣置換掉,然后再通入氫氣,置換氮氣,約5min后,將四口燒瓶加熱至200℃,保持40min,以活化催化劑.停止加熱,使燒瓶在冰水浴中冷卻,迅速加入1mol/L的氫氧化鈉溶液和含有標準樣品的丙二醇溶液.開啟磁力攪拌器,控制反應溫度,進行催化加氫脫氯反應,反應過程一直通入氫氣.不同時間間隔取樣1 mL,置于冰箱,避光凍存,便于后續的前處理和檢測.
試驗研究了不同反應溫度,不同初始濃度和不同催化劑用量對催化加氫脫氯的影響.
1.3 樣品前處理過程
在1mL二噁英樣品溶液中加入5μL C6HCl5/甲苯 (10μg/mL)的內標液,混勻.然后以1 000r/min的轉速離心15min,將小管中的上清液轉入至另一小管,將原管中沉淀用正己烷超聲提取5min,離心,取上清液,過程重復2次.將取得的上清液合并,超聲10min,轉移分層后的上層液體,對殘余下層液體用正己烷超聲提取2次,合并提取液,氮吹至1mL,用于GC-MS檢測.
1.4 儀器分析
GC7890/MS 5975的氣相條件:進樣口溫度為250℃,載氣:He,流速為1.4mL/min,不分流進樣.進樣量:1μL.
氣相色譜升溫程序為:100℃保持4min,25℃·min-1至170℃,然后以5℃/min升至270℃,保持5min.
質譜條件:電離方式EI,電子轟擊能量為70eV,離子源溫度為:230℃,掃描方式為選擇離子監測(SIM)模式.C6HCl5的特征離子為178,215,250;1,2,7,8-TCDD的特征離子為194,257,322.
2 結果與討論
2.1 1,2,7,8-TCDD的色譜圖和標準曲線
1,2,7,8-TCDD的 GC-MS圖譜如圖1所示,標準曲線如圖2所示.1,2,7,8-TCDD的檢測限為1ng/mL,樣品回收率為98.9%~102.1%.
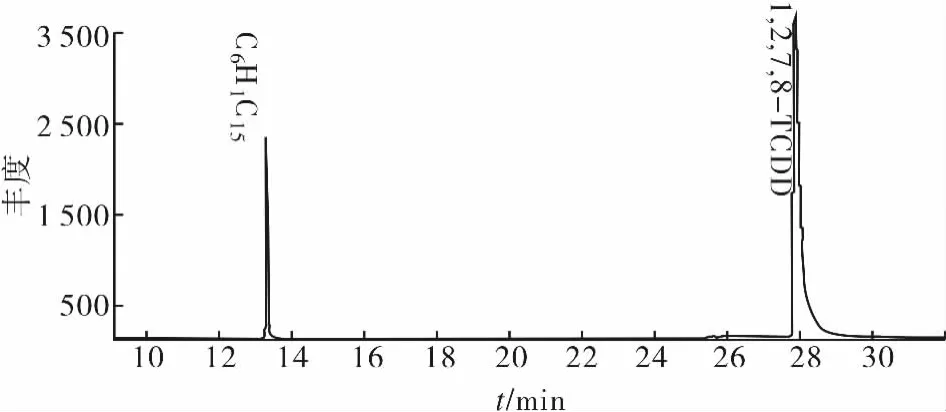
圖1 1,2,7,8-TCDD及內標的色譜圖Fig.1 GC-MS chromatogram of 1,2,7,8-TCDD and internal standard compound C6HCl5
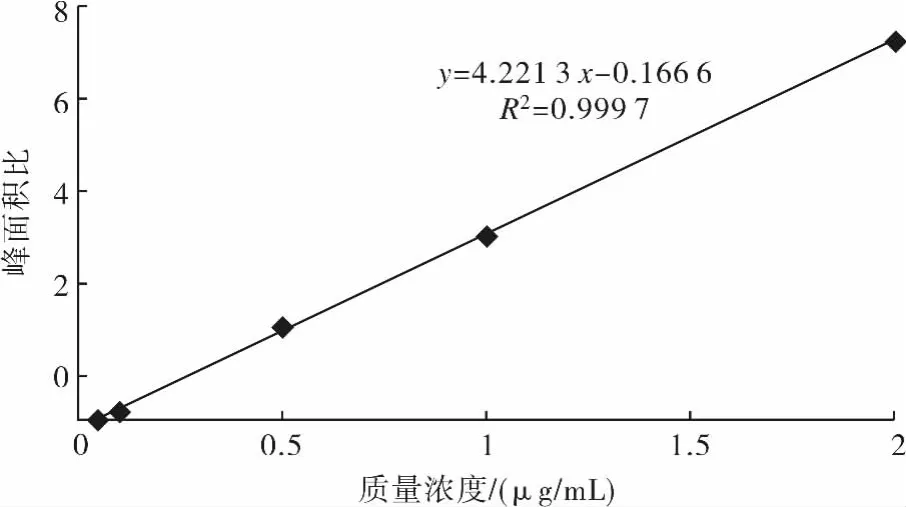
圖2 1,2,7,8-TCDD的標準曲線Fig.2 The calibration curve of 1,2,7,8-TCDD
2.2 溫度對反應的影響
為了研究溫度對催化加氫脫氯的影響,選取30、45、60℃三個不同反應溫度進行實驗,初始質量濃度為5μg/mL,反應時間150min,其實驗結果如表1所示.
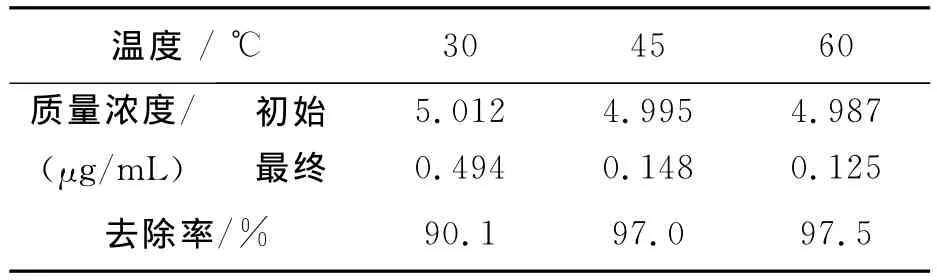
表1 不同反應溫度對1,2,7,8-TCDD去除率的影響Table 1 Effect of reaction temperature on the removal of 1,2,7,8-TCDD
由表1可知,30℃時,其去除率已達90.1%,隨著溫度升高,其去除率逐漸增大,45℃時的去除率達97.0%,說明升高溫度有利于催化加氫反應的進行.這可以從兩方面解釋,首先,根據阿倫尼烏斯方程,溫度升高,反應速率常數增大.當反應物濃度保持不變時,反應速率與反應速率常數成正比,因此,反應溫度升高,加氫反應速率加快;其次,由菲克定律可知,隨著溫度的升高,反應物和生成物的擴散速率加快,從而導致反應物與催化劑的接觸頻率增加,并可使生成物與催化劑較容易分離,從而使加氫反應速率加快.因此,適當地升高反應溫度,反應速率會明顯加快.但當反應溫度過高時,反應速率的提高就不明顯了,這可能是過高的溫度,導致反應物和氫氣不利于在催化劑表面上的吸附和活化,使反應速率的增加不明顯.本實驗中,溫度繼續升高到60℃時,去除率則為97.5%.表明溫度繼續升高,去除率已變化不大.從減少能耗方面考慮,反應溫度以45℃為宜,故后面的實驗選取45℃作為反應溫度.
2.3 初始質量濃度對去除率的影響
為了研究初始質量濃度對去除率的影響,在反應溫度為45℃時,對初始質量濃度分別為1,5,10,25μg/mL的1,2,7,8-TCDD丙二醇溶液進行了催化加氫反應,反應時間為150min,結果如表2所示.
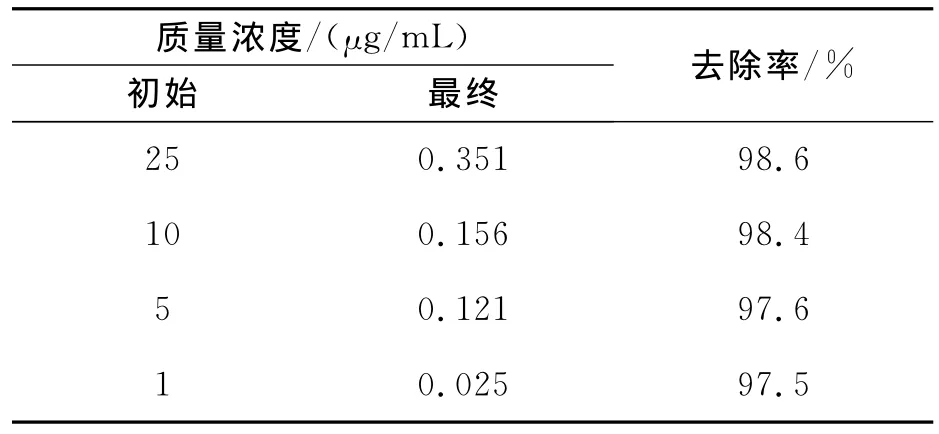
表2 初始質量濃度對1,2,7,8-TCDD去除率的影響Table 2 Effect of initial concentration on the removal of 1,2,7,8-TCDD
由表2可知,在用Pd/C催化1,2,7,8-TCDD的加氫脫氯反應中,1μg/mL的二噁英反應液在150min時能較好地發生加氫脫氯反應,其殘余量為0.025μg/mL,去除率為97.5%,5μg/mL的二噁英在150min時的去除率為97.6%.當質量濃度增大到10μg/mL和25μg/mL時,去除率在98%以上.表明 1,2,7,8-TCDD的催化加氫反應與初始質量濃度變化關系較小.無論是較高初始質量濃度25μg/mL還是較低濃度1μg/mL條件下,丙二醇/水反應液中的1,2,7,8-TCDD均能實現較好的加氫脫氯反應.徐杰等[17]研究了初始質量濃度為30μg/mL和600μg/mL三氯新15min加氫脫氯反應,其去除率分別為100%和98%.當質量濃度增大到4 500μg/mL和10 000μg/mL延長反應時間也能夠去除,表明無論是高濃度,還是低濃度,該類污染物均可以用催化加氫的方法脫氯去除.這是由于有機氯化物的催化加氫脫氯過程是一個不可逆過程,只要有足夠的反應時間,有機氯污染物最終都可以完全反應而徹底去除.
2.4 反應時間對去除率的影響
本實驗研究了反應時間對1μg/mL 1,2,7,8-TCDD催化加氫脫氯去除率的影響,結果如圖3所示.
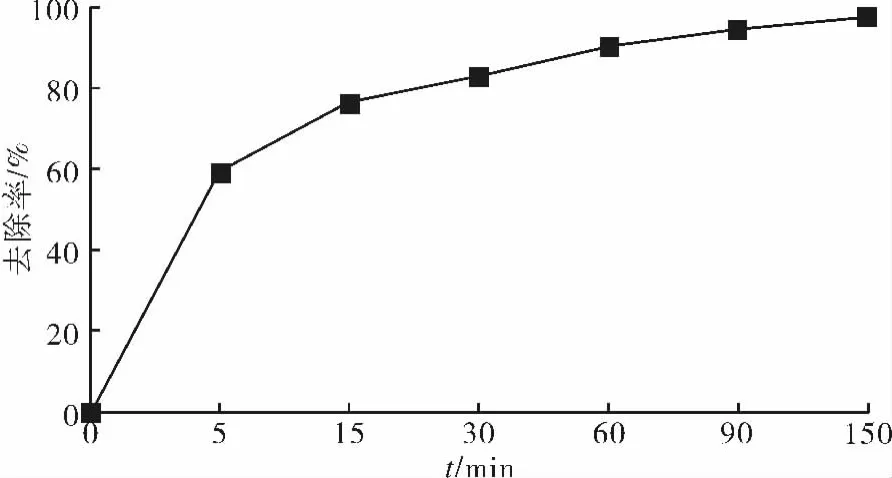
圖3 反應時間對1,2,7,8-TCDD(1μg/mL)去除率的影響Fig.3 Effect of reaction time on the removal of 1,2,7,8-TCDD (1μg/mL)
由圖3可知1,2,7,8-TCDD催化加氫反應主要發生在前15min內,反應5min時的去除率達到59.0%,15min時的去除率達到76.3%,其質量濃度下降較快.30min后的去除率變化不大.說明隨著1,2,7,8-TCDD在丙二醇中濃度的降低,其加氫反應的速率也變得越來越慢.可能的原因是因為反應物的濃度隨著反應進行而不斷降低,其在丙二醇/水中的擴散和在催化劑上的吸附也將變得越來越難,使得吸附在催化劑Pd/C上的質量濃度減少,從而使1,2,7,8-TCDD催化加氫反應速率變慢.反應時間在150min時,去除率超過97%.
2.4 催化劑質量濃度對去除率的影響
在催化加氫脫氯反應中催化劑起著十分重要的作用,催化劑活性的高和低、穩定性的好與壞,催化劑的用量多少都會直接影響到脫氯反應的效果.本實驗選取 Pd/C作為 1,2,7,8-TCDD加氫反應催化劑,通過調節催化劑的質量濃度來討論其對去除率的影響.實驗結果如圖4所示.
圖4表明,隨著催化劑質量濃度的逐漸增加,催化加氫反應的去除率先增加后減少.催化劑質量濃度為0.125,0.25,0.5g/mL時的去除率分別為90.8%,95.1%,97.1%.表明增大催化劑的質量濃度有利于脫氯反應的進行.但當催化劑的質量濃度從0.5g/mL增加到1g/mL時,1,2,7,8-TCDD的去除率并未繼續增加反而有所降低,其去除率為94.6%.可能由于催化劑用量的增加,導致了活性中心增多,但造成了每個活性中心反應物濃度下降,從而降低了反應速率.根據試驗結果,確定催化劑的最佳用量為0.5g/mL.

圖4 Pd/C催化劑用量對去除率的影響Fig.4 Effect of Pd/C catalyst dosage on the removal of 1,2,7,8-TCDD
貴金屬催化加氫脫氯反應由于反應條件溫和、降解率高,而成為去除有機氯代化合物的有效手段.催化加氫脫氯反應,會生成HCl,而HCl會對催化劑造成中毒,因此催化加氫脫氯反應通常在堿性條件下進行.本試驗中,加入NaOH的濃度為1mol/L,以保證HCl能被完全中和.二噁英的催化加氫脫氯產物是低氯代或不帶氯的二噁英或呋喃.氯原子按一級動力學被一個接一個脫除,反應如圖5所示.在本試驗中,檢測到了一些二氯代的二噁英以及不帶氯的母體二噁英化合物.且隨著反應時間的增加,母體化合物的濃度峰高也增大,表明脫氯的最終產物就是二噁英的母體化合物.
盡管當前的用貴金屬催化還原脫氯方法修復PCDD/Fs污染是有效的,但也存在一些缺點,如降解不徹底時產生二次廢液,復雜的催化劑回收/清洗過程及催化劑的使用壽命等.因此,還必須對催化加氫脫氯的去除二噁英的實際應用開展進一步的研究.
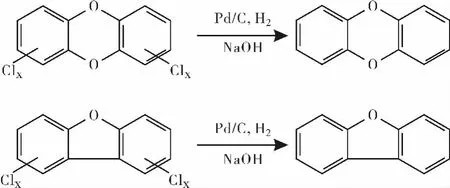
圖5 氯代二噁英的催化脫氯反應式Fig.5 The equations of catalytic dechlorination of PCDD/Fs
3 結 語
催化加氫脫氯反應是一個去除有機氯代化合物的有效手段.通過使用氫氣或是氫轉移試劑作為氫源、利用加氫催化劑在堿性條件下與氯代化合物進行反應,從而消除氯代化合物上的氯原子達到去除的目的.本研究利用H2作為氫源,質量分數5%Pd/C作為加氫催化劑,α-丙二醇/水(1∶1)作為溶劑,在 NaOH 堿性條件下對1,2,7,8-TCDD催化加氫反應進行了探討.結果表明,當反應溫度為45℃,催化劑用量為0.5g/mL,反應時間為150min時,1,2,7,8-TCDD 的 去 除 率 達97.0%,1,2,7,8-TCDD 初始質量濃度對催化加氫脫氯的去除率沒有影響.
[1]Weber R.Relevance of PCDD/PCDF formation for the evaluation of POPs destruction technologies-review on current status and assessment gaps [J].Chemosphere,2007,67:S109-S117.
[2]Kulkarni P S,Crespo J G,Afonso C A M.Dioxins sources and current remediation technologies—a review [J].Environ Int,2008,34:139-153.
[3]Altarawneh M,Dlugogorski B Z,Kennedy E M,et al.Mechanisms for formation,chlorination,dechlorination and destruction of polychlorinated dibenzo-pdioxins and dibenzofurans (PCDD/Fs)[J].Prog Energy Combust,2009,35:245-274.
[4]Stanmore BR.The formation of dioxins in combustion systems[J].Combustion and Flame,2004,136(3):398-427.
[5]McGregor D B,Partensky C,Wilbourn J,et al.An IARC evaluation of polychlorinated dibenzo-p-dioxins and polychlorinated dibenzofurans as risk factors in human carcinogenesis [J].Environ Health Perspect,1998,106(suppl 2):755-760.
[6]周莉菊,馮家滿,趙由才.二噁英的毒性及環境來源[J].工業安全與環保,2006,32(11):49-51.ZHOU Li-ju,FENG Jia-man,ZHAO You-cai.The Toxicity of Dioxin and the Source in Environment.[J].Industrial Safety and Environmental Protection,2006,32(11):49-51.(in chinese)
[7]Zhang F,Chen J,Zhang H,et al.The study on the dechlorination of OCDD with Pd/C catalyst in ethanol-water solution under mild conditions[J].Chemosphere,2007,68:1716-1722.
[8]Ghattas A,Abu-Reziq R,Avnir D,et al.Exhaustive hydrodechlorination of chlorinated aromatic environmental pollutants to alicyclic compounds[J].Green Chem,2003(5):40-43.
[9]Ukisu Y,Miyadera T.Dechlorination of polychlorinated dibenzo-p-dioxins catalyzed by noble metal catalysts under mild conditions [J].Chemosphere,2002,46:507-510.
[10]Yang Z,Xia C,Zhang Q,et al.Catalytic detoxification of polychlorinated dibenzo-p-dioxins and polychlorinated dibenzofurans in fly ash[J].Waste Manage,2007,27:588-592.
[11]Zhang F,Chen J,Zhang H,et al.Dechlorination of dioxins with Pd/C in ethanol-water solution under mild conditions [J].Separation and Purification Technology,2008,59:164-168.
[12]Cobo M,Conesa J A,Correa C M D.Effect of the reducing agent on the hydrodechlorination of dioxins over 2wt%Pd/γ-Al2O3[J].Appl Catal B:Environ,2009,92:367-376.
[13]Ukisu Y,Miyadera T.Hydrogen-transfer hydrodechlorination of polychlorinated dibenzo-p-dioxins and dibenzofurans catalyzed by supported palladium catalysts[J].Appl Catal B:Environ,2003,40:141-149.
[14]Ukisu Y,Miyadera T.Dechlorination of dioxins with supported palladium catalysts in 2-propanol solution[J].Appl Catal A:Gen,2004,271:165-170.
[15]Mitoma Y,Uda T,Egashira N,et al.Approach to highly efficient dechlorination of PCDDs,PCDFs,and coplanar PCBs using metallic calcium in ethanol under atmospheric pressure at room temperature[J].Environ Sci Technol,2004,38:1216-1220.
[16]Mitoma Y,Tasaka N,Takase M,et al.Calciumpromoted catalytic degradation of PCDDs,PCDFs,and coplanar PCBs under a mild wet process[J].Environ Sci Technol,2006,40:1849-1854.
[17]徐杰,夏傳海,梁鑫淼,等.一種多鹵代苯氧基鹵代苯酚類化合物的催化加氫脫鹵的方法:中國, 02132909.5[P].2003-03-19.XU Jie,XIA Chuan-hai,LIANG Xin-miao,et al.A method about catalytic hydrodehalogenation of multi-halogenated phenoxy halogenated phenolic compounds:China, 02132909.5 [P].2003-03-19.(in Chinese)

