慢性阻塞性肺疾病各期抗M2受體抗體mRNA表達水平及機理分析
張 偉,姚玉強,谷明明,孫璐璐,韓 佳
(1.山東中醫藥大學附屬醫院,山東 濟南 250011;2.山東中醫藥大學,山東 濟南 250014)
慢性阻塞性肺疾病各期抗M2受體抗體mRNA表達水平及機理分析
張 偉1,姚玉強2*,谷明明2,孫璐璐2,韓 佳2
(1.山東中醫藥大學附屬醫院,山東 濟南 250011;2.山東中醫藥大學,山東 濟南 250014)
目的:通過觀察慢性阻塞性肺疾病(COPD)不同時期大鼠模型組的抗M2受體抗體mRNA表達水平、心肌細胞的病變程度,來分析COPD在不同分期對心臟的影響。方法:健康雄性Wistar大鼠32只,隨機分為4組(正常組A、COPD組B、COPD急性加重組C、COPD并發肺心病組D)。通過氣管內滴入脂多糖和被動吸煙的方法建立COPD大鼠模型,COPD模型大鼠再次氣管滴入LPS造成急性加重,在COPD的基礎上尾靜脈注射三氯化鐵建立COPD并發肺心病模型。RT-PCR法檢測血中抗M2受體抗體mRNA含量,電鏡觀察心臟結構變化。結果:抗M2受體抗體mRNA在B、C組表達均升高(P<0.05),在D組表達最高,較AB組均有明顯增高(P<0.01),電鏡下心組織損傷程度依次明顯,抗M2受體抗體mRNA的表達水平與在電鏡下觀察的心肌細胞損傷程度有相關性。結論:M2受體抗體在大鼠COPD并發肺心病模型組中最高,表明COPD病程后期繼發肺心病與對M2受體的自身免疫密切相關。大鼠心肌細胞病理改變程度與M2受體抗體mRNA表達水平相關,提示抗M2受體抗體對COPD病程中心臟病變的發生與發展具有重要作用。
慢性阻塞性肺疾病;抗M2受體抗體mRNA;大鼠
慢性阻塞性肺疾病(COPD)是一種以不完全可逆性氣流受限及氣道持續性炎癥為特征的疾病,呈進行性發展,臨床上以進行性呼出氣流減少、呼氣末容量增大、低氧血癥、高碳酸血癥和進行性肺動脈高壓為特征。屬于中醫學“肺脹”“喘證”“咳嗽”“痰飲”等范疇,臨床表現為咳、痰、喘、胸部脹悶等。肺心病是COPD的常見轉歸,在COPD的病理生理過程中,由于炎性因子或介質、血管內皮、血小板、黏附因子的作用,導致COPD患者肺動脈高壓,引起心功能損害,結構改變,引起右心衰竭。近幾年的研究表明,在慢性阻塞性肺疾病發病過程中,心臟主要受體的功能有明顯的變化,并發現循環血中免疫復合物增加與心功能異常有相關性。[1]這些提示在COPD的發病過程中,可能也有心臟受體抗體的免疫學機制參與,最終導致肺心病的形成。本研究在實驗室中模擬制作COPD不同時期的大鼠模型,通過檢測各模型組的抗M2受體抗體mRNA的表達水平,并觀察心、肺組織病理改變,揭示COPD發病過程中與心肌損害程度的關系。
1 材料與方法
1.1 實驗動物 健康雄性Wistar大鼠(山東大學提供,許可證號SCXK魯20090001)32只,體質量(200±20)g。飼料為標準塊料(山東中醫藥大學提供),飼養在20~25 ℃,濕度40%的動物房內,自由攝食飲水。
1.2 試劑儀器 脂多糖(LPS)(美國Sigma公司)三氯化鐵FeCl3(濟南星聯星科技有限公司),RT-PCR試劑盒(北京康為世紀生物科技有限公司),煙熏箱(100cm×80cm×50cm)及煙熏裝置(自制),指定品牌香煙,水合氯醛(山東大學齊魯醫院,批號:20120209),勻漿機(IKAwoks,型號:T25basic),電子天平(梅特勒-托利多(常州)稱重設備系統有限公司,型號:APA6000F),光鏡病例圖像分析(OLYMPCIS,型號CX-32rfl),PCR擴增儀(ABI公司,型號:7300,軟件:7300SystemSDSsoftware),冷凍離心機(上海安亭科學儀器廠,型號:TGL-16B),70 ℃水浴箱(杭州奧盛,型號:K10CD),電子顯微鏡(日本電子,型號JEM-1200EX),圖像處理系統(美國GATAN)。
1.3 方法
1.3.1 模型建立 用隨機數字表法將大鼠隨機分為4組:正常組(A)、COPD組(B)、COPD急性加重組(C),COPD合并肺心病組(D),每組8只,雄性。適應性喂養3d。第1,14天大鼠麻醉后氣管內滴LPS0.2mL(200μg),第2~28天給予大鼠每天2次香煙煙熏,每次煙熏香煙12支,持續時間大約1h,間隔4h(滴脂多糖當天不煙熏)。被動吸煙方法:將大鼠放入自制的有機玻璃染毒箱(100cm×80cm×50cm)內,將香煙放入自制煙熏裝置中,點燃后,用打氣筒將香煙煙霧注入染毒箱內(此操作頻率為1支煙/5min),進行大鼠被動吸煙染毒。為減少香煙燃燒所產生的水蒸氣對大鼠的影響,采用冷凝管降低香煙溫度、濕度,并在箱底放置適量硅膠干燥劑。第28天氣管再次滴LPS制作COPD急性加重模型。從第16天每3天經尾靜脈緩慢注射0.6%FeCl3(0.2mL/100g大鼠)制作COPD合并肺心病模型。
1.4 動物處理及指標檢測
1.4.1 一般情況觀察 包括大鼠的活動度、對外界反應的靈敏度、皮毛光澤、口唇鼻毛色澤、體質量、飲食、呼吸等情況。
1.4.2 取材及指標檢測 大鼠用水合氯醛按0.3mL/100g腹腔注射麻醉,用經肝素鈉沖管的5mL注射器經腹主動脈抽取5mL新鮮血液后,放血處死。迅速剪開胸腔取出心肺組織,用冰水沖洗血跡,用濾紙吸去水分,一部分放入裝有福爾馬林的病理瓶,經10%中性福爾馬林48h充分固定,梯度酒精脫水,二甲苯透明,石蠟包埋,連續4μm切片2張,分別進行常規HE染色。另一部分放入石蠟盤中,垂直心肌纖維方向,切成1mm×1mm×2mm大小,放入-70 ℃,備電鏡觀察。血液經1 200r/min低溫4 ℃離心15min后取血漿,-70 ℃保存,RT-PCR法檢測抗M2受體抗體mRNA的表達。方法如下:2 500r離心20min,取血漿上清液1mL,采用LiquidSampleRNAReagent、氯仿/異丙醇法提取組織中RNA,按逆轉錄試劑盒說明操作,逆轉錄成cDNA后進行PCR擴增。PCR反應條件為95 ℃預變性10min,95 ℃變性15s,60 ℃退火1min,40個循環。抗M2受體抗體mRNA堿基序列:上游:5'-CgCTCCTTgATgCTACTg-3',下游:5'-TTgCTgCCCTTgTTgTAC-3'。
2 統計學方法
3 結果
3.1 大鼠一般情況觀察 正常組大鼠活動度可,對外界反應靈敏,皮毛光亮,口唇鼻無紫紺,體質量較其他組大鼠重,飲食呼吸可。COPD組大鼠活動度尚可,對外界反應靈敏,皮毛黃暗,無光澤,可聞及呼吸音、哮鳴音,活動無明顯受限。COPD急性加重期大鼠活動受限,對外界反應靈敏,皮毛黃暗,無光澤,可聞及呼吸音、哮鳴音,口唇紫紺,本組死亡率最高。COPD合并肺心病組大鼠活動受限,活動后心跳明顯加快,呼吸急促,口唇紫紺,哮鳴音明顯。
3.2 血抗M2受體抗體mRNA表達 見圖1。
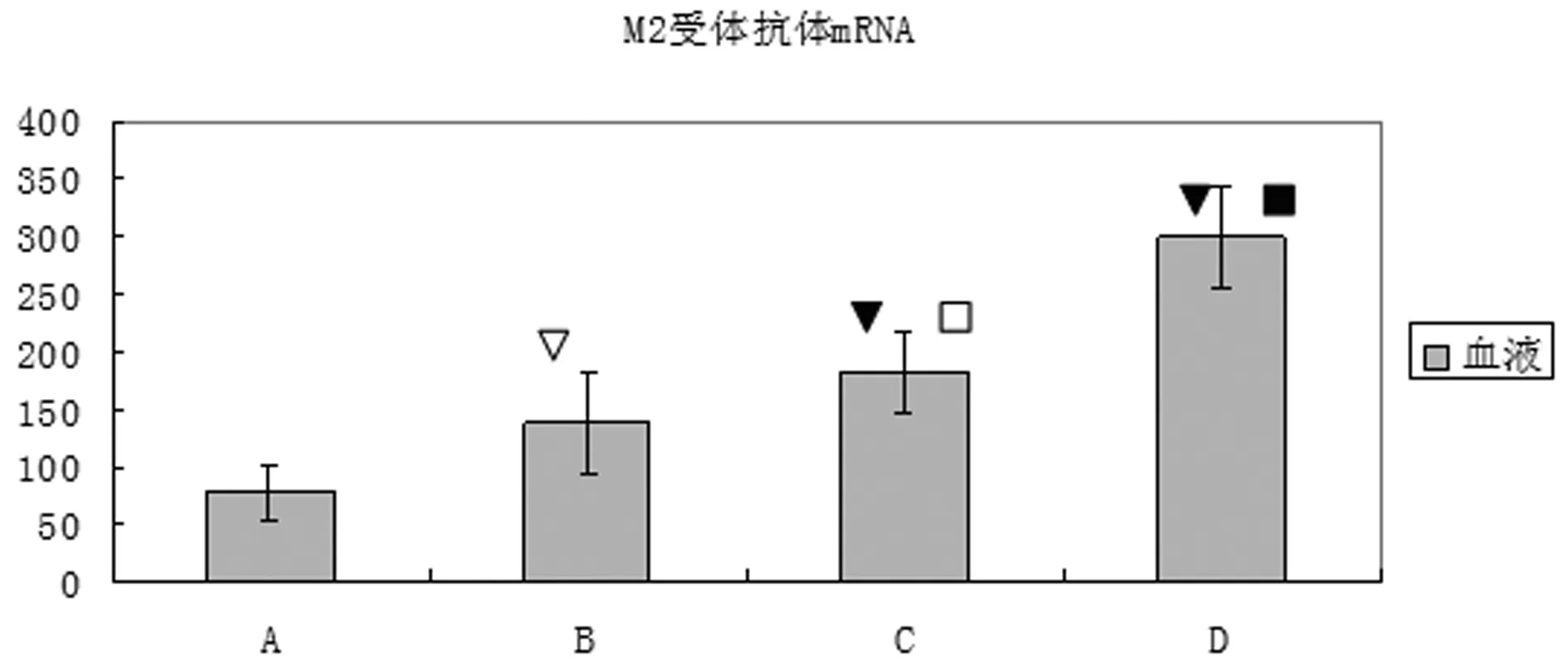
注:△▲與正常組對照,□■與CODP組對照:△□P<0.05,▲■P<0.01。圖1 各組大鼠血漿抗M受體抗體mRNA含量
抗M2受體抗體mRNA在B組,C組,D組的表達依次增高C,D組較A組有明顯增高(P<0.01)。D組表達最高,較AB均有明顯增高(P<0.01)。
3.3 電鏡下心臟超微結構 見圖2。
正常對照組A:心肌細胞正常,線粒體豐富。COPD組B:心肌內血管上皮部分損傷。COPD急性加重組C:核膜受損,線粒體腫脹,纖維排列不規則。COPD并發肺心病組D:核膜不完整,線粒體腫脹,纖維排列不規則,模糊。
4 討論
目前發現多種心臟病患者血清中存在抗心臟M2膽堿能受體的自身抗體。Magnusson等[2]在研究原發性擴張性心肌病中發現患者血清中存在抗心臟β1腎上腺素能受體的自身抗體,之后又有研究發現, 在該病患者血清中存在抗心臟M2膽堿能受體的自身抗體。國外研究小組的研究還證明[3],利用β1或M2受體表位肽段長期免疫動物,可造成心臟發生類似IDCM的形態學改變,類似肺心病的病理改變。這些提示在肺心病出現右心衰竭的發病過程中,可能也有心臟受體抗體的免疫學機制參與,心肌內多種抗體:心肌線粒體ADP/ATP載體抗體、抗肌球蛋白抗體、抗β1受體抗體、抗心臟M2膽堿能受體抗體,尤其可能是M2受體自身抗體的參與。另一方面,近年來的研究表明,在慢性阻塞性肺疾病發病過程中,心臟主要受體的功能有明顯的變化,并發現循環血中免疫復合物增加與心功能異常有相關性。本實驗發現在COPD模型組也出現抗M2受體抗體的表達增高,并且濃度與心肌損害程度有一定相關性,同時與光鏡電鏡下觀察到COPD不同時期的心肌損害程度有一定相關性,提示在COPD疾病狀態下已經開始出現心臟病變,心肌損害因素已經產生,這對于COPD時期預防肺心病形成具有重要意義。同時本實驗也表明,COPD時期已經出現自身免疫系統的紊亂,也可能伴隨有除抗M2受體抗體外的多種自身抗體的產生異常,從一定程度上闡述COPD的發病伴隨有自身免疫功能的異常,可能為COPD的發病因素提供新的方向以及為COPD的治療和肺心病的預防提供新的途徑。

圖2 電鏡下心臟組織超微結構
中醫學認為,COPD主要病機乃“虛、痰、瘀”,病理變化為本虛標實、虛實夾雜的證候,氣虛血瘀的病理變化貫穿整個病程。急性加重期以實為主,穩定期以虛為主,病位在肺,與心、肝、脾、腎諸臟密切相關[4]。本病多屬漸積而成,秉承纏綿,經常反復發作,難期根治。若患者久病體衰,導致心氣不足,心脈上通與肺,氣血鼓動無力,就會出現血脈瘀滯。反過來瘀血會導致氣機升降失常,進一步加重病情[5]。同時肺脹是以肺氣脹滿不能收斂為主要特征,氣機升降是其重要病機[6]。心肺在生理上密切相關,功能上相互作用,病理上相互影響。心肺兩臟調節氣血運行的作用密切相關,氣血運行失常是肺脹發生的重要原因。
肺心病起病首先以肺為重,即首先出現的癥狀和特點以肺系為主,最終形成肺心病并累及至心系。中醫認為:COPD屬于肺心同病,以肺、心為中心兼及五臟。雖然肺心病的最終發展結果一定是五臟功能失調,但是五臟受損的輕重程度不同,不同臟腑在肺心病的發病中所起的作用不同,心肺是主要病位,是發病核心。本實驗進一步認證了五臟一體觀的科學性。把“見肺之病,知肺傳心,當先調心”作為治療COPD,預防肺心病發生的重要指導思想。
[1]Gershwin,M.E.riskfactorsandcomorbiditiesinprimarybiliarycirrhosis:Acontrolledinterview-basedstudyof1032patients[J].Hepatology,2005,42(5):1194-1202.
[2]宋一平,崔德健,茅培英.慢性阻塞性肺病大鼠模型的建立及藥物干預的影響[J].軍醫進修學院學報,2001,22(2):99-102.
[3]JohnWA,JoanHB.G-proteiningrowthandapoptosis:lessonsfromtheheart[J].Oncogene,2011(20):1626-1634.
[4]林琳,吳蕾,許銀姬.慢性阻塞性肺疾病五臟相關理論之病機傳變模式探討[J].江蘇中醫藥,2008,40(8):67-69.
[5]考希良,張偉.從瘀探討肺纖維化的中醫病因病機[J].吉林中醫藥,2012(10):1250-1251.
[6]張偉,孫璐璐.肺間質與筋的關系及慢性阻塞性肺疾病治療新思路[J].吉林中醫藥,2012(6):550-551.
R541.5
A
1003-5699(2013)06-0609-03
“泰山學者”建設工程專項經費資助(ts20110819)及山東省自然科學基金項目(Y2006C114)。
張 偉(1963-),男,主任醫師,教授,博士,博士研究生導師。研究方向:中醫肺病學。
*[通信作者] 姚玉強,Tel:18766400195,E-mail:254586177@qq.com。
2012-11-26)

