射頻消融聯合化療治療周圍型中晚期非小細胞肺癌療效觀察
蒲德利,廖江榮
肺癌在我國惡性腫瘤發病率及死亡率已位居第一。大多數肺癌患者確診時已失去手術根治的機會,中晚期非小細胞肺癌(NSCLC)只能采取綜合治療手段,惡性腫瘤屬于全身性疾病,包括局部治療及全身治療。射頻消融術(RFA)用于肝癌局部治療療 效 明 確[1],對 肺 癌 的 治 療 也 有 報 道[2-3]。 我 科 自2009年8月至2012年03月采用RFA聯合GP方案化療治療周圍型NSCLC 16例取得滿意效果,現將資料報道如下。
1 材料與方法
1.1 材料
1.1.1 入選病例標準 所有的病例通過纖維支氣管鏡 (纖支鏡)或經皮肺穿刺病理組織學確診為NSCLC;既往均無腫瘤治療史;KPS功能狀態評分 >60分;按UICC國際NSCLC分期標準屬于Ⅲ期或Ⅳ期者;無遠處轉移(除胸部外);不能耐受或拒絕開放手術切除的原發性肺癌;肝腎功能、凝血功能、血常規基本正常;腫瘤最大徑大于3 cm者;CEA均增高。
1.1.2 臨床資料 32例NSCLC患者,分為觀察組16例:男12例,女 4例,年齡 48~76歲,平均 61歲。 癌胚抗原(CEA)28.3~205.6 ng/ml,平均 87.5 ng/ml。其中鱗狀細胞癌5例,腺癌11例。腫瘤最大徑為3.1~10.4 cm,其中最大徑3.0~5.0 cm 5例,5.0~7.0 cm 3例,7.0~9.0 cm 6例,9 cm以上2例。對照組16例:男14例,女2例,年齡45~78歲,平均61 歲。 CEA 21.5~218.2 ng/ml,平均 91.3 ng/ml。 其中鱗狀細胞癌3例,腺癌13例。腫瘤最大徑3.2~9.8 cm,其中最大徑3.0~5.0 cm 6例,5.0~7.0 cm 5例,7.0~9.0 cm 4例,9 cm以上1例。兩組上述資料具可比性。
1.1.3 儀器與設備 射頻消融儀為RFA-Ⅰ型多極RFA,由北京博萊德光電技術開發有效公司提供,微電極展開后最大直徑2.0~4.0 cm,CT機:CT引導裝置為SIEMENS SOMATOMSensation 6螺旋CT。
1.2 方法
1.2.1 治療方法 觀察組術前給予嗎啡,采用RFA多極電極,先行CT平掃,根據圖像選取最佳穿刺部位及進針角度。常規消毒后將RFA多極電極穿刺到腫瘤部位,根據腫瘤大小打開子電極,每次消融90℃持續10~15 min,并根據病灶大小及數量決定射頻次數,退針時電凝止血。術后1周予吉西他濱聯合順鉑靜脈化療 (吉西他濱1 000 mg/m2d 1,d 8聯合順鉑30 mg/m2d 1~3),每3周為1個周期。對照組用相同方案化療,不用RFA治療。其中觀察組有4例在治療1個月后復查,腫瘤周邊有對比劑強化,CEA仍高,再次行RFA,兩組均行4個周期化療。兩組治療6個月后比較近期療效及不良反應。1.2.2 療效評價 RFA在肺癌中的應用目前尚無統一的療效判斷標準,我們將術前與術后腫瘤體積變化、瘤內有無血供、增強CT值、增強后有無強化、血清CEA作為療效判斷標準。治療后 1、2、6個月復查胸部CT平掃結合增強掃描和血清CEA。如腫瘤完全消融(腫瘤體積縮小,瘤內無血供,增強CT值小于5 HU,增強無強化)相當于腫瘤完全消失(CR);腫瘤部分消融(腫瘤體積縮小或無變化,瘤內有少許血供,增強CT值5~15 HU,增強腫瘤周邊不規則強化),相當于腫瘤部分緩解(PR);腫瘤無變化(腫瘤體積無變化,瘤內仍有血供,增強CT值大于15 HU,增強腫瘤強化)相當于腫瘤穩定(NC);腫瘤進展(腫瘤體積增大,瘤內仍有豐富血供,增強CT值大于30 HU,增強腫瘤明顯強化)相當于腫瘤進展(PD),完全緩解(CR)、部分緩解(PR)、腫瘤穩定(NC)、腫瘤進展(PD)按WHO實體瘤近期客觀療效指標判定。CEA下降說明治療有效,升高提示腫瘤復發或惡化。
1.2.3 不良反應 術中有無咳嗽、胸痛、發熱、咯血、電極致燙傷;術畢復查CT平掃有無氣胸、肺內出血、胸腔積液。術后復查CT有無肺部感染,繼發性肺膿腫。化療后觀察骨髓抑制、胃腸反應、脫發等。
1.3 統計學方法
采用SPSS13.0統計軟件。組間比較采用t檢驗,P≤0.05為差異有統計學意義。
2 結果
2.1 近期療效
兩組均在治療6個月后比較,觀察組有效率為81.3%,其中腫瘤最大徑7 cm以上有4例在RFA 1個月后復查胸部增強CT后,腫瘤周邊有強化,再次RFA術;對照組有效率為43.8%,兩組有效率(CR+PR)相比差異有統計學意義 (P<0.01),見圖1、表 1。
2.2 CT值變化
觀察組16例患者均在術前、術后即刻、術后1個月針對RFA腫瘤進行CT值測定,術前平均CT值為47.23 HU,術后立即26.67 HU,術后1個月平掃:14.12 HU,術后1個月增強22.25 HU。術前和術后即刻或術后1個月平掃測CT值差異有統計學意義(P<0.01)。術后1個月平掃和增強測CT值比較差異無統計學意義(P>0.05)。見表2。
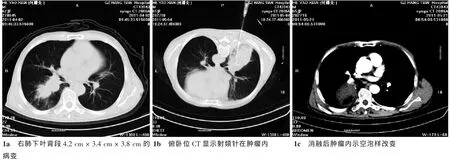
圖1 右下肺鱗癌病例RFA術前后圖像
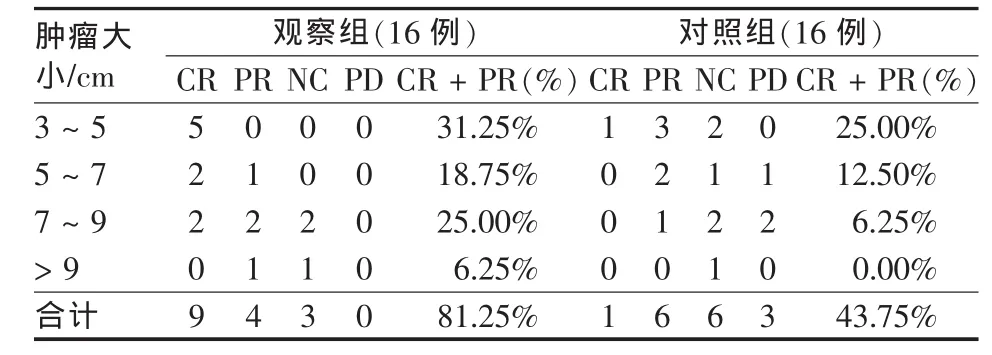
表1 觀察組和對照組近期療效比較(例)
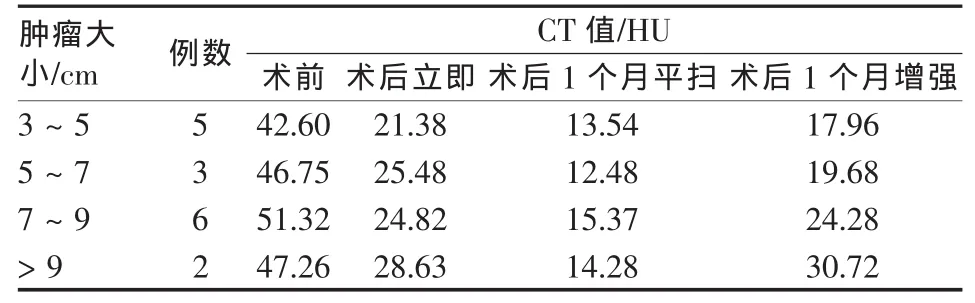
表2 CT值變化
2.3 生存期
隨訪 6、9、12、15、18、21 和 24 個月 時的 生存率,詳見圖2,觀察組中位生存期為18個月,對照組為15個月,兩組比較差異無統計學意義 (P>0.05)。
2.4 不良反應
2.4.1 觀察組 RFA術中有咳嗽2例、胸痛3例、發熱1例未予特殊處理,自行好轉;咯血2例予白眉蛇毒凝血酶1 ku肌注后無咯血;無一例電極燙傷。術畢有氣胸3例,肺壓縮20%~60%,其中2例經胸腔穿刺抽氣后肺復張,1例胸腔閉式引流2 d復查肺復張拔管,肺內出血2例予氨甲環酸靜脈滴注3 d、頭孢呋辛抗炎5 d復查吸收,術后繼發性肺膿腫1例,經抗炎處理好轉。化療后觀察組骨髓抑制5例(31.3%),胃腸反應10例(62.5%),脫發8例(50.0%)。
2.4.2 對照組 骨髓抑制6例(37.5%)、胃腸反應11例(68.8%)、脫發6例(37.5%)。兩組骨髓抑制、胃腸反應經對癥處理后恢復正常,脫發在治療完成后逐漸長出。兩組間不良反應差異無統計學意義(P>0.05)。
3 討論
中晚期NSCLC治療療效多年來一直困擾著抗癌工作者,各家嘗試多種綜合治療手段,主要局部聯合全身治療。局部治療除手術外有消融、放射性I125粒子組織間放療及局部灌注化療等,全身治療包括全身化療、分子靶向治療、免疫治療等。如何聯用均有報道,各有優缺點。
多電極高溫射頻利用射頻電流,使組織內極性分子發生高速震蕩產生摩擦,產生熱能,使局部溫度升高,當達到90℃,可有效地快速殺死局部腫瘤細胞。同時可使腫瘤周圍的血管組織凝固形成一個反應帶,有利于防止腫瘤轉移,腫瘤周圍正常肺組織可通過血液循環和呼氣散熱,腫瘤周圍正常肺組織的導電性及導熱性差,使局部熱量不易散發,積聚在消融區的邊緣,使能量可以充分集中在病變部位[4];腫瘤的實體部分壞死更加完全[5]。多電極子針同時展開構成的最大徑約4.0 cm的球形,使消融范圍最大增加到5.0 cm。因此,RFA治療肺部腫瘤是可行而有效的。
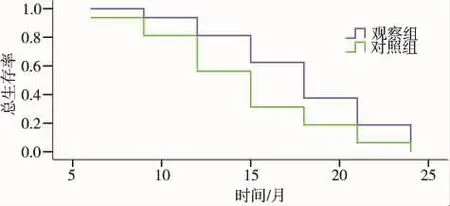
圖2 兩組生存曲線(壽命表法)
RFA治療后機體免疫功能和抗腫瘤能力可得到明顯增強[6],大量腫瘤組織凝固性壞死,減輕了腫瘤組織的免疫抑制作用;腫瘤細胞加熱后可以合成熱休克蛋白(HSP),HSP具有遞呈抗原的作用,激發特異抗腫瘤CD8+T淋巴細胞反應,兩方面共同作用使免疫功能得到一定程度的提高[8],可增加化療的敏感性[8]。高溫熱療可以使腫瘤細胞的抗原決定簇改變空間結構,從而改變其抗原性,激發機體特異性的免疫應答,殺傷同源性的腫瘤細胞。RFA可重復治療。
本研究療效判斷以術前與術后腫瘤體積變化、瘤內有無血供,術前,術后CT值變化,增強后有無強化,血清CEA作為標準。結果顯示觀察組與對照組比較,近期療效有顯著差異,且腫瘤最大徑越小,療效越好,與玄云鵬等[9]和 Rossi等[10]報道一致。 兩組生存期:觀察組中位生存期為18個月,對照組為15個月,兩組比較無顯著差異(P﹥0.05),可能與病例數較少和隨訪時間較短有關。兩組不良反應,觀察組在術中及術后咳嗽、胸痛、發熱、咯血、氣胸、肺內出血、胸腔積液、繼發性肺膿腫均較輕,經積極處理好轉。對化療不良反應:觀察組骨髓抑制5例、胃腸反應10例、脫發為8例;對照組骨髓抑制6例、胃腸反應11例、脫發6例,兩組之間不良反應無顯著差異(P>0.05)。
綜上所述,RFA聯合GP方案化療治療周圍型中晚期NSCLC,較單純化療提高療效,生存時間延長,不良反應輕,操作簡便安全。RFA聯合全身化療可作為一種治療中晚期NSCLC的有效方法,值得關注。
[1]Oshowo A,Gillams A,Harrison E,et al.Comparison of resection and radiofrequency ablation for treatment of solitary colorectal Ivermetastases[J].Br J Surg,2003,90: 1240-1243.
[2]胡 牧,支修益,劉寶東,等.CT引導三維重建經皮穿刺射頻消融治療晚期肺癌近期療效評價 [J].腫瘤研究與臨床,2010,22: 26-28.
[3]黃子林,吳沛宏,趙 明,等.經皮射頻消融治療局部晚期肺癌 78例臨床分析[J].中華醫學雜志,2008,88:2751-2754.
[4]劉寶東,支修益,劉 磊,等.CT引導下射頻消融治療中晚期非小細胞肺癌的近期療效觀察 [J].中國肺癌雜志,2009,12: 775-779.
[5]孫志超,肖湘生.射頻消融治療肺癌的現狀與進展[J].介入放射學雜志,2007,16:781-784.
[6]吳沛宏,趙 明,范衛君,等.肺部實體腫瘤射頻消融治療的近期療效觀察[J].中華放射學雜志,2002,36: 321-324.
[7]張衛強,索曉惠,林 華.高溫射頻消融對非小細胞肺癌患者免疫功能的影響 [J].中國全科醫學,2002,5:197-198,200.
[8]趙 健,吳一龍,王遠東,等.射頻消融聯合放化療治療局部晚期非小細胞肺癌[J].腫瘤防治研究,2004,31:495-497.
[9]玄云鵬,王明釗.射頻消融治療肺癌的研究進展[J].國際腫瘤學雜志,2009,36:606-609.
[10] Rossi S,Dore R,Cascina A,et al.Percutaneous computed tomography-guided radiofrequency thermal ablation of small unresectable lung tumours [J].Eur Respir J,2006,27: 556-563.

