64層螺旋CT 雙期血管成像在肺隔離癥術前評估中的應用
周靜然,楊峰,余河,熊偉
肺隔離癥是一種少見的肺內先天性發育異常疾病,手術治療是肺隔離癥的主要治療方法,手術中的重點和難點是尋找和處理異常血管[1]。64 層螺旋CT容積掃描及三維重建技術能較好地立體顯示供血動脈的起源、行程及引流靜脈,為術前評估提供了詳細的資料。本文回顧性分析本院2008年12月-2012年12月12例肺隔離癥患者的術前CT 血管造影資料,旨在評價CT 血管成像對肺隔離癥手術治療的指導價值。
材料與方法
1.臨床資料
本組12例肺隔離癥患者中男8例,女4例,年齡16~55歲,平均46歲。臨床上有反復咳嗽、咳痰、發熱、胸痛病史11例,有咯血病史4例。1 例患者無自覺癥狀,在常規健康體檢時發現。所有病例均經手術病理證實。
2.檢查方法
采用GE LightSpeed 64 層螺旋CT 機,掃描參數:管電壓120kV,管電流200mA,層厚0.625mm,重建間隔0.625mm,螺距1.375,床進速為55mm/r,標準重建模式。掃描范圍從肺尖至上腹部,先平掃,然后行增強掃描。采用高壓注射器將非離子對比劑碘海醇(350mg I/ml)經手背靜脈或肘靜脈注入,注射流率3~4ml/s,劑量1~1.5ml/kg,延遲20~25s后行動脈期掃描,延遲40~45s行靜脈期掃描。
3.圖像處理
圖像后處理采用GE 4.3 或4.5 工作站,分別將動脈期和靜脈期掃描數據進行重組,重組方法包括容積再現(VR),最大密度投影(MIP)和薄層最大密度投影(TSMIP)。
4.圖像分析
利用動脈期的圖像對主動脈、肺動脈、肺靜脈進行分析,觀察肺隔離癥的異常供血動脈的起源、粗細、走行及引流靜脈的歸屬。利用靜脈期圖像分析病灶的大小、形態、血供程度,手術術式的選擇和經過的解剖結構,所有圖像由胸心外科醫師和放射科醫師共同探討完成診斷。
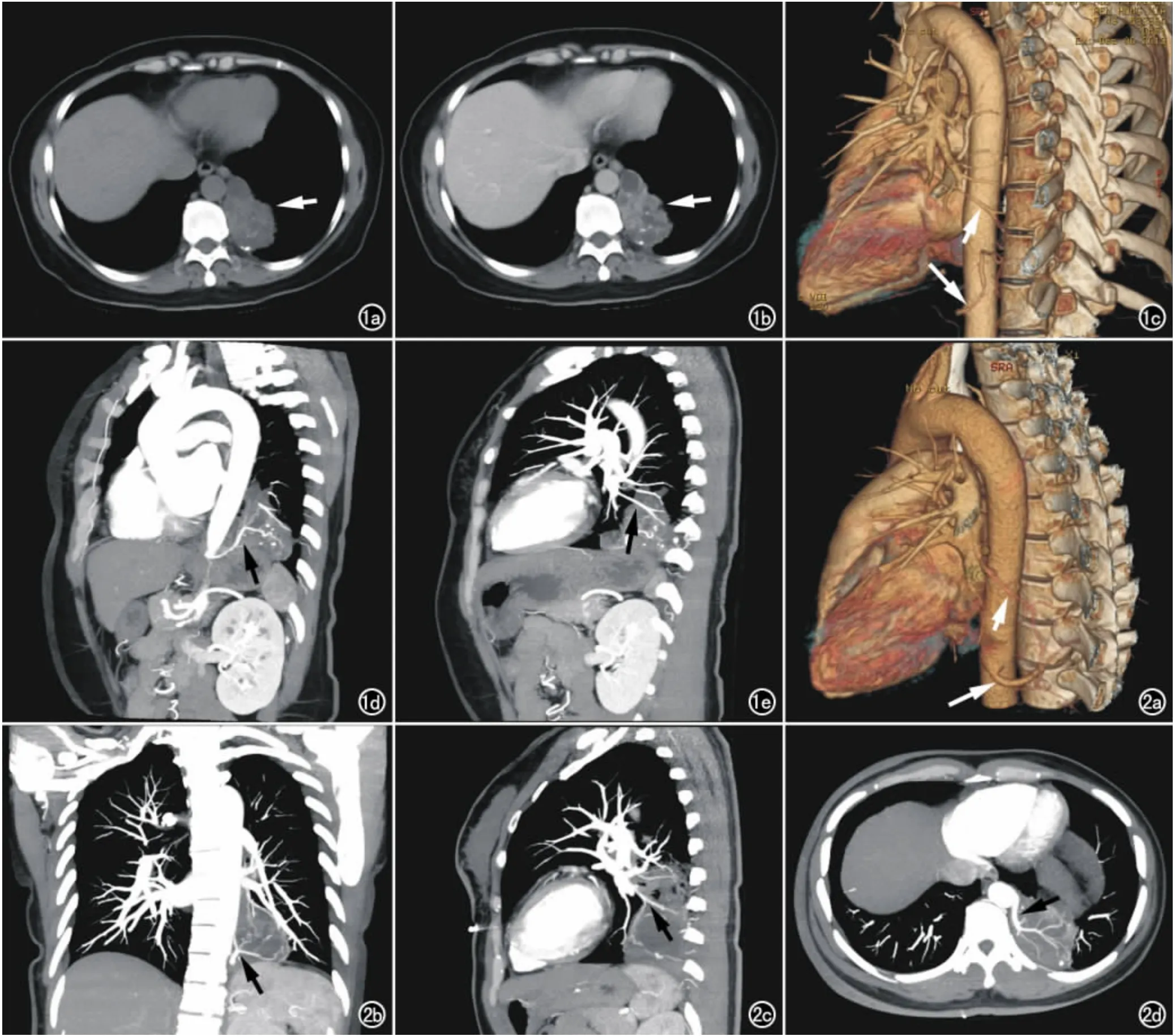
圖1 左肺下葉后基底段葉內型肺隔離癥。a)平掃示左下肺囊實性腫塊(箭);b)靜脈期增強掃描示實性部分明顯強化,囊性部分不強化(箭);c)VR 示肺隔離癥供血動脈位于胸主動脈下段(長箭),引流靜脈為下肺靜脈(短箭);d)TSMIP示供血動脈(箭)與腫塊間的關系;e)TSMIP示引流靜脈(箭)與腫塊間的關系。 圖2 左肺下葉后基底段葉內型肺隔離癥。a)VR 示肺隔離癥供血動脈位于胸主動脈下段(長箭),引流靜脈為下肺靜脈(短箭);b)TSMIP示供血動脈(箭)進入腫塊后分出多只小血管;c)TSMIP示引流靜脈(箭)與供血動脈有類似的改變;d)MIP示供血動脈位于胸主動脈下段(箭)。
結 果
12例肺隔離癥患者均為單發病灶,其中11 例為葉內型,1例為葉外型,病灶位于左肺下葉后基底段9例,右肺下葉后基底段3例。按照病灶形態、密度及強化特征分為3類:①囊性腫塊6例,均為多房性,囊內為液體成分,囊壁厚薄不等;②囊實性腫塊4例,表現為實質性成分內出現多個囊性區,囊性區為液體也可合并有氣體,無強化,實性成分厚度不等,可明顯強化(圖1a、b);③實性腫塊,呈單發軟組織腫塊2例,有明顯強化,邊緣清楚。
12例病灶均發現來自體循環的供血動脈。術前CT 血管成像顯示供血動脈的起源、數量、走形與引流靜脈與術中所見有較好的相關性,12例患者共發現12支供血動脈,手術均準確結扎;12支供血動脈分別發自胸主動脈(9支)(圖1~2)、腹主動脈上段(2支)、腹腔干(1支)(圖3),靜脈引流均為肺靜脈。1例葉外型行單純隔離肺組織切除術,11例葉內型行肺葉切除術;2支腹主動脈及1支腹腔干供血動脈采用暴露足夠血管長度再行結扎;供血動脈血管粗細不均,直徑5~26mm,與手術結果相符,其中3支供血動脈粗大,結扎血管時先將患者收縮壓降低至90mmHg后再行結扎。

圖3 右肺下葉后基底段葉外型肺隔離癥。a)VR 示供血動脈來自腹腔干(長箭),引流靜脈為肺靜脈(短箭);b)TSMIP示供血動脈(長箭)、引流靜脈(短箭)與腫塊間的關系;c)MIP示供血動脈(箭)來源于腹腔干。
CT 動脈期血管成像可以清晰顯示主動脈及其分支血管,通過多種重組方法可以重點顯示異常血管,而靜脈期圖像雖然為動靜脈重疊圖像,血管較為復雜,但通過對比雙期CT 血管圖像可以很容易識別動脈性病變或靜脈性病變,能顯示肺隔離癥的血供及引流靜脈的細節和全貌。雙期CT 血管成像能更好地評價肺隔離癥腫塊與供血動脈和引流靜脈的關系。
討 論
肺隔離癥是一種少見的先天性發育異常的肺部疾病,是一種支氣管肺前腸畸形[2]。病理基礎為病變肺組織與正常肺組織分離,包繞或不包繞胸膜,病變肺組織接受體循環動脈系統供血,通常供血動脈來自胸主動脈及腹主動脈上段。本病病因尚未完全清楚[3]。
根據隔離肺組織有無完整的胸膜與正常肺組織分界,肺隔離癥分為葉內型(intralobar sequestration,ILS)和葉外型(extralobar sequestration,ELS)兩種,本組11例為葉內型,1例為葉外型。靜脈引流的不同是鑒別葉內型與葉外型肺隔離癥的關鍵。葉內型肺隔離癥的引流靜脈通常為下肺靜脈,95%經同側肺靜脈引流至左心房,有5%的病例經半奇靜脈-奇靜脈系統引流至肋間靜脈或上腔靜脈達右心房[4]。葉外型肺隔離癥的引流靜脈通常為體靜脈,變異很大,少數可以引流入下肺靜脈。本組12例病例引流靜脈均為同側下肺靜脈。
外科手術治療是根治肺隔離癥的主要方法,術前了解病變的大小、形態、供血程度、供血動脈的位置數目走行以及靜脈的引流非常重要,可以有效地避免術中血管收縮引起的大出血。過去一般認為動脈造影是診斷肺隔離癥顯示異常血管的金標準,但是有一定創傷性,且不能同時顯示肺內病灶情況。隨著醫學影像技術的發展,CT 血管重建技術操作簡單成熟,目前已成為肺隔離癥術前診斷的最重要的無創傷性的檢查方法[5]。多層螺旋CT 具備多種重建模式和三維立體顯示功能,可以從多方位、多角度觀察、評價。多種后處理技術的結合應用,可以準確、直觀、全面顯示病變部位、范圍、程度,為臨床手術治療方案的制訂提供更豐富的影像學信息,改變了臨床醫生僅根據MRI、DSA等二維圖像選擇術式及判定腫瘤與血管的關系。本組病例采用VR、MIP、TSMIP對病灶及血管進行重組。
絕大多數ILS患者經肺靜脈回流至心臟,僅少數患者經體循環回流。ELS患者則多見奇靜脈、門靜脈回流。經肺靜脈回流患者的肺靜脈明顯較一般肺靜脈粗大(圖2b),這些解剖結構決定了ELS可以單純切除隔離肺組織,而ILS 則需要切除肺葉。本組1 例ELS單純切除隔離肺組織,11 例ILS 均行肺葉切除術。手術時探查異常血管是關鍵操作,并且要警惕部分患者存在2支或以上異常血管[6],本組病例共發現12支異常體循環供血動脈,其中1例患者有肺動脈參與循環,與手術結果相符。部分異常血管起源于腹主動脈(本組2例),在結扎時充分游離血管周圍粘連,暴露出足夠血管長度后再行結扎,否則異常動脈損傷后可能回縮入膈下,造成無法縫扎而致大量出血。對于異常血管粗大、供血豐富、年齡較大的患者(本組3例),結扎異常血管時應格外小心,應先降低患者收縮壓至90mmHg(12kPa)后再行結扎,并且關閉異常血管后要注意患者的血壓變化,對于血壓升高過多的患者可用藥物降壓。
綜上所述,64層螺旋CT 血管重建技術能很好地顯示異常血管起源、走行及形態,能幫助臨床醫生全面的了解病變供血、引流血管及與周圍結構的解剖關系,制定手術方案,避免術中損傷血管而產生大出血,具有重要的臨床應用價值。
[1] 李棟,張志泰,區頌雷,等.肺隔離癥的診治分析[J].中華胸心血管外科雜志,2012,28(3):135-137.
[2] Gezer S,Tastepe I,Sirmali M,et al.Pulmonary sequestration:a single-institutional series composed of 27cases[J].J Thoracic Cardiovasc Surg,2007,133(4):955-959.
[3] 李樹本,何建行,楊運有,等.葉內型肺隔離癥的診斷和外科治療[J].中華胸心血管外科雜志,2006,22(4):271-272.
[4] Colin R,Cooke R.Bronchopulmonary sequestration[J].Respir Care,2006,51(6):661-664.
[5] Kang M,Khandelwal N,Ojili V,et al.Multidetector CT angiography in pulmonary sequestration[J].J Comput Assist Tomogr,2006,30(6):926-932.
[6] 高樹庚,程貴余,孫克林,等.肺隔離癥23例臨床診治分析[J].中華醫學雜志,2007,87(23):1616-1617.

