用于藥物研發的細胞色素P450酶3A4體外肝細胞模型的研究進展
饒小惠,陳 鋒,潘明新,汪 艷
(南方醫科大學珠江醫院1.再生醫學研究所,2.肝膽二科,廣東廣州 510280)
藥物研發對醫療進步有著十分重要的作用。20世紀80年代以來,針對心血管、腫瘤、消化系統和疼痛等疾病的新藥研發,為疾病治療提供了更多選擇,提高了健康水平、生活質量及平均壽命[1]。藥物研發是一個昂貴而且耗時的過程,盡管隨著科技進步及投入增加,但是仍然有90%的研發新藥不能成功進入臨床。20世紀90年代以來,成功上市的新藥呈逐年下降趨勢,1996年有53種新藥通過美國FDA認證,但是到2010年僅有15種[2]。導致新藥研發失敗的原因有很多,其中一個主要原因是研發后期出現的各種藥物毒性反應和藥效作用不顯著;藥物研發過程會對候選藥物的藥代動力學、藥效學以及毒理學特征進行確認,但傳統研發體系缺乏在早期能夠準確高效分析藥物代謝作用和毒性反應的技術工具。
大部分藥物進入體內后的代謝過程主要經肝細胞完成。肝細胞含有各種參與體內外物質生物轉化的酶類。細胞色素P450酶(cytochrome P450,CYP)是一類含血色素巰基結構的單加氧酶蛋白超家族,是完成相關底物的去毒/生物活化作用的重要藥物代謝酶。其中,CYP3A亞家族在肝CYP中含量最高,約占30%,是主要的藥物代謝酶類。目前發現 CYP3A包括有 CYP3A4,CYP3A5,CYP3A7及CYP3A43等。CYP3A4在肝細胞中含量最高達40%,其他組織如小腸、腎、肺和腦組織等也有CYP3A4的低水平表達。Ghosh等[3]近期研究發現,CYP3A4不僅參與了藥物代謝,還有保護神經元細胞的作用。CYP3A4參與了50%的臨床用藥的代謝過程,藥物代謝譜非常廣泛,激素、免疫抑制劑、鈣離子通道阻滯劑、咖啡因及抗生素等。其中硝苯地平、咪達唑侖及睪酮是CYP3 A4的特異性底物,常被用于CYP3A4活性水平檢測。有些藥物,如曲格列酮和胺碘酮等,經CYP3A4代謝后能產生肝不良反應,從而影響了其在臨床的應用。一些環境致癌物質(如黃曲霉素B1)也具有CYP3A4代謝依賴性的肝細胞毒性作用。另外,CYP3A4與藥物相互作用也是密切相關的,大量臨床用藥已被證明可以誘導或抑制CYP3A4的活性,使與這些藥物合用的其他藥物的血漿濃度降低或升高,導致聯合用藥的療效減弱或增強甚至產生毒性作用。如特非那定、米貝地爾、阿司咪唑及西伐他丁,由于藥物相互作用已經退出了市場。
鑒于CYP3A4在藥物代謝過程中的重要作用,藥物研發過程需要一個能夠再現體內CYP3A4代謝作用的體外模型,用來集中評價CYP3A4對備選藥物代謝作用和水平,以及備選藥物對CYP3A4活性作用的影響。以肝藥物代謝功能為主要對象,現今用于藥物開發的體外模型有:①以亞細胞結構微粒體為作用單位的體外代謝模型。亞細胞結構模型中,人肝細胞微粒體是現今最常用的體外模型,因為其來源廣,價格低廉且使用簡單。② 以細胞為作用單位的代謝模型(簡稱,細胞模型)。超黏體(supersomes)是基因工程昆蟲細胞產生的微粒體,含有較高活性的CYP3A4;其他體外模型還有含有微粒體成分的人肝細胞S9成分等[4]。這些體外模型無法真實反映體內CYP3A4對藥物的代謝情況,也不能用于預測體內藥物代謝水平的定量分析,因此應用范圍有限。③組織器官代謝模型。組織和器官代謝模型是利用組織塊或完整器官進行體外藥物代謝測試的模型。這些模型雖然在最大程度上保證了代謝主體的完整性,這無疑有利于最大程度地再現體內代謝過程,但其來源罕有并且組織活性維持困難以及成本高,所以大多難以常規使用。
細胞是機體內最小的完整功能執行者;而細胞模型是較單純的生化模型、細胞器模型,具有更能體現機體生理活動的結構基礎和功能能力;較組織器官代謝模型,在技術應用上具有更大的可行性。以細胞為基本功能單位成分的分析模型(cell-based assay,CBA)是現代藥物研發技術中受到推崇而日益增多使用的模型工具[5]。因此,本文綜述了目前已知的CYP3A4生理功能特征、表達調控機制以及基于已知相關機制進行體外細胞模型構建的細胞種類、構建策略和方式。
1 CYP3A4的表達調控
清楚了解CYP3A4的表達調控機制,是構建理想相關細胞模型的前提和基礎理論之一。CYP3A4基因位于染色體7q21.1的P450酶基因簇。CYP3A4的生理性表達包括2個階段,分別為轉錄前調控及轉錄后調控。而轉錄前調控又可分為2個層面,一個是構成性表達,即生理狀態下的持續表達;另一個是誘導性表達,當受到配基活性分子刺激后,表達量增加。
1.1 CYP3A4的轉錄前調控
CYP3A4基因的5'開放區長35.8 kb,而只有13 kb才是肝特異性的調控區域,該區域包含了一系列的啟動子及增強子元件(圖1)。
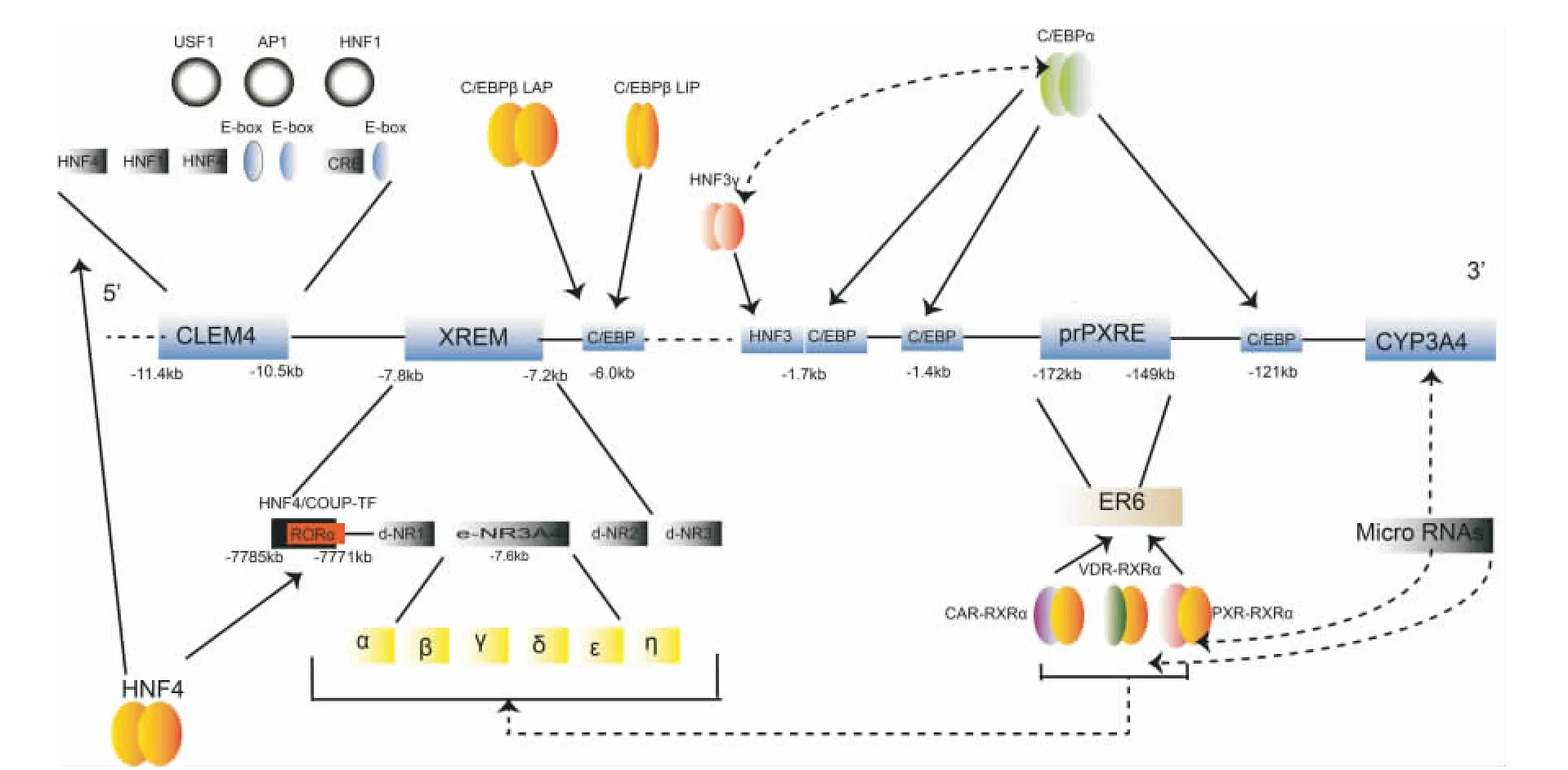
圖1 細胞色素氧化酶(CYP)3A 4細胞內調控.CLEM:構成性肝增強子模塊件;AP:激活蛋白;C/EBP:CCATT增強子結合蛋白;HNF:肝細胞核因子;USF:上游刺激因子;prPXRE:孕烷X受體反應元件;RXR:維A酸X受體;PXR:核因子X受體;XREM:外源性反應增強模塊;CAR:雄甾烷受體;VDR:維生素D受體.
1.1.1 CYP3A4 的誘導性表達
CYP3A4的啟動子位于調控序列的近端(-362/+53),近端孕烷 X受體反應元件(proximal pregnane-X-receptor response element,prPXRE)作為最小的啟動子,是一個AG(G/T)TCA反向回文序列的六聚體,相互之間被6個核苷酸間隔開。其次是位于CYP3A4轉錄起始點上游-7.8 kb/-7.2 kb的一個遠端外源性反應增強子模塊(xenobiotic-responsive enhancer module,XREM)。核因子孕烷X受體(pregnane X receptor,PXR)是調控CYP3A4轉錄的一個最重要的轉錄因子,PXR與維甲酸X受體(retinoid X receptor,RXR)α形成異源二聚體,與prPXRE及XREM等元件發生結合,介導CYP3A4的誘導表達[6]。研究指出,PXR啟動子及內含子1的單核苷酸多態性(single nucleotide polymorphisms,SNP),與 CYP3A4 表達水平的多態性相關[7]。另有發現,人肝細胞中PXR的3'端非翻譯區可以被miR-148a識別,miR-148a表達水平與PXR蛋白水平呈反向關系,生理性地影響到CYP3A4的誘導性/構成性表達水平。最近研究發現一個新的與利福平激活CYP3A4轉錄相關的調控元件eNR3A4,主要由同向重復的α及β半位點組成,相互之間被4個核苷酸隔開,位于轉錄起始點上游-7.6 kb處,是PXR激活CYP3A4轉錄必不可少的一個調控元件[8]。
1.1.2 CYP3A4 的構成性表達
肝源性細胞中CYP3A4表達水平普遍較其他組織來源細胞高,逐漸發現肝組織有高表達的一系列特異性核因子,如肝細胞核因子(hepatic nuclear factor,HNF)4α,HNF1α,FoxA2,SP-1 和 FoxA3[9]等,參與了 CYP3A4 的構成性表達。
構成性肝增強子模塊(constitutive liver enhancer module,CLEM)4 位 于 - 11.4 kb/- 10.5 kb,是 調 控CYP3A4構成性表達的一個特異性重要元件。CLEM4長900 bp,由一系列順式作用元件組成,HNF1α,HNF4α,上游刺激因子(upstream stimulatory factor 1,USF1)及 激活蛋白(activator protein,AP)1共同作用于CLEM4,協同激活該增強子的作用[10]。
在CYP3A4的5'開放區還存在有幾個CCAAT增強子結合 蛋 白 α (CCAAT enhancer-binding protein alpha,C/EBPα)的結合位點。C/EBP蛋白家族作為一類普遍存在的轉錄因子參與了組織分化、炎癥反應以及肝臟再生等多種生物學過程[11]。研究發現,C/EBPα通過與 -121,-1393及-1659 bp 3個位點結合,參與了CYP3A4的構成性表達。在肝細胞中,HNF3γ的結合位點位于-1718 bp處,并且與C/EBPα有協同作用,可以增強C/EBPα對CYP3A4的構成性表達[12]。還有研究發現,C/EBPα結合位點突變,對CYP3A4誘導性表達也會產生影響。
C/EBPβ-肝激活蛋白(liver activating protein,LAP)及C/EBPβ-肝 抑 制 蛋 白 (liver inhibitory protein,LIP)是C/EBPβ的2種不同亞型,其作用的元件是一個新的288 bp的增強子,位于-5.59 kb處。在病理狀態下(如炎癥),隨著2種亞型的比例變化,導致CYP3A4的表達水平發生變化[13]。此外,構成性雄甾烷受體(constitutive androstane receptor,CAR)及維生素 D 受體(vitamin D receptor,VDR)也是調控CYP3A4表達的重要轉錄因子,作用位點與PXR相似,提示這些轉錄因子的靶基因作用具有重疊性特點,這也正是造成CYP3A4具有廣泛的作用底物譜的基礎機制之一。
最近研究還發現,微RNA通過對CYP3A4的3’端非翻譯區的干擾,對CYP3A4蛋白的表達進行調控;微RNA不僅能直接調控CYP3A4,還能干擾VDR和PXR等轉錄因子的表達,而間接影響CYP3A4的表達[14]。
1.2 CYP3A4的轉錄后調控
CYP3A4不僅受到轉錄前的調控,還受到轉錄后的調控。在細胞漿中,CYP3A4轉錄翻譯后還會受到磷酸化修飾,主要發生在Ser478,Thr264及Ser420 3個氨基酸殘基,而且當CYP3A4磷酸化后,使其易于泛素化而被降解[15]。
2 常用的CYP3A4體外細胞模型
用于藥物代謝的CYP3A4體外細胞模型分為肝源性及非肝源性(圖2)。常用的非肝源性細胞包括:細菌,酵母菌和昆蟲細胞等。然而非肝源性細胞與肝源性細胞相比,其表達的藥物代謝酶種類單一,且缺少肝特異性因子,不能如實反映藥物在體內的代謝過程,所以在體外藥物代謝分析過程中,使用肝源性細胞模型具有明確理論優勢。常用的肝源性細胞模型主要包括原代肝細胞及肝細胞系。
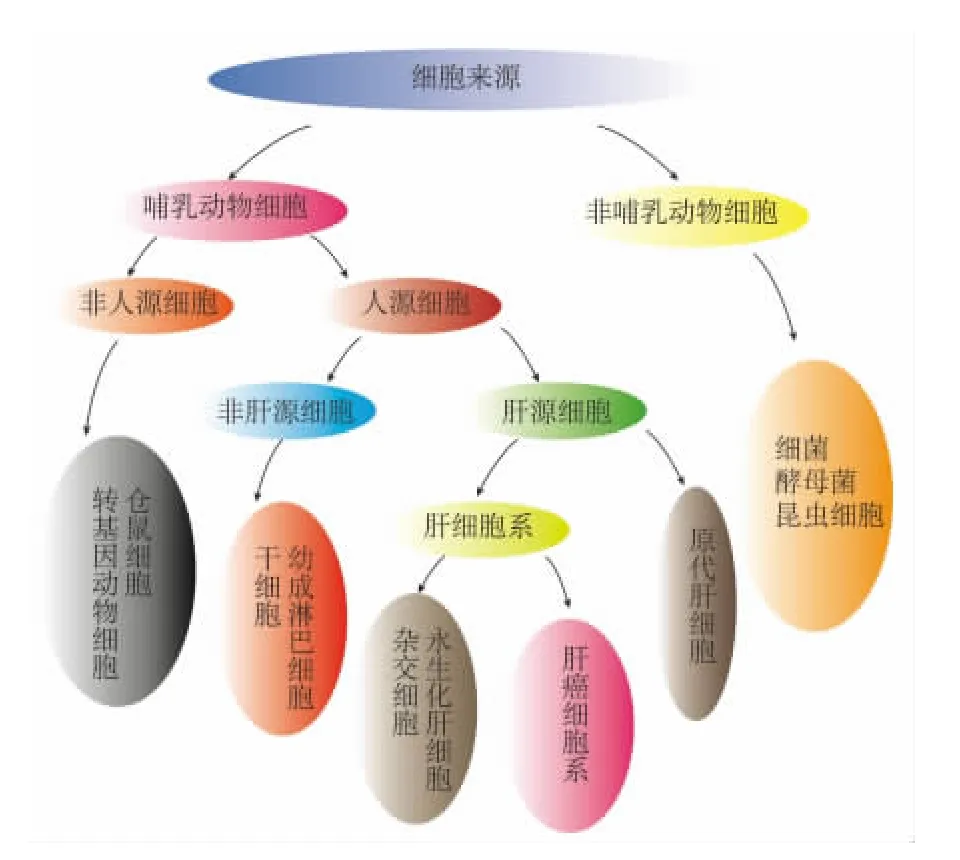
圖2 用于藥物代謝的CYP3A4體外細胞模型
2.1 原代肝細胞在藥物代謝中的應用
人原代肝細胞是最適合用于藥物代謝的CYP3A4體外細胞模型,它完整表達了Ⅰ相和Ⅱ相代謝酶以及其他參與分子,能比較準確地模擬藥物在人體內的代謝作用,是體外藥物代謝的金標準[16]。目前,人原代肝細胞常用于CYP3A4相關的藥物代謝研究,如CYP3A4的時間依賴性抑制[17]和藥物相互作用等。但是由于細胞來源短缺,人群差異性大和體外培養細胞表型維持困難等缺點,所以廣泛應用人原代肝細胞比較困難。由于人原代肝細胞來源稀缺,藥物篩選的實踐工作中還常常會用到動物來源原代肝細胞。然而動物來源肝細胞,常用如大鼠和豬原代肝細胞,與人類肝細胞的藥物代謝酶種類和代謝譜并不一致[18]。因此,目前有研究關注于尋找常用動物肝細胞與人肝細胞的藥物代謝作用的相似性關系,希望提高動物模型的預測價值。
2.2 細胞系體外模型在藥物代謝中的應用
由于原代肝細胞來源有限以及體外培養困難等缺點,細胞系體外模型具有體外增殖能力,遺傳和功能表型相對穩定,并且培養條件比較簡單而易于實驗室間統一標準,較原代肝細胞更便于用于藥物代謝CBA。細胞系可分為肝源性及非肝源性,常用于藥物代謝的非肝源性細胞系有Caco-2細胞,HeLa細胞等;Wahlang等[19]用1α,25-雙羥維生素D3 誘導的 Caco-2 單層細胞模型來研究它的膜通透性和代謝,發現CYP3A4的抑制劑伊曲康唑和P-糖蛋白的抑制劑維拉帕米可提高目標化合物通透性,為增加該藥的口服生物利用度提供了新的途徑。而肝源性細胞系的生理功能與原代肝細胞更為相似,而且保留了部分藥物代謝酶活性,所以較非肝源性細胞更常用于藥物代謝。目前相關報道中常用的肝源性細胞系如下。
①HepG2是目前最常用的永生化肝癌細胞系,分離自高分化肝細胞腫瘤,就其各種肝性表型在分子和細胞水平的特點,也是了解得比較全面的細胞系。在標準培養條件下,HepG2的CYP表達水平非常低下,如CYP3A4的mRNA及代謝活性比原代肝細胞低2~3個數量級。但經過不同方式的優化后,這些分子表達水平有所提高,使HepG2成為廣泛用于CYP3A4相關的藥物代謝實驗的最常用的體外細胞模型[20]。如 1,25-(OH)2D3,麝香保心丸及辣椒素等對CYP3A4表達的誘導作用[21-23];五味子提取物對 CYP3A4的抑制性研究[24]。
②HepaRG細胞分離自一例丙肝病毒陽性女性患者的肝癌組織,早期常用于乙肝病毒研究[25]。當接種密度低時,HepaRG細胞呈未分化的細長形態;加入二甲亞砜培養后隨著細胞生長,細胞能逐漸分化,形成典型的條索狀肝細胞樣克隆。而且,與HepG2細胞相比,HepaRG細胞能表達一系列的CYP酶,如CYP3A4,CYP2B6及CYP2C9等。因此,HepaRG細胞被認為是原代肝細胞最理想的替代者,用于CYP3A4的藥物誘導及抑制研究[26-27]。最近,有學者優化HepaRG的培養條件,用于藥物代謝及毒性研究[28]。
③BC2細胞來源于一例男性患者的肝腫瘤組織,可以在體外生長同時分化,并能在幾周內保持比較穩定的分化狀態。分化后的細胞具有很強的蛋白、糖原及尿素的合成功能,表 達 一 系 列 的 CYP酶(CYP1A1/2,CYP2A6,CYP2B6,CYP2C9,CYP2E1及CYP3A4)及Ⅱ相代謝酶。同時,BC2細胞對CYP酶誘導劑敏感,如加入地塞米松刺激后,CYP3A4表達可提高5倍[29]。之后該研究組在BC2細胞群中,以P-糖蛋白高水平表達為標準,篩選出較BC2在藥物轉運和代謝酶方面表達水平高的亞細胞株[30]。
④Huh7細胞是另一種商業化并且被廣泛應用的肝癌細胞系。Huh7細胞在體外增殖停止后,逐漸分化成熟。有學者通過基因芯片對分化成熟的細胞進行基因表達分析,發現P450酶,Ⅱ相代謝酶及相關的轉錄因子等表達明顯增高。特別是CYP3A4的代謝活性達到了原代肝細胞的30%,并且能被利福平誘導及酮康唑抑制。同時,Huh7細胞經黃曲霉素B1處理后,可產生明顯的CYP3A4依賴性細胞毒性[31]。因此,Hosomi等[32]用 Huh7 細胞研發了一個高敏感性的檢測系統,研究藥物CYP3A4依賴性的細胞毒性,有利于藥物開發早期的藥物篩選。
3 高表達CYP3A4的體外細胞模型建立及技術進展
為了獲得一個準確可靠的藥物研發體外細胞模型,隨著對肝細胞藥物代謝酶表達調控的深入了解和相關技術進步,不斷嘗試通過各種辦法建立高表達CYP3A4的體外細胞模型。
3.1 永生化原代肝細胞
原代肝細胞保留了肝完整的功能,是研究藥物代謝的金標準。然而,原代肝細胞在體外不能增殖,所以不能被廣泛推廣。學者們試圖通過讓原代肝細胞永生化,使其能在體外培養擴增。原代肝細胞永生化的方法主要是轉染編碼腫瘤病毒基因、原癌基因或端粒酶的質粒[33]。隨著研究的進展,出現了雜交細胞,條件永生化肝細胞及從轉基因動物分離的細胞系。但是,原代肝細胞永生化后,細胞表型發生改變,特別是CYP3A4表達低下,所以并不適合用于CYP3A4相關性藥物代謝研究。
3.2 CYP3A4過表達體外細胞模型
肝源性細胞系普遍存在的主要問題是處于去分化或低分化狀態,各類代謝酶表達水平低下或不全。因此,相關改造的核心目標集中在如何恢復和提高肝特征功能表型。另一種改造細胞的方法是,通過轉染編碼CYP3A4的質粒,在細胞系中過表達CYP3A4,提高細胞系在 CYP3A4相關性藥物代謝的應用潛質。各種各樣的非肝源性宿主細胞如細菌、酵母菌、昆蟲細胞和哺乳動物細胞等,已經被成功改造。1991年,文獻報道在B淋巴細胞樣干細胞中成功表達[34]。1998年,Chen等[35]已成功在中國倉鼠肺細胞中表達CYP3A4,并用于黃曲霉素B1、環磷酰胺及雜色曲霉素的代謝研究。HepG2作為應用最廣泛的肝癌細胞系,大量文獻報道在HepG2中成功過表達CYP3A4,并用于CYP3A4相關的藥物代謝及毒性研究[36-37]。
3.3 可誘導CYP3A4過表達體外細胞模型
隨著對CYP3A4表達調控研究的深入,有學者認為CYP3A4在細胞系中表達降低是由CYP3A4相關的轉錄因子及輔助因子表達減少導致的。Nibourg等[38]比較了HepG2及原代肝細胞的轉錄因子表達,發現 C/EBP α mRNA只達到原代肝細胞的15%,HNF3α是25%,HNF1α是40%。有學者通過轉染編碼特異性轉錄因子(C/EBPα,HNF3γ,PXR)的質粒 ,成功在 HepG2提高了 CYP3A4的表達。Küblbeck等[39]改造出了一種嵌合轉錄因子,即在PXR及CAR末端加入一段很強的激活域,轉染C3A細胞后增強了CYP3A4的表達,特別是利福平誘導后,CYP3A4 mRNA提高了約30倍。雖然在細胞中過表達相關轉錄因子可以增強CYP3A4的表達,但是仍然達不到原代肝細胞的表達水平。因為CYP3A4在細胞內的表達調控是一個多因子參與的復雜的調控網絡,單個或若干個轉錄因子的表達提高,并不能使CYP3A4的表達恢復到正常水平,所以還需對CYP3A4表達調控做進一步的研究。
3.4 干細胞模型研究
盡管已有大量研究著力于提高CYP3A4的表達水平,但是至今仍無法獲得理想的CYP3A4體外細胞模型,學者們開始尋求新的策略,如采用干細胞誘導分化的肝樣細胞。干細胞具有多向分化及增殖功能,大量文獻報道通過不同的方法成功誘導人胚胎干細胞分化成肝樣細胞,并對其基因蛋白及功能進行了檢測,發現肝樣細胞表現出很多肝特異性的表型[40]。人誘導多能干細胞是一種從分化成熟體細胞逆向分化而來的干細胞,可以獲取不同遺傳背景人群的人誘導多能干細胞,從而建立特異性的體外肝樣細胞模型進行肝毒性研究[41-42]。然而,干細胞誘導分化的肝樣細胞表達CYP3A4水平較低,在藥物代謝上受到一定限制,所以還有待進一步提高功能。再如,依據肝組織生理結構特點,結合生物材料和微加工技術等,構建模擬肝臟微環境的三維細胞培養體系,可以獲得包括藥物代謝酶在內的多種肝性特征表型遠高于傳統培養系統的肝細胞模型[43-45]。這些模型在藥物代謝、毒理以及病理學的基礎和應用研究方面都正在產生越來越重要的影響。
4 展望
生理性體外細胞模型在藥物研發過程中具有重要應用價值,原代肝細胞模型仍然是其中金標準。很多研究正在逐漸對肝源性和非肝源性細胞系進行改造,使其中CYP酶的表達能力更接近于原代肝細胞水平。尤其是關于CYP3A4研究比較傾向于豐富和成熟。獲得能夠準確預測CYP3A4依賴性藥物代謝的體外細胞模型是本領域的研究目標,為此,學者們嘗試了各種方法,如改良培養條件;采用基因工程的辦法在細胞系中過表達CYP3A4或相關調控因子;肝細胞永生化等。雖然不斷進步,但目前尚都不能達此目標。干細胞研究,尤其是人胚胎干細胞及人誘導多能干細胞的迅速進展為CYP3A4依賴性模型的建立提供了新思路。現在已經可以通過各種辦法使其向肝樣細胞分化,并獲得不同程度和水平的各種肝特異性的功能;但如何使各方面表型達到成熟水平,還是一個亟待解決的問題。新型生物工程學技術從構建模擬肝組織生理微環境的角度,顯著提高了體外肝細胞模型的參考價值。將以上思路互相借鑒融合,有可能獲得預測能力顯著提高的CYP3A4藥物代謝體外細胞模型。
[1]Khanna I.Drug discovery in pharmaceutical industry:productivity challenges and trends[J].Drug Discov Today,2012,17(19-20):1088-1102.
[2]Mullard A.2010 FDA drug approvals[J].Nat Rev Drug Discov,2011,10(2):82-85.
[3]Ghosh C,Marchi N,Desai NK,Puvenna V,Hossain M,Gonzalez-Martinez J,et al.Cellular localization and functional significance of CYP3A4 in the human epileptic brain[J].Epilepsia,2011,52(3):562-571.
[4]Feng Y,Mitchison TJ,Bender A,Young DW,Tallarico JA.Multiparameter phenotypic profiling:using cellular effects to characterize small-molecule compounds[J].Nat Rev Drug Discov,2009,8(7):567-578.
[5]Liddle C,Goodwin BJ,George J,Tapner M,Farrell GC.Separate and interactive regulation of cytochrome P450 3A4 by triiodothyronine,dexamethasone,and growth hormone in cultured hepatocytes[J].J Clin Endocrinol Metab,1998,83(7):2411-2416.
[6]Lamba J,Lamba V,Strom S,Venkataramanan R,Schuetz E.Novel single nucleotide polymorphisms in the promoter and intron 1 of human pregnane X receptor/NR1I2 and their association with CYP3A4 expression[J].Drug Metab Dispos,2008,36(1):169-181.
[7]Takagi S,Nakajima M,Mohri T,Yokoi T.Post-transcriptional regulation of human pregnane X receptor by micro-RNA affects the expression of cytochrome P450 3A4[J].J Biol Chem,2008,283(15):9674-9680.
[8]Toriyabe T,Nagata K,Takada T,Aratsu Y,Matsubara T,Yoshinari K,et al.Unveiling a new essential cis element for the transactivation of the CYP3A4 gene by xenobiotics[J].Mol Pharmacol,2009,75(3):677-684.
[9]Lamba V,Panetta JC,Strom S,Schuetz EG.Genetic predictors of interindividual variability in hepatic CYP3A4 expression[J].J Pharmacol Exp Ther,2010,332(3):1088-1099.
[10]Matsumura K,Saito T,Takahashi Y,Ozeki T,Kiyotani K,Fujieda M,et al.Identification of a novel polymorphic enhancer of the human CYP3A4 gene[J].Mol Pharmacol,2004,65(2):326-334.
[11]Ramji DP,Foka P.CCAAT/enhancer-binding proteins:structure,function and regulation[J].Biochem J,2002,365(Pt 3):561-575.
[12]Rodríguez-Antona C, Bort R, Jover R,Tindberg N,Ingelman-Sundberg M,Gómez-Lechón MJ,et al.Transcriptional regulation of human CYP3A4 basal expression by CCAAT enhancer-binding protein alpha and hepatocyte nuclear factor-3 gamma[J].Mol Pharmacol,2003,63(5):1180-1189.
[13]Martínez-Jiménez CP, Gómez-Lechón MJ, Castell JV,Jover R.Transcriptional regulation of the human hepatic CYP3A4:identification of a new distal enhancer region responsive to CCAAT/enhancer-binding protein beta isoforms(liver activating protein and liver inhibitory protein)[J].Mol Pharmacol,2005,67(6):2088-2101.
[14]Pan YZ,Gao W,Yu AM.MicroRNAs regulate CYP3A4 expression via direct and indirect targeting[J].Drug Metab Dispos,2009,37(10):2112-2117.
[15]Wang Y,Liao M,Hoe N,Acharya P,Deng C,Krutchinsky AN,et al.A role for protein phosphorylation in cytochrome P450 3A4 ubiquitin-dependent proteasomal degradation[J].J Biol Chem,2009,284(9):5671-5684.
[16]LeCluyse EL. Human hepatocyte culture systems for the in vitro evaluation of cytochrome P450 expression and regulation[J].Eur J Pharm Sci,2001,13(4):343-368.
[17]Li AP,Doshi U.Higher throughput human hepatocyte assays for the evaluation of time-dependent inhibition of CYP3A4[J].Drug Metab Lett,2011,5(3):183-191.
[18]Martignoni M,Groothuis GM,de Kanter R.Species differences between mouse,rat,dog,monkey and human CYP-mediated drug metabolism,inhibition and induction[J].Expert Opin Drug Metab Toxicol,2006,2(6):875-894.
[19]Wahlang B,Pawar YB,Bansal AK.Identification of permeability-related hurdles in oral delivery of curcumin using the Caco-2 cell model[J].Eur J Pharm Biopharm,2011,77(2):275-282.
[20]Yoshitomi S,Ikemoto K,Takahashi J,Miki H,Namba M,Asahi S.Establishment of the transformants expressing human cytochrome P450 subtypes in HepG2,and their applications on drug metabolism and toxicology[J].Toxicol In Vitro,2001,15(3):245-256.
[21]Li S,Miao XH.Induction of CYP3A4 by 1alpha,25-dihydroxyvitamin D3 in HepG2 cells[J].Chin J Hepatol(中華肝臟病雜志),2008,16(3):220-223.
[22]Jiang B,Cai F,Gao S,Meng L,Liang F,Dai X,et al.Induction of cytochrome P450 3A by Shexiang Baoxin Pill and its main components[J].Chem Biol Interact,2012,195(2):105-113.
[23]Han EH,Kim HG,Choi JH,Jang YJ,Lee SS,Kwon KI,et al.Capsaicin induces CYP3A4 expression via pregnane X receptor and CCAAT/enhancer-binding protein β activation[J].Mol Nutr Food Res,2012,56(5):797-809.
[24]Wan CK,Tse AK,Yu ZL,Zhu GY,Wang H,Fong DW.Inhibition of cytochrome P450 3A4 activity by schisandrol A and gomisin A isolated from Fructus Schisandrae Chinensis[J].Phytomedicine,2010,17(8-9):702-705.
[25]Gripon P, Rumin S, Urban S, Le Seyec J,Glaise D,Cannie I,et al.Infection of a human hepatoma cell line by hepatitis B virus[J].Proc Natl Acad Sci USA,2002,99(24):15655-15660.
[26]Kaneko A,Kato M,Sekiguchi N,Mitsui T,Takeda K,Aso Y.In vitro model for the prediction of clinical CYP3A4 induction using HepaRG cells[J].Xenobiotica,2009,39(11):803-810.
[27]McGinnity DF, Zhang G, Kenny JR, Hamilton GA,Otmani S,Stams KR,et al.Evaluation of multiple in vitro systems for assessment of CYP3A4 induction in drug discovery:human hepatocytes,pregnane X receptor reporter gene,and Fa2N-4 and HepaRG cells[J].Drug Metab Dispos,2009,37(6):1259-1268.
[28]Anthérieu S,Chesné C,Li R,Guguen-Guillouzo C,Guillouzo A.Optimization of the HepaRG cell model for drug metabolism and toxicity studies[J].Toxicol In Vitro,2012,26(8):1278-1285.
[29]Gómez-Lechón MJ,Donato T,Jover R,Rodriguez C,Ponsoda X,Glaise D,et al.Expression and induction of a large set of drug-metabolizing enzymes by the highly differentiated human hepatoma cell line BC2[J].Eur J Biochem,2001,268(5):1448-1459.
[30]O'Connor JE,Martínez A,Castell JV,Gómez-Lechón MJ.Multiparametric characterization by flow cytometry of flow-sorted subpopulations of a human hepatoma cell line useful for drug research[J].Cytometry A,2005,63(1):48-58.
[31]Sivertsson L,Ek M,Darnell M,Edebert I,Ingelman-Sundberg M,Neve EP.CYP3A4 catalytic activity is induced in confluent Huh7 hepatoma cells[J].Drug Metab Dispos,2010,38(6):995-1002.
[32]Hosomi H,Fukami T,Iwamura A,Nakajima M,Yokoi T.Development of a highly sensitive cytotoxicity assay system for CYP3A4-mediated metabolic activation[J].Drug Metab Dispos,2011,39(8):1388-1395.
[33]Maruyama M,Kobayashi N,Westerman KA,Sakaguchi M,Allain JE,Totsugawa T,et al.Establishment of a highly differentiated immortalized human cholangiocyte cell line with SV40T and hTERT[J].Transplantation,2004,77(3):446-451.
[34]Crespi CL,Penman BW,Steimel DT,Gelboin HV,Gonzalez FJ.The development of a human cell line stably expressing human CYP3A4:role in the metabolic activation of aflatoxin B1 and comparison to CYP1A2 and CYP2A3[J].Carcinogenesis,1991,12(2):355-359.
[35]Chen Q,Wu J,Yu Y.Establishment of transgenic cell line CHL-3A4 and its metabolic activation[J].Chin J Prev Med(中華預防醫學雜志),1998,32(5):281-284.
[36]Tolosa L, Donato MT, Pérez-Cataldo G, Castell JV, Gómez-Lechón MJ.Upgrading cytochrome P450 activity in HepG2 cells cotransfected with adenoviral vectors for drug hepatotoxicity assessment[J].Toxicol In Vitro,2012,26(8):1272-1277.
[37]Aoyama K,Yoshinari K,Kim HJ,Nagata K,Yamazoe Y.Simultaneous expression of plural forms of human cytochrome P450 at desired ratios in HepG2 cells:adenovirus-mediated tool for cytochrome P450 reconstitution[J].Drug Metab Pharmacokinet,2009,24(3):209-217.
[38]Nibourg GA, Huisman MT, van der Hoeven TV,van Gulik TM,Chamuleau RA,Hoekstra R.Stable overexpression of pregnane X receptor in HepG2 cells increases its potential for bioartificial liver application[J].Liver Transplant,2010,16(9):1075-1085.
[39]Küblbeck J,Reinisalo M,Mustonen R,Honkakoski P.Up-regulation of CYP expression in hepatoma cells stably transfected by chimeric nuclear receptors[J].Eur J Pharm Sci,2010,40(4):263-272.
[40]Brolén G,Sivertsson L,Bj?rquist P,Eriksson G,Ek M,Semb H,et al.Hepatocyte-like cells derived from human embryonic stem cells specifically via definitive endoderm and a progenitor stage[J].J Biotechnol,2010,145(3):284-294.
[41]Rashid ST,Corbineau S,Hannan N,Marciniak SJ,Miranda E,Alexander G,et al.Modeling inherited metabolic disorders of the liver using human induced pluripotent stem cells[J].J Clin Invest,2010,120(9):3127-3136.
[42]Ghodsizadeh A, Taei A, Totonchi M, Seifinejad A,Gourabi H,Pournasr B,et al.Generation of liver disease-specific induced pluripotent stem cells along with efficient differentiation to functional hepatocyte-like cells[J].Stem Cell Rev,2010,6(4):622-632.
[43]Toh YC,Lim TC,Tai D,Xiao G,van Noort D,Yu H.A microfluidic 3D hepatocyte chip for drug toxicity testing[J].Lab Chip,2009,9(14):2026-2035.
[44]Ploss A,Khetani SR,Jones CT,Syder AJ,Trehan K,Gaysinskaya VA,et al.Persistent hepatitis C virus infection in microscale primary human hepatocyte cultures[J].Proc Natl Acad Sci USA,2010,107(7):3141-3145.
[45]Wang Y,Toh YC,Li Q,Nugraha B,Zheng B,Lu TB,et al.Mechanical compaction directly modulates the dynamics of bile canaliculi formation[J].Integr Biol(CAMB),2013,5(2):390-401.

