兒童惡性腫瘤化療后相關死亡原因分析
毛彥娜,劉 煒,李彥格,宋麗麗,周建文,管玉潔
(鄭州市兒童醫院血液腫瘤科 河南鄭州 450052)
惡性腫瘤目前仍是導致兒童死亡的主要原因,最常見的兒童惡性腫瘤為白血病、淋巴瘤、神經母細胞瘤、腦瘤及軟組織腫瘤等,隨著腫瘤化療方案的不斷優化,目前5 a無事件生存率(evant free survival,EFS)已得到顯著提高,但仍有很多患兒因化療后各種并發癥死亡。為進一步降低兒童惡性腫瘤的死亡率、提高生存率,現對血液腫瘤科惡性腫瘤患兒化療后死亡原因進行分析與總結。
1 對象與方法
1.1 對象 2002年2月至2011年5月在鄭州市兒童醫院血液腫瘤科明確診斷為惡性腫瘤并住院治療的患兒共995例,化療后死亡共82例,男58例,女孩24例,年齡為8個月~12歲,中位年齡7歲,院外死亡者不納入統計。
1.2 診斷分類 所有診斷明確的病例均通過骨髓形態及細胞化學染色、骨髓免疫學分型及組織活檢病理學診斷。82例死亡病例中急性淋巴細胞白血病占38例、急性髓系白血病16例、噬血細胞綜合癥13例、神經母細胞瘤8例、非霍奇金淋巴瘤3例、橫紋肌肉瘤2例、腎母細胞瘤2例。
1.3 統計學方法 采用SPSS 13.0軟件進行統計學分析,樣本率間比較用χ2檢驗;計量資料的均數采用t檢驗。
2 結果
2.1 骨髓抑制期內合并感染死亡率居死亡原因之首 82例死亡病人中,臨床符合感染死亡病人58例(明確病原學檢查的26例),原發病相關死亡的16例(化療后復發的10例,化療后原發病未緩解或進展6例),單純化療中出血的4例,腫瘤溶解綜合征2例,應用左旋門冬酰胺酶后引起急性壞死性胰腺炎的2例。
2.2 合并癥相關死亡分析 感染相關死亡是最主要的致死原因,就感染的可能影響因素分析見表1。
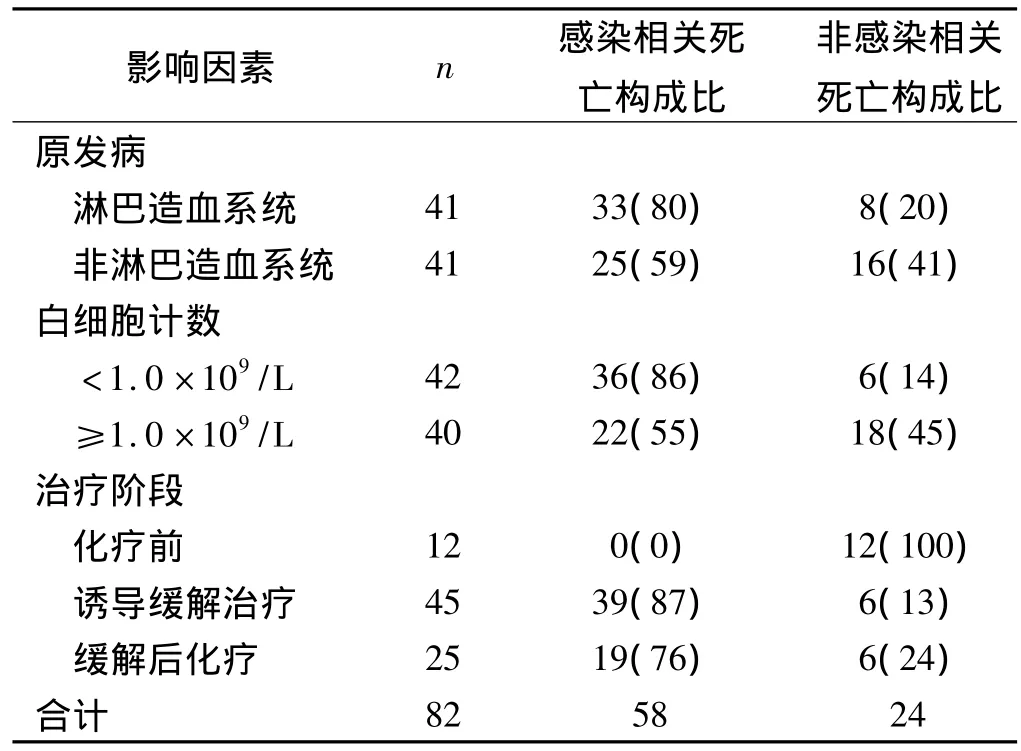
表1 不同影響因素感染相關死亡病例分析[n,(%)]
2.2.1 感染與原發病的種類:82例明確診斷的惡性腫瘤死亡患兒中根據疾病種類的不同,感染相關死亡發生率為:淋巴造血系統惡性腫瘤占80%、非淋巴造血系統惡性腫瘤占59%,差異有統計學意義(χ2=18.523,P=0.000)。
2.2.2 感染與白細胞計數:對82例死亡患兒的外周學白細胞計數進行統計分析回示,白細胞計數<1.0×109/L的42例患兒中合并感染死亡的36例(86%),白細胞≥1.0×109/L的40例患兒中合并感染死亡的22例(55%),兩組間比較差異有統計學意義(χ2=20.475,P=0.000)。
2.2.3 感染與治療階段:本組82例死亡患兒中12例死于化療前,但無感染相關死亡,誘導緩解治療階段死亡的占39例(87%),緩解后化療感染死亡相關的占19例(76%),兩組間比較有統計學意義(χ2=14.415,P=0.001)。
2.2.4 感染病原菌:58例感染相關死亡的患兒中明確病原菌的有26例,各種不同的病原菌發生感染32例次,革蘭氏陰性菌發生例次最多16例次,其中大腸埃希菌占6例次,肺炎克雷伯菌4例次,銅綠假單胞菌2例次;革蘭氏陽性球菌感染6例次,主要包括金黃色葡萄球菌3例次,糞腸球菌及草綠色鏈球菌各1例次;真菌感染10例次,曲霉菌及念珠菌各5例次。主要感染部位為肺部感染,其次為菌血癥及腸道感染。
3 討論
過去幾十年中化療經歷了由單一化療藥物治療到多藥聯合化療的演變使得惡性腫瘤的預后有了不同程度的提高,但惡性腫瘤特別是白血病及淋巴瘤化療后感染仍然是腫瘤病人治療相關死亡的主要原因[1],部分病人感染原及感染部位明確,使抗感染治療有的放矢,預后及治療費用均易于估計。但有相當大一部分病人為粒細胞低下伴發熱,感染原及感染部位不明確,依賴于經驗性治療,當經驗性治療無效時,臨床治療變得較為困難,因此預防及控制感染仍是降低治療相關性并發癥死亡的重要措施。
本組資料中顯示化療后感染的主要病原菌為革蘭氏陰性桿菌,感染部位主要為肺部與國內報道相一致[2],另外近年真菌感染呈上升趨勢,其發病率僅次于革蘭氏陰性桿菌,深部侵襲性曲霉菌在真菌感染中占首位,其臨床表現常不典型、病死率高、診斷困難[3]。
患兒化療后骨髓抑制期內嚴重的中性粒細胞減少時感染死亡發生率明顯增加[4]與本組資料中顯示白細胞計數<1.0×109/L時感染死亡率明顯高于白細胞≥1.0×109/L相一致。兒童惡性腫瘤患者化療后引起嚴重細菌感染的發生率要高于成人可能與兒童體液免疫、細胞免疫系統發育不成熟有關[5],盡管更高效的廣譜抗生素不斷的被大量應用于臨床很大程度上降低了惡性腫瘤化療后感染相關死亡率,但大量的臨床資料及文獻報道表明感染仍是威脅此類病人的主要死亡原因。根據2008年NCCN(National Comprehensive Cancer Net)指南關于惡性腫瘤化療后粒細胞減少癥一旦出現發熱感染癥狀,在病原體或感染灶未明確時,1 h內立即靜脈應用高效廣譜抗生素經驗性治療,用藥需兼顧到革蘭氏陰性菌及革蘭氏陽性菌[6]。如應用抗生素治療抗菌素5 d無效,或粒細胞計數恢復正常后仍發熱不退、C-反應蛋白持續升高時即應高度懷疑深部霉菌感染[7],應加用抗真菌藥物,2008年美國感染病協會IDSA曲霉病治療臨床實踐指南中,伏立康唑被推薦作為侵襲性曲霉菌患者的首選治療[8]。
在本研究中,不同惡性腫瘤類型其感染相關死亡率差異有統計學意義,淋巴系惡性腫瘤合并感染死亡率高于非淋巴系惡性腫瘤,造成此種原因的結果可能與淋巴系統惡性腫瘤損害淋巴細胞免疫系統從而減弱了機體對抗病原菌的功能有關。原發病相關死亡僅次于感染因素,主要包括化療后復發的10例,化療后原發病未緩解或進展4例,化療前原發病死亡的2例主要與腫瘤細胞耐藥、兩次化療間中性粒細胞減低持續時間長不能及時給與相應化療方案及高強度化療藥物有關。研究82例死亡患兒中,死亡階段主要發生于化療的早期誘導緩解期治療階段,因而誘導緩解期應密切觀察治療相關合并癥的發生,合并感染時應及時調整化療方案如降低化療藥物劑量及化療強度,在病原菌不明情況下治療兼顧革蘭氏陰性、陽性菌同時要聯合抗真菌藥物,早期、足量、足療程應用。
本組死亡82例患兒均為院內惡性腫瘤患兒,不包括治療期間因經濟原因放棄治療的院外死亡病例,因此本資料信息不能完全反應兒童惡性腫瘤化療后相關死亡的精確構成比,有待更多的病例隨訪,以便深入研究。
[1]湯靜燕,薛惠良,陳靜.兒童白血病化療后合并全身性真菌感染診斷及治療體會[J].中國小兒血液,2005,10(6):241-243.
[2]盛琦,陳同辛,張勤,等.治療相關性白血病患兒死亡原因分析[J].臨床兒科雜志,2005,(8):542-543.
[3]Wang A,Fan S,Yang Y,et al.Nosocemial infections among pediatric hematology patients:results of a retrospective incidence study at a Pediatrc hospital in China[J].J pediatr Hematol oncol,2008,(30):674-678.
[4]Athale U H,Chan A K.Hemorrhagic complications in pediatric hematologic malignancies[J].Semin Thromb Hemost,2009,(33):408-415.
[5]Ridola V,Chachaty E,Raimondo G,et al.Candida infections in children treated with conventional chemotherapy for solid tumor(Transplant recipisnts excluded):the institute gustave roussy pediatric department experience[J].Pediatric Blood Cancer,2008,42(4):332.
[6]Hughes W T,Armstrong D,Bodey G P,et al.2002 guidelines for the use of antimicrobial agents in neutropenic patients with cancer[J].Clin Infect Dis,2002,(34):730-751.
[7]Crassard N,Hadden H,Piens M A,et al.Invasive aspergillosis in a Paediatric haematology department:a 15-year review[J].Mycoses,2008,(51):109-116.
[8]Paul M,Yahav D,Fraser A,et al.Empirical antibiotic monotherapy for febrile neutropenia:systematic review and metu-analysis of randomized controlled trials[J].J Antimicrob Chemother,2006,(57):176-189.

