燃燒法快速合成CuO/Cu2O及其光催化研究
李秀萍,趙榮祥,高肖漢
(遼寧石油化工大學 化學化工與環境學部,遼寧 撫順 113001)
Cu2O是一種典型的金屬缺位p型半導體,是少有的能被可見光激發的半導體材料,其禁帶寬度約為2.0 eV.Cu2O無毒,制備成本低,可以直接利用太陽光將有機物降解,不產生二次污染物,理論利用效率較高,是一種極具開發前景的綠色環保催化劑之一.研究表明,目前銅的氧化物制備方法有浸漬法[1,2]、沉積法[3,4]和蒸發[5]等.有大量文獻報道了氧化亞銅制備方法[6~9],也有文獻報道通過負載和浸漬方法使銅的氧化物與其他載體進行復合作為催化劑[10~15],但 Cu2O/CuO復合氧化物催化劑還未見報道.實驗采用抗壞血酸一種新型燃燒劑和還原劑,硝酸銅為氧化劑,低溫燃燒法制備銅的氧化物和復合物,在加熱過程中發生強烈的氧化還原反應,燃燒產生熱量,可自我維持燃燒.這種方法合成路線簡單、容易實現、合成時間短、無需煅燒和洗滌,即可制備出銅的不同氧化物.
1 實驗部分
1.1 實驗儀器及藥品
1.1.1 實驗儀器
紫外分光光度計(721型,天津精密儀器四廠),電磁攪拌器(D2004W,上海梅穎浦儀器儀表制造有限公司),可見燈(LZG2300-1000,飛利浦牌),XRD衍射儀(D/max-RB-12Kw轉耙X射線衍射儀,日本理學),掃描電子顯微鏡(LEO型,德國LED公司),紫外掃描分光光度計(UV1100,上海天美科學儀器公司).
1.1.2 實驗藥品
Cu(NO3)2·3H2O(沈陽市試劑二廠),抗壞血酸C6H8O6(沈陽市試劑五廠),雙氧水(沈陽化學試劑二廠),鹽酸(濟南市萬隆化工有限公司),氫氧化鈉(沈陽銘邦偉業化工有限公司),甲基藍(天津金鉑蘭精細化工有限公司).
1.2 銅的氧化物制備
按照銅與抗壞血酸的摩爾比稱取硝酸銅和抗壞血酸于燒杯中,加水溶解,溶液由藍色變為淺黃色繼而又變為黃綠色同時生成氣泡,在電熱套上加熱,溶液變為深綠色.深綠色溶液中有紅棕色的沉淀,待水分即將蒸發完畢,溶液變成黑色溶膠同時發泡,繼續加熱溶液發生燃燒伴有藍色火焰和火星,最后得到黑色粉末狀銅的氧化物.
1.3 銅的氧化物制備機理
根據實驗現象可知反應過程為硝酸銅中二價銅離子被抗壞血酸還原為一價銅離子,一價銅離子部分被水中溶解的氧氧化為二價銅離子,二價銅的藍色和一價銅的黃色混合為黃綠色,慢慢一價銅被氧化成二價銅的越來越多,溶液由黃綠色轉變為深綠色.一價銅不穩定生成氧化亞銅紅棕色沉淀,二價銅與剩余的抗壞血酸燃燒生成氧化銅,所以最后生成的氧化亞銅和氧化銅的復合物.剩余抗壞血酸的量決定銅的氧化物為氧化亞銅還是氧化銅.抗壞血酸的量少,被其還原的一價銅離子被水中氧全部氧化成二價銅離子,生成氧化銅;抗壞血酸的量增加被還原的銅一部分被水中的氧氧化成二價銅離子,生成氧化銅和氧化亞銅的復合物,若抗壞血酸足夠,銅離子只有一價銅的形式,一價銅離子與抗壞血酸燃燒生成氧化亞銅.

1.4 銅的氧化物光催化實驗
稱取一定質量上述制備的銅的氧化物于燒杯中,用量筒量取甲基藍溶液100 mL置于燒杯中.將配制好的溶液放在磁攪拌器上攪拌30 min,在可見光照射一定時間后,用離心機分離,測量吸光值,根據公式(4)計算甲基藍的降解率.

式中:C0和Ct分別為甲基藍溶液的初始濃度和t時刻的濃度;

式中:A0與C0成正比;A0為濃度為C0的甲基藍溶液的紫外吸光度;

式中:At與Ct成正比;At為濃度為Ct的甲基藍溶液的紫外吸光度;
將方程式(2)、(3)代入方程式(1)經整理有方程式(4):

由方程(4)可知,降解率隨著吸光值A的減小而增大,吸光值A越小降解率越高,所以本實驗條件考察時就看條件發生改變時吸光值A如何變化,如果條件發生改變,吸光值A增大代表降解率降低,吸光值A減小代表降解率增大.實驗條件考察時就是找最小的吸光值為最佳降解效果.本實驗研究光照時間、催化劑用量、pH、H2O2使用對光催化效果的影響.
2 結果與討論
2.1 銅的氧化物XRD 表征

圖1 燃燒劑用量對復合物考察Fig.1 Effect of fuel agent on the composites*—氧化銅;Δ—氧化亞銅
圖1為燃燒劑(抗壞血酸)用量考察,由圖1可知銅與抗壞血酸的摩爾比在0.25、0.5時,其XRD圖峰數較少,產物為氧化銅.摩爾比在1以上出現2θ角為42.4(°)新的峰值,1∶2以上出現2θ 為29.6(°),65.8(°)新的衍射峰,根據文獻[1]的查閱與(JCPDS No.05-0667)可知新出現的峰屬于立方晶系的氧化亞銅,隨著燃燒劑用量的增大氧化亞銅的(111)、(200)、(220)晶面的峰增高.說明通過改變燃燒劑的用量可制備出不同含量的氧化亞銅和氧化銅的復合物.在燃燒劑與硝酸銅摩爾比為0.5∶1和0.25∶1時制備的是氧化銅,1∶1以上為氧化銅和氧化亞銅的復合物.這是由于燃燒劑抗壞血酸又是還原劑,當增加抗壞血酸的量,二價的銅被還原為一價的銅,所以產物為氧化亞銅和氧化銅的復合物.當抗壞血酸的量足夠,可制備出氧化亞銅單體.
2.2 銅的氧化物的掃描電鏡表征
由圖2a可以看出當硝酸銅與抗壞血酸之比為1∶5時所生成氧化銅和氧化亞銅的復合物,其形貌為小的顆粒狀,顆粒相互連接構成網狀結構,顆粒比較分散.圖2b硝酸銅與燃燒劑之比為1∶0.25時生成的是氧化銅,是粒徑較大的塊狀結構.說明改變燃燒劑用量能制備出形貌不同、銅的不同氧化物.圖2c是粒徑較大的塊狀的氧化銅和氧化亞銅復合氧化物.圖2d為粒徑較小的氧化亞銅顆粒.

圖2 Cu2O/CuO復合氧化物的掃描電鏡Fig.2 SEM images of Cu2O/CuO Composites Oxide
2.3 銅的光催化研究
2.3.1 不同催化劑的考察
選擇硝酸銅與抗壞血酸的摩爾比為1∶0.25,1∶1,1∶5,1∶10 四種催化劑按照實驗方法 1.4 進行光催化實驗,其結果見圖3.由圖3可以看出硝酸銅與抗壞血酸摩爾比為1∶10的樣品光催化效果最佳,這可能是由實驗選擇的可見光造成的,而硝酸銅與抗壞血酸摩爾比為1∶10的樣品為氧化亞銅,且此樣品的氧化亞銅的(111)峰最強,有文獻[16]報道氧化亞銅的(111)晶面是可見光催化效果最好的晶面.半導體基異質結界面和缺陷,可以促進光生電子和空穴,這些電子和空穴可有效提高光的催化反應.硝酸銅與抗壞血酸摩爾比為1∶5的樣品為氧化亞銅和氧化銅的復合物.硝酸銅與抗壞血酸摩爾比為1∶0.25時為氧化銅,幾乎沒有光催化效果,本實驗考慮到催化劑的分離、回收以及重復使用情況,選擇硝酸銅與抗壞血酸摩爾比為1∶5的樣品為氧化亞銅和氧化銅的復合物為光催化劑.

圖3 不同催化劑對光催化效果的影響Fig.3 Effects of catalysts on the photo-catalysis
2.3.2 催化劑用量考察
圖4是催化劑用量(即在100 mL甲基藍溶液中加入催化劑的質量,mg)對光催化影響,由圖可知,60 mg/100 mL甲基藍溶液時,光催化80 min溶液的降解率最高,繼續多加催化劑,催化效果不但沒有改善,反而由于催化劑的量太大自身的顏色影響催化效果.

圖4 催化劑用量對光催化影響Fig.4 Effects of amount of catalyst on the photo-catalysis
2.3.3 雙氧水用量考察
圖5雙氧水用量對光催化性能的影響,由圖5可以看出,加入光催化劑的質量均為60 mg的情況下,光催化100 mL甲基藍溶液,加入雙氧水和沒加入雙氧水的催化效果沒有太大改變,說明雙氧水對本實驗的光催化沒有起到促進作用.這可能是由于Cu+→Cu2+可以使催化劑具有儲存和釋放氧的能力,無需雙氧水的促進作用.所以本實驗不用加入雙氧水來促進光催化的進行.

圖5 雙氧水用量對光催化性能的影響Fig.5 Effect of the amount of H2O2 on the photo-catalysis
2.3.4 pH值的影響
催化劑用量為60 mg加入到100 mL甲基藍溶液中,加入鹽酸或氫氧化鈉改變溶液的pH,在不同的pH值下測定溶液的吸光度,計算溶液的降解率如圖6所示.由圖6可以看出,當溶液的pH為7時,在120 min時溶液的降解率最高,溶液本身即為中性,所以本實驗不用另加鹽酸或者氫氧化鈉改變溶液的酸堿度.
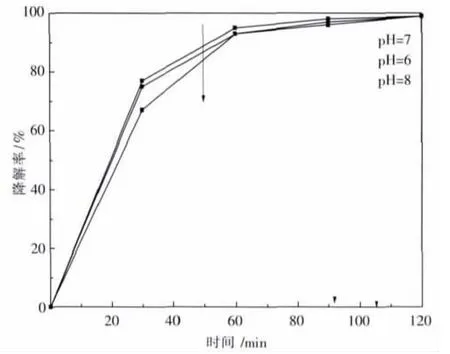
圖6 pH值對光催化性能的影響Fig.6 Effect of pH value on the photo-catalysis
2.3.5 時間考察
按上述所得,在100 mL甲基藍溶液中只加入60 mg的光催化劑,在不同的時間段用紫外掃描分光光度計進行掃描,其結果見圖7,由圖可知,氧化銅與氧化亞銅復合氧化物催化甲基藍完全褪色的時間為90 min.

圖7 時間對光催化的影響Fig.7 Effect of time on the photo-catalysis
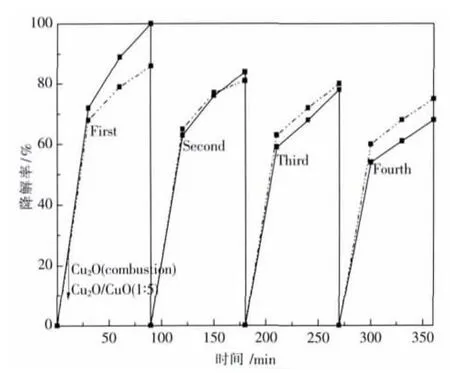
圖8 催化劑重復使用對光催化影響Fig.8 Effects of catalyst recycling times on the photo-catalysis
2.3.6 催化劑重復使用
在100 mL甲基藍溶液中只加入60 mg的氧化亞銅或氧化銅和氧化亞銅復合氧化物為催化劑,進行催化劑重復使用考察,由圖8可見氧化亞銅的光催化效果隨著催化劑重復使用次數的增加,催化效果逐漸下降,而以氧化銅與氧化亞銅為催化劑的光催化效果稍有改變,且以氧化銅與氧化亞銅為催化劑回收效果好,幾乎沒有損失.而氧化亞銅粉末顆粒過于細小難于回收,這也是氧化亞銅光催化效果急劇降低的主要原因.
3 結論
(1)抗壞血酸既為燃燒劑又為還原劑,改變其用量可制備出銅的不同氧化物:氧化銅,氧化銅與氧化亞銅的復合物、氧化亞銅.
(2)不同的氧化物對光催化效果不同,氧化亞銅在可見光下催化效果較好.但氧化亞銅難于回收重復使用,氧化銅與氧化亞銅復合氧化物單次光催化效果不如氧化亞銅,兩次以后光催化效果好于氧化亞銅.所以從回收和環保效果看氧化銅與氧化亞銅復合氧化物效果更好,氧化銅與氧化亞銅復合氧化物90 min可使溶液褪為無色,光催化完畢.
(3)以氧化銅和氧化亞銅為催化劑進行光催化無需加入任何試劑,只需加入催化劑即可,更加環保,無二次污染,且催化劑可回收、多次重復使用.
[1] Zhou Bo,Liu Zhiguo,Wang Hongxia.Visible photocatalytic activity of flowerlike Cu2O/Cu nanocomposites[J].Chmical Journal of Chinese Universities,2010,31(1):141 -144.
[2] Ren Linlin,Zeng Yuping,Jiang Dongliang.Preparation,characterization and photocatalytic activities of Ag-deposited porous TiO2sheets[J].Catalysis Communications,2009,10(5):645-649.
[3]Li F B,Li X Z.Photocatalytic properties of gold/gold ionmodified titanium dioxide for wastewater treatment[J].Appl Catal A:Gen,2002,228(1-2):15-27.
[4] Li Dongme, Xia Xi. Preparation ofnano phaseCuO composite powder and its electro - chemical behavior[J].Journal of Inorganie Materials,2001,16(11):1208 -1210.
[5]Arabatzis I M ,Stergiopoulos T ,Andreeva,et al D.Characterization and photocatalytic activity of Au/TiO2thin films for azo - dye degradation [J].Journal of Catalysis,2003,220(15):127-135.
[6]梅光軍,師偉,解科峰,等.納米氧化亞銅的制備及其光催化性能研究[J].資源環境與工程,2007,21(3):335-338.
(Mei Guangjun,Shi Wei,Xie Kefeng,et al.Preparation and performance of photocatalytic degradation of nano-sized cuprous oxide[J].Resources Environment& Engineering,2007,21(3):335 -338.)
[7]朱紅飛,陳乾旺,牛和林.在酸性條件下合成氧化亞銅納米立方體[J].無機化學學報,2004,20(10):1172-1176.
(Zhu Hongfei,Chen Qianwang,Niu Helin.Growth of cuprite nanocubes under acidic conditions[J].Chinese Journal of Inorganic Chemistry,2004,20(10):1172 -1176.)
[8]陳善亮,朱耿臣,應鵬展.納米氧化亞銅電化學法制備及光催化研究進展[J].環境化學,2011,30(5):976-981.
(Chen Shanliang, Zhu Gengchen, Ying Pengzhan.Development of electrochemical preparation and photocatalytic chacterization of nano -Cu2O[J].Environmental Chemistry,2011,30(5):976 -981.)
[9]宋繼梅,張小霞,焦劍.立方狀和球狀氧化亞銅的制備及其光催化性質[J].應用化學,2010,27(11):1328-1332.
(SongJimei, ZhangXiaoxia, Jiao Jian. Synthesis and photocatalytic properties of Cu2O microcubes and nanospheres[J].Chinese Journal of Applied Chemistry,2010,27(11):1328 -1332.)
[10]趙江紅,劉振宇.載體炭對CuO/AC(F)催化-吸附劑干法催化氧化苯酚的影響[J].新型碳材料,2005,20(2):115-120.
(Zhao Jianghong,Liu Zhenyu.Effect of carbon upporton CuO/AC(F)catalyst-sorbentsused for catalytic dryoxidation of phenol[J].New Carbon Materials,2005,20(2):115-120.)
[11]王哲,趙曦,萬海勤.焙燒溫度對CuO在γ-Al2O3載體上的分散和催化CO完全氧化性能的影響[J].無機材料學報,2008,23(3):454-458.
(Wang Zhe,Zhao Xi,Wan Haiqin,et al.Influence of calcination temperature on the dispersion behavior and CO oxidation properties of CuO/γ - Al2O3catalyst[J].Chinese Journal of Inorganic Chemistry,2008,23(3):454 -458.)
[12]周曉龍,曹建春,陳敬超.Ag/CuO復合材料反應合成熱力學分析[J].稀有金屬材料與工程,2009,38(12):2111-2115.
(Zhou Xiaolong, CaoJianchun, Chen Jingchao, et al.Thermodynamics analysis for Ag/CuO composites by reactive synthesis[J].Rare Metal Materials and Engineering,2009,38(12):2111 -2115.)
[13]鄧凡政,祝愛俠,楊睿.CuO/Cu2(OH)3Cl的制備及其光催化降解染料光譜性能研究[J].光譜學與光譜分析,2006,26(2):299-301.
(Deng Fanzheng,Zhu Aixia,Yang Ru.Study on preparation of CuO/Cu2(OH)3Cl powder and its spectrum behavior for photo- degradation decoloration of dyes[J].Spectroscopy and Spectral Analysis,2006,26(2):299 -301.)
[14]衡秋麗,肖峰,駱建敏.納米CuO:不同形貌的制備及對高氯酸銨熱分解催化性能[J].無機化學學報 ,2005,29(2):359-363.
(Heng Qiuli,Xiao Feng,Luo Jianmin. Nano - CuO:Preparation with different morphologies and catalytic performance for thermal decomposition of ammonium perchlorate [J].Chinese Journal of Inorganic Chemistry,2005,29(2):359 -363.)
[15] Zhu L Y,Chen Y,Sun Y,et al.Phase - manipulable synthesis of Cu-based nanomaterials using ionic liquid 1-butyl-3 - methyl- imidazole tetrafluoroborate[J].Cryst Res Technol,2010,4(45):398 -404.
[16]周波,劉志國,王紅霞,等.花狀Cu2O/Cu復合材料的光催化性能[J].高等學校化學學報,2010,31(1):141-144.
(Zhou Bo, Liu Zhiguo, Wang Hongxia, et al. Visible photocatalytic activity offlowerlike Cu2O/Cu nano -composites[J].Chemical Journal of Chinese Universities,2010,31(1):141-144.)

