甲烷合成工藝和催化劑探討
(惠生工程(中國)有限公司,天津 300090)
天然氣是我國的三大石化能源之一。相比以煤炭為原料生產合成油、醇醚及經由甲醇生產聚烯烴等其它煤化工產品,煤制天然氣的工藝裝置較少,廢熱能夠循環利用,單位熱值投資成本低,能夠有效減少建設投資,降低投資風險。因此煤制天然氣是煤化工產業值得關注和有望較快發展的技術路線,具有廣闊的市場前景[1]。
1 甲烷合成工藝
煤制天然氣中合成氣制備的工藝流程與目前已經非常成熟的煤制合成氨、合成甲醇的流程基本一致。但是甲烷合成反應熱非常高,大約在合成氣熱值的20%左右,合成氣中每轉化1%的CO,絕熱升溫60~70℃。因此解決絕熱溫升和設計合理的甲烷合成回路成為了煤制天然氣成功的關鍵。
煤制天然氣中甲烷合成分為直接和間接甲烷合成兩類。
1.1 直接甲烷合成
煤的直接甲烷合成是煤在一定的溫度和壓力下,在一個反應器中用煤直接制產品富甲烷氣的工藝。其特點是沒有明顯的煤氣化和甲烷合成兩個過程。
主要過程是首先將原料煤破碎為一定顆粒大小,然后利用循環載氣流將其加入到氣化反應器中,在溫度為400℃~900℃,壓力為14MPa時,利用炭—堿金屬催化劑在CO或CO2和H2混合的情況下,生成含有CO和H2以及少量甲烷的氣體。該方法一步生成甲烷但是產品氣中甲烷含量較低,僅有24.76%[2,3]。
1.2 間接甲烷合成
間接甲烷合成,也稱兩步法煤甲烷合成工藝。根據催化劑的耐硫特性,又分為間接非耐硫工藝和間接耐硫工藝兩種。
1.2.1 間接非耐硫甲烷合成
1.2.1.1 原理
煤制天然氣間接非耐硫甲烷合成過程如圖1所示。
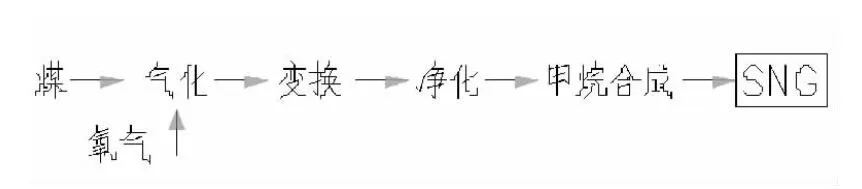
圖1 煤制天然氣間接非耐硫甲烷合成全流程示意圖
甲烷合成主要的反應如下:
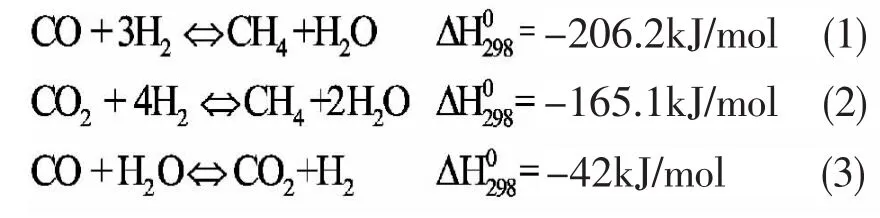
由上式可推知反應氣進料的模數要求為:

1.2.1.2 氫碳比對反應產物CH4含量的影響
由表1可知,隨著H2/CO減小,反應產物中的CH4含量先增加后變小,在H2/CO為3.00和2.99左右時達到最大。隨著H2/CO的減小,反應產物中H2含量逐漸減小,CO含量逐漸增大,兩者的變化規律是相反的。由此規律可知,若煤制天然氣的最終產品為LNG時,為了獲得較高含量的CH4和液化時處理惰性組分氫H2更容易,H2/CO應在3左右為宜。

表1 H2/CO比對CH4含量的影響
1.2.1.3 工藝介紹
對于煤制天然氣來說,合成氣中CO含量高,反應速度快,放熱量大。因此單純的單級絕熱升溫的做法是不可行的。為了讓反應平穩地進行,可以采用1)稀釋法:用甲烷合成反應后的循環氣來稀釋合成原料氣;2)冷激法:在反應器催化床層之間,不斷加入低溫的新鮮氣;3)外冷列管法:外冷列管式反應器就是將催化劑裝在列管內,管外為冷卻水。這三種降低溫升的方法優缺點見表2。

表2 甲烷合成反應器降低溫升方法比較
近年來德國 Lurgi、英國 DAVY、和丹麥TOPSOE的甲烷合成技術取得了較大進展[4]。由于甲烷合成反應強度較大,為了獲得高的甲烷含量上述三家公司的甲烷合成技術都采用多個絕熱固定床反應器串聯的甲烷合成工藝。即將甲烷合成反應分成幾段來進行,并分段回收反應熱。其中前兩個主甲烷合成爐采用串并聯結合的形式。主甲烷合成爐的溫度采用循環氣稀釋的方法控制,兩個主甲烷合成爐出口都設有高壓廢熱鍋爐,通過副產高壓蒸氣并過熱回收高品位熱量,后兩個反應爐溫度屬于中溫,進行補充甲烷合成反應,設有脫鹽水加熱器和低壓廢熱鍋爐,回收低品位的熱量。
1.2.2 間接耐硫甲烷合成
美國煤氣研究院于1978年開發了耐硫甲烷合成工藝,使用了硫化鉬催化劑,在常壓至6.8MPa,240~649℃的操作條件下 H2/CO比可從3變化到0.4,硫含量可達1%。該工藝集耐硫、變換與甲烷合成于一身,可減少裝置投資,節省操作、維修和燃料費用。
2 甲烷合成催化劑
甲烷合成技術中,催化劑是技術中的關鍵。甲烷合成催化劑按甲烷合成的方式分為直接甲烷合成催化劑和間接甲烷合成催化劑兩種。
2.1 直接甲烷合成催化劑
煤直接甲烷合成所用催化劑為堿金屬催化劑,有效順序為Ce>K>Na>Li。該催化劑是利用含水的堿金屬鹽或堿金屬氫氧化物水溶液與含碳的固體化合物混合浸漬干燥形成的。該催化劑有利于甲烷合成反應,可促進水煤氣變換反應,而且還具有耐硫不易高溫燒結和降解的特點[5]。
2.2 間接甲烷合成催化劑
2.2.1 間接非耐硫甲烷合成催化劑
2.2.1.1 間接非耐硫催化劑比較
對于CO、CO2加氫甲烷合成反應,具有高催化活性的活性組分是 Ru,Ni,Fe,Co 等。Fe基催化劑活性低,需在高溫高壓下操作,并易因積碳而失活。Co基催化劑反應選擇性較差。Ru基催化劑比的活性高,但Ru作為貴金屬,價格昂貴,且Ru(CO)x絡合物易升華造成活性組分流失。因此,近年來Ni基催化劑成為CO甲烷合成催化劑的發展方向[6]。
目前Lurgi公司、英國DAVY公司和丹麥TOPSOE的甲烷合成工藝都采用的傳統的非耐硫Ni基催化劑,CO轉化率≥98%以上,催化劑的選擇性好,幾乎沒有副反應(見表3)。
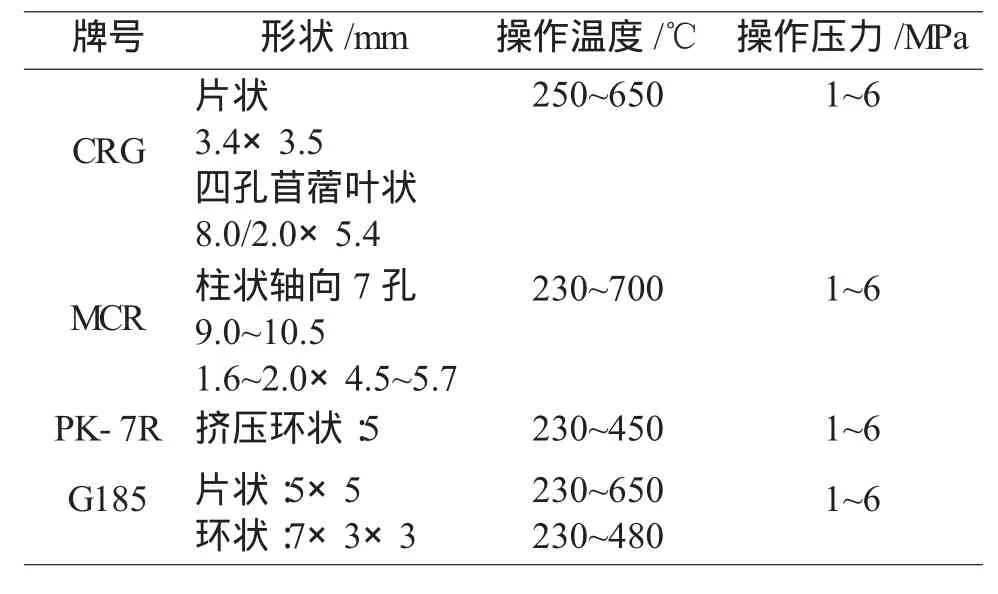
表3 幾種間接非耐硫甲烷合成催化劑對比
2.2.1.2 間接非耐硫催化劑失活原因
由圖2主甲烷合成反應床層溫度分示意圖可知,在Ni基催化劑作用下,甲烷合成反應速度非常快,在反應爐頂部附近就達到了熱點溫度。因此甲烷合成爐催化劑的裝填量不是由反應時間決定的,而是由下面三個因素造成的[4]。
①鎳燒結:對于鎳燒結比較公認的說法是積碳燒結。式(5)和式(6)為析碳反應,當溫度較低時,析碳主要反應為式(5),當反應溫度較高時,析碳的主要反應為式(6)。圖3是燒結對床層熱點溫度的影響示意圖,由圖可知隨著催化劑燒結時間的增加,甲烷合成爐熱點溫度不斷下移。②催化劑中毒:砷、鹵化氫、硫是還原態Ni基催化劑的毒物,易產生催化劑中毒失活的現象。圖4是催化劑中毒對床層熱點溫度影響的示意圖,有圖可知隨著硫中毒時間增加,床層熱點溫度將不斷下移。③羰基鎳形成:在溫度低于200℃,鎳基催化劑中的活性組分鎳和CO反應生成羰基鎳。因此要避免低溫下,CO和催化劑的接觸,以免影響催化劑的活性。
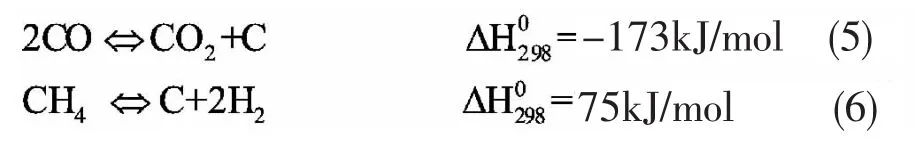
2.2.2 間接耐硫甲烷合成催化劑
GI公司用浸漬法開發了一種從鉬、釩或鎢中選出的金屬沉積在ZrO2上的催化劑。使用該催化劑原料氣中的硫含量可以超過4%,且轉化率和甲烷合成選擇性分別在75%和48%以上。此外國內也開發了兩種耐硫甲烷合成催化劑。一種是臨潼化肥所和中國科技大學聯合開發的耐硫甲烷合成催化劑。該催化劑系浸漬型鉬系催化劑,在H2/CO為1∶1時操作,能耐700℃的高溫;另一種是華東理工大學無機化工研究所開發的SDM型耐硫甲烷合成催化劑。該催化劑主活性物為MoS2,CO轉化率大于75%,甲烷選擇性超過51%,且活性高,機械強度好,還可硫化再生。
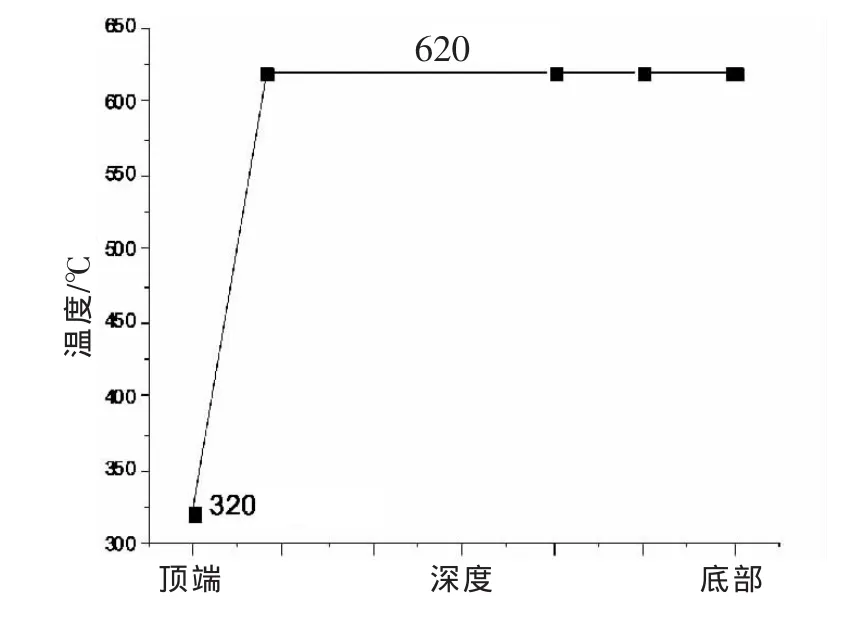
圖2 主甲烷合成爐反應床層溫度示意圖
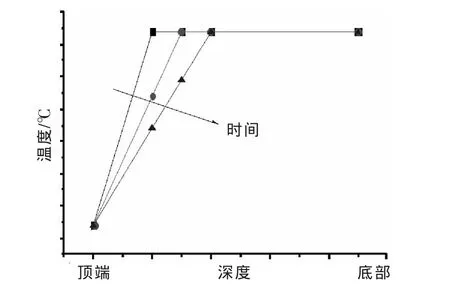
圖3 燒結對床層熱點溫度的影響
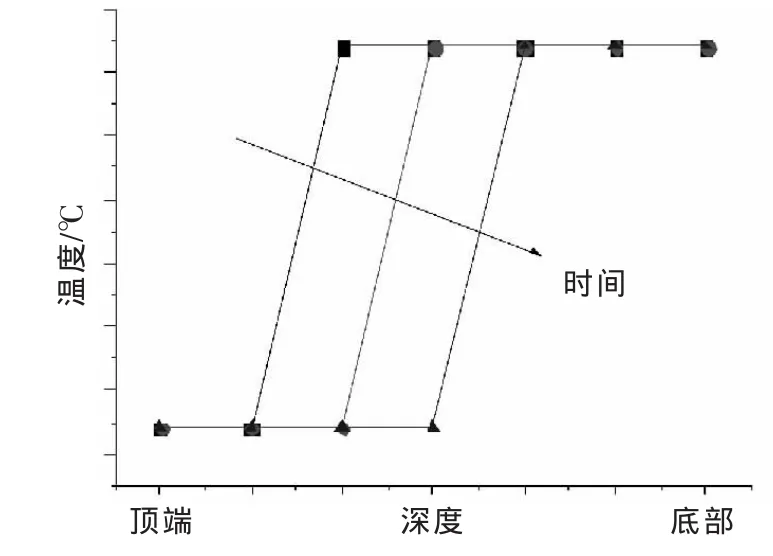
圖4 催化劑硫中毒對床層熱點溫度的影響
3 結束語
富煤缺油少氣的能源格局特點決定了我國使用煤作為油、氣的替代能源的必要性。多年來國家一直鼓勵通過煤炭的清潔利用發展替代能源和化工產業。煤制天然氣正是立足于我國的能源結構的特點,通過煤炭的高效利用和清潔合理轉化,生產清潔能源的工藝。目前,國內煤制天然氣仍處于工業化起步階段。開發工業化的煤制天然氣工藝技術以及加強甲烷合成催化劑的研究,大力發展煤制天然氣的生產建設是十分必要的。
[1]張海濱.淺析我國發展煤制天然氣的必要性及其風險[J].中國高新技術企業,2009(6):92-93.
[2]劉芹,邢濤.淺析煤制天然氣的工藝流程與經濟性[J].化工設計2010,20(3):25-27.
[3]張成.CO與CO2甲烷合成反應研究進展[J].化工進展,2007,26(9):1269-1273.
[4]于廣鎖.甲烷合成反應體系研究綜述[J].化肥設計,1998,(36):14-16.
[5]路霞,陳丗恒.CO甲烷合成Ni基催化劑的研究進展[J].石油化工,2010,39(3):340.
[6]周學良編.催化劑[M].北京:化學工業出版社,2002,101-103.

