阿德福韋治療慢性乙型肝炎停藥時病原學狀態與預后觀察*
宋閩寧 黃文琪 閔 峰
中國人民解放軍一七四醫院感染科(福建 廈門,361003)
應用核苷類似物治療慢性乙型肝炎(CHB),可減少肝癌、肝硬化的發生[1]。由于乙肝病毒(HBV)高復制率、低保真性的特點,易出現突變,經過藥物壓力(包括作用靶點、藥物動力學屏障、耐藥基因屏障、抗病毒藥物療效和耐藥通路)的篩選,再經由環境適應(肝內復制空間和適應性)過程,最終出現耐藥病毒株,因而,長期用藥,耐藥遲早會發生[2,3]。耐藥將給臨床帶來一系列的問題,尤其是將給患者帶來再治療困難及經濟負擔。如何避免耐藥的發生,成為目前抗病毒治療重要的問題。近年國內外肝病學會均修改了診治指南及專家共識[4~7],預防耐藥的發生主要包括嚴格選擇治療對象,加強患者的治療依從性,初治時首選強效及高耐藥屏障藥物以及加強耐藥檢測及優化治療方案。由于歷史原因,我國應用阿德福韋酯(ADV)人數眾多,目前也已進入了長程治療階段。部分患者也因不同復雜原因停或改/加藥。研究并分析這組資料,對于預防或尋找可能安全停藥的預測指標,也可對其他核苷類似物(NAs)治療終點的停藥處理有一定的參考價值,并可能減少耐藥的發生。本研究將2006年1 月-2007年1 月陸續入組的我院門診或住院CBH 患者,治療至2013年2 月的用藥情況與停藥結果進行相關分析,結果如下。
1 資料與方法
1.1 一般資料 2006年1 月至2007年1 月我科住院或門診收治的CHB 共209 例,男155 例,女54 例;年齡18~58 歲,平均41.1 歲。HBeAg 陽性130 例。ALT 121~394U/L,HBV DNA4~8 lg 拷貝/ml。診斷均符合2005年中華醫學會修訂的《慢性乙型肝炎防治指南》[3]標準。簽知情同意書。
1.2 觀察方法 入院行肝生物化學指標、血常規,凝血功能、HBV DNA 定量、HBV-M 定量檢測、肝臟超聲或CT 檢查。經臨床診斷評估,全部患者均符合抗病毒治療標準。口服ADV10mg,1 次/d。每3 個月復診,總療程6年。
1.3 檢測項目 肝功能檢測采用美國Abbott 公司生產的全自動生物化學分析儀檢測肝功能;HBV-M 定量檢測采用美國Abbott 公司的試劑 (Architect 12000,電化學發光法);HBV DNA 定量采用Taqman熒光定量PCR 法(廈門安普利科技有限公司靈敏度為1000 拷貝/ml)。耐藥檢測:PCR 產物直接測序(末端終止法,上海申友公司的試劑及檢測)。
1.4 統計學方法 應用SPSS 12.0 統計軟件包分析,率的比較用χ2檢驗,以P <0.05 為差異有統計學意義。
2 結果
2.1 患者目前狀況 209 例患者經過6年,仍繼續治療者73 例(73/209,35.0%),其中治療前33 例(33/73)HBeAg 陽性者中10 例 (10/33,39.3%)獲HBeAg/抗-HBe 血清轉換,8 例HBeAg 轉陰(8/33,24.2%);68 例HBV DNA <3 lg 拷貝/ml (68/73)。HBV 未 變 異 者 換/加 藥 71 例 (71/209,33.9%),其中包含停藥后復發患者;rtA181/T/S 變異者換/加藥5 例(5/209,2.4%)。停藥60 例,占28.7% (60/209)。
2.2 60 例中規范與不規范停藥患者臨床轉歸與病原學結果分析 結果見表1。
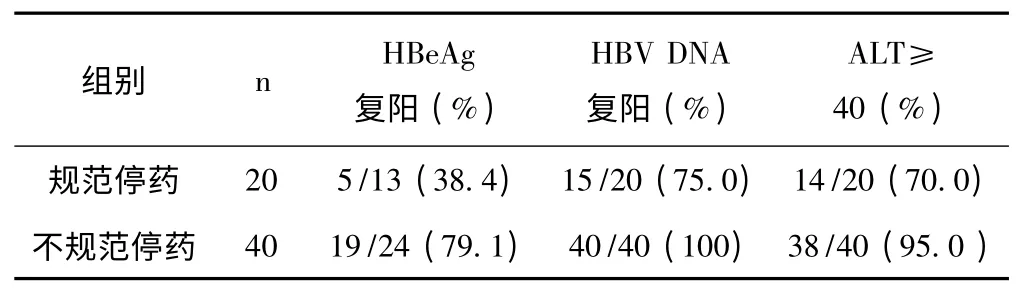
表1 規范與不規范停藥患者2年轉歸臨床比較[n (%)]
20 例于符合指南停藥標準時停藥(規范停藥),40 例則因不同原因,未達指南停藥標準時自動選擇停藥(不規范停藥)。觀察期兩年,規范停藥組20例中13 例抗-HBe 轉陰,原7 例HBeAg 陰性者,HBV DNA 均轉陰。不規范停藥組40 例中治前HBeAg 陽性24 例,HBeAg 陰性16 例。15 例治療部分應答,HBV DNA 下降后停藥,2 例未應答停藥,23 例完全應答后未達療程停藥。停藥2年時觀察,規范停藥患者HBeAg 復陽5 例(5/13,38.4%),HBV DNA 復陽15 例(15/20,75%);不規范停藥患者HBeAg 復陽19 例(19/24,79.1%),HBV DNA 復陽40 例(40/40,100%)。兩組患者臨床轉歸與病原學對照,規范停藥復發率低于不規范停藥,統計學處理P >0.05。ALT 復發兩組無差異。
2.3 服藥時間與停藥后復發的關系 結果見表2。* HBV DNA 上升≥2 lg 拷貝/ml 設為復發開始時間;與規范停藥組同時段比較,△P <0.05 (χ2=6.5),#P <0.05 (χ2=7.6)
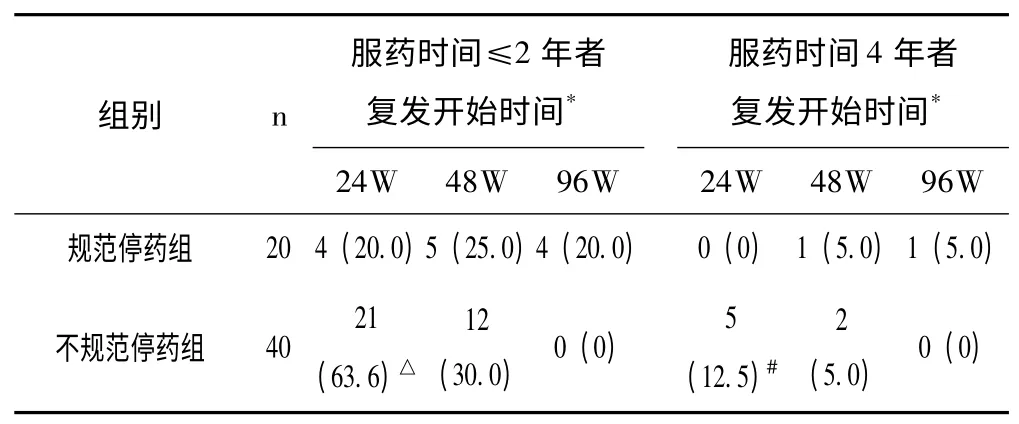
表2 兩組患者服藥時間與復發的關系[n (%)]
根據患者停藥是否規范,服藥時間長短與復發時間進行分析。將HBV DNA 上升≥2 lg 拷貝/ml 設為復發開始時間。不規范停藥組患者治療≤2年者,24周時復發21 例(21/40,63.6%)。與規范停藥組24周時復發4 例(4/20,20.0%)對照,統計學處理差異具有顯著性意義(χ2=6.5,P <0.05)。不規范停藥組患者治療4年者,5 例24 周內復發(5/40,12.5%),與規范停藥組24 周無復發(0/20,0%)對照,差異具顯著性意義(χ2=7.6,P <0.05)。規范停藥組5 例停藥96 周后仍未復發。
3 討論
慢性乙型肝炎抗病毒治療,耐藥是遲早會發生的,耐藥可使抗病毒治療失效,導致肝臟疾病進展、病毒學突破、生化學突破、血清學逆轉及組織學惡化,發生肝炎急性惡化,肝臟失代償和肝衰竭、肝移植失敗。耐藥發生的相關因素與病毒復制的數量和速率、病毒聚合酶的保真度、藥物的選擇壓力、耐藥病毒株的復制適應性、藥物的基因屏障等多種因素有關[8]。由于NAs 抗病毒作用的局限性,目前國內外防治指南雖有療程標準[9],但達到停藥標準停止治療后復發率高。因此近期有學者提出HBsAg 定量檢測水平作為停藥指標[10,11]具有較好的參考意義。但目前國內檢測試劑未能統一,批間、室間均有一定差異,基層醫院難以接受昂貴的定量檢測費用。如何規避風險,緩解耐藥壓力,尋找相對安全停藥模式,可能是解決的辦法之一[12~14]。
本研究結果顯示規范停藥復發率低于不規范停藥患者,ALT 復發程度相仿。用治療時間與復發時間對照,治療時間≤2年及4年組,不規范停藥組,24周復發率高于規范用藥組,具統計學差異(χ2=6.5、7.6,P 均<0.05),與Reijnders 的觀察相仿[15]。規范停藥組有5 例96 周后仍未復發。由于病例較少,尚需進一步擴大病例觀察。探索安全的停藥間期,可能對緩解用藥副反應及經濟壓力有益處。
本研究提示:HBeAg 轉換是較可靠的停藥指標。無論治療時間是2年或4年,達治療終點規范停藥組,24周復發率顯著低于不規范停藥組。規范停藥2年復發率低于不規范停藥,但無統計學差異。抗病毒治療對重度肝損害患者不良預后影響較小。以上資料為因各種原因需停藥患者提供了管理方面的參考依據。
[1]Sung JJ,Tsoi KK,Wong VW,et al.Meta-analysis:Treatment of hepatitis B infection reduces risk of hepatocellular carcinoma [J].Aliment Pharmacol Ther,2008,28 (9):1067 -1077.
[2]陳成偉,陳從新,陳士俊,等。核苷和核苷酸類藥物治療慢性乙型肝炎的耐藥及其管 理[J].實用肝臟病雜志,2013,16(1):1 -8.
[3]Lok AS,Zoulim F,Locarnini S,et al.Antiviral drug-resistant HBV:standardization of nomenclature and assays and recommendations for management [J].Hepatology,2007 Jul,46 (1):254 -265.
[4]中華醫學會肝病學分會,中華醫學會感染病學會.慢性乙型肝炎防治指南[J].(2005年版)臨床肝膽病雜志,2006,22 (1):1 -15.
[5]Lok AS,McMahon BJ.Chronic hepatitis B:update 2009 [J].Hepatology,2009,50 (3):661 -662.
[6]European Association For The Study Of The Liver.EASL clinical practice guidelines:Management of chronic hepatitis B virus infection[J].J Hepatol,2012,57 (1):167 -185.
[7]Liaw YW,KaoJII,Piratvisuth T,et al.Asian-Pacific consensus statement on the management of chronic hepatitis B:a 2012 update [J].Hepatol Int,2012,6 (3):531 -561.
[8]Zhang NP,Reijnders JG,Perquin M,et al.Frequency and clinical outcomes of flares related to nucleos (t)ide analogue therapy in patients with chronic hepatitis B [J].J Viral Hepat,2011,18 (7):252 -257.
[9]Liaw YF,Leung N,Kan JH,et al.Asian-Pacific consensus statement on the management of chronic hepatitis B:2008 update [J].Hepatol Int,2008,2 (3):263 -283.
[10]Van BF,Trojan J,Deterding K,et al.Evolution of adefovir-resistant HBV polymerase gene variants after switching to tenofovir disoproxil fumarate monotherapy [J].Antivir Ther,2012,17 (6):1049 -1058.
[11]ljaz S,Arnold C,Dervisevic S,et al.Dynamics of lamivudine resisranthepatitis B virus during adefovir monotherapy VerSUS lamivudine plusadefovir combination therapy [J].J Med Virol,2008,80:l160 -1170.
[12]Chae HB,Kim MJ,Seo EG,et al.High efficacy of adefovir and entecavir combination therapy in patients with nucleoside-refractory hepatitis B [J].Korean J Hepatol,2012,18 (1):75 -83.
[13]Yang HJ,Lee JH,Kim YJ,et al.Antiviral efficacy of combination therapy with entecavir and adefovir for entecavir/lamivudine -resistant hepatitis B virus with or without adefovir resistance [J].J Med Virus,2012,84 (3):424 -430.
[14]Yuen MF,Lai CL.Treatment of chronic hepatitis B:Evolution over two decades [J].J Gastroenterol Hepatol,2011,26 (1):138 -143.
[15]Reijnders JG,Perquin MJ,Zhang N,et al.Nucleos (t)ide analogues only induce temporary hepatitis B e antigen seroconversion in most patients with chronic hepatitis B [J].Gastroenterology.2010,139 (2):491 -498.

