當歸腹痛寧滴丸治療腸易激綜合征的藥效學研究
杜麗東, 吳國泰, 景 琪, 劉五州, 李應東, 任 遠*
(1.甘肅中醫學院, 甘肅 蘭州 730000; 2.甘肅省中藥藥理與毒理學重點實驗室, 甘肅 蘭州 730000)
[藥 理]
當歸腹痛寧滴丸治療腸易激綜合征的藥效學研究
杜麗東1,2, 吳國泰1,2, 景 琪1, 劉五州1, 李應東1, 任 遠1,2*
(1.甘肅中醫學院, 甘肅 蘭州 730000; 2.甘肅省中藥藥理與毒理學重點實驗室, 甘肅 蘭州 730000)
目的 觀察當歸腹痛寧滴丸 (當歸油) 對腸易激綜合征模型大鼠的治療作用, 探討作用機制。 方法 采用8種刺激誘導大鼠建立腸易激綜合征模型, 隨機分為正常組、 模型組、 陽性組 (匹維溴銨)、 當歸腹痛寧滴丸高、 中、 低劑量組, 每組 10 只, 連續給藥 31 d, 定期測定各組大鼠的體質量、 攝食量、 排便情況、 自主運動量, 末次給藥后測定胃排空率和腸推進率, 放射免疫法測定血清以及結腸勻漿 5-HT、 血漿和結腸勻漿 P物質 (SP)、 血管活性腸肽(VIP) 水平。 結果 給予當歸腹痛寧滴丸后, 大鼠攝食量和排便量增加, 固體粒狀糞便增多, 隨后體質量和攝食明顯增加,運動量接近正常,依次為當歸腹痛寧滴丸高、中劑量組。大鼠胃排空率增加和腸推進率減小亦如此。當歸腹痛寧滴丸使大鼠血清 5-HT水平下降, 血漿 VIP水平升高, 和結腸勻漿 5-HT水平下降, 以高劑量組為明顯。 結論 當歸腹痛寧滴丸對腸易激綜合征具有一定的治療作用, 其作用機制與抑制腦腸軸 5-HT和 VIP過度分泌和向正常水平恢復有關。
當歸腹痛寧滴丸; 腸易激綜合征; 胃腸功能;5-羥色胺;P物質; 血管活性腸肽
腸易激綜合征 (IBS) 是現代社會環境下消化系統的多發病和常見疾病,表現為腹部不適或腹痛,胃腸動力異常,大便性狀改變以及神經精神改變為特征的癥候群,因其缺乏形態學、生化等特異改變, 病因多樣且發病機制尚不明確[1]。 研究表明[2,3], 腸 易激綜合 征 病 人中存在 5-羥色胺 (5-HT)、 P物質 (SP)、 血管活性腸肽 (VIP) 等胃腸激素水平異常;多數患者伴有抑郁、焦慮、緊張等情緒變化,長期的精神神經異常因素可通過腦-腸軸引起胃腸運動、分泌功能障礙,進而引起腸易激綜合征加劇。
當歸腹痛寧滴丸 (國藥準字 Z62020027) 是蘭州和盛堂制藥有限公司生產的腸溶滴丸,主要成分為當歸油,具有解痙止痛的作用,適用于感染性腹瀉引起的急性腹痛,婦女痛經及產后宮縮痛等。前期研究顯示當歸油具有鎮靜、鎮痛、改善胃腸 動 力 等 作 用[4-6]。本 研 究 采 用 復 合 因 素 誘導大鼠建立腸易激綜合征模型,觀察當歸腹痛寧滴丸對模型大鼠的治療作用,并探討其對血液和腸組織中 5-HT水平、 胃腸激素 ( SP、 VIP) 水平的影響,為當歸腹痛寧滴丸用于治療腸易激綜合征提供實驗依據。
1 實驗材料
1.1 動物 SD大鼠, SPF級, 雌雄各半, 體質量160 ~180 g, 由甘肅中醫學院實驗動物中心提供,合格 證 號 SCXK ( 甘) 2011-0004。 喂 標 準 飼 料(由甘肅中醫學院實驗動物中心提供), 飼養溫度:(20 ±2)℃, 相對濕度 60% ~70%, 適應 7 d 后開始實驗。
1.2 藥品與試劑 當歸腹痛寧滴丸 (含當歸油的腸溶滴丸, 丸芯質量 20 mg, 口服, 頓服 10 ~15粒或日服2 次, 每次 10 ~15 粒) 由蘭州和盛堂制藥有限公司生產, 批號 121002; 匹維溴銨片由法國蘇威制藥公司生產, 批號 620016;5-HT、SP、VIP放射免疫試劑盒及 DAB顯色劑均購自武漢博士德生物工程有限公司;其他試劑均為分析純。
1.3 儀器 冰柜 (北京福意電器有限公司); 烘箱 (上海島韓實業有限公司); 振蕩器 (哈爾濱市東明醫療儀器廠); 噪聲測定儀 (北京天安聯合科技有限公司); 電子天平 (德國賽多利斯);GC-911-C-放射免疫計數器 ( 中國科技大學實業總公司); 敞箱 (80 cm×80 cm×40 cm) 為自制。
2 實驗方法
2.1 造模、 分組與給藥 參考文獻并改進[7-8], 60只 SD大鼠隨機分為正常組 (10 只) 和模型組(50 只)。 正常組大鼠分性別每籠 5 只常規飼養,不給任何刺激。模型組大鼠每籠1只孤養,并加以不可預見性刺激,刺激因子包括禁水禁食、晝夜顛倒、冷刺激、熱刺激、致痛、制動、高速震蕩和噪聲共8種, 刺激因子在 40 d 內隨機安排, 每天 1種,每種刺激出現5次,每種刺激不連續出現,造模40 d。 應激刺激操作方法, 禁水禁食:24 h 內斷水斷糧; 晝夜顛倒: 于早 7 ∶00 時將動物放入暗室中, 不開燈使動物處于黑暗狀態; 至晚19 ∶00時將暗室中照明燈打開,使動物處于光照狀態,直至次日早7時取出;冷刺激:將大鼠置于4℃冰柜中15 min 后取出; 熱刺激: 將大鼠置于 45 ℃的烘箱中 15 min 后取出; 致痛: 用止血鉗夾住大鼠距尾尖 1 cm處 (用力不宜過大, 動物發出哀叫聲即可) 持續 2 min; 制動: 將大鼠置于固定器中 5 h;高速震蕩:將大鼠放入振蕩器中,高速水平震蕩(110 r/min) 15 min 后取出; 噪聲: 將大鼠置于玻璃鐘罩內, 給 150 db 鬧鈴刺激 10 min。
將模型動物隨機分為模型組、陽性組 (灌胃匹維溴銨 15.0 mg/kg體質量,相當于臨床成人日用量的 7倍)、 當歸腹痛寧滴丸高、 中、 低劑量(分別灌胃當歸腹痛寧滴丸 120、 60、 30 mg/kg,相當于臨床成人日用量的 14 倍、7 倍和 3.5 倍),每組 10 只, 按性別每籠 5 只常規飼養, 按 10 mL/kg體質量容量灌胃, 正常組與模型組大鼠灌胃等容量蒸餾水, 連續31 d。
2.2 檢測指標與方法
2.2.1 體質量、攝食量 分別在給藥前和給藥第9、 第 19、 第 29 天上午 9 ∶00 時加飼料 100 g, 次日9 ∶00 時稱定剩余飼料質量, 并稱定動物體質量, 計算24 h 攝食量, 攝食量 = (食物總量 -食物余量) /體質量。
2.2.2 排便情況 分別在給藥前和給藥第 10、 第20、 第 30 天, 在直徑 60 cm的圓盆中盛滿水 (水溫 10 ℃ ±1 ℃), 水中央放置直徑 10 cm的柱形平臺, 平臺面高出水面約 1 cm, 將各組大鼠置于平臺上,觀察各大鼠2 h內排便情況,定形糞便記錄粒數,不定形或稀便記錄排便次數;并對每粒或每次糞便性狀評分,泄瀉稀便計0分,軟便無定形計1分,軟便定形計2分,固體定形計3分,累積記錄各大鼠2 h內糞便的評分。
2.2.3 自主運動量[9]自制敞箱 ( 高 40 cm, 長寬均為80 cm,周壁為黑色, 白色地面用黑線劃分為面積相等的 25 塊), 在暗的、無噪音、 安靜的房間進行。 敞箱中央上方1 m處懸掛1 個100W燈泡。 給藥前和給藥第10、 第 20、 第 30 天將每只大鼠置于光潔敞箱的中央, 以 5 min 內大鼠穿越地面方塊數作為水平運動得分, 以 5 min 內直立次數為垂直運動得分,將得分加和表示大鼠的運動量,每只大鼠測定一次。
2.2.4 胃腸動力[10]第 31 天給藥 1 h 后 (事先已禁食不禁水 12 h),各組大鼠灌胃半固體糊2.0 mL/只 (配制方法:16 g奶粉、 8 g蔗糖、 5 g活性炭、 10 g小鼠飼料粉 (過 80 目篩) 加入 250 mL的 5%的羧甲基纖維素懸液中, 充分攪拌混勻), 30 min 后股動脈放血, 取血約 1 mL加入抗凝管制備血漿, 另取血約2 mL自然凝固4 h制備血清,頸椎脫臼處死大鼠,開腹,結扎幽門和賁門,取胃,用濾紙擦干后稱定全質量,然后沿胃大彎剪開胃體,洗去胃內容物后擦干,稱凈重。迅速取出小腸,分離系膜,輕輕直鋪于水平白色臺面上,測量小腸全長 (幽門至回盲部距離) 及推進距離 (幽門至半固體糊前沿的距離)。 分別計算胃排空率和腸推進率。
胃排空率 (%) = [(灌胃半固體糊質量 -胃內殘留糊質量) /灌胃半固體糊質量] ×100%, 其中胃內殘留糊質量=胃全質量-胃凈質量; 腸推進率(%) =(推進距離/小腸全長) ×100%
2.2.5 血清 或血漿、 結 腸勻漿 5-HT、 SP和 VIP水平 大鼠動脈血室溫凝固 4 h, 低溫離心 3 000 r/min ×15 min, 分離血清 -20 ℃保存, 抗凝血低溫離心 4 000 r/min ×15 min, 分離血漿 -20 ℃ 保存, 按試劑盒說明書測定血清 5-HT、 血漿 SP和VIP水平; 測完腸推進后迅速摘取大鼠肛門上方3 cm處結腸 1 ~2 cm, 用生理鹽水洗凈內容物, 稱重后加入冷生理鹽水手動研磨制備 10%的組織勻漿, 于 4 000 r/min ×20 min 離心, 取上清 -20 ℃保存, 按試劑盒說明書測定組織勻漿 5-HT、 SP和VIP水平。
2.3 統計學方法 各組數據采用 SPSS13.0 統計軟件處理, 以均數 ±標準差 () 表示, 多組間比較采用單因素方 差分析 (one-way ANOVA),兩組間比較采用 t檢驗, P<0.05 差 異 具 有統計學意義。
3 實驗結果
3.1 當歸腹痛寧滴丸對腸易激綜合征模型大鼠體質量的影響 見表1。
表1 當歸腹痛寧滴丸對腸易激綜合征模型大鼠體質量檢測結果 (, n=10)Tab.1 Effects on rats’ w eight(, n=10)

表1 當歸腹痛寧滴丸對腸易激綜合征模型大鼠體質量檢測結果 (, n=10)Tab.1 Effects on rats’ w eight(, n=10)
注: 與正常組比較,**P<0.01; 與模型組比較,#P<0.05
組別 劑量/( mg·kg-1)給藥前體質量/ g給藥后體質量/g第 10 天 第20 天 第30天正常組 —221.0 ±24.1 234.2 ±27.3 259.9 ±25.4 298.4 ±19.3模型組 — 187.5 ±18.2** 193.0 ±20.0** 211.6 ±18.7** 232.4 ±28.6**陽性組 15 184.7 ±22.5** 199.6 ±23.7 235.2 ±15.5# 258.9 ±21.3#當歸腹痛寧滴丸高劑量組 120 185.0 ±15.6** 203.5 ±25.8 232.0 ±15.2# 263.2 ±30.8#當歸腹痛寧滴丸中劑量組 60 180.8 ±19.2** 196.3 ±29.1 228.8 ±21.3 246.9 ±24.7當歸腹痛寧滴丸低劑量組 30 184.2 ±22.9**198.3 ±23.2 221.6 ±22.0 239.0 ±27.2
與正常組比較,造模后各大鼠體質量明顯減輕(P<0.01),給藥第 10 天, 各組大鼠體質量均有增加,與模型組比較,各給藥組組間差異均無統計學意義; 給藥第 20 天和第 30 天, 各組大鼠體質量明顯增加,陽性組和當歸腹痛寧滴丸高劑量組增加顯著 (P<0.05)。
3.2 當歸腹痛寧滴丸對腸易激綜合征模型大鼠攝食量的影響 見表2。
與正常組比較, 造模后各組大鼠24 h 內平均攝食量明顯減少 (P<0.01),給藥第 10 天, 各組大鼠平均攝食量均有增加,與模型對照組比較,各給藥組組間差異均無統計學意義; 給藥第20 天, 各組大鼠24 h內平均攝食量明顯增加, 與模型組比較, 陽性組和當歸腹痛寧滴丸高劑量組增加顯著 (P<0.05, P<0.01); 給藥第 30 天, 陽性組、 當歸腹痛寧滴丸高、中、 低劑量組增加顯著 (P<0.05, P<0.01)。
表2 當歸腹痛寧滴丸對腸易激綜合征模型大鼠攝食量的影響 (, n=10)Tab.2 Effects on feed consum ption in rats(, n=10)
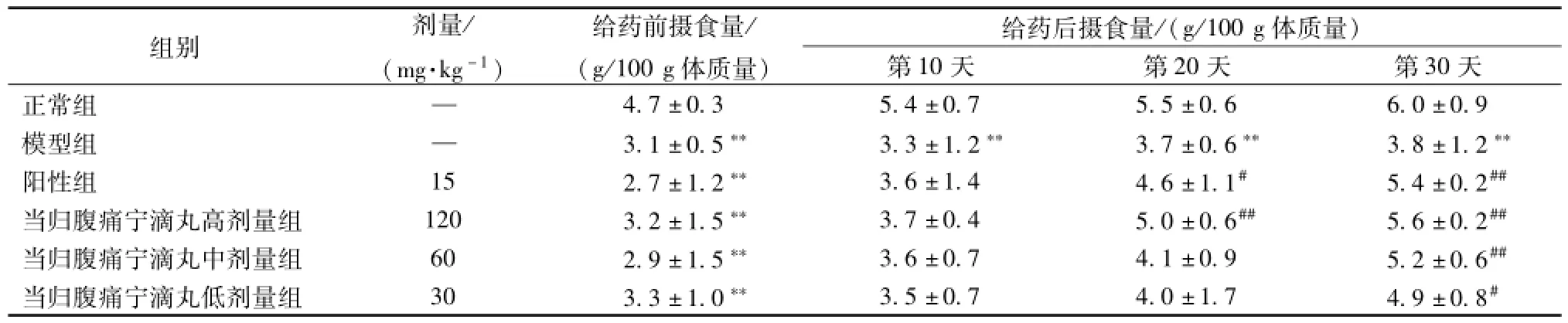
表2 當歸腹痛寧滴丸對腸易激綜合征模型大鼠攝食量的影響 (, n=10)Tab.2 Effects on feed consum ption in rats(, n=10)
注: 與正常組比較,**P<0.01; 與模型組比較,#P<0.05,##P<0.01
組別 劑量/(mg·kg-1)給藥前攝食量/(g/100 g體質量)給藥后攝食量/(g/100 g體質量)第10 天 第20 天 第30天正常組 —4.7 ±0.3 5.4 ±0.7 5.5 ±0.6 6.0 ±0.9模型組 — 3.1 ±0.5** 3.3 ±1.2** 3.7 ±0.6** 3.8 ±1.2**陽性組 15 2.7 ±1.2** 3.6 ±1.4 4.6 ±1.1# 5.4 ±0.2##當歸腹痛寧滴丸高劑量組 120 3.2 ±1.5** 3.7 ±0.4 5.0 ±0.6## 5.6 ±0.2##當歸腹痛寧滴丸中劑量組 60 2.9 ±1.5** 3.6 ±0.7 4.1 ±0.9 5.2 ±0.6##當歸腹痛寧滴丸低劑量組 30 3.3 ±1.0** 3.5 ±0.7 4.0 ±1.7 4.9 ±0.8#
3.3 當歸腹痛寧滴丸對腸易激綜合征模型大鼠排 便情況的影響 見表3, 表4。
表3 當歸腹痛寧滴丸對腸易激綜合征模型大鼠排便量的影響 (, n=10)Tab.3 Effects on the quantities of stool in rats(, n=10)

表3 當歸腹痛寧滴丸對腸易激綜合征模型大鼠排便量的影響 (, n=10)Tab.3 Effects on the quantities of stool in rats(, n=10)
注: 與正常組比較,*P<0.05,**P<0.01; 與模型組比較,#P<0.05
組別 劑量/(mg·kg-1)給藥前排便粒數或次數 /(n/2 h)給藥后排便粒數或次數/(n/2 h)第10 天 第20 天 第30天正常組 —4.2 ±1.9 5.1 ±2.1 4.9 ±2.4 5.4 ±2.3模型組 — 6.9 ±1.5** 7.6 ±1.8* 7.3 ±1.7* 6.8 ±1.8陽性組 15 6.7 ±1.5** 5.4 ±2.1# 5.2 ±2.3# 5.1 ±2.2當歸腹痛寧滴丸高劑量組 120 7.2 ±2.4** 6.5 ±2.5 5.0 ±1.9# 5.0 ±1.7#當歸腹痛寧滴丸中劑量組 60 7.0 ±2.1** 7.4 ±2.9 7.2 ±2.5 4.5 ±2.6#當歸腹痛寧滴丸低劑量組 30 6.2 ±2.3**7.3 ±3.0 7.6 ±2.1 6.0 ±2.2
如表3所示,與正常組比較,造模后各大鼠2 h內排便量明顯增多 (P<0.01), 給藥第 10 天,與模型組比較, 陽性組大鼠排便量減少 (P<0.05); 給藥第20 天, 陽性組和當歸腹痛寧滴丸高劑量組大鼠排便量減少 (P<0.05); 給藥第 30天,當歸腹痛寧滴丸高、中劑量組大鼠排便量明顯減少 (P<0.05)。
表4 當歸腹痛寧滴丸對腸易激綜合征模型大鼠糞便性狀總評分的影響 (, n=10)Tab.4 Effects on scores of stool characteristics in rats(, n=10)
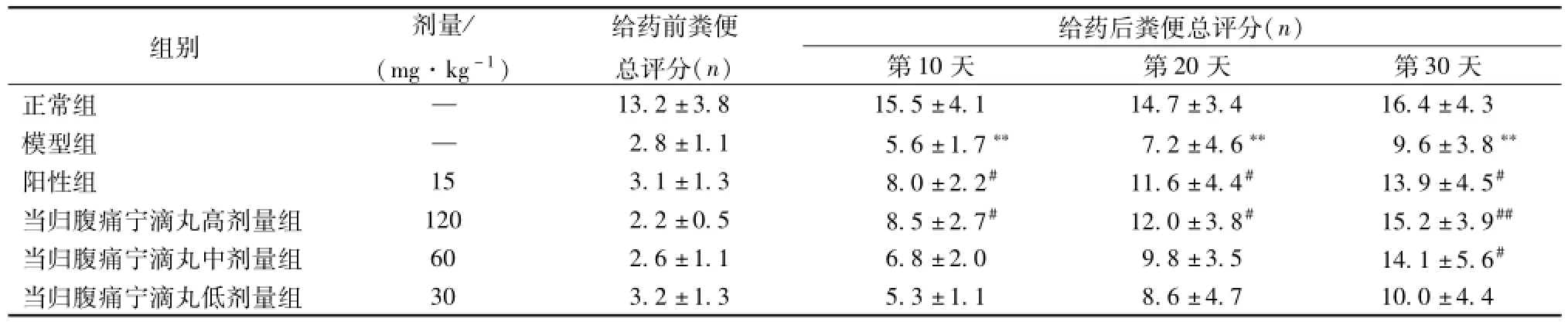
表4 當歸腹痛寧滴丸對腸易激綜合征模型大鼠糞便性狀總評分的影響 (, n=10)Tab.4 Effects on scores of stool characteristics in rats(, n=10)
注: 與正常組比較,**P<0.01; 與模型組比較,#P<0.05,##P<0.01
組別 劑量/(mg·kg-1)給藥前糞便總評分(n)給藥后糞便總評分(n)第10 天 第20 天 第30天正常組 —13.2 ±3.8 15.5 ±4.1 14.7 ±3.4 16.4 ±4.3模型組 — 2.8 ±1.1 5.6 ±1.7** 7.2 ±4.6** 9.6 ±3.8**陽性組 15 3.1 ±1.3 8.0 ±2.2# 11.6 ±4.4# 13.9 ±4.5#當歸腹痛寧滴丸高劑量組 120 2.2 ±0.5 8.5 ±2.7# 12.0 ±3.8# 15.2 ±3.9##當歸腹痛寧滴丸中劑量組 60 2.6 ±1.1 6.8 ±2.0 9.8 ±3.5 14.1 ±5.6#當歸腹痛寧滴丸低劑量組30 3.2 ±1.3 5.3 ±1.1 8.6 ±4.7 10.0 ±4.4
結果顯示,與正常組比較,造模后各大鼠均出現稀便和無定形軟便 (P<0.01), 給藥第 10 天,與模型對照組比較,各給藥組大鼠稀便減少,以無定形軟便為主,陽性組和當歸腹痛寧滴丸高劑量組組間差異有統計學意義 (P<0.05); 給藥第 20天,陽性組和當歸腹痛寧滴丸高劑量組大鼠固體粒狀糞便增多 (P<0.05); 給藥第 30 天, 陽性組、當歸腹痛寧滴丸高、中劑量組大鼠糞便性狀接近正常 (P<0.05, P<0.01)。
3.4 當歸腹痛寧滴丸對腸易激綜合征模型大鼠自主運動量的影響 見表5。
與正常組比較,造模后各大鼠均出現蜷縮、喜臥、萎靡等狀態,環境敏感性增高,自主運動量減少 (P<0.01),與模型組比較,給藥第 10 天和第20天, 各給藥組大鼠運動量增加, 但組間差異無統計學意義; 給藥第 30 天, 陽性組、 當歸腹痛寧滴丸高劑量組大鼠運動量接近正常 (P<0.05,P<0.01)。
3.5 當歸腹痛寧滴丸對腸易激綜合征模型大鼠胃腸動力的影響 見表6。
表5 當歸腹痛寧滴丸對腸易激綜合征模型大鼠自主運動量的影響 (, n=10)Tab.5 Effects on autonom ic activities in rats(, n=10)
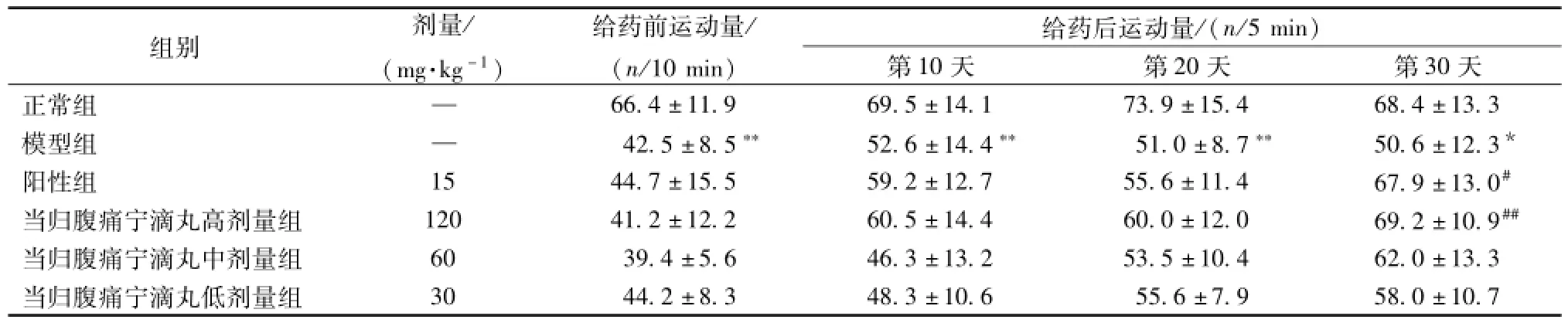
表5 當歸腹痛寧滴丸對腸易激綜合征模型大鼠自主運動量的影響 (, n=10)Tab.5 Effects on autonom ic activities in rats(, n=10)
注: 與正常組比較,*P<0.05,**P<0.01; 與模型組比較,#P<0.05,##P<0.01
組別 劑量/(mg·kg-1)給藥前運動量/( n/10 min)給藥 后運 動量 /( n/5 min)第10 天 第20 天 第30天正常組 —66.4 ±11.9 69.5 ±14.1 73.9 ±15.4 68.4 ±13.3模型組 — 42.5 ±8.5** 52.6 ±14.4** 51.0 ±8.7** 50.6 ±12.3*陽性組 15 44.7 ±15.5 59.2 ±12.7 55.6 ±11.4 67.9 ±13.0#當歸腹痛寧滴丸高劑量組 120 41.2 ±12.2 60.5 ±14.4 60.0 ±12.0 69.2 ±10.9##當歸腹痛寧滴丸中劑量組 60 39.4 ±5.6 46.3 ±13.2 53.5 ±10.4 62.0 ±13.3當歸腹痛寧滴丸低劑量組30 44.2 ±8.3 48.3 ±10.6 55.6 ±7.9 58.0 ±10.7
表6 當歸腹痛寧滴丸對腸易激綜合征模型大鼠胃排空率和腸推進率的影響 (, n=10)Tab.6 E ffects on gastric em ptying ratesand intestinal propulsion rates in rats(, n=10)
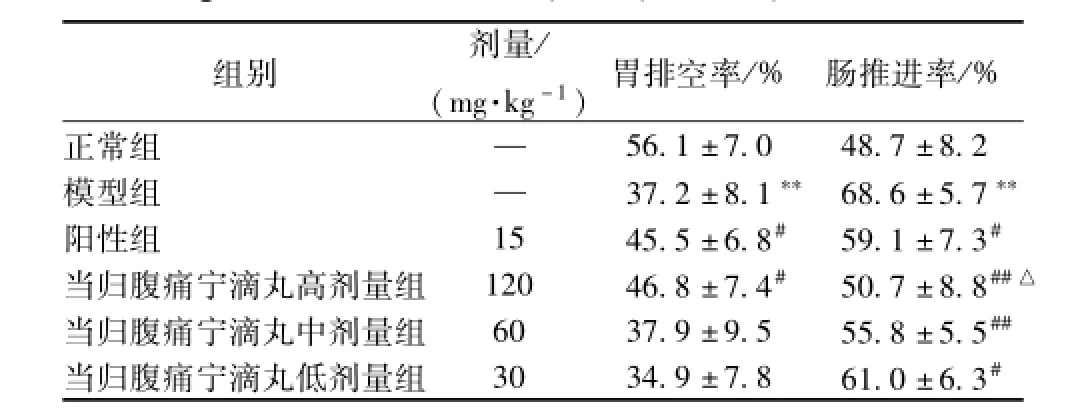
表6 當歸腹痛寧滴丸對腸易激綜合征模型大鼠胃排空率和腸推進率的影響 (, n=10)Tab.6 E ffects on gastric em ptying ratesand intestinal propulsion rates in rats(, n=10)
注: 與正常組比較,**P<0.01; 與模 型組比較,#P<0.05,##P<0.01; 與陽性組比較△P<0.05
組別 劑量/(mg·kg-1) 胃排空率/% 腸推進率/%正常組 —56.1 ±7.0 48.7 ±8.2模型組 — 37.2 ±8.1** 68.6 ±5.7**陽性組 15 45.5 ±6.8# 59.1 ±7.3#當歸腹痛寧滴丸高劑量組 120 46.8 ±7.4# 50.7 ±8.8##△當歸腹痛寧滴丸中劑量組 60 37.9 ±9.5 55.8 ±5.5##當歸腹痛寧滴丸低劑量組 30 34.9 ±7.8 61.0 ±6.3#
與正常組比較,模型組大鼠胃排空率明顯減小、 腸推進率明顯加快 (P <0.01), 與模型組比較,陽性組和當歸腹痛寧滴丸高劑量組大鼠胃排空率明顯增加 (P<0.05), 陽性組和當歸腹痛寧滴丸各劑量組大鼠腸推進率明顯減小 (P<0.05,P<0.01)。
3.6 當歸腹痛寧滴丸對腸易激綜合征模型大鼠血清 5-HT、 血漿 SP和 VIP水平的影響 見表 7。
與正常組比較, 模型組大鼠血清 5-HT水平明顯升高、血漿 SP和 VIP水平均明顯降低 ( P<0.01), 與模型組比較, 陽性組和當歸腹痛寧滴丸各劑量組大鼠血清 5-HT水平明顯下降、 陽性組血漿 SP水平和當歸腹痛寧滴丸高劑量組血漿 VIP水平明顯升高 (P<0.05, P<0.01)。
3.7 當歸腹痛寧滴丸對腸易激綜合征模型大鼠結腸勻漿 5-HT、 SP和 VIP水平的影響 見表 8。
表 7 當歸腹痛寧滴丸對腸易激綜合征模型大鼠血清 5-HT、 血漿 SP和 VIP水平的影響 (, n=10)Tab.7 Effects on serum 5-HT, p lasma SP or VIP levels in rats(, n=10)

表 7 當歸腹痛寧滴丸對腸易激綜合征模型大鼠血清 5-HT、 血漿 SP和 VIP水平的影響 (, n=10)Tab.7 Effects on serum 5-HT, p lasma SP or VIP levels in rats(, n=10)
組別 劑 量 /( mg·kg-1) 5-TH/( ng·mL-1) SP/(pg·mL-1) VIP/( pg·mL-1)正常組 —173.22 ±30.01 46.64 ±5.07 35.68 ±3.32模型組 — 231.58 ±26.16** 37.52 ±6.41** 28.40 ±5.34**陽性組 15 196.25 ±41.60# 45.67 ±4.68# 29.91 ±4.95當歸腹痛寧滴丸高劑量組 120 165.18 ±35.92## 40.05 ±5.80 37.20 ±4.86##△△當歸腹痛寧滴丸中劑量組 60 192.35 ±30.89## 39.86 ±5.57 29.45 ±5.78當歸腹痛寧滴丸低劑量組 30 202.45 ±25.20#35.60 ±6.47 26.07 ±4.20注: 與正常組比較,**P<0.01; 與模型組比較,#P<0.05,##P<0.01; 與陽性組比較,△△P<0.01
表 8 當歸腹痛寧滴丸對腸易激綜合征模型大鼠結腸勻漿 5-HT、 SP和 VIP水平的影響 (, n=10), n=10)Tab.8 Effects on 5-HT, SP and VIP levels in colon homogenates in rats(
注: 與正常組比較,**P<0.01; 與模型組比較,#P<0.05,##P<0.01; 與陽性組比較,△P<0.05
組別 劑 量 /( mg·kg-1) 5-TH/( ng·g-1) SP/( pg·g-1) VIP/( pg·g-1)正常組 —76.42 ±7.90 29.95 ±8.14 70.44 ±6.30模型組 — 95.15 ±8.51** 41.16 ±6.04** 75.06 ±8.37陽性組 15 64.37 ±7.45## 35.36 ±5.35# 65.79 ±4.95##當歸腹痛寧滴丸高劑量組 120 81.12 ±5.80## 30.50 ±7.72## 59.24 ±5.93##△當歸腹痛寧滴丸中劑量組 60 85.58 ±6.05# 36.78 ±5.86 67.70 ±7.17當歸腹痛寧滴丸低劑量組30 92.25 ±8.37 38.62 ±5.04 68.08 ±6.97
與正常組比較, 模型組大鼠結腸勻漿 5-HT和SP水平明顯升高 (P<0.01), 但結腸勻漿 VIP水平變化不明顯;與模型對照組比較,陽性組和當歸腹痛寧滴丸高、 中劑量組大鼠結腸勻漿 5-HT水平明顯下降 (P<0.05, P<0.01), 陽性組和當歸腹痛寧滴丸高劑量組大鼠結腸勻漿 SP和 VIP水平明顯下降 (P<0.05, P<0.01)。
4 討論
目前腸易激綜合征動物模型主要是以中樞 (社會心理因素) 或外周 (腸道炎癥、感染因素)為刺激靶點建立的腸易激綜合征模型,能模擬腸易激綜合征臨床的部分特征,但僅從腸易激綜合征病理生理學機制的某一個方面著手,均不能完全反應腸易激綜合征復雜的發病機制和病理生理學特征[11],本研究根據腸易激綜合征患者的發病特點和主要病因,遴選出8種致病因素作為模型復制的刺激因子,采用隨機排列,使動物不可預見刺激作用,造模40 d, 基本出現了腸易激綜合征臨床病人具備的大體癥狀,且未見動物死亡,模型比較穩定,更適合進行藥效評價和基礎研究。
當歸腹痛寧滴丸是以甘肅道地藥材當歸油為主要原料,采用現代制劑工藝制成的中藥制劑,已經取得了良好的社會和經濟效益, 研究報道[12], 當歸腹痛寧滴丸對嬰幼兒秋季腹瀉有良好的療效,服藥作用快, 無不良反應。 另有報道[13], 當歸腹痛寧滴丸對胃腸平滑肌具有明顯的松弛作用,可延緩胃腸排空時間,其作用機理是阻滯M受體、α受體、 H1受體和直接抑制平滑肌, 優于阿托品類與罌粟堿等解痙藥,還有明顯的鎮痛、消炎和抗菌作用。
最新研 究 發 現[6,14-15],當 歸 油 對 兔 離 體 胃 底、胃體、十二指腸、空腸和回腸平滑肌均具有舒張作用,且呈現劑量依賴關系;對正常小鼠胃排空有一定的延緩作用,對正常小鼠小腸推進未見明顯作用;對模型小鼠胃排空和小腸推進亢進現象具有明顯的改善效應;當歸揮發油能改善實驗性胃腸動力障礙,可能與促進乙酰膽堿和胃腸激素的分泌有關。本研究發現, 持續給藥20 d, 高劑量當歸腹痛寧滴丸 (120 mg/kg)能顯著改善模型大鼠的攝食量、 排便量和糞便性狀; 持續給藥30 d, 高、 中劑量當歸腹痛寧滴丸 (120、 60 mg/kg) 能進一步改善模型大鼠的自主運動、調節胃腸動力,結果提示當歸腹痛寧滴丸對腸易激綜合征消化系統癥狀具有一定的治療作用。
5-HT、 VIP和 SP是主要的胃腸激素, 也是存在于中樞神經系統和腸神經系統與腸易激綜合征發生有直接關系的腦-腸肽, 在調節內臟感覺和運動起重要作用[16]。 研究報道[17], 腸易激綜合征患者外周組織 5-HT水平增高是內臟痛覺過敏的主要發病機制;本研究發現,模型大鼠血清和結腸組織5-HT水平明顯增高, 當歸腹痛寧滴丸高、 中劑量治療 30 d 后, 模型大鼠血清和結腸組織 5-HT水平明顯下降,有利于提高內臟痛閾,消除腸道過敏;本研究中, 腸易激綜合征模型大鼠結腸組織 SP水平增加, 血漿 SP水平降低。 結腸中SP水平的增加可能與模型動物排便增加,胃腸運動亢進有關,與前期研究結果一致[18]; 當歸腹痛寧滴丸高劑量能明顯降低結腸組織 SP水平, 從而改善胃腸動力,消除腸道過敏。 VIP是抑制胃腸運動的主要神經遞質之一,具有松弛胃腸平滑肌、促進腸道水和電解質的分泌的功能[19]。 本 研 究 發 現 模 型 大 鼠 血 漿VIP水平均明顯降低, 但結腸勻漿 VIP水平變化不明顯; 當歸腹痛寧滴丸高劑量治療 30 d 后血漿 VIP水平明顯升高而結腸 VIP水平明顯下降, 對胃腸運動亢進具 有 一 定 的 調 節 作用, 與 文獻[20-21]報 道 一致,具體機制有待進一步研究。
綜上所述,當歸腹痛寧滴丸可能通過降低腸道敏感性、止瀉、降低腸推進率等改善胃腸道癥狀,進一步緩解精神神經異常等治療腸易激綜合征;作用機制與抑制腦腸軸 5-HT和 VIP過度分泌, 促使其向正常水平恢復等多個環節有關。
[1] 張細元, 鄒開芳, 侯曉華.腸易激綜合征病因研究進展[ J] .臨床消化病雜志, 2003, 15(4) :189-191.
[ 2 ] 王景杰, 高峰, 黃裕新, 等.IBS 患者胃腸運動功能的臨床研究[J].西安交通大學學報: 醫學版, 2002, 23 (4): 423-424.
[ 3 ] Monnikes I, Arnold R, Florin I, et al.The combination of medical treatment p lus multi-component behavioral therapy is superior to medical treatment alone in the therapy of irritable bowel syndrome[ J] .Am J Castroenterol, 2000, 95 ( 4 ) : 981-994.
[4] 楊慶利, 朱玉真,朱文華, 等.當歸揮發油的藥理作用研究[J].蘭州醫學院學報, 1986, (3):20-27.
[ 5 ] Matsumoto K, Kohno S, Ojima K, et al.Effects ofmethylenechloride-soluble fraction of Japanese angelica rootextract, ligustilide and butylidenephthalide, on pentobarbital sleep in grouphoused and socially isolated mice[ J] .Life Sci, 1998, 62(23):2073-2082.
[6] 程小平, 吳國泰,劉峰林, 等.當歸揮發油對實驗性胃腸動力障礙的作用及機制研究[J].中藥藥理與臨床, 2011,27(4):54-56.
[7] 劉清華, 李定國.腸易激綜合征動物模型復制思路和方法[J].國外醫學·消化系疾病分冊, 2002, 22(3):154.
[ 8 ] Katz R J, Roth K A, Carroll B.Acute and chronic stress effects on open field activity in the rat:implications for amodel of depression [ J] .Neuro Sci Bio Behave Rev, 1981, 5 ( 2 ) : 247-251.
[9] 方 圓, 高峻鈺.嗎啡依賴自然戒斷后大鼠造抑郁樣模型探討[ J] .中國藥物依賴性雜志, 2011, 20(1) :26-28.
[10] 尹愛武, 高鵬飛, 麻黎偉.厚樸枳實配伍對大鼠胃動力的影響[ J] .中國實驗方劑學雜志, 2011, 17(15) :175-177.
[11] 徐俊榮, 羅金燕.腸易激綜合征動物模型研究進展[J].基礎醫學與臨床, 2006, 26(8):902-904.
[12] 張嘉昆.當歸腹寧滴丸治療嬰幼兒秋季腹瀉 20 例[ J].新藥與臨床, 1988, 7(2):105-106.
[13] 孫紹武, 王積福.當歸腹寧滴丸治療腹痛 162 例觀察[J].中國中西醫結合雜志, 1992, 12(9):531-533.
[14] 王瑞瓊, 吳國泰, 任 遠, 等.當歸揮發油對兔離體胃腸平滑肌張力的影響[J].甘肅中醫學院學報, 2010, 27(1):12-14.
[15] 洪秋菊, 吳國泰, 王瑞瓊, 等.當歸揮發油對小鼠胃排空和腸推進的影響[J].甘肅中醫, 2011, 24(3):45-46.
[16] Mach T.The brain-gutaxis in irritable bowel syndrome—clinical aspects[ J].Med SciMonit, 2004, 10(6) :RA125-31.
[17] Monnikes H, Ruter J, Konig M, etal.Differential induction of c-fos expression in brain nuclei by( noxious) and non-noxious colonic distension:Role of afferent C fibersand 5-HT3receptors[ J] .Brain Res, 2003, 966(2) :253-264.
[18] 李兆申, 董文珠, 鄒多武.腸易激綜合征腸黏膜 SP、 VIP、CGRP變化的研究[ J].第二軍醫大學學報, 2003, 24(2):47-151.
[19] Evangelista S.Involvement of tachykinin in intestinal in flammation[J] .Curr Pharm Des, 2001, 7(1) :19-30.
[20] 林 琳, 趙志泉, 閻 驗, 等.腸易激綜合征與胃腸多種肽類激素的相關研究[J].中華消化雜志, 2003, 23 (8): 501-502.
[21] 張紅杰, 林 琳, 趙志泉.胃腸肽類激素與腸易激綜合征發病間的關系[J].南京醫科大學學報: 自然科學版,2003, 23(6):527-529.
Pharm acodynam ics of Danggui Futongning Dropping Pills in rat w ith irritable bowel syndrom e
DU Li-dong1,2, WU Guo-tai1,2, JING Qi1, LIUWu-zhou1, LIYing-dong1, REN Yuan1,2*
AIM To study the therapeutic effect of Danggui Futongning Dropping Pills( angelica oil) in rat with irritable bowel syndrome.METHODS Mice'models for irritable bowel syndrome were induced by eight types of stimulations.Sixty SD rat were divided into the normal control group, the model group, positive control group ( Pinaverium Bromide Tablets) , high-dose, middle-dose, low-dose Danggui Futongning Dropping Pills group.The treatment lasted for 31 days.Body weights, appetite, defecation, independent exercise of all ratswere recorded.The rate of gastric emptying and small intestinal propulsion rate were measured.The 5-HT in serum,substance P( SP) and vasoactive intestinal peptide( VIP) in plasma or 5-HT, SP, VIP in colon homogenateswere evaluated by radioimmunoassay.RESULTS With the treatment of Danggui Futongning Dropping Pills, the food intake and stool quantity increased.Consequently, body weights and appetite increased as well.The independent movement returned to normal level.High-dose Danggui Futongning Dropping Pillsgroup performed the best and followed bymiddle-dose group.The same resultsobserved in those two groups for emptying rates and intestinal propulsion rates.The 5-HT levels in serum and in colonic homogenate significantly reduced but VIP levels in plasma increased markedly.The SP and VIP contents significantly decreased in colonic homogenate.CONCLUSION Thetherapeutic effect of Danggui Futongning Dropping Pills on irritable bowel syndrome is obvious.The mechanism could be related to inhibition against the excessive secretion of5-HT and VIP in brain-gut-axis.
Danggui Futongning Dropping Pills;irritable bowel syndrome( IBS);gastrointestinal function;5-HT;substance P( SP) ;vasoactive intestinal peptide(VIP)
R285.5
:A
1001-1528(2014)12-2445-07
10.3969/j.issn.1001-1528.2014.12.001
2013-12-24
“十二五” 國家科技支撐計劃項目子課題 (2011BAI05B0206); 甘肅省自然科學基金項目 (1212RJZA079); 甘肅省中藥藥理與毒理學重點實驗室開放基金項目 (ZDSYS-KJ-2012-004 )
杜麗東 (1978—), 女, 碩士, 講師, 研究方向: 中藥藥理與毒理。 Tel:13919030726, E-mail:lidong-du@126.com
*通信作者: 任 遠 ( 1963—), 男, 教授, 博士生導師, 研究方 向: 中藥藥理與毒理。 Tel: (0931 ) 8762653, E-mail:Leyuan816@ 163.com
(1.Cansu College of Traditional Chinese Medicine, Lanzhou 730000, China;2.Cansu Provincial Key Laboratory of Pharmacology and Toxicology of TCM, Lanzhou 730000, China )

