如何防止堿洗滌塔的堿結晶
趙大偉,呂尚新,趙 勇,王志防
(中國石油撫順石化公司洗滌劑化工廠,遼寧 撫順 113001)

撫順石化公司洗滌劑化工廠的烷基化裝置是以氫氟酸作催化劑,將苯和直鏈烯烴進行烷基化反應,生成直鏈烷基苯。當烷基化反應需在氫氟酸催化劑的作用下進行,反應完成后會產生一些含酸尾氣,排放到堿洗滌塔,經中和后放空至大氣。在裝置開停工期間,需要用氮氣吹掃酸區設備,產生的含酸廢氣也排放到堿洗滌塔,經中和后放空至大氣。堿洗滌塔入口管線是否暢通,直接影響烷基化裝置的正常運行和裝置開停工操作的順利進行。因此,本文從堿液組分含量和沉淀-溶解平衡理論角度進行系統分析,力求找到堿液結晶的原因和避免堿液結晶的措施,提出通過優化堿洗滌塔操作達到消除堿結晶的目的,從而使烷基苯裝置實現平穩、安全、長周期運行。
1.堿系統流程簡介
KOH水溶液與酸發生中和反應并放熱,具有強腐蝕性,呈現強堿性。
含氫氟酸氣體具有腐蝕性和毒性,不能直接送往正常氣體排放系統。因此,所有酸性氣體的放空閥和安全閥都要通過酸排放總管連接到堿洗滌塔。排放的含氫氟酸氣體首先送入擋板式氣液分離罐,從擋板式分離罐分離出來的酸性氣體進入堿洗滌塔,在堿洗滌塔中與KOH溶液逆流接觸進行洗滌,從堿洗滌塔頂部出來、中和后的氣體送往非酸性排放總管,最后送往火炬放空。
堿洗滌塔內氫氟酸的中和反應過程如下:
KOH溶液經循環泵連續循環到堿洗滌塔頂部。KOH溶液中通常含有質量分數為5~10%的KOH,循環KOH溶液中的KOH濃度一般由質檢人員每天檢查分析一次,特殊情況下需加樣分析。
簡單的堿洗滌塔工藝流程如圖1所示。
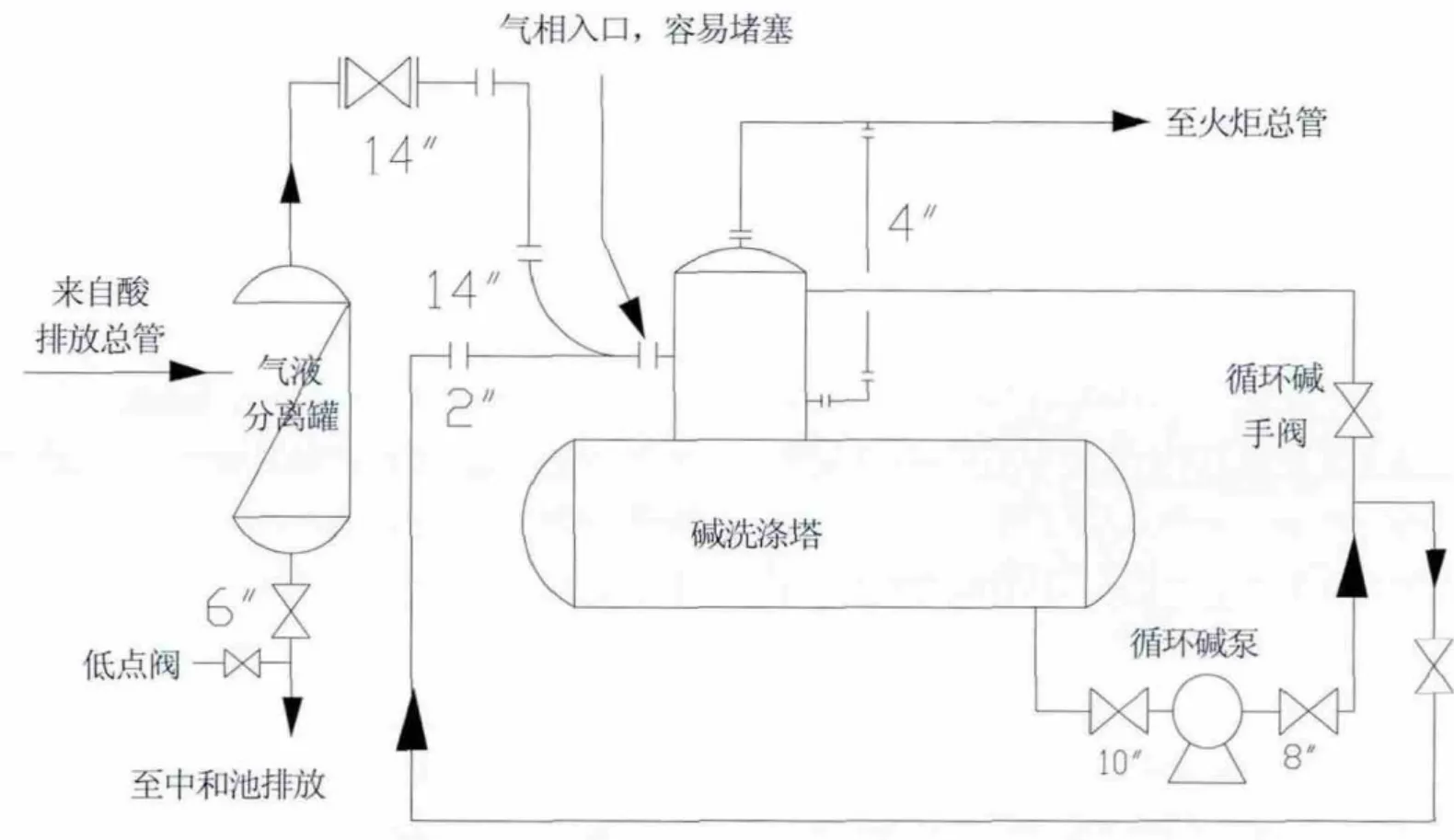
圖1 堿洗滌塔系統物料流向示意圖
烷基化裝置堿的洗滌塔在日常運行中經常會出現的問題有:
1)堿洗滌塔氣相入口處堵塞,造成酸區的酸性不凝氣無法排放,導致酸區排放總管超壓;以及該處2〞堿噴射管線堵塞,造成無堿液與酸氣中和,降低了堿塔中和酸氣的能力。為此,需要專業人員定期拆卸堿洗滌塔的入口三通管,然后人工清理堵塞部位。清理期間,需要使用吊車、搭建臨時工作平臺以及多人配合作業,可見其工作量之大。而且,清理時還需要停用酸排總管。總之,該項操作存在很多風險隱患。
2)雙法蘭液位計引壓管和現場玻璃板引壓管,造成無法準確指示堿液位。
3)循環堿孔板流量計引壓管,造成無法準確循環堿流量,導致循環堿泵投用聯鎖困難。
4)循環堿泵出口壓力表引壓管和現場壓力表,無法準確指示泵出口壓力,影響循環堿泵運行監護。
5)備用循環堿泵備用時間過長時,將造成盤車困難。嚴重時,需要拆泵頭修理。
6)循環堿泵低點排放閥和其他管線低點閥,采樣點引壓管和暖泵線。
7)循環堿采樣點引壓管線堵塞,造成無法采樣,需要停循環堿泵,由專業人員拆開、疏通。
2.從沉淀-溶解平衡理論角度得出沉淀-溶解常數
在無機化學中,一般把溶解度小于0.01g/100g H2O的電解質稱為難溶電解質。在含有難溶電解質固體的飽和溶液中,存在著固體電解質與由它溶解所生產的離子之間的平衡。這涉及到固相和液相離子兩相間的平衡,稱為多相離子平衡。
當溶解和結晶的速率相等時,建立起平衡,即為沉淀-溶解平衡。此時的溶液為飽和溶液。沉淀-溶解平衡是一種動態平衡,即固體在不斷溶解、沉淀也在不斷生成。
所以,堿液系統中有以下兩種主要化學平衡:
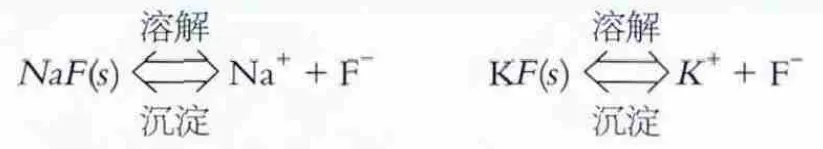
另外,還有微量Ca+,Mg+等陽離子,也與F-發生化學反應(從表6中,堿結晶體的分析數據可知)。顯然,這是一種多相離子平衡。與化學平衡一樣,固體物質的濃度不列入平衡常數表達式中。其標準平衡常數為:
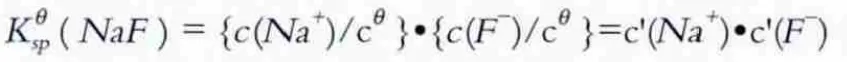
溶度積常數需要用實驗方法測定。溶度積常數和其他平衡常數一樣,也受溫度的影響,但影響不太大,通常可采用常溫下測得的數據。
根據沉淀的生成和溶解規律,將溶液中陽離子和陰離子的濃度(不管它們的來源)與標準濃度cq相比后,代入表達式,得到的乘積稱為離子積,用Q表示。把Q和相比較,有以下三種情況:
此即溶度積規則。它是判斷沉淀生成和溶解的重要依據。根據溶度積規則,在難溶電解質溶液中生成沉淀的條件是離子積大于溶度積。
可通過化學物性數據手冊查找出相應的物理參數,見表1。
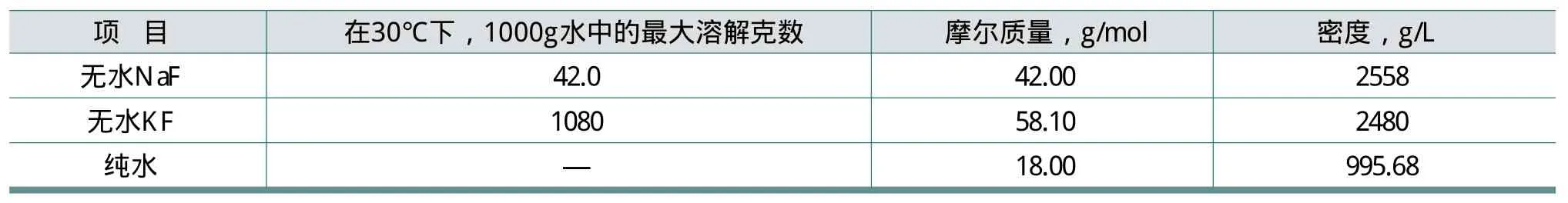
表1 相應的物理參數
通過表1可以看出,KF和NaF的密度大,加入1L水中后,它們的體積可以忽略不計,即溶液的體積仍然約為1L。由表1得到無水NaF在30℃下1000g水中的最大溶解克數為42.0。所以,無水NaF在30℃下、1000g水中的最大溶解度為42.0g/L。
然后,需要把溶解度單位由g/L換算成mol/L。已知NaF的摩爾質量為42.00g/mol,設NaF溶解度為cmol/L,可得:
由NaF的沉淀-溶解水解平衡,可知Na+和F-的溶解度相等(或者說平衡濃度),推算如下:
NaF飽和溶液的沉淀-溶解平衡:
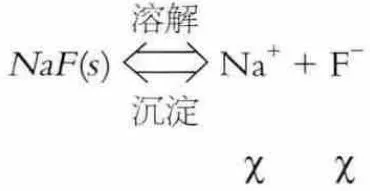
平衡濃度c'為mol/L
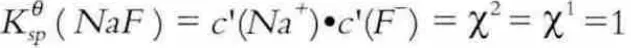
同理,得到
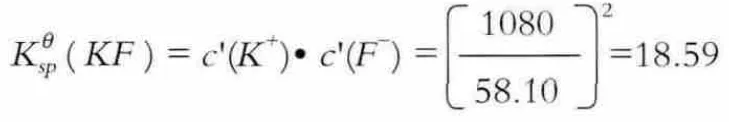
3.該理論在實際操作中的應用
3.1 循環堿樣數據分析
循環堿樣分析數據代入離子積計算公式進行分析,結果見表2。
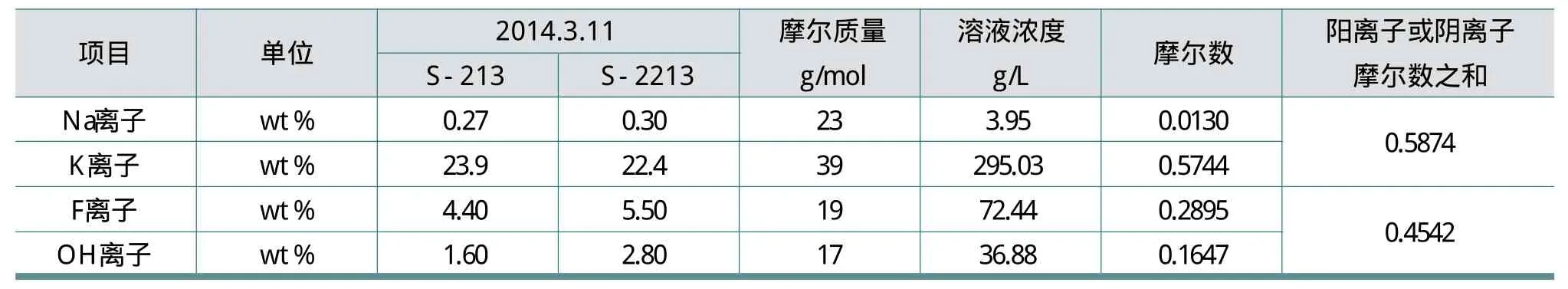
表2 采集循環堿樣品分析的數據
根據上面敘述的離子積Q的計算方法(堿液中實測的離子含量數據計算離子積Q),以堿液密度為1317.1g/L(質檢車間實測數據),計算2014年3月11日S-2213的分析數據如下:
Na+離子的含量為:0.3%×1317.1g/L=3.95g/L
F-離子的含量為:5.5%×1317.1g/L=72.44g/L
K+離子的含量為:22.4%×1317.1g/L=295.03g/L可得離子積
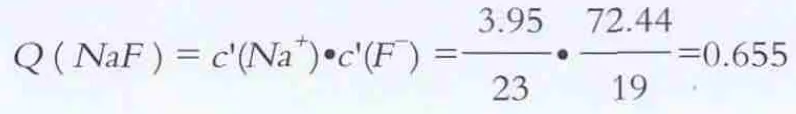
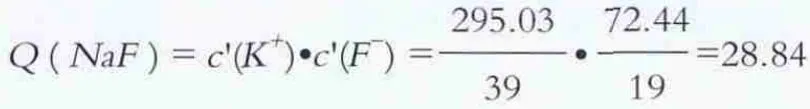
根據溶度積規則可以判斷出,溶液呈過飽和狀態時,有KF晶體從堿洗滌塔內堿溶液中會析出,直到堿溶液呈飽和狀態。
但是,堿洗滌塔實際上并未出現大量的堿結晶體析出,只有易結晶部位出現管線堵塞。出現這種分析誤差的原因有三:一是實際的堿液溫度約60℃,理論計算的堿液溫度為30℃,溫度高可以溶解更多的KF晶體;二是原子吸收分析方法出現分析誤差,即陽離子的摩爾數之和大于陰離子的摩爾數之和;三是由于堿液在堿洗滌塔系統中快速循環,造成懸濁的微小KF晶體存在堿液中。
以堿濃度為1317.1kg/m3或g/L(質檢車間實測數據),根據上面的計算公式,得出溶液濃度數據,見表3。再根據離子積Q的計算公式,得出不同組分的NaF在堿液中的離子積Q數據,見表4。
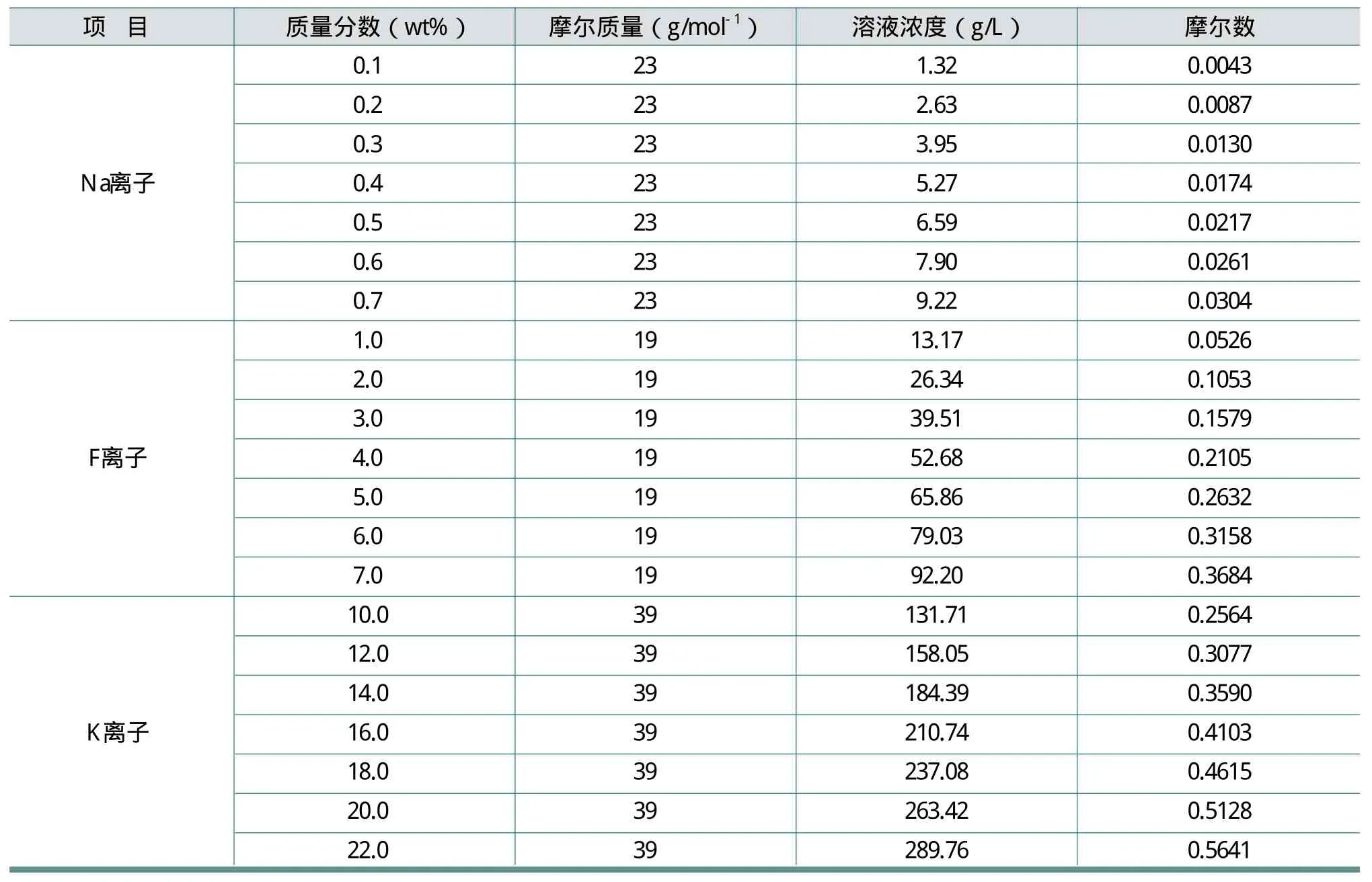
表3 堿洗滌塔的溶液濃度

表4 不同組分的NaF在堿液中的離子積
通過表3和表4的數據可以得出有代表性的結論:一是在Na離子質量分數為0.5%和F離子質量分數為5%時,將會后NaF晶體從堿液中析出;二是在K離子質量分數為16%和F離子質量分數為5%時,將會出現KF晶體從堿液中析出。
最后,根據離子積Q的計算公式,可以得出不同組分的KF在堿液中的離子積Q數據,見表5。
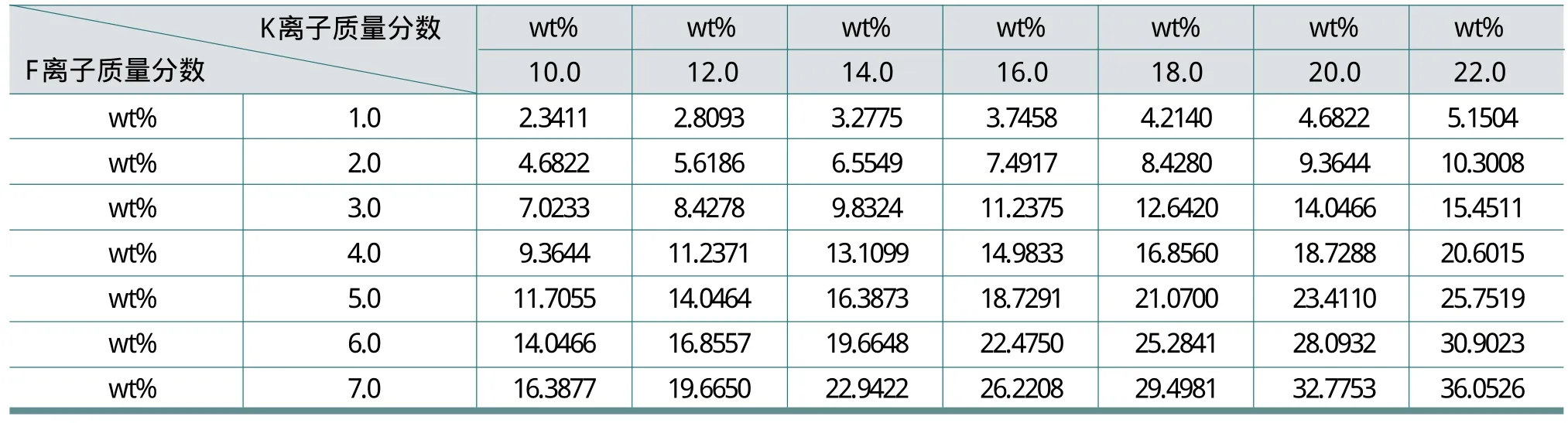
表5 不同組分的KF在堿液中的離子積
在日常操作中,由于各個易結晶的部位都遠離主管線,造成易結晶部位的溫度偏低(約為環境溫度,特別是冬季容易堿液結晶)。所以,表5中的離子積數據是以30℃的物理參數計算得出的。
3.2 從堿結晶體的組成數據進行分析
采取堿洗滌塔氣相入口處堿結晶體分析數據,見表6。
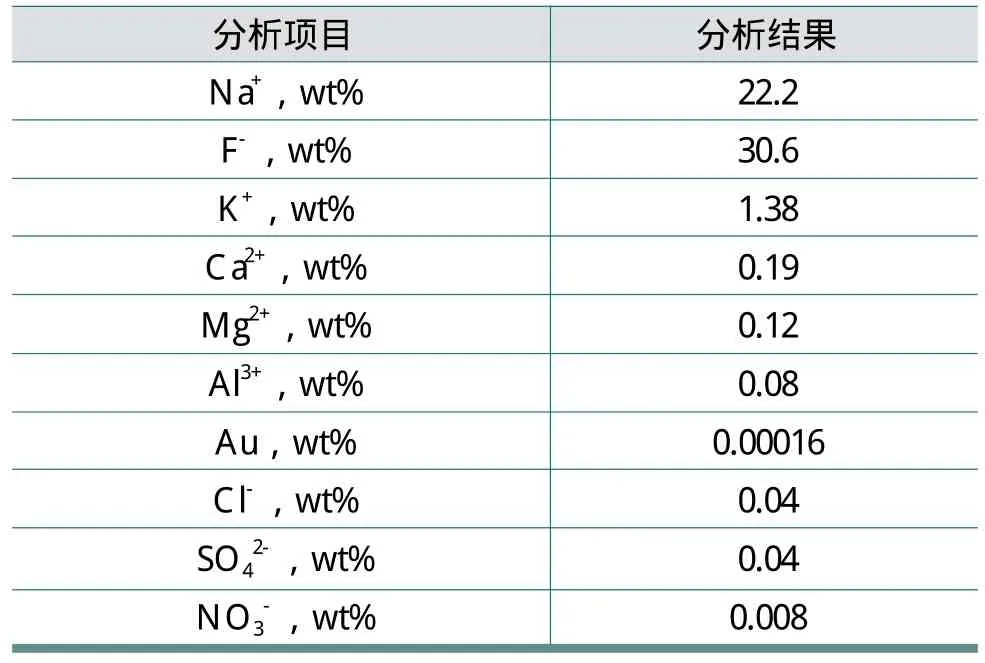
表6 C-207堿塔固體結晶物分析數據
通過分析表6,可知Na離子、F離子和K離子組分是結晶物的主要組成。出現這種情況的原因:一是2012年期間,對外購堿液中鈉離子的含量無有效監控,以至于其Na離子的含量高于現在的堿液。二是KF的沉淀-溶解常數是NaF的沉淀-溶解常數的18.59倍。在堿洗滌塔氣相入口處堿液不斷流動沖刷的過程中,溶解了部分KF結晶體,造成該處NaF結晶體的含量高于KF結晶體。
3.3 易堵塞部位原因分析
堿洗滌塔氣相入口處堵塞的原因:一是堿液中F離子、Na離子和K離子含量超標;二是由于該部位的特殊性,即2''堿噴射器噴出的堿液與酸排放總管的酸氣在該部位發生中和反應,造成該部位堿液中F離子的含量高于其他部位;三是酸排總管末端吹掃氮氣的流量偏小,造成進入堿洗滌塔的酸氣濃度過高;四是2''堿液噴射器噴出的堿液流速過小,造成堿液無法迅速留進塔內,以至于堿液中懸浮的結晶體靜止沉淀、聚集堵塞管線。
雙法蘭液位計引壓管、現場玻璃板引壓管和循環堿采樣點引壓管線等部位易堵塞的原因:一是堿液中F離子、Na離子和K離子的含量超標;二是這些部位內的堿液處于相對靜止狀態;三是這些部位遠離主管線,造成其內部堿液的溫度低于堿液系統的溫度(飽和堿液的溫度降低時,造成溶解度降低,導致堿液析出結晶體)。
4.針對堿結晶應采取的控制手段及建議
1)通過定期采樣分析,嚴格監控堿洗滌塔內堿液中氟離子質量分數≤0.4%或者KF的質量分數≤1.2%。根據UOP詳細操作規程,KOH溶液中通常保持7~10%wt的KOH、0~3%wt的KF(折合成F離子質量分數為0~0.098%)。為了使KOH循環液中的KOH保持高含量、KF保持低含量,循環KOH須用Ca(OH)2進行再生。目前,撫順洗化廠堿洗滌塔內堿液中的F離子含量嚴重超標,因此需要采取措施降低F離子的含量。
2)嚴格監控外購堿液的主要質量指標:KOH質量分數≥18%,Na離子質量分數≤0.1%,F離子含量≤0.1%;
3)嚴格地將2''堿噴射器噴出的堿液流量監控在合適的范圍;
4)嚴格地將酸排放總管末端氮氣吹掃流量監控在3Nm3/h。
5.結論
烷基化裝置堿洗滌塔入口管線經常堵塞,影響撫順洗化廠的長周期平穩運行,是長期困擾洗化廠的難題。
通過嚴格監控堿液的組成和進行適當的工藝調整,可有效解決堿洗滌塔結晶帶來的一系列問題。因此,該項調整操作對防止KOH容器內堿結晶具有可參考性和應用價值。
解決好影響烷基苯裝置安、穩、長、滿、優運行的問題,是洗化技術專家和操作工人長期不懈努力從事的工作。為了烷基苯裝置實現安、穩、長、滿、優運行,我們將繼續持之以恒、不斷深入地查找并探討解決目前存在的影響生產的各種隱患。
[1]烷基化裝置操作規程[Z].
[2]烷基化裝置開、停工詳細操作規程[Z].
[3]劉光啟,馬連湘,劉杰.化學化工物性數據手冊[M].2002.5.
[4]夏清,陳常貴.化工原理[M].天津:天津大學出版社,2005.
[5]高職高專化學教材編寫組.無機化學-2版[M].北京:高等教育出版社,2000(2001年重印).

