微波輔助離子液體中銅摻雜TiO2光催化劑的制備及微波強化光催化活性
王雷清,施忠芬,畢先鈞
(1.云南師范大學化學化工學院,云南昆明 650500;2.云南農業職業技術學院畜牧獸醫系,云南昆明 650031)
水污染日益成為困擾我國環境工作者的主要問題,國家相關部門也在污水治理方面竭盡全力,但目前全國的污水處理率僅為20%[1]。半導體催化劑TiO2可以吸收紫外光發生本征激發,形成電子-空穴對,電子和空穴分別向催化劑表面轉移,與有機物發生氧化還原反應,使其最終降解為無機小分子,達到污水處理的目的[2]。但是,TiO2的禁帶較寬(Eg=3.2 eV),對可見光的響應差,因此,部分研究者希望通過金屬摻雜、非金屬摻雜、金屬或非金屬元素共摻雜、復合材料負載等方法實現:①拓展TiO2對可見光的響應,使其吸收波長從紫外光區向可見光區移動;②提高TiO2光催化效率,使該項技術能用于處理大氣環境污染物、工業廢水和生活污水中的有機污染物[3-9]。
近年來,微波在處理環境污染物如染料、酚等有機污染物中的應用越來越廣泛。微波本身降解效果不理想,與紫外光等其他物理場協同作用時效果較好[10]。Yang等[11]用微波、紫外光協同效應降解五氯酚廢水,以雙氧水為催化劑,降解效果較好,雙氧水產生的羥基增強了微波、紫外光的協同降解效能。郭雅靜等[12]用微波-紫外輻射降解苯酚,機理研究表明,苯酚降解時苯環生成苯氧類及苯醌類,后開環形成小羧酸分子,最終降解為二氧化碳和水,降解率可達到65%左右。此外,微波是一種先進的體相加熱手段,被廣泛用于材料制備。在微波爐中微波以2 450 MHz的振蕩頻率穿透物質,微波爐內的極性分子,如水、有機污染物等以每秒24.5億次的速度快速振蕩,并且分子極性越大,振蕩的幅度越大,升溫速度越快。
離子液體的表面張力小,可以均勻成核,形成的顆粒比表面積大,作為一種新型溶劑在納米材料的制備中被廣泛采用。此外,有文獻報道,在離子液體中制備納米TiO2,由于離子液體的存在,可以抑制TiO2由銳鈦礦型向金紅石型的轉變,同時增大催化劑的比表面積和表面羥基含量[11-14]。
本課題組開展了微波輔助離子液體介質中金屬離子摻雜TiO2光催化劑的制備,以及微波強化光催化活性的研究,旨在進一步提高TiO2催化劑的光催化活性[15-16]。根據文獻報道,金屬離子Cu2+摻雜能夠使TiO2催化劑的光催化性能得以提高[17]。本文進一步研究微波輔助離子液體介質中Cu2+摻雜TiO2光催化劑的制備,并考察在紫外光照降解條件下,微波輻射對其降解甲基橙的強化作用,以求進一步改善金屬離子摻雜型TiO2催化劑的光催化性能。
1 實驗部分
1.1 試劑與儀器
硝酸銅、鈦酸丁酯、1-甲基咪唑、溴代正丁烷均為分析純。
XH-300UL電腦微波超聲波紫外光組合催化合成儀;XH-200A電腦微波固液相合成/萃取儀;NOVE2000-e型表面分析儀;XL30ESEM-TMP型掃描電子衍射顯微鏡;Ten Sor27型紅外光譜儀。
1.2 TiO2-Cu催化劑的制備
TiO2-Cu催化劑的制備過程為,在250 mL燒杯中加入17.5 mL乙醇、一定量離子液體、3.4 mL鈦酸丁酯,混合攪拌均勻,得混合液。將一定量的硝酸銅溶于二次蒸餾水中,逐滴加入上述混合液中攪拌1 h,得白色溶膠。抽濾、洗滌,得白色凝膠,微波干燥后進行煅燒,即得不同條件下制備的TiO2-Cu催化劑,置于干燥器中備用。
1.3 光催化活性的測定
光催化降解反應在電腦微波超聲波組合催化合成儀中進行。每次實驗向盛有50 mL 10 mg/L甲基橙溶液的250 mL燒杯中加入50 mg TiO2-Cu催化劑,放入催化合成儀中,恒溫(25℃)條件下,分別在微波(500 W)、250 W高壓汞燈(波長為365 nm)和微波(500 W)-高壓汞燈(250 W)(分別簡寫為MW、UV和MW-UV)3種條件下作用2 h(反應器距紫外光源15 cm)。反應完成后取5 mL降解液轉入潔凈離心管中,放入離心機以4 000 r/min兩次離心,離心時間為20 min。取上層清液用可見分光光度計于最大吸收波長(464 nm)處測定吸光度A,計算降解率η=(A0-A)/A0×100%(其中A0為甲基橙降解前的吸光度,A為甲基橙降解后的吸光度)。
催化劑的可見光光催化測試:將甲基橙溶液放入燒杯中,加入一定量的光催化劑后,將其置于昆明市呈貢區云南師范大學校園內的合適地方,在中午12:00至下午4:00時間段的太陽光下照射后,參照以上分析步驟計算甲基橙降解率。
空白實驗表明,在沒有催化劑只有光照的情況下,甲基橙溶液的濃度不變;在有催化劑存在而無光照時,室溫下放置相同時間后,甲基橙溶液的濃度也無明顯變化。考察催化劑樣品重復使用次數時,把靜置1 d的降解液除去上層清液后,首先將樣品進行烘干,然后在一定溫度下進行煅燒處理,以除去催化劑表面吸附的雜質后,再重復前面的降解步驟。
2 結果與討論
2.1 離子液體用量對TiO2-Cu光催化活性的影響
離子液體用量對催化劑的光催化活性影響見圖1。
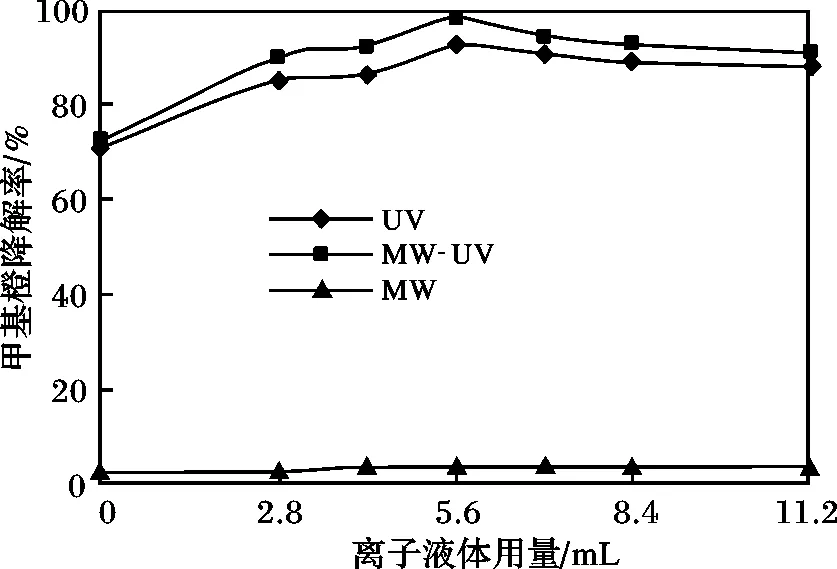
圖1 離子液體加入量對TiO2-Cu光催化活性的影響Fig.1 The influence of volume of the ionic liquids on TiO2-Cu photo-catalytic activity
由圖1可知,隨著離子液體加入量的增加,甲基橙的降解率先迅速升高后略有下降。當離子液體加入量為5.6 mL時,甲基橙的降解率達到極大值,在MW、UV、MW-UV 3種條件下,甲基橙降解率分別為3.78%,92.98%,98.39%,并且 3 種降解條件下的降解率始終是MW-UV>UV>MW,這說明在用紫外光照降解甲基橙時,微波輻射具有強化TiO2-Cu催化降解甲基橙的作用;當離子液體加入量大于5.6 mL時,由于離子液體用量的增多,使催化劑表面的羥基更易于形成氫鍵,致使TiO2-Cu光催化活性反而下降。因此,離子液體最佳加入量為5.6 mL。
離子液體用量分別為 2.8,5.6,7.0 mL 條件下制得的TiO2-Cu催化劑IR圖,見圖2。

圖2 不同離子液體用量制備TiO2-Cu紅外譜圖Fig.2 IR spectrum of TiO2-Cu at different ionic liquid dosageA.2.8 mL;B.5.6 mL;C.7.0 mL
由圖 2可知,3條曲線在 3 421.6 cm-1和1 631.7 cm-1均有分別屬于羥基的伸縮振動和彎曲振動吸收峰,且峰面積從上到下先增大后減小。由于催化劑中羥基的數目增加,致使TiO2-Cu的光催化活性得以提高;但當離子液體量達到7.0 mL時,曲線C出現了氫鍵特征吸收峰,這表明催化劑中羥基的數目減少,導致催化劑光催化活性降低。相關文獻報道,羥基是活性物種,可以引起物質的氧化反應,是主要氧化劑之一。催化劑中羥基數目的增多,紫外光照時易形成活性羥基,其催化活性就較高;在紫外光照射條件下,若同時再施以微波輻射作用,則微波電磁場的作用會使反應體系溫度快速升高(催化降解反應屬于分解反應,為吸熱反應),從而加快了光催化反應的進行,必然會產生更多的中間體;另一方面,中間體在微波場的作用下,發生高速振動,導致中間體的鍵斷裂,形成小分子,促進了自由基反應的進行,從而使催化劑的光催化活性得以提高。
2.2 微波干燥功率對TiO2-Cu光催化活性的影響
圖3為微波干燥功率對TiO2-Cu光催化活性的影響。

圖3 微波干燥功率對TiO2-Cu光催化活性的影響Fig.3 The influence of microwave drying power on TiO2-Cu photo-catalytic activity
由圖3可知,隨著微波干燥功率的增加,甲基橙的降解率先迅速增加后略有下降,當微波干燥功率為210 W時,甲基橙的降解率達到極大值。微波干燥主要是除去凝膠中的水分,水分子是極性分子,微波作用時極性分子的劇烈運動產生相互碰撞,摩擦生熱,使液態水迅速升溫氣化而達到干燥的目的。微波是體加熱,使催化劑內部和外部可以均勻受熱,此功率下催化劑可以有效干燥,去除自由移動的水分,利于研磨,使所得到的催化劑的粒徑比較均勻,團聚較少,催化劑的比表面積增大,進而促進催化劑與甲基橙溶液充分接觸,提高了催化劑對甲基橙的降解率。但微波功率過大時,催化劑表面自由移動的水分出去后,結合水及表面的羥基會繼續失水,造成催化劑表面的羥基數目減少,活性位點降低,致使催化劑的光催化活性下降[15-16]。因此,最佳微波干燥功率為210 W。
2.3 微波干燥時間對TiO2-Cu光催化活性的影響
圖4為微波干燥時間對TiO2-Cu光催化活性的影響。
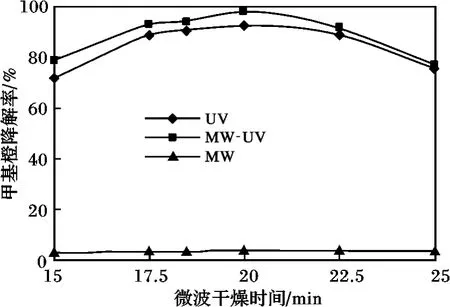
圖4 微波干燥時間對TiO2-Cu光催化活性的影響Fig.4 The influence of microwave drying time on TiO2-Cu photo-catalytic activity
由圖4可知,隨著干燥時間增加,甲基橙的降解率先增加后下降,當微波干燥時間為20 min時,甲基橙的降解率達到極大值。微波干燥時間較短時,凝膠中的水分不能充分汽化,研磨就不能充分進行,粒子團聚現象就嚴重,導致所制得的催化劑在紫外光照時形成的電子-空穴對易堆積發生復合;但微波干燥時間過長時,水分完全汽化,凝膠表面的Ti─OH鍵會發生斷裂,致使分子脫水,制得的催化劑表面的Ti─OH鍵數目減少,紫外光照射時,Ti─OH鍵斷裂形成的活性羥基數目少,微波輻射時活性位點減小,從而導致催化劑的光催化活性降低。因此,最佳微波干燥時間為20 min。
2.4 煅燒溫度對TiO2-Cu光催化活性的影響
圖5為煅燒溫度對TiO2-Cu光催化活性的影響。
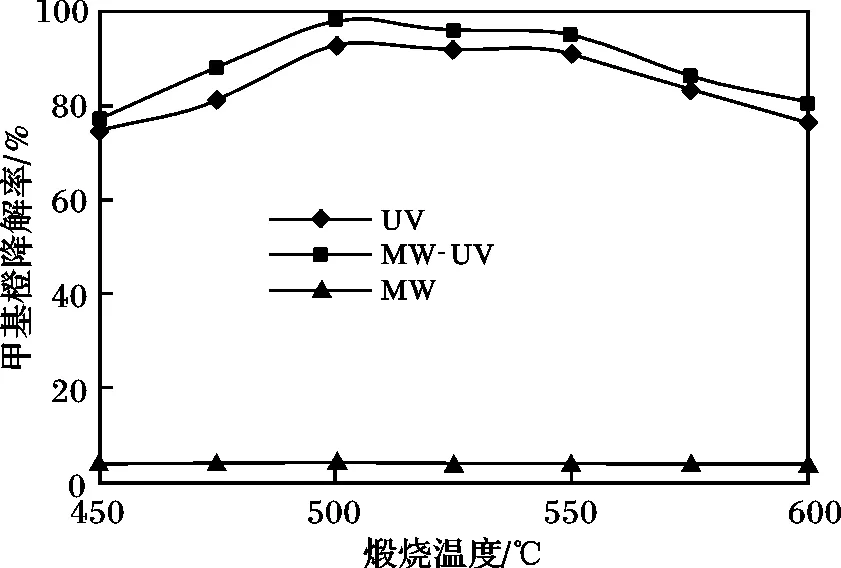
圖5 煅燒溫度對TiO2-Cu光催化活性的影響Fig.5 The influence of calcined temperature on TiO2-Cu photo-catalytic activity
由圖5可知,煅燒溫度對催化劑活性的影響較大,隨著煅燒溫度升高,甲基橙的降解率先增大后減小,當煅燒溫度為500℃時,甲基橙的降解率達到極大值,在MW、UV、MW/UV 3種條件下,甲基橙降解率分別為 3.78%,92.98%,98.39%,并且 3 種降解條件下的降解率始終是MW/UV>UV>MW,這進一步說明在用紫外光照降解甲基橙時,微波輻射具有強化TiO2-Cu催化降解甲基橙的作用。分析其原因為:當煅燒溫度恰當時,催化劑中TiO2主要以銳鈦礦型存在(2θ:25.459,37.900,48.141,54.117,55.104,62.918,68.842,70.405,75.195 與標準比色卡84-1286銳鈦礦型二氧化鈦特征衍射角一致),銳鈦礦型TiO2表面有更多的羥基與鈦元素相連,經紫外光照射時,銳鈦礦型催化劑可以吸收紫外光子的能量發生電子的躍遷,產生電子-空穴對;再加上微波輻射作用時,可以使催化劑表面的羥基迅速受熱,生成游離基團,同時微波可以抑制電子-空穴對的復合,催化劑表面溫度升高,羥基和空穴成為活性位點,使有機污染物被氧化,生成小分子的化合物[11-12,14-16]。因此,最佳煅燒溫度為 500 ℃。
圖6為煅燒溫度分別為 475,500,550℃時TiO2-Cu催化劑的紅外譜圖。

圖6 不同煅燒溫度下TiO2-Cu紅外譜圖Fig.6 IR spectrum of TiO2-Cu at different calcined temperatureA.475 ℃;B.500 ℃;C.550 ℃
由圖6可知,3個溫度條件下,羥基的伸縮振動特征吸收峰分別出現在 3 421.6,3 421.6,3 419.7 cm-1處(1 350.1 cm-1處的吸收峰屬于Ti─OH的特征吸收峰),而Ti─O─Ti鍵的伸縮振動吸收峰分別出現在634.6,646.1,592.1 cm-1處,這表明溫度低于500℃時,溫度升高,羥基的伸縮振動吸收峰沒有發生變化,Ti─O─Ti鍵的伸縮振動吸收峰向高波數方向移動,催化活性增強;溫度高于500℃時,隨著溫度升高,羥基和Ti─O─Ti鍵的伸縮振動吸收峰均向低波數方向移動,催化活性隨之下降。
2.5 煅燒時間對TiO2-Cu光催化活性的影響
圖7為煅燒時間對TiO2-Cu光催化活性的影響。
由圖7可知,隨著煅燒時間的增長,甲基橙的降解率先增加后降低,當煅燒時間為2 h時,甲基橙的降解率達到極大值,在MW、UV、MW/UV 3種條件下,甲基橙降解率分別為 3.78%,92.98%,98.39%,并且3種降解條件下的降解率始終是MW/UV>UV>MW,這同樣說明在用紫外光照降解甲基橙時,微波輻射具有強化TiO2-Cu催化降解甲基橙的作用。當煅燒時間為2 h時,催化劑顆粒沒有出現燒結現象,其擁有較高的比表面積,可以與溶液充分接觸,致使催化劑具有較高的光催化活性;而煅燒時間過長時,催化劑顆粒出現過度燒結現象,晶型被破壞,表面的羥基也會發生變化,使晶面的催化活性位點減少,甚至消失,導致其光催化活性降低。因此,最佳煅燒時間為2 h。

圖7 煅燒時間對TiO2-Cu光催化活性的影響Fig.7 The influence of calcined time on TiO2-Cu photo-catalytic activity
2.6 銅摻雜量對TiO2-Cu光催化活性的影響
圖8為銅摻雜量TiO2-Cu光催化活性的影響。

圖8 銅摻雜量對TiO2-Cu光催化活性的影響Fig.8 The influence of n(Cu)/n(Ti)mole ratio on TiO2-Cu photo-catalytic activity
由圖8可知,隨著銅摻雜量的增多,甲基橙的降解率先升高后下降,在銅摻雜量為n(Cu)/n(Ti)=0.025時,甲基橙的降解率達到極大值,在MW、UV、MW/UV 3種條件下,甲基橙降解率分別為3.78%,92.98%,98.39%,并且3種降解條件下的降解率始終是MW/UV>UV>MW。其原因可能是銅摻雜量較低時,銅元素摻入到TiO2晶格的間隙位,Cu2+的價電子排布為d9,易得電子,形成穩定結構,故成為電子的接受體,延長了TiO2中電子-空穴的復合時間,使其光催化活性提高。
不同銅摻雜量條件下制備的TiO2-Cu催化劑的紅外光譜,見圖9。

圖9 不同銅摻雜量條件下制備TiO2-Cu的IR譜圖Fig.9 IR spectrum of TiO2-Cu at different Cu/Ti molar ratioA.n(Cu)/n(Ti)=0;B.n(Cu)/n(Ti)=0.010;C.n(Cu)/n(Ti)=0.025
由圖9可知,銅摻雜量n(Cu)/n(Ti)分別為0,0.010,0.025 條件下,羥基的伸縮振動吸收峰依次出現在 3 419.7,3 421,3 421 cm-1處,這表明銅摻雜后,羥基的伸縮振動吸收峰向高波數方向移動,羥基的能量提高,催化劑的光催化活性增強。由于Cu2+具有較強的溶劑化作用,易于羥基的附著,紫外光照射時,在銅的表面可以累積更多的表面羥基,形成游離活潑羥基,羥基可以有效的吸收微波能,使局部溫度迅速升高,加快自由基反應,甲基橙迅速被氧化為小分子二氧化碳和水。
不同銅摻雜量條件下制備的TiO2-Cu催化劑的XRD圖,見圖10。
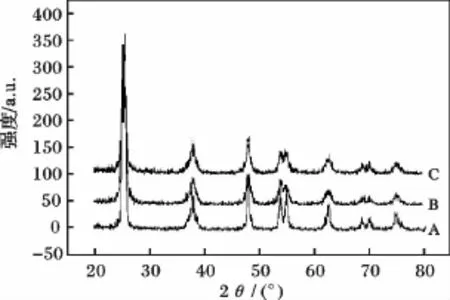
圖10 不同銅摻雜量條件下制備TiO2-Cu的XRD圖Fig.10 XRD pattern of TiO2-Cu at different Cu/Ti molar ratioA.n(Cu)/n(Ti)=0;B.n(Cu)/n(Ti)=0.010;C.n(Cu)/n(Ti)=0.025
根據jade軟件分析,101晶面的粒徑分別為17.8,10.9,13.4 nm,與沒有摻雜的純 TiO2相比,銅摻雜后TiO2-Cu的粒徑減小。Cu2+與Ti4+離子半徑相近,Cu的3d電子數較多,更易于與O結合,替換TiO2晶格中的Ti,使晶格畸變,鍵長和鍵角發生變化,從而造成TiO2-Cu粒徑變小[18];另外,晶格畸變使分子的極性增大,表面的氫鍵打開,在微波輻射作用下,催化劑表面形成活性羥基,再加之紫外光照射時引發自由基反應,有機物被礦化,最終形成無污染的小分子,使催化劑的光催化活性提高。
由圖10可知,與純TiO2相比,銅摻雜后TiO2-Cu催化劑部分晶面的不對稱性提高,極性增強,在微波輻射作用下,可以迅速啟動極性基團的定向振動,使TiO2-Cu表面的水脫附下來,形成羥基,再加之紫外光照射時催化劑吸收光子的能量,造成電子的躍遷,產生電子-空穴對,致使有機物中的鍵斷裂,形成新的中間產物,中間產物在微波的作用下,也會急速振動,體系溫度升高,有機污染物鍵被打開,致使其被氧化成無污染的小分子,從而導致催化劑的光催化活性提高。
2.7 可見光對TiO2-Cu光催化活性的影響
在可見光照條件下,TiO2-Cu對甲基橙溶液的降解率見表1。

表1 太陽光下TiO2-Cu對甲基橙的降解率Table 1 The degradation rate of methyl orange for TiO2-Cu in sun light
由表1可知,隨著可見光照射時間的延長,甲基橙的降解率逐漸提高,照射4 h時,甲基橙幾乎達到完全降解,這表明銅摻雜TiO2-Cu催化劑具有良好的吸收可見光的性能,也說明銅摻雜可以使銳鈦礦型TiO2的吸收帶紅移。彭金輝等[18]對銅、鐵、鎳元素摻雜銳鈦礦型TiO2進行了第一性原理計算,得出摻雜銳鈦礦相TiO2活性提高最顯著的金屬元素為銅,銳鈦礦型TiO2的禁帶寬度為3.2 eV,銅元素摻入間隙位、橋位、置換位,禁帶寬度分別為1.984,1.907,1.775 eV,銅比鐵、鎳更易取代 TiO2中的鈦原子,銅處于置換位時禁帶寬度最窄。
2.8 TiO2-Cu的SEM表征及比表面積分析
離子液體用量5.6 mL,硝酸銅與鈦酸丁酯的物質的量比為0.025,微波干燥時間20 min,干燥功率210 W,煅燒溫度550℃,煅燒時間2 h條件下,制備TiO2-Cu催化劑的SEM,見圖11。
由圖11可知,TiO2-Cu催化劑的粒徑為納米級別,微粒近似球形,球形的比表面積較大,穩定性較好,可以充分接觸甲基橙溶液,提高催化活性。
最佳條件下制備TiO2-Cu對氮氣的吸附脫附,見圖12,BET法求得煅燒溫度為500℃時,催化劑的比表面積為 85.201 m2/g,孔容積為 0.162 9 cm3/g,平均孔徑為3.825 nm。圖13為TiO2-Cu催化劑的半孔寬與孔容積及導數關系圖,利用DFT方法分析求得催化劑的半孔寬為2.171 4 nm。

圖11 TiO2-Cu催化劑的SEM圖Fig.11 SEM spectrum of TiO2-Cu catalyst

圖13 TiO2-Cu催化劑的DFT曲線Fig.13 DFT analysis of TiO2-Cu catalyst
從以上分析數據可以看出,TiO2-Cu催化劑的比表面積較大,增加了與降解物的接觸面,導致催化活性提高。另外,催化劑還擁有較高的孔容積、平均孔徑和半孔寬,這為光生-電子空穴對和活性羥基從催化劑表面形成后向溶液中移動提供了空間,同樣導致催化劑具有較高的光催化活性。
3 結論
(1)微波輔助離子液體中制備TiO2-Cu催化劑的最優條件為:離子液體用量5.6 mL,硝酸銅與鈦酸丁酯的物質的量之比為0.025,微波干燥時間20 min,干燥功率210 W,煅燒溫度500℃,煅燒時間2 h。
(2)TiO2-Cu催化劑在微波、紫外、微波-紫外3種降解條件下,甲基橙降解率分別為 3.78%,92.98%,98.39%。這表明在紫外光照條件下,微波輻射具有強化TiO2-Cu催化降解甲基橙的作用。
(3)TiO2-Cu催化劑具有粒徑均勻、比表面積、孔容積、平均孔徑和半孔寬都較大等特點,這也是TiO2-Cu催化劑擁有較高的光催化活性的主要原因。
[1]袁麗欣.淺談城市水污染問題及防治對策[J].科技資訊,2012,36(1):141-144.
[2]白玉娜,左勝利,于迎春.氮-硫共摻雜二氧化鈦光催化劑的制備及其可見光催化活性[J].化學研究,2013,24(4):355-360.
[3]Junya O,Akira Y,Kentaro T.Modification of metal nanoparticles with TiO2and metal-support interaction in photodeposition[J].ACS Catalysis,2011,1:187-192.
[4]蔣文建,孫婧,畢先鈞.微波助離子液體中S摻雜TiO2催化劑的制備及其微波強化光催化活性[J].化學工程與技術,2013,3(4):114-121.
[5]Wen Yanyuan,Ding Hanming.Preparation and photo-catalytic activity of Ag-AgCl modified anatase TiO2nanotubes[J].Chin J Cata,2011,32:36-45.
[6]楊艷瓊,王昭,畢先鈞.微波助離子液體中納米TiO2/PMMA復合材料的制備及光催化性能[J].分子催化,2008,22(4):362-367.
[7]Sun Qiong,Xu Yiming.Sensitization of TiO2with aluminum phthalocyanine:Factors influencing the efficiency for chlorophenol degradation in water under visible light[J].The Journal of Physical Chemistry C,2009,113:12387-12394.
[8]Zhang Lihong,Li Peijun,Zong Qiang.Photo-catalytic degradation of polycyclic aromatic hydrocarbons on soil surfaces using TiO2under UV light[J].Journal of Hazardous Materials,2008,158:478-484.
[9]Wang He,Lu Z G,Xi L J,et al.Facile and rapid synthesis of highly porous wire like TiO2as anodes for lithium-ion batteries[J].ACS Applied Materials & Interfaces,2012,4:1608-1613.
[10]楊波,余剛,趙緒新.物理場協同作用降解有機污染物研究進展[J].環境污染與防治,2010,32(8):66-70.
[11]Yang Shaogui,Fu Hongbo,Sun Cheng,et al.Rapid photocatalytic destruction of pentachlorophenol in F-Si-co-modified TiO2suspensions under microwave irradiation[J].Journal of Hazardous Materials,2009,161(2):1281-1287.
[12]郭雅靜.微波紫外耦合輻射降解吸附態苯酚的研究[D].哈爾濱:哈爾濱工業大學,2011.
[13]Liu Z,Huang S,Wang W.A refined force field for molecular simulation of imidazolium-based ionic liquids[J].The Journal of Physical Chemistry B,2004,108(34):12978-12989.
[14]張桂琴,畢先鈞.微波助離子液體中鋅-鐵共摻雜納米TiO2光催化劑的制備及其光催化活性[J].化學研究,2011,22(5):55-62.
[15]孫婧,蔣文建,張桂琴,等.微波助離子液體中鋅摻雜納米TiO2的制備及微波強化光催化氧化活性[J].工業催化,2013,21(3):27-33.
[16]蔣文建,孫婧,畢先鈞.微波助離子液體中硫-釹共摻雜納米TiO2的制備及微波強化光催化氧化活性[J].工業催化,2013,21(9):32-37.
[17]胡慶華,張蔚萍,王建國.Cu2+/TiO2納米纖維摻雜比對一氯甲烷光催化降解的影響[J].無機鹽工業,2010,42(11):23-24.
[18]何承東,彭金輝.摻雜銳鈦礦型二氧化鈦光催化性能的第一性原理計算[D].昆明:昆明理工大學,2011.

