飼料蛋白水平對大規格草魚生長、飼料利用和氮代謝相關酶活性的影響
李 彬 梁旭方 劉立維 袁小琛 朱文歡 李 杰
?
飼料蛋白水平對大規格草魚生長、飼料利用和氮代謝相關酶活性的影響
李 彬 梁旭方 劉立維 袁小琛 朱文歡 李 杰
(華中農業大學水產學院, 農業部淡水生物繁育重點實驗室, 武漢 430070)
為探討飼料蛋白水平對草魚()生長、飼料利用和氮代謝的影響, 以魚粉和酪蛋白為蛋白源制備蛋白水平分別為15%、20%、25%、30%和35%的5種等能(13.71 kJ/g)飼料飼養草魚[(209±10) g] 8周。結果表明: 飼料蛋白水平對草魚的增重率、特定生長率、飼料效率均影響顯著(<0.05), 其中25%蛋白組最高。通過二次多項式的回歸分析得出: 當飼料蛋白水平為26.50%和27.20%的時候, 特定生長率和飼料效率分別達到最高。15%蛋白組的攝食率顯著高于其他蛋白組(<0.05)。蛋白質保留率和蛋白質效率隨蛋白水平的升高而顯著降低(<0.05)。各蛋白組的成活率、血清丙氨酸轉氨酶活性和血清天冬氨酸轉氨酶活性均無顯著差異(>0.05)。血清總蛋白、血清尿素氮、肝臟天冬氨酸轉氨酶活性、肝臟谷氨酸脫氫酶活性和肌肉腺苷酸脫氨酶活性隨蛋白水平的升高顯著增加(<0.05), 而肝臟丙氨酸轉氨酶活性先增加后穩定, 這表明高蛋白組(30%和35%蛋白組)相對于低蛋白組(15%和20%蛋白組)有較多的蛋白質用于分解代謝提供能量。
草魚; 蛋白質; 生長; 飼料利用; 氮代謝
蛋白質作為魚類配合飼料中重要的營養物質, 不僅能夠提供魚體合成蛋白質所需的氨基酸, 還能提供生長和代謝所需的能量[1], 是決定魚類生長的關鍵因素。飼料中蛋白質含量過低會限制魚體生長, 導致無法按時達到上市規格, 影響經濟效益。然而, 當飼料中蛋白質含量過高時, 不僅增加了飼料成本, 而且魚類通過氧化脫氨基作用將過量的蛋白質用于能量消耗或以脂肪的形式儲存起來而非用于體蛋白的沉積, 產生較多的氨氮排泄物, 從而導致養殖水體污染加重, 不利于魚類的生長和生態環境的可持續發展[2—4]。目前, 有關草魚的蛋白質研究大多集中在營養需求與飼料利用上, 對草魚氮代謝方面研究較少。
草魚()隸屬于鯉形目鯉科雅羅魚亞科草魚屬, 是我國優良養殖品種之一, 具有生長快、肉味鮮美、養殖成本低、市場容量大等特點。受養殖條件和實驗成本的影響, 關于草魚的研究多針對于草魚幼魚, 對大規格的草魚鮮有報道。然而大規格草魚是實際養殖中必經且重要的階段, 因此, 研究大規格草魚對實際生產具有重要的指導意義, 并產生更大的經濟效益。本實驗旨在探討飼料蛋白水平對大規格草魚生長、飼料利用、血清生化指標和氮代謝相關酶活的影響, 為大規格草魚飼料配方的優化提供理論依據和參考。
1 材料與方法
1.1 實驗飼料
以秘魯魚粉和酪蛋白為蛋白源, 魚油和大豆油為脂肪源制備5組不同蛋白水平的等能飼料。飼料蛋白實測值分別為15.65%、20.82%、25.88%、30.78%和36.01% (分別用15%、20%、25%、30%和35%表示), 飼料的蛋白能量比為11.47—26.38 mg/kJ, 飼料配方和實測飼料成分見表1。飼料原料購于武漢盛天宇飼料有限公司和武漢富龍飼料有限公司。飼料原料粉碎后全部通過60目篩, 按照添加量從小到大的順序逐級攪拌混勻, 用顆粒飼料機制成直徑 3 mm的硬顆粒飼料, 風干后于?20℃保存備用。
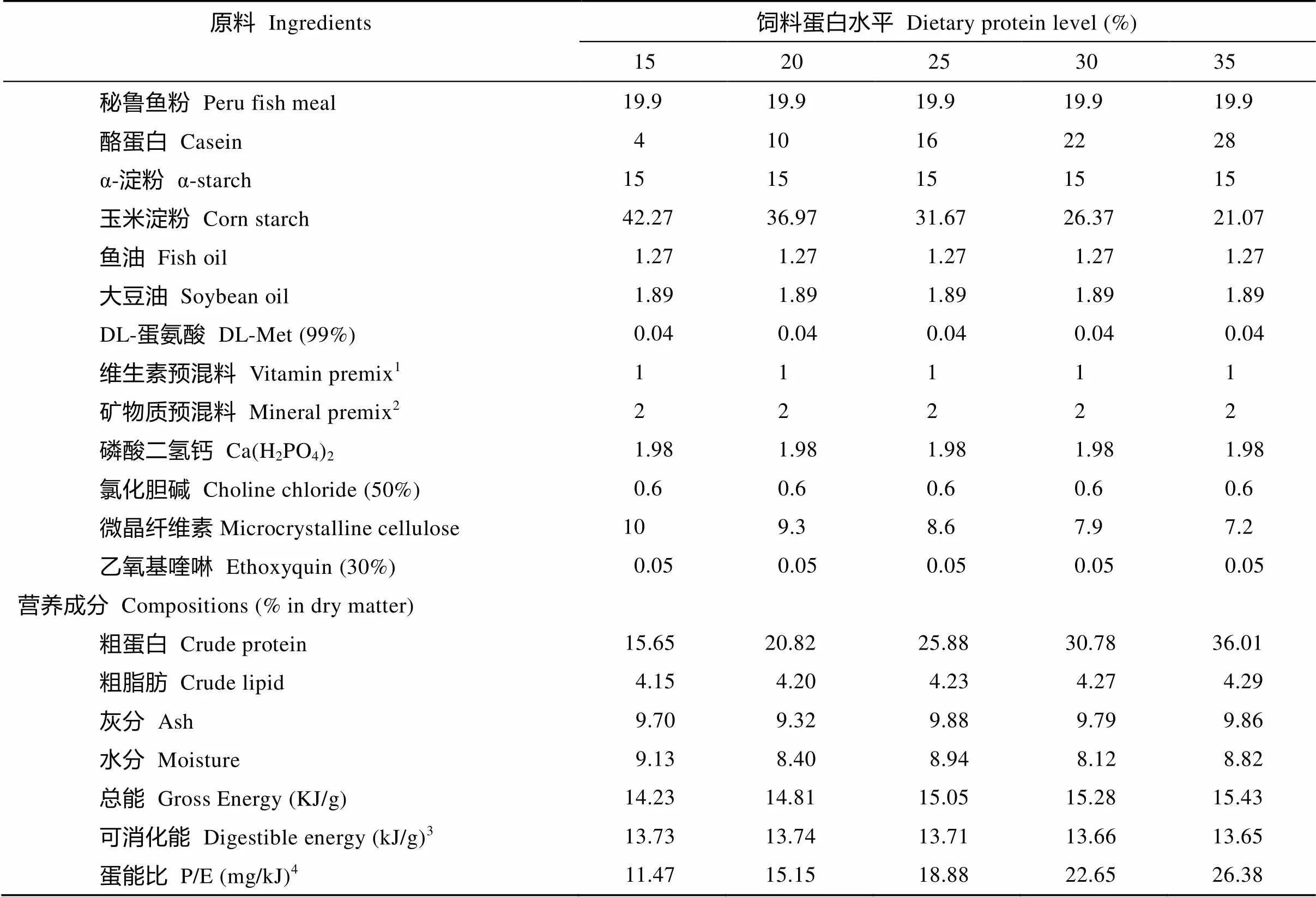
表1 實驗飼料配方和基本成分
注: 1. 維生素預混料(每千克飼料): 維生素A, 2000 IU; 維生素B1, 5 mg; 維生B2, 5 mg; 維生素B6, 5 mg; 維生素B12, 0.025 mg; 維生素D3, 1200 IU; 維生素E 21 mg; 維生素K32.5 mg; 葉酸, 1.3 mg; 生物素, 0.05 mg; 泛酸鈣, 20 mg; 肌醇, 60 mg; 抗壞血酸(35%), 110 mg; 煙酸, 25 mg; 2. 礦物質預混料(每千克飼料): 硫酸錳, 10 mg; 硫酸鎂, 10 mg; 氯化鉀, 95 mg; 氯化鈉, 165 mg; 硫酸鋅, 20 mg; 碘化鉀, 1 mg; 硫酸銅, 12.5 mg; 硫酸鐵, 105 mg; 亞硒酸鈉, 0.1 mg; 3. 可消化能計算值(蛋白質16.7 kJ/g, 脂肪37.6 kJ/g, 碳水化合物16.7 kJ/g)[5]; 4. 蛋能比: 蛋白mg/可消化能kJ
Note: 1. Vitamin premix (per kg of diet): vitamin A, 2000 IU; vitamin B1, 5 mg; vitamin B2, 5 mg; vitamin B6, 5 mg; vitamin B12, 0.025 mg; vitamin D3, 1200 IU; vitamin E 21 mg; vitamin K32.5 mg; folic acid, 1.3 mg; biotin, 0.05 mg; pantothenic acid calcium, 20 mg; inositol, 60 mg; ascorbic acid (35%), 110 mg; niacinamide, 25 mg; 2. Mineral premix (per kg of diet): MnSO4, 10 mg; MgSO4, 10 mg; KCl, 95 mg; NaCl, 165 mg; ZnSO4, 20 mg; KI, 1 mg; CuSO4, 12.5 mg; FeSO4, 105 mg; Na2SeO3, 0.1 mg; 3. Calculated digestible energy (16.7, 37.6 and 16.7 kJ/g for protein, lipid and carbohydrate)[5]; 4. P/E: Protein/Digestible energy
1.2 實驗用魚與飼養條件
養殖實驗在華中農業大學水產養殖基地的池塘中進行, 池塘平均水深約3 m。實驗所用草魚購自湖北省仙桃排湖漁場, 正式實驗前將草魚放入網箱 (2 m × 2 m × 2 m)中暫養, 每天8:00和16:00以商業飼料飽食投喂, 使之逐漸適應環境和配合飼料。暫養2周后, 對實驗魚饑餓 24h, 挑選出體格健壯、規格一致[(209 ±10) g] 的草魚隨機分入15(5個實驗組, 每組3個重復)個網箱(2m × 2m × 2m)中, 每個網箱12尾。整個實驗周期均定時(8:00, 16:00)采用飽食投喂, 實驗期為8周。實驗期間水溫27.5—33.5℃, pH 7.62—8.08, 溶氧>6 mg/L, 氨氮<0.5 mg/L, 亞硝酸鹽<0.15 mg/L, 光照周期為自然光照周期。
1.3 樣品收集與分析
養殖實驗開始前將6尾魚置于?80℃冰箱保存。在養殖實驗結束后, 實驗魚饑餓24h, 以MS-222麻醉(100 mg/L), 然后計數并稱重。每個網箱中取3尾魚置于?80℃冰箱中保存, 用于測定全魚粗蛋白含量。另取3尾魚以無菌注射器自尾靜脈取血, 然后解剖取背部肌肉和肝臟, ?80℃保存待測。將采集的血液樣品在37℃下凝血1—2h (不加抗凝劑), 4℃冰箱過夜(讓血塊凝固), 4℃條件下, 3000 r/min 離心10min, 小心吸取上層血清, ?80℃保存待測。
飼料和魚體常規成分測定采用AOAC(1995)的方法。水分含量在105℃烘箱中烘至恒重測定。粗蛋白含量采用凱氏定氮法(Kjeltec 2300 Analyzer, Foss Tecator, Sweden)測定樣品含氮量, 再乘以6.25得粗蛋白含量。粗脂肪采用索氏抽提法(乙醚為溶劑)。灰分含量在馬弗爐中 550℃灼燒至恒重測定。能量采用氧彈儀(Parr Instrument Company, Moline, IL, USA)測定。血清樣品送至武漢大學中南醫院檢測總蛋白、尿素氮、丙氨酸轉氨酶和天冬氨酸轉氨酶, 以上指標均采用全自動生化分析儀(Abbott Laboratories, Abbott Park, IL, USA)測定。肝臟中的丙氨酸轉氨酶、天冬氨酸轉氨酶、谷氨酸脫氫酶以及肌肉中的腺苷酸脫氨酶的活性均采用南京建成生物工程研究所試劑盒測定。酶活性單位定義: 在 37℃條件下, 每分鐘酶解1 μmol底物為1個活力單位(U)。組織勻漿液中蛋白濃度采用考馬斯亮藍法測定[6], 以牛血清白蛋白為基準物。
1.4 計算公式
增重率(Weight gain,, %)=100×(終末體重?初始體重)/初始體重;
特定生長率(Specific growth rate,, %/d)= 100×(ln末重?ln初重)/實驗天數;
成活率(Survival rate,, %)=100×成活魚尾數/投放魚尾數;
攝食率(Feed rate,, %BW/d)=100×總攝食量/ [實驗天數×(初總重+末總重)/2] ;
飼料效率(Feed efficiency rate,)=(終末體重?初始體重)/攝食量;
蛋白質保留率(Protein retention efficiency,, %)=100×(終末魚體蛋白質重?初始魚體蛋白質重)/蛋白質攝入量;
蛋白質效率(Protein efficiency ratio,)=(終末體重?初始體重)/蛋白質攝入量。
1.5 數據統計與分析
實驗數據采用“平均值±標準誤”表示, 使用統計軟件SPSS 17.0對實驗數據進行單因素方差分析(One-way ANOVA), 差異顯著時通過 Duncan’s方法進行多重比較, 以<0.05為差異顯著性標準。
2 結果
2.1 飼料蛋白水平對草魚生長和飼料利用的影響
由表2可知, 飼料蛋白水平對各組的成活率無顯著影響(>0.05), 而對增重率、特定生長率、飼料效率、攝食率、蛋白保留率和蛋白質效率均有顯著影響(<0.05)。25%蛋白組的增重率、特定生長率和飼料效率均最高, 顯著高于15%和35%蛋白組(<0.05), 但與30%蛋白組無顯著差異(>0.05)。15%蛋白組的攝食率顯著高于其他組(<0.05)。20%和25%蛋白組的蛋白質保留率顯著高于30%和35%蛋白組(<0.05), 但與15%蛋白組無顯著差異(>0.05)。隨著飼料蛋白水平的增加, 蛋白質效率逐漸降低, 30%和35%蛋白組的蛋白質效率無顯著差異(>0.05), 兩組均顯著低于15%、20%和25%蛋白組(<0.05)。
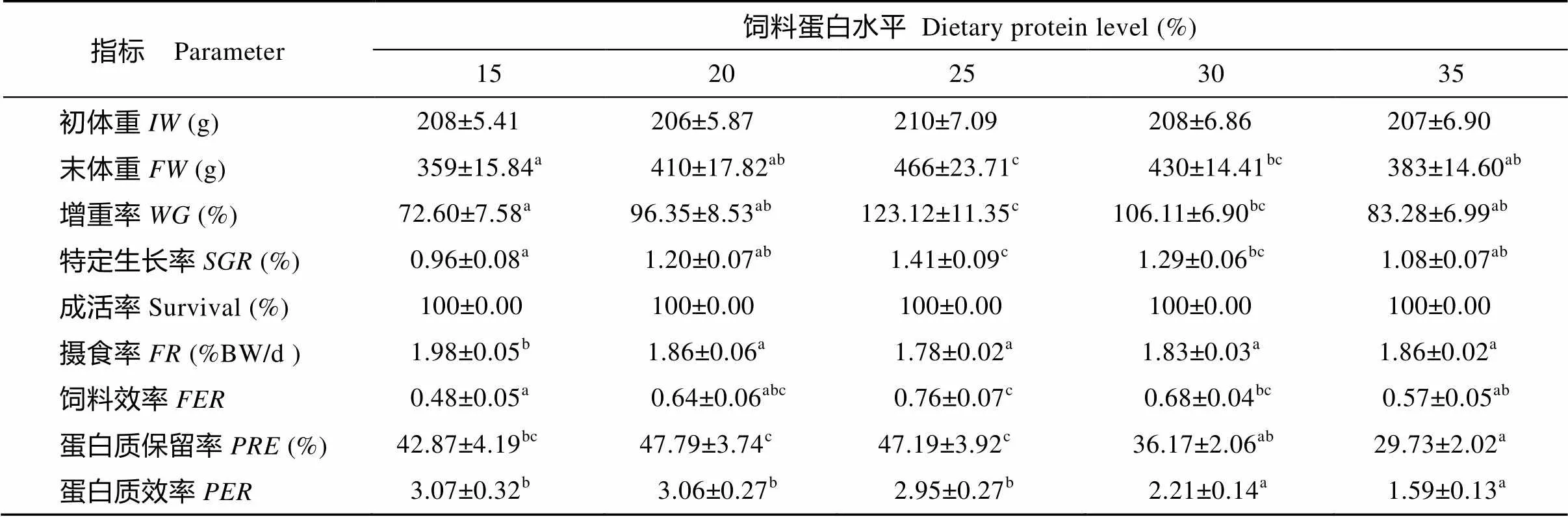
表2 飼料蛋白水平對草魚生長和飼料利用的影響
注: 表中數值(平均值±標準誤)為3個重復的平均值。數值后不同的上標字母表示差異顯著(<0.05),下同
Note: Values (mean±SE) are the means of triplicate. Values in each column with different superscripts have significant difference (<0.05). The same applies bellow
通過二次多項式的回歸分析, 得到增重率和飼料效率與飼料蛋白水平的關系, 回歸方程分別為:= –0.00342+ 0.1802–1.0504,2 = 0.9601 (圖1);= –0.00202+ 0.1088–0.7314,2 = 0.9623 (圖2)。當飼料蛋白水平為26.50%時, 草魚的特定生長率達到最高; 當飼料蛋白水平為27.20 %時, 草魚的飼料效率達到最高。
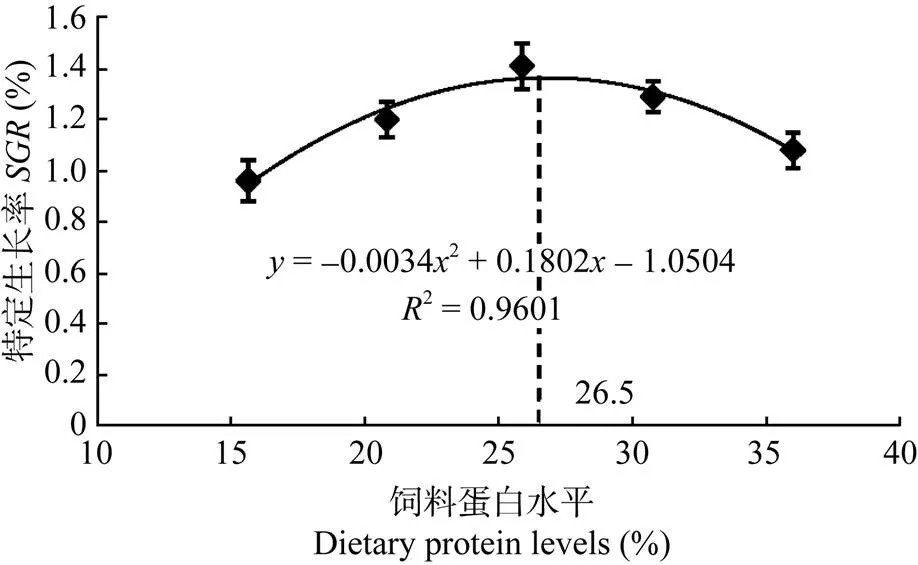
圖1 飼料蛋白水平對草魚特定生長率的影響
2.2 飼料蛋白水平對草魚血清生化指標的影響
由表3可以看出, 各組血清丙氨酸轉氨酶和天冬氨酸轉氨酶均無顯著性差異(>0.05)。30%和35%蛋白組血清總蛋白顯著高于15%蛋白組(<0.05), 20%和25%蛋白組與其他組無顯著性差異(>0.05)。血清尿素氮含量隨著飼料蛋白水平的升高而增加, 35%蛋白組顯著高于15%、20%和25%蛋白組(<0.05), 與30%蛋白組無顯著性差異(>0.05)。
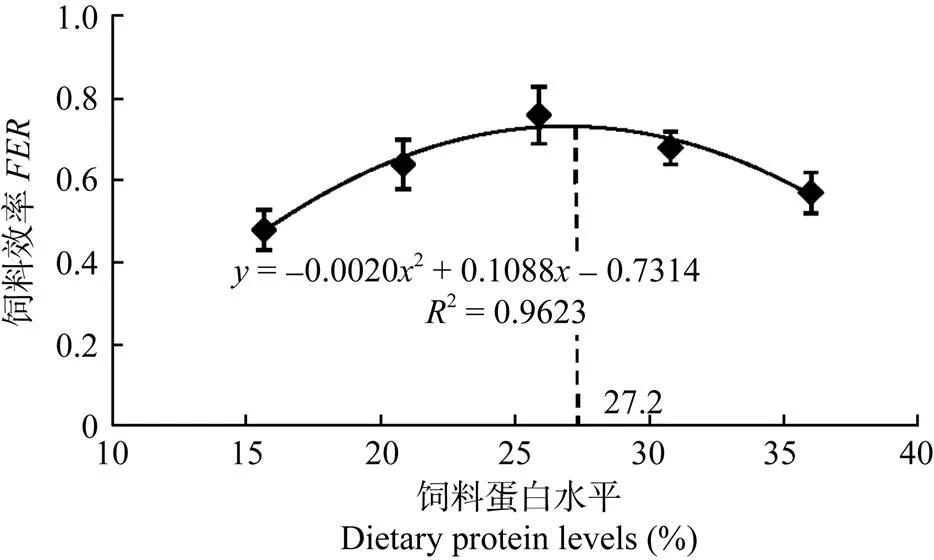
圖2 飼料蛋白水平對草魚飼料效率的影響
2.3 飼料蛋白水平對草魚氮代謝相關酶活性的影響
如表4所示, 25%、30%和35%蛋白組的肝臟丙氨酸轉氨酶活性顯著高于15%和20%蛋白組(<0.05), 15%和20%蛋白組之間無顯著性差異(>0.05)。肝臟天冬氨酸轉氨酶、谷氨酸脫氫酶和肌肉腺苷酸脫氨酶的活性隨著飼料中蛋白水平的增加而升高, 35%蛋白組顯著高于15%和20%蛋白組(<0.05), 15%和20%蛋白組之間無顯著性差異(>0.05), 30%和35%蛋白組之間無顯著性差異(>0.05)。
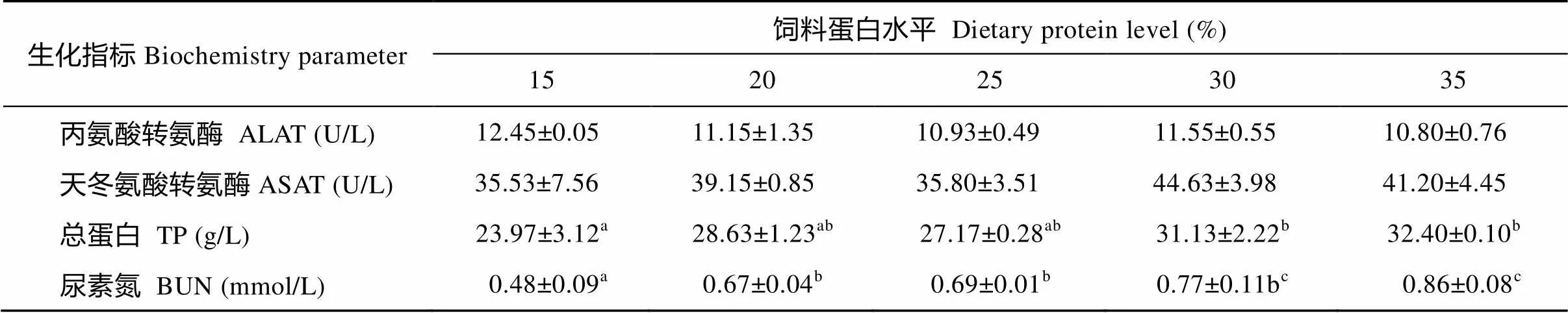
表3 飼料蛋白水平對草魚血清生化指標的影響
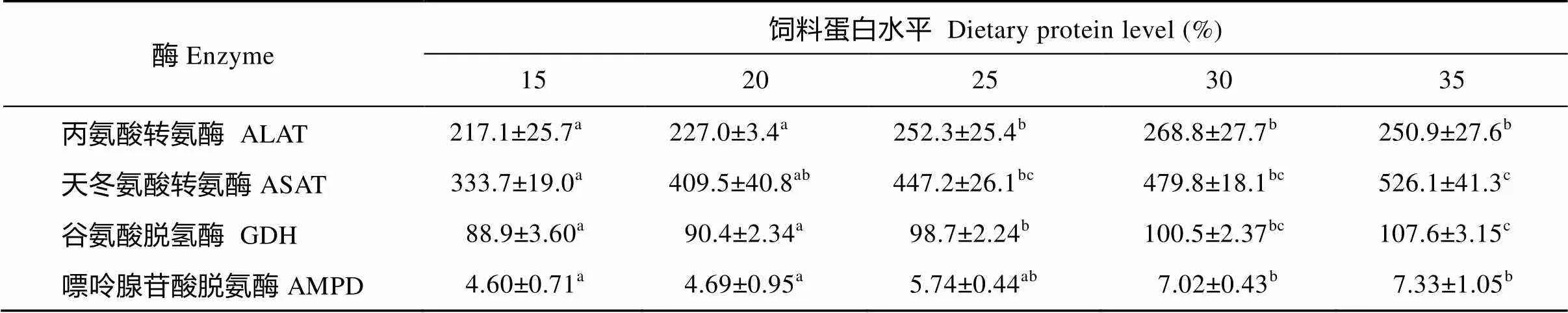
表4 飼料蛋白水平對草魚氮代謝相關酶活性的影響(U/g 蛋白)
3 討論
3.1 飼料蛋白水平對草魚生長和飼料利用的影響
本實驗通過二次多項式的回歸分析得到, 當飼料蛋白水平為26.50%時, 草魚的特定生長率達到最高; 當飼料蛋白水平為27.20%時, 草魚的飼料效率達到最高。蔣湘輝等[20]以魚粉為蛋白源, 得出0.75 g草魚最適蛋白需求為25%; 李愛杰[21]指出, 草魚成魚階段的蛋白需求為22%—25%; 廖朝興等[22]以酪蛋白為蛋白源, 得出10 g草魚的最適蛋白需求為28.2%; 王勝[16]以酪蛋白和明膠為蛋白源, 得出7.43 g草魚的最適蛋白需求為39.14%。造成這些差異的原因有很多, 如飼料能量水平、飼料蛋白源、魚體規格和養殖水溫等。Shiau,[23]指出, 隨著飼料中能量水平的升高, 石斑魚的最適蛋白需求量逐漸降低。飼料蛋白源中氨基酸組成的平衡性是蛋白源影響蛋白需求的主要原因。Takeda,[24]用魚粉和沙丁魚肉為蛋白源養殖杜氏鰤() 4周后, 獲得最適蛋白需求量為55%, 而以魚粉、豆餅和肉粉為蛋白源飼養, 最適蛋白需求量為50%[25]。隨著魚體的生長, 其蛋白需求量逐漸降低。Chen和Tasi[26]研究表明1.5 g左右的石斑魚的蛋白需求量為54%, 而規格為20—30 g時的蛋白需求量為40%—50%。有關研究表明, 魚類蛋白質需求量隨水溫升高而增加。在水溫分別為22—26℃和26—33℃時, 擬石首魚()的蛋白需求量分別為35%和44%[27]。
3.2 飼料蛋白水平對草魚血清生化指標的影響
血液生化指標能反映魚類的生理代謝狀態, 與營養狀況密切相關, 生化指標的變化可以闡明營養素在機體代謝變化的作用機制。丙氨酸轉氨酶和天冬氨酸轉氨酶是動物體內氨基酸代謝中重要的酶類, 在正常情況下血清中的轉氨酶活性較低, 當動物體受到營養不良或者脅迫作用, 尤其是肝臟受損時, 往往導致血清中丙氨酸轉氨酶和天冬氨酸轉氨酶含量升高[28, 29]。在本實驗中, 血清丙氨酸轉氨酶和天冬氨酸轉氨酶的活性并未受飼料蛋白水平的顯著影響, 表明各組魚體肝臟健康狀況良好。血清總蛋白在一定程度上可以代表飼料中蛋白質的營養水平及動物對蛋白質的消化吸收程度。在本實驗中隨著飼料中粗蛋白水平的增加, 血清總蛋白濃度升高, 但高蛋白組之間無顯著性差異, 這說明蛋白水平超過最適需求時, 草魚不能對其有效地消化吸收, 血清總蛋白沉積率并不增高, 多余的蛋白質被浪費掉。血清尿素氮可以較準確反映動物體內蛋白質的代謝情況, 蛋白質代謝良好時, 血清尿素氮濃度較低。在本實驗中隨著飼料蛋白水平的升高, 血清尿素氮的含量增加, 表明高蛋白組的草魚代謝負擔較重, 這與Preston,[30]和Bibiano Melo,[31]的研究結果一致。
3.3 飼料蛋白水平對草魚氮代謝相關酶活性的影響
飼料中的蛋白質降解成氨基酸后主要通過轉氨基作用和脫氨基作用進一步在體內轉化、代謝, 其中主要的關鍵酶是谷氨酸脫氫酶和腺苷酸脫氨酶, 還有輔助轉氨基的主要關鍵酶是丙氨酸轉氨酶和天冬氨酸轉氨酶。同哺乳動物類似, 魚類也主要通過聯合脫氨基作用滿足機體脫氨基的需要, 而轉氨酶在聯合脫氨基作用中起關鍵作用, 轉氨酶活力的大小反映了氨基酸代謝強度的大小, 雖然魚類體內轉氨酶眾多, 但其中卻以丙氨酸轉氨酶和天冬氨酸轉氨酶最為重要, 二者在魚類蛋白質代謝中起著重要作用。肝臟是蛋白質代謝的重要場所, 肝臟中轉氨酶活性可以反映蛋白質代謝狀況[32]。Alexis,.[33]對鯔魚()和Bibiano Melo,.[31]對克林雷氏鯰()研究表明肝臟轉氨酶隨著飼料蛋白含量的升高而增加, 并伴隨著氨氮排泄增加。在本實驗中, 15%和20%蛋白組的兩種轉氨酶活性差異不顯著, 而25%蛋白組顯著高于15%和20%蛋白組。由于低蛋白組的非蛋白能所占比例較高, 魚體不需要大量分解蛋白質提供能量, 此時飼料中的蛋白質主要參與蛋白質的合成用于魚體的生長。25%蛋白組的特定生長率最高, 說明魚體內蛋白質代謝無論是合成代謝還是分解代謝都高于低蛋白組, 作為體內蛋白質代謝最重要的參與者, 丙氨酸轉氨酶和天冬氨酸轉氨酶活性理應顯著增高。在高蛋白水平下非蛋白能減少, 大量的蛋白質被脫氨基用于供能, 此時兩種轉氨酶活性應該增高。然而本實驗結果表明, 30%和35%蛋白組的丙氨酸轉氨酶和天冬氨酸轉氨酶活性較25%蛋白組均沒有顯著增高, 但天冬氨酸轉氨酶活性有增高的趨勢, 此結果與Sa,.[34]一致, 當飼料中蛋白水平過量時, 丙氨酸轉氨酶和天冬氨酸轉氨酶活性并沒有受到顯著影響。
與其他脊椎動物相比, 魚類是排氨型動物, 蛋白質代謝產生大量氨, 在有氧情況下, 氨主要來源于肝臟轉氨脫氨作用和肌肉的嘌呤核苷酸循環。環境氧降低時, 肝中產生的氨降低, 而肌肉中產生的氨增加。谷氨酸脫氫酶在魚類肝臟中活性很強, 很多氨基酸在轉氨酶的作用下轉化成谷氨酸參與代謝, 是氨基酸分解代謝的關鍵酶, 其活性的高低在一定程度上反映了體內蛋白質分解代謝的情況[32]。本實驗表明, 隨著飼料蛋白水平的增加, 谷氨酸脫氫酶活性顯著升高, 說明高蛋白組有大量的蛋白質被分解代謝提供能量, 造成蛋白質浪費, 同時氨氮排泄也相應的增多[35]。類似的結果在虹鱒()[36]、克林雷氏鯰()[31]上有所報道。
腺苷酸脫氨酶是參與嘌呤核苷酸循環和能量代謝的重要酶類。嘌呤核苷酸循環是肌肉脫氨供能的主要途徑, 其關鍵脫氨酶是腺苷酸脫氨酶。在嘌呤核苷酸循環中, 腺苷酸脫氨酶將腺嘌呤核苷酸催化脫氨生成次黃嘌呤核苷酸, 此循環是消耗天冬氨酸脫掉氨基而供能的過程[37]。在脊椎動物肌肉中大多數的氨都是腺苷酸脫氨酶產生的, 特別是魚類的肌肉中, 該酶活性在骨骼肌中最高[38]。在本實驗中, 30%和35%蛋白組顯著高于15%和20%蛋白組, 與谷氨酸脫氫酶活性的變化趨勢一致, 表明在高蛋白組有較多的蛋白質用于供能, 肌肉中氨的含量相應增加, 對魚體健康產生不利影響。
綜上所述, 隨著飼料蛋白水平的升高, 肝臟天冬氨酸轉氨酶、谷氨酸脫氫酶、肌肉腺苷酸脫氨酶活性以及血清尿素氮含量顯著增加。通過特定生長率和飼料效率的回歸方程得出, 大規格草魚(209 ± 10) g的最適蛋白需求為26.50%—27.20%。
[1] National Research Council (NRC). Nutrient Requirements of Fishes [M]. Washington, D C: National Academic Press. 1993, 57—63
[2] Tibbetts S M, Lall S P, Anderson D M. Dietary protein requirement of juvenile American eel () fed practical diets [J]., 2000, 186(1—2): 145—155
[3] Kim K W, Wang X J, Bai S C. Optimum dietary protein level for maximum growth of juvenile olive flounder(Temminck et Schlegel) [J]., 2002, 33(9): 673—679
[4] Yang S D, Liou C H, Liu F G. Effects of dietary protein level on growth performance, carcass composition and ammonia excretion in juvenile silver perch () [J]., 2002, 213(1): 363—372
[5] Jover M, Fernandez-Carmona J, Del R?o M C,. Effect of feeding cooked-extruded diets, containing different levels of protein, lipid and carbohydrate on growth of red swamp cray?sh () [J]., 1999, 178(1): 127—137
[6] Bradford M M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding [J]., 1976, 72(1): 248—254
[7] Khan M S, Ang K J, Ambak M A,. Optimum dietary protein requirement of a Malaysian freshwater catfish,[J]., 1993, 112(2): 227—235
[8] Jauncey K. The effects of varying dietary protein level on the growth, food conversion, protein utilization and body composition of juvenile tilapias () [J]., 1982, 27(1): 43—54
[9] Papaparaskeva-Papoutsoglou E, Alexis M N. Protein requirements of young grey mullet,[J]., 1986, 52(2): 105—115
[10] Elangovan A, Shim K F. Growth response of juvenilefed isocaloric diets with variable protein levels [J]., 1997, 158(3): 321—329
[11] Tibbetts S M, Lall S P, Anderson D M. Dietary protein requirement of juvenile American eel () fed practical diets [J]., 2000, 186(1): 145—155
[12] Chou R L, Su M S, Chen H Y. Optimal dietary protein and lipid levels for juvenile cobia () [J]., 2001, 193(1): 81—89
[13] Ozório R O A, Valente L M P, Correia S,. Protein requirement for maintenance and maximum growth of two-banded seabream () juveniles [J]., 2009, 15(1): 85—93
[14] Chen Y J, Tian L X, Yang H J,. Effect of protein and starch level in practical extruded diets on growth, feed utilization, body composition, and hepatic transaminases of juvenile grass carp,[J]., 2012, 43(2): 187—197
[15] Salhi M, Bessonart M, Chediak G,. Growth, feed utilization and body composition of black catfish,, fry fed diets containing different protein and energy levels [J]., 2004, 231(1): 435—444
[16] Wang S. Studies on protein and essential amino acid requirements of grass carp,[D]. Thesis for Doctor of Science. Sun Yat-Sen University, Guangzhou. 2006 [王勝. 草魚幼魚蛋白質和主要必需氨基酸需求的研究. 博士學位論文, 中山大學, 廣州. 2006]
[17] Wilson R P, Halver J E. Protein and amino acid requirements of fishes [J]., 1986, 6(1): 225—244
[18] Lee S M, Jeon I G, Lee J Y. Effects of digestible protein and lipid levels in practical diets on growth, protein utilization and body composition of juvenile rockfish () [J]., 2002, 211(1): 227—239
[19] Kim L O, Lee S M. Effects of the dietary protein and lipid levels on growth and body composition of bagrid catfish,[J]., 2005, 243(1): 323—329
[20] Jiang X H, Liu G, Jin G H,. Effect of dietary protein and lipid levels on growth and body composition of[J]., 2010, 23(1): 24—27 [蔣湘輝, 劉剛, 金廣海, 等. 養殖魚類飼料蛋白需要量的研究進展. 水生生物學報, 2010, 23(1): 24—27]
[21] Li A J. Nutrition and Feed of Aquatic Animal [M]. Beijing: Chinese Agricultural Press. 1996, 220 [李愛杰. 水產動物營養與飼料學. 北京: 中國農業出版社. 1996, 220]
[22] Liao C X, Huang Z Z. The dietary protein requirement of grass carp on different growth stage [J].,1987, 1(1): 1—5 [廖朝興, 黃忠志. 草魚在不同生長階段對飼料蛋白質需要的研究. 淡水漁業, 1987, 1(1): 1—5]
[23] Shiau S Y, Lan C W. Optimum dietary protein level and protein to energy ratio for growth of grouper () [J]., 1996, 145(1): 259—266
[24] Takeda M, Shimeno S, Hosokawa H,. The effect of dietary Calorie-Protein ratio on the growth, feed conversion and body composition of young yellowtail [J]., 1990, 41(1): 443—447
[25] Jover M, Garcia-Gomez A, Tomas A,. Growth of mediterranean yellowtail () fed extruded diets containing different levels of protein and lipid [J]., 1999, 179(1): 25—33
[26] Chen H Y, Tsai J C. Optimal dietary protein level for the growth of juvenile grouper () fed semipurified diets [J]., 1994, 119(2): 265—271
[27] Daniels W H, Robinson E H. Protein and energy requirements of juvenile red brum () [J]., 1986, 53(3): 243—252
[28] Barcellos L J G, Kreutz L C, de Souza C,. Hematological changes in jundiá (Quoy and Gaimard) after acute and chronic stress caused by usual aquacultural management, with emphasis on immunosuppressive effects [J]., 2004, 237(1): 229—236
[29] Barton B A, Iwama G K. Physiological changes in fish from stress in aquaculture with emphasis on the response and effects of corticosteroids [J]., 1991, 10(1): 3—26
[30] Preston R L, Schnakenberg D D, Pfander W H. Protein utilization in ruminants I. Blood urea nitrogen as affected by protein intake [J]., 1965, 86(3): 281—288
[31] Bibiano Melo J F, Lundstedt L M, Metón I,. Effects of dietary levels of protein on nitrogenous metabolism of(Teleostei: Pimelodidae) [J]., 2006, 145(2): 181—187
[32] Smutna M, Vorlova L, Svobodova Z. Pathobiochemistry of ammonia in the internal environment of fish [J]., 2002, 71(2): 169—181
[33] Alexis M N, Papaparaskeva-Papoutsoglou E. Aminotran-s-ferase activity in the liver and white muscle offed diets containing different levels of protein and carbohydrate [J]., 1986, 83(1): 245—249
[34] Sa R, Pousao-Ferreira P, Oliva-Teles A. Effect of dietary protein and lipid levels on growth and feed utilization of white sea bream () juveniles., 2006, 12(4): 310—321
[35] Kim K I, Kayes T B, Amundson C H. Purified diet development and revaluation of the dietary protein requirement of fingerling rainbow trout () [J]., 1991, 96(1): 57—67
[36] Sánchez-Muros M J, García-Rejón L, García-Salguero L,. Long-term nutritional effects on the primary liver and kidney metabolism in rainbow trout. Adaptive response to starvation and a high-protein, carbohydrate-free diet on glutamate dehydrogenase and alanine aminotransferase kinetics [J]., 1998, 30(1): 55—63
[37] Lowenstein J M. Ammonia production in muscle and other tissues: the purine nucleotide cycle [J]., 1972, 52(2): 382—414
[38] Lushchak V I, Storey K B. Influence of exercise on the distribution of enzymes in trout white muscle and kinetic properties of AMP-deaminase from free and bound fractions [J]., 1994, 13(5): 407—418
EFFECTS OF DIETARY PROTEIN LEVELS ON GROWTH, FEED UTILIZATION AND THE ENZYMES ACTIVITY ON NITROGEN METABOLISM OF GRASS CARP ()
LI Bin, LIANG Xu-Fang, LIU Li-Wei, YUAN Xiao-Chen, ZHU Wen-Huan and LI Jie
(Key Lab of Freshwater Animal Breeding, Ministry of Agriculture, College of Fisheries, Huazhong Agricultural University, Wuhan 430070, China)
The present study was to investigate the effect of dietary protein levels on growth, feed utilization and nitrogen metabolism of grass carp (). Five isoenergetic diets (13.71 kJ/g) were formulated with 15%, 20%, 25%, 30% and 35% protein level. Fish (209 ± 10 g) were randomly distributed into five groups each with three replicates and were fed twice daily (08:00 and 16:00) to apparent satiation for 8 weeks. The results showed that weight gain and feed utilization were significantly affected by dietary protein levels (<0.05). Fish fed the diet with 25% protein had the highest weight gain, specific growth ratio and feed efficiency ratio than other groups. Protein retention efficiency and protein efficiency ratio inversely correlated with dietary protein levels (<0.05).There were no significantly differences on survival, activities of serum alanine aminotransferase and serum aspartate aminotransferase (>0.05). The dietary optimal protein for grass carp fromandestimated using the second order polynomial regression was ranged from 26.5% to 27.2%. Serum total protein, blood urea nitrogen, the activities of aspartate aminotransferase, glutamate dehydrogenase in liver and adenosine 5′-monophosphate deaminase in muscle were significantly increased with the increasing of dietary protein levels (<0.05). This denoted increased catabolism of protein to supply energy with the increasing of dietary protein levels.
; Protein; Growth; Feed utilization; Nitrogenmetabolism
2013-09-10;
2013-12-18
國家重點基礎研究發展計劃“973”項目(2009CB118702); 水產養殖動物營養需求與高效配合飼料開發項目(公益性行業(農業)科研專項)(201003020)資助
李彬(1988—), 男, 江蘇連云港人; 碩士研究生; 研究方向為水產動物營養與飼料。E-mail: 08libin@163.com
梁旭方, 教授; E-mail: xufang_liang@hotmail.com
S965.1
A
1000-3207(2014)02-0233-08
10.7541/2014.35

