強阿片藥物對阿片耐受的晚期癌癥患者肝功能的影響
王曉芳,王玉梅
0 引言
30%~70%的晚期癌癥患者存在疼痛,其中中重度疼痛的發生率為40%~50%,重度疼痛的發生率為25%~30%[1]。癌癥中晚期的疼痛治療,目前仍以阿片類控制為主,按WHO三階梯止痛治療原則,強阿片類藥物是控制中重度癌痛的金標準[2-3]。目前,我國癌痛治療的現狀為:①多數地區癌痛治療處于普及階段;②普遍存在止痛治療不充分現象;③臨床醫師對止痛藥物認識不足,缺乏足夠使用經驗;④開始重視個體化治療,但缺乏可供參考的詢證醫學證據。
強阿片類藥物存在身體依賴、精神依賴、過度鎮靜及呼吸抑制等嚴重的不良反應。這些不良反應在不規范應用以上藥物及藥物濫用時比較常見。由于患者、家屬缺乏癌痛治療知識,醫護人員忽視疼痛治療,癌痛規范化治療知識不足,缺少循證醫學證據,在應用強阿片類藥物時,尤其是腫瘤晚期患者需要止痛治療時,患者、家屬及醫護人員均顧慮重重。嗎啡、羥考酮及芬太尼等藥物均經肝臟代謝,針對普遍關注的應用阿片類藥物的安全性問題,本文選取肝功能水平為研究指標,探討應用阿片類藥物對肝功能的影響。
1 資料與方法
1.1 一般資料 收集2011年1月至2013年12月于我院寧養病房首次住院后使用強阿片類藥物30 d及以上的晚期惡性腫瘤患者52例(惡性腫瘤診斷均經病理或物理檢查證實)。男28例,女24例,年齡48~83歲,平均(67.44±10.15)歲。
所有患者在用藥初期均有中重度疼痛,并嚴格按照三階梯止痛原則及美國國立綜合癌癥網絡(National Comprehensive Cancer Network,NCCN)成人癌痛治療指南中國版的方法,接受系統規范的鎮痛治療。統計患者的疼痛情況、強阿片類藥物使用情況、用藥時間、用藥前、用藥后1周、2周、1個月以及住院期間最后一次化驗時肝功能水平。患者的強阿片類藥物用量按照NCCN成人癌痛治療指南中國版阿片類藥物的劑量轉換標準進行換算。具體轉換方法見附表。
患者初始時使用羥考酮鎮痛19例、芬太尼透皮貼劑鎮痛31例、嗎啡即釋片鎮痛2例,均使用嗎啡即釋片作為爆發痛解救藥,最小用量60 mg/d,最大用量720 mg/d,平均(102.12±97.16)mg/d。患者在院期間經及時評估、及時調整用藥,均緩解至輕度至無痛狀態。最終使用羥考酮鎮痛11例、芬太尼透皮貼劑鎮痛40例、嗎啡即釋片鎮痛1例,均使用嗎啡即釋片作為爆發痛解救藥,最小用量60 mg/d,最大用量1 440 mg/d,平均(258.46±246.12)mg/d。

表1 根據單次劑量研究,與嗎啡相比,不同阿片類藥物口服及腸外給藥的等效劑量換算表
1.2 不同系統的晚期惡性腫瘤 其中頭頸部腫瘤3例(舌癌1例、鼻咽癌1例、喉癌1例),肺癌13例,乳腺癌1例,消化系統腫瘤27例(胃癌6例、肝癌3例、膽管癌1例、十二指腸癌1例、胰腺癌7例、結直腸癌9例),泌尿系腫瘤5例(腎癌1例、前列腺癌3例、膀胱癌1例),婦科腫瘤3例(宮頸癌2例、子宮癌肉瘤1例),血液系統腫瘤(骨髓瘤1例)。其中1例同時患有前列腺癌及結腸癌。
1.3 統計學處理 采用SPSS 17.0軟件包進行統計學分析,用藥前后肝功的比較使用配對樣本t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 嗎啡使用時間 52例患者于我院首次住院后,使用強阿片類藥物達到耐受劑量的時間最長為249 d,最短為26 d,平均(74.98±53.32)d。
2.2 長期使用阿片類藥物對患者肝功能的影響 在患者用藥期間監測血清肝功能的各項指標,用藥后1周、2周、1個月及患者在院期間最后一次化驗的血清肝功能指標與用藥前分別進行配對t檢驗,用藥1周后各組P值均>0.05,差異無統計學意義。用藥2周后谷丙轉氨酶組P值<0.05,差異有統計學意義,余各組P值均>0.05,差異無統計學意義。用藥1個月后,各組P值均>0.05,差異無統計學意義。出院前最后一次監測中,谷草轉氨酶、直接膽紅素、間接膽紅素組P值均<0.05,差異有統計學意義。
對肝癌及存在肝轉移的患者用藥后1周、2周、1個月及患者在院期間最后一次化驗的血清肝功能指標與用藥前分別進行配對t檢驗,用藥1周后直接膽紅素組P值<0.05,差異有統計學意義,余各組P值均>0.05,差異無統計學意義。見表2。
對最終每日使用強阿片類藥物超過300 mg的患者用藥后1周、2周、1個月及患者在院期間最后一次化驗的血清肝功能指標與用藥前分別進行配對t檢驗,用藥1周后直接膽紅素組P值<0.05,差異有統計學意義,余各組P值均>0.05,差異無統計學意義。見表3。

表2 52例晚期癌癥患者使用強阿片類藥物各時期肝功能指標的變化

表3 肝癌及存在肝轉移患者用藥各時期肝功能指標的變化
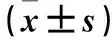
表4 最終使用強阿片類藥物超過300 mg/d用藥各時期肝功能指標的變化
3 討論
癌痛規范化治療包括全面的癌痛評估、個體化的治療方法、患者及家屬宣教等各方面。盡管影響疼痛評估和處理的因素是多方面的,但根據我國目前的情況,患者不愿主動報告疼痛情況,專業的醫護人員對阿片類藥物存在誤解,仍然是疼痛評估和處理的主要障礙[4-6]。藥物鎮痛對于絕大多數晚期癌性疼痛患者來說是唯一可能接受并可受益的治療方法,合理用藥可使大多數患者的疼痛得到緩解[7-8]。
由于強阿片類藥物無非甾體藥物及弱阿片藥物的“天花板效應”,因此,強阿片類藥物成為晚期癌癥治療的基本用藥。根據美國食品藥品監督管理局(Food and drug administration,FDA) 標準,阿片耐受是指已經按時服用阿片類藥物至少1 周以上,且每日總量至少為口服嗎啡50 mg、羥考酮30 mg、氫嗎啡酮8 mg、羥嗎啡酮25 mg 或其他等效藥物,芬太尼貼劑劑量至少為25 g/h;不滿足上述持續止痛時間及劑量要求時定義為阿片未耐受。 本次研究中,所有患者均達到阿片耐受標準,在使用阿片耐受劑量1周、2周及1月后,患者肝功能各項指標(除谷丙轉氨酶)水平變化均無顯著差異,但住院期間最后一次監測與用藥初期肝功能指標比較時,谷草轉氨酶、直接膽紅素、間接膽紅素水平存在差異。
有最后一次肝功能水平結果的患者42例,其中谷草轉氨酶及直接膽紅素水平升高大于正常水平1倍的患者10例,6例存在肝轉移,2例為胰腺癌患者,2例為肺癌患者。余患者轉氨酶水平雖有變化,但均未達正常水平1倍。間接膽紅素水平升高大于正常水平1倍的患者4例,其中2例存在肝轉移,2例為胰腺癌患者。這4例患者的肝功能其他指標水平亦顯著升高。余患者間接膽紅素水平雖有變化,但均未達正常水平1倍。考慮患者最終出現肝功能水平的變化為病情進展、肝臟功能衰退所致。而患者在用藥2周后谷丙轉氨酶水平較用藥前降低,且存在統計學差異,考慮原因為:在給予止痛藥物的同時,我們對已存在肝功能異常的患者使用保肝藥物治療;其他如抗感染、營養補液等治療手段,在病程初期對患者一般狀態改善起到積極作用。
在臨床實踐中,醫生在選擇應用藥物時,需考慮藥物對肝功能損傷的可能性。尤其當藥物需用在患有肝癌或肝轉移的患者時,更需慎重考慮。嗎啡、羥考酮及芬太尼等藥物均經肝臟代謝,對于肝臟功能異常的患者以上藥物時,由于存在藥物蓄積,加重呼吸抑制等不良反應的發生。本研究中,對21例確診為肝癌或存在肝轉移的患者用藥前后血清肝功能(除直接膽紅素)水平進行了對比,用藥前后肝功能水平差異無統計學意義。本組患者使用強阿片類藥物的最終劑量為60~480 mg/d,使用時間為26~162 d,均無呼吸抑制等嚴重不良反應發生。
本研究中,使用大劑量嗎啡的患者18例,超大劑量嗎啡患者4例,患者的肝功能(除直接膽紅素)各項指標在用藥后1周、周、1個月及出院前最后一次監測與用藥初期相比較均無顯著改變。一般認為,大劑量嗎啡為口服嗎啡(或其等效量)≥300 mg/d,而≥600 mg為超大劑量[9]。由于臨床醫生普遍缺乏長期大量應用強阿片類藥物的經驗,患者止痛效果不佳且阿片類藥物使用劑量較大時,醫生常常顧慮重重,同時患者及家屬也抗拒進一步加大阿片類藥物用量,導致治療不充分,達不到滿意的治療效果。本研究結果證實,經過合理、規范地應用強阿片類藥物,患者可以在有效鎮痛的同時不引起明顯的肝功能損傷。
本研究中患有肝癌或肝轉移的患者以及最終使用嗎啡量超過300 mg/d的患者在用藥1周后直接膽紅素水平存在顯著差異,這一情況需引起注意。眾所周知,強片類藥物引起的不良反應常見于用藥初期或藥物過量時,而嗎啡能促使膽道括約肌收縮,引起膽系內壓上升,對膽紅素水平造成影響。因此,在使用強阿片類藥物過程中強調需檢測患者肝功能水平。
綜上所述,本研究中大部分患者(44/52)均為在病程終末期接受嗎啡耐受劑量甚至大劑量強阿片類藥物治療。在其用藥期間對肝功能水平監測,發現在用藥2周及1月內肝功能各項指標在用藥前后無顯著改變,為臨床長期應用強阿片類藥物的安全性提供了支持。但仍需注意的是,盡管這些患者在用藥初期均無顯著肝功能損傷,但對于已經存在肝功能損傷的患者的鎮痛治療仍需強調監測肝功水平,根據個體化情況調整用藥。
參考文獻:
[1] van den Beuken-van Everdingen MHJ,de Rijke JM,et al.Prevalence of pain in patients with cancer:a systematic review of the past 40 years[J].Ann Oncol ,2007,18:1437-1449.
[2] World Health Organization.Cancer Pain Relief,Second Edition[J].Geneva,Switzerland:World Health Organization,1996:1-69.
[3] Indelicato RA,Portenoy RK.Opioid rotation in the management of refractory cancer pain[J].J Clin Oncol,2002,20:348-352.
[4] Meeker MA,Finnell D,Othman AK.Family caregivers and cancer pain management:a review[J].J Fam Nurs,2011,17:29-60.
[5] Jacobsen R,Liubarskiene Z,Moldrup C,et al.Barriers to cancer pain management:a review of empiricalresearch[J].Medicina (Knas),2009,45:427-433.
[6] Jacobsen R,Moldrup C,Christrup L,et al.Patient-related barriers to cancer pain management:a systematic exploratory review[J].Scand J Caring Sci,2009,23:190-208.
[7] 劉鵬輝,廖國清,王紅梅,等.芬太尼透皮貼劑與口服嗎啡控釋片治療轉移性骨腫瘤疼痛的療效比較[J].中國醫院用藥評價與分析,2011,11(8):736-737.
[8] Sun KB,Hye WS,Young JC,et al.Noninterventional observational study using high-dose controlled-release oxycodone (CR oxycodone) for cancer rain management in outpatient clinics[J].Pain Med,2013,14:1866-1872.
[9] 李小梅,董艷娟,李慧莉,等.阿片耐受與慢性癌痛的阿片類藥物治療[J].中國疼痛醫學雜志,2012,18,(9):561-565.

