中成藥說明書內容分析與藥學服務
張艷華,趙慶軍
0 引言
中成藥因其獨特的療效,在臨床廣泛應用。藥品說明書對醫生、藥師或患者合理使用中成藥具有指導作用。日常工作中發現中成藥說明書中藥理毒理、相互作用等安全性信息,沒有西藥說明書中描述詳盡。為了了解中成藥說明書的現狀,進一步提高中成藥說明書質量,保障中成藥臨床安全合理的應用,促進中成藥說明書內容的規范化,本文對324份中成藥說明書內容調查分析,提出進一步規范中成藥說明書內容的建議,以提高用藥安全性和藥學服務質量。
1 資料與方法
收集我院應用的具有國藥準字Z的324份說明書(包括16份注射劑),對照國家食品藥品監督管理局第24號令公布的《藥品說明書和標簽管理規定》(以下簡稱<管理規定>)和國食藥監注[2006]283號發出的《中藥、天然藥物處方藥說明書格式》(以下簡稱<格式>)、《中藥、天然藥物處方藥說明書內容書寫要求》(以下簡稱<書寫要求>)和《中藥、天然藥物處方藥說明書撰寫指導原則》(以下簡稱<指導原則>)逐一統計其中各項,并進行分析討論。
2 結果
324份說明書中,僅63份有不良反應內容(19.44%),118份有禁忌內容(36.42%),239份有注意事項內容(73.17%),3份有相互作用內容(0.93%),2份有臨床試驗(0.62%),45份有藥理毒理(13.89%)。中成藥說明書項目內容調查表見表1。
3 分析
3.1 成分 《書寫要求》規定,此項應列出處方中所有的藥味或有效部位、有效成分等。注射劑還應列出所用的全部輔料名稱。對于處方已列入國家保密技術項目的品種,以及獲得中藥一級保護的品種,可不列此項,本次調查有2份未標注可能屬于保護品種,322份有此項(占99.38%)。但是,16份注射劑中,有6份的標注為所含的中藥藥味。中藥藥味只是成分來源,而并非發揮藥效的有效成分,此種標注不利于中藥注射劑的發展。還有3份注射液未標注輔料,也未注明使用了何種提取液。
3.2 功能主治 中成藥的功能主治是以中醫理論為依據而制訂的,是指導臨床正確用藥的依據,對正確認識中成藥的治療作用具有導向作用,應充分體現中醫的辨證施治。本次調查的標注率是100%,但多數說明書都采用了中西合璧的標注。如:某廠家的百癬夏塔熱片,其標注是:消除異常粘液質、膽液質及敗血,消腫止癢。用于治療手癬、體癬、足癬、花斑癬、銀屑病、過敏性皮炎、帶狀皰疹、痤瘡等。還有的完全使用現代醫學術語標注。如:某廠家的舒血寧注射液的標注是:擴張血管,改善微循環。用于缺血性心腦血管疾病、冠心病、心絞痛、腦栓塞、腦血管痙攣等。類似的標注和中醫理論的整體觀和辨證施治有根本區別,不適合臨床應用,易出現藥不對癥,結果輕則無效,重則加劇癥狀,此即所謂的“遵循中醫藥理論,劇毒變良藥;違背中醫藥理論,無毒變有毒[1]”。
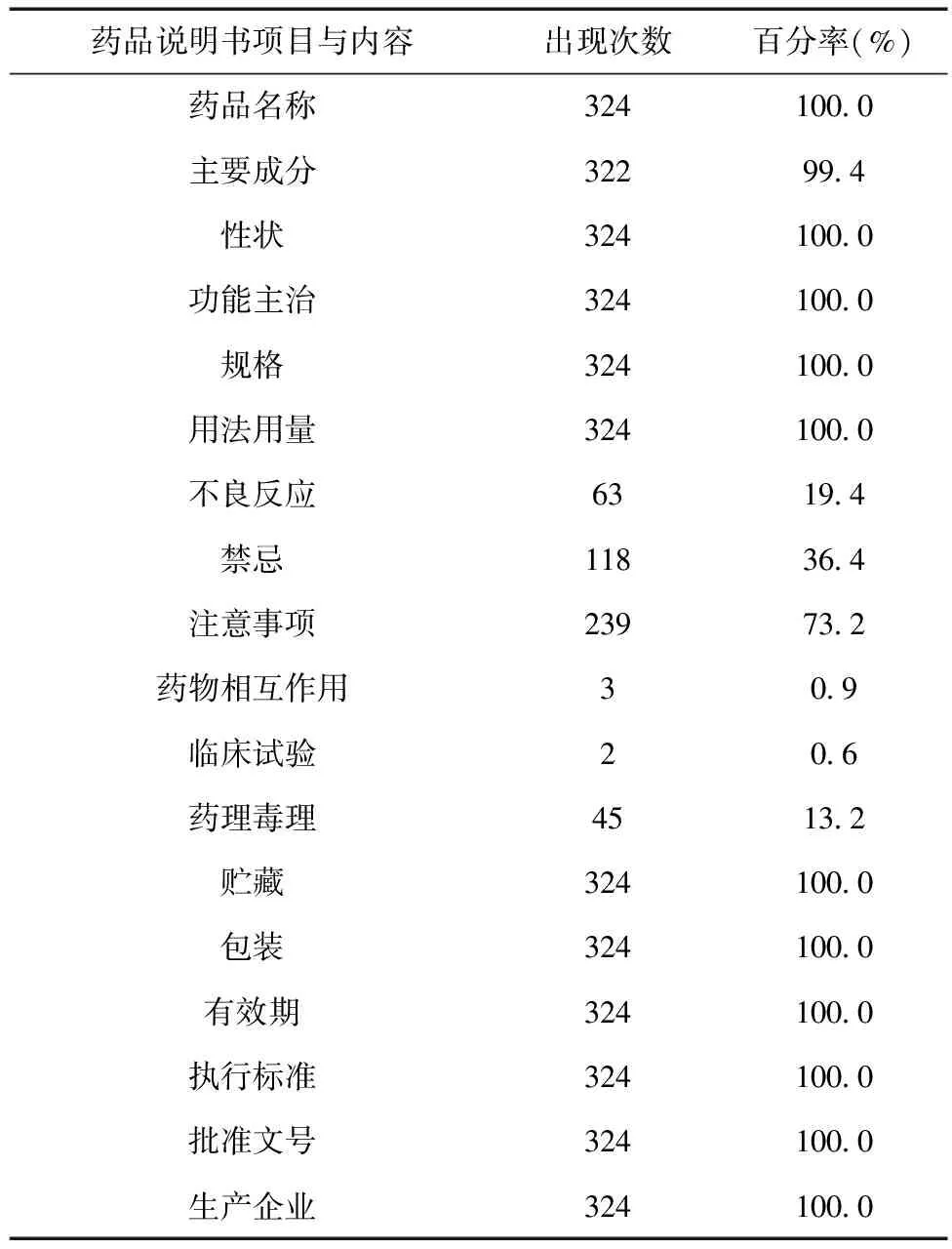
表1 中成藥說明書項目內容調查表(n=324)
3.3 不良反應 藥品不良反應是合格藥品在正常用法用量下出現的與用藥目的無關或意外的有害反應,涉及用藥的安全性。《書寫要求》中對不良反應項的規定為“應當實事求是地詳細列出該藥品不良反應。并按不良反應的嚴重程度、發生頻率或癥狀的系統性列出。”但是324份說明書只有63份標注內容,占19.44%。而其中大部分藥品可能導致不良反應,如:某廠生產的注射用雙黃連(凍干)說明書未標注不良反應項,而實際雙黃連注射劑以過敏反應和輸液反應為主,包括嚴重過敏性休克、呼吸困難、剝脫性皮炎[2]。還有同一有效成分不同廠家的藥品說明書的不良反應項標注不同,如:成分均為三七總皂苷的兩種藥物,分別為注射用血塞通(凍干)、注射用血栓通(凍干)。前者的不良反應標注:頭面部發紅、潮紅,輕微頭脹痛是本品用藥時常見反應;偶有輕微皮疹出現,尚可繼續用藥;若發現嚴重不良反應,應立即停藥,并進行相應處理。后者的不良反應標注:尚不明確。這就說明兩個廠家的態度和責任心有所差異。據相關部門統計,目前已知可以引起不良反應的中藥材有243味,中藥制劑233種[3]。長期以來,許多人誤認為中藥安全可靠,沒有不良反應,加之絕大多數說明書未對不良反應進行標注,使患者隨意加大藥量或延長療程,造成中藥的濫用和誤用,如:木通事件、魚腥草注射液事件等。隨著現代藥品信息的發展,結合藥品不良反應監測網絡,應不斷在說明書中補充藥品新的不良反應,標明其主要活性成分和與其他藥品配伍時是否會發生不良反應,以指導臨床合理用藥,避免或減少藥品不良反應的發生。
3.4 禁忌和注意事項 這兩項內容均涉及用藥安全性,是說明書中需要詳細描述的。本次調查有118份、239份分別對禁忌和注意事項進行標注,分別占36.42%、73.17%,但多數標注過于簡單,如:禁食生冷、辛辣、油膩;脾胃虛寒者禁用;孕婦慎用等。對實際用藥過程中需慎用、影響藥品療效、避免聯合應用的注意事項卻沒有明確標明。禁忌必須根據臨床應用、十八反、十九畏、妊娠禁忌等進行科學分析,明確規定哪些人禁用、忌用該種藥品[4]。注意事項需說明使用該藥品時必須注意的問題,內容較多,應詳細介紹。有些說明書禁忌與注意事項混淆,如:愈傷靈膠囊的禁忌標注為“尚不明確”,其注意事項標注為“孕婦忌服”。有些不同廠家生產的同一品種的“禁忌”和“注意事項”內容不一致,表現為一個標注“尚不明確”,另一個標注具體內容。這些不準確、不規范的描述會給使用者帶來安全隱患,易造成用藥不良后果和醫患糾紛,應當改進。
3.5 藥物相互作用 《書寫要求》規定,如進行過相關研究,應詳細說明哪些或哪類藥物與本藥品產生相互作用,并說明相互作用的結果。本次調查只有3份(0.93%)明確標注藥物相互作用,106份(32.72%)標注“尚無本品與其他藥物相互作用的信息。”2份缺項。這與趙海平等搜集《新編國家中成藥(2011版)》中常用品種的統計分析結果相似,并且相互作用的表述簡單,僅局限在傳統的藥物禁忌范圍,具有現代研究內容的表述甚少[5]。黎奔等[6]研究認為,中西藥合用時,通過抑制或增強CYP450酶的含量和活性,從而對藥物的代謝、作用時間和作用強度產生影響,如:銀杏葉提取物與地高辛、華法林等合用時,需密切留意血藥濃度的變化,或盡量不合用,以避免可能發生的藥物相互作用;甘草和五味子都具有CYP誘導作用,臨床上生甘草或五味子及其制劑與部分西藥(如巴比妥類、苯妥英納、胰島素、華法林等)合用,有可能使后者代謝加速、半衰期縮短、藥效減弱。目前,中成藥與其他藥物的聯合應用是一種必然趨勢,盡可能詳細表述有關藥物相互作用的內容是非常必要的。
3.6 臨床試驗 依照2005年2月28日國際食品藥品監督管理局發布的《藥品注冊管理辦法》的規定,所有的藥品都應進行臨床試驗,并應標注此項內容。本次調查的說明書中只有2份進行了臨床試驗,僅占0.62%。其他322份藥品說明書都沒有包含此項內容,目前的循證醫學要求醫生的治療要有科學的文獻依據,臨床試驗結果是醫生用藥重要的參考內容。
3.7 藥理毒理 本次調查的說明書中只有45份(13.89%)有藥理毒理項,其內容只有藥理作用,而無毒理研究,其他279份說明書都缺失此項。藥理作用研究結果可佐證功能主治,同時對擴大治療范圍具有積極意義;毒理研究所做的致癌、致畸、致突變實驗對判斷臨床安全性很重要,藥理毒理中沒有毒理內容將使安全用藥缺少可靠的依據。
3.8 藥代動力學 本次調查的324份說明書均缺失此項。藥代動力學是研究給藥后藥物及其代謝產物在體內隨時間而變化的過程的學科,包括半衰期、達峰值等內容,對指導臨床用藥很重要。沒有藥代動力學就沒有藥物的作用時間,無法推斷用法用量,尤其是中藥注射劑屬于中藥西制,不研究藥代動力學,其結果即令人生疑,導致其不能很好地走向世界。
4 討論
4.1 重視特殊人群的用藥 特殊人群主要指老人、兒童、孕婦和哺乳期婦女,由于其特殊的生理特點,藥物的應用更需慎重。根據《書寫要求》和《指導原則》的精神,有關“孕婦及哺乳期婦女用藥”、“兒童用藥”、“老年用藥”的論述可以在“注意事項”下表述。本次324份說明書中,只有18份(占5.56%)和11份(占3.40%)分別在注意事項中特別提到了孕哺婦女用藥和兒童用藥問題,而對老人用藥問題沒有一份提及。目前,人口老齡化日益明顯,老人的特點是生理和心理均處于衰退狀態,且同時患有多種疾病,用藥種類較多,因此,對老年人用藥問題要進行更多的關注與研究。藥品說明書應該詳細、準確地提供這方面內容,根據藥理毒理、歷史文獻等科學分析,明確規定特殊人群用藥。現實情況是中成藥說明書這方面內容甚少,臨床應用也僅憑經驗,其安全性令人擔憂[7]。雖然法規也認可特殊人群用藥可在注意事項中體現,但筆者仍然建議把這些內容放在其本來的位置上,令使用者一目了然,體現對特殊人群用藥的重視程度。
4.2 避免藥品不良反應發生 中藥注射劑改變了傳統的中藥給藥方式,使藥物可直接進入人體組織、血液或器官中,作用更迅速,其不良反應的發生也更容易,尤其是隨著品種的增多和使用的日益廣泛。一些中藥注射劑在臨床應用中屢次發生嚴重不良反應,如:魚腥草注射液、刺五加注射液等[8],這是由于藥品說明書中沒有詳細提及該藥的不良反應,或含糊其辭,對有過敏性休克、過敏反應、急性腹痛嘔吐、呼吸困難、肺水腫等反應避重就輕,僅標注“偶見過敏反應”或“尚不明確”,且與不及時添加已發生的不良反應有關。導致臨床醫師和患者對不良反應不重視,以至于發生嚴重后果。由此可見,只有在藥品說明書中詳細標注不良反應內容,引起使用者的足夠重視,才能最大限度地避免不良反應的發生。
4.3 加強中成藥說明書的管理 藥品說明書是一種法定文件,它既是指導臨床合理用藥的主要資料,又是裁定醫療事故中用藥是否得當的重要依據。通過以上分析不難發現,與化學藥品相比,中成藥說明書內容標注詳細、完整、規范的寥寥無幾,其中不良反應、禁忌、注意事項、藥物相互作用、藥理毒理、特殊人群用藥等對臨床有重要參考價值的項目缺失嚴重,描述簡單。中藥企業應借鑒國外先進經驗,加強對中藥的研究,尤其對臨床有重要參考價值的項目,及時添加藥品說明書內容。國家藥監部門應遵照《藥品管理法》,借助網絡信息、對不符合規定的說明書進行整頓,盡快統一標準(尤其中藥注射劑),對不及時更新說明書內容的企業,應加大懲處力度,使說明書內容達到科學、規范、準確的標準,更好地指導臨床應用[9]。
4.4 提高藥學服務質量,促進合理使用中成藥 通過對324份中成藥說明書的逐一分析,發現其中項目缺失、內容不規范問題嚴重,給臨床用藥帶來不便,也給用藥安全帶來隱患。為提高藥學服務質量,國家管理部門應加強中成藥說明書的管理力度,不斷完善充實其內容,方便藥學人員對所提供的藥品的適應證、作用原理、作用途徑、作用特點、作用強弱、使用方法、配伍禁忌、不良反應等性能有全面的了解,更好地為患者提供藥學服務[10]。
參考文獻:
[1] 許雯.中藥注射劑說明書中存在問題的分析與討論[J].中國醫藥指南,2010,8(34):168-170.
[2] 陳冬裕.對現行中成藥說明書的調查和思考[J].中國藥房,2009,20(9):718-720.
[3] 陳偉,穆秀珍,馬金蘭.110份中成藥說明書的調查分析[J].中國藥師,2009,12(5):676-677.
[4] 扈福,扈曉雯.從中藥注射劑說明書思考用藥安全性問題[J].中國藥房,2009,20(36):2879-2880.
[5] 趙海平,廖正根,羅云,等.中成藥說明書中“藥物警戒”內容的問題分析及建議[J].中成藥,2012,34(9):1832-1835.
[6] 黎奔,熊潔萍,陳朝,等.中西藥物合用對細胞色素P450酶的調控作用[J].廣東醫學,2010,31(20):2730-2732.
[7] 孟菲,李學林.中藥注射劑說明書存在問題分析[J].中國藥房,2011,22(27):2857-2859.
[8] 李全斌,喬明艷,錢洪波,等.藥瓶說明書存在問題及建議[J].中國藥房,2008,19(28):33.
[9] 智永剛,潘蕾羽,匡麗萍.藥物流行病學方法在中藥注射劑上市后安全性研究中的應用[J].中國藥房,2010,21(16):11.
[10]朱軍,陳富超,陳琴華,等.對中藥說明書調查分析[J].中國藥房,2008,19(6):476.

