魚腥草注射液的質量穩定性研究
曾茂貴 李穎
魚腥草注射液是魚腥草經水蒸氣蒸餾的揮發油飽和水溶液滅菌制成的注射液。主要有效成分包括:癸酰乙醛、甲基正壬酮、月桂烯、癸醛等[1-2],具有抗病毒、抗菌[3]、增強機體免疫功能[4-5]、抑制炎癥對毛細血管通透性的增加、鎮痛[6]、抗過敏、平喘、止咳祛痰[7-8]等作用。近年來,魚腥草注射液在臨床上的應用日漸廣泛,其不良反應也逐漸凸現。由魚腥草注射液靜脈滴注所引起的皮膚過敏、過敏性休克、呼吸困難、水腫、胃腸反應、聽力、視力下降等不良反應[9-13]時有發生。其中某些不良反應較為嚴重[14],甚至危及生命[15]。有研究表明[16],魚腥草注射液有效成分之一癸酰乙醛(魚腥草素)化學性質不穩定,極易發生聚合,這可能是魚腥草注射液發生過敏的原因之一,提示魚腥草注射液的不良反應可能與成分有關。但是,魚腥草注射液中所含的揮發性成分復雜且微量,而目前的質量控制方法僅限于某個成分的含量測定,在其質量研究領域留下了空白。本研究采用頂空固相微萃取—氣相色譜—質譜聯用方法,由成分分析入手,全面、系統地考察魚腥草注射液中揮發性成分的種類和含量隨時間的變化情況,對魚腥草注射液中揮發性成分的質量穩定性達到比較全面的把握,也為中藥注射液穩定性研究提供了思路。
1 儀器與材料
1.1 實驗材料
魚腥草注射液(福建三愛藥業有限公司,批號:120604,120611,120502)
1.2 實驗儀器
Thermo Polaris Q氣相色譜—質譜聯用儀(美國Thermo-Finnegan公司)SPME萃取手柄、聚二甲基硅氧烷(PDMS,100μm)萃取頭、聚二甲基硅氧烷/二乙烯基苯(PDMS/DVB,60μm)萃取頭、15 ml帶聚四氟乙烯瓶塞的頂空取樣瓶(美國Supelco公司)色譜柱HP-5 MS毛細管色譜柱(30 m×0.25 mm,0.25 μm)(日本島津公司)ODS(C18)固相萃取頭100 mg/1 ml(大連依利特分析儀器有限公司)601數顯超級恒溫水浴(江蘇金壇市華歐實驗儀器廠)CP225D型、BS423S型分析天平(北京賽多利斯儀器系統有限公司)SHH-250SD型藥品穩定性試驗箱(重慶市永生實驗儀器廠)。
2 實驗條件與方法
2.1 實驗條件
2.1.1 色譜條件 色譜柱HP-5 MS毛細管色譜柱(30 m×0.25 mm,0.25 μm);載氣為氦氣;進樣口溫度 250℃;升溫程序:初始溫度 60℃,保持5分鐘,以6℃/min升溫至240℃;恒流模式,流速 0.8 ml/min,不分流。
2.1.2 質譜條件 電子轟擊(EI)離子源;電子能量70 ev;離子阱溫度230℃;質量掃描范圍m/z:30~500 amu。質譜數據運用NIST98標準譜庫進行檢索。
2.2 實驗方法
2.2.1 長期穩定性試驗 將規定批號的魚腥草注射液在溫度25℃ ±2℃、相對濕度(60±10)%的條件下放置,分別于0個月、3個月、6個月、9個月、12個月取樣一次。
2.2.2 加速穩定性試驗 將規定批號的魚腥草注射液在溫度40℃ ±2℃、相對濕度(75±5)%的條件下放置,分別于0個月、1個月、2個月、3個月、6個月取樣一次。
2.2.3 頂空固相微萃取—氣相色譜—質譜法(HS-SPMEGC-MS)分析穩定性研究期間樣品所含的揮發性成分 分別以兩個不同批號魚腥草注射液為研究對象(批號:120611,120502),精密吸取供試品5 ml,置15 ml帶聚四氟乙烯瓶塞的頂空取樣瓶中,經超級恒溫水浴加熱至55℃,預平衡40分鐘,使用聚二甲基硅氧烷(PDMS,100μm)固相微萃取頭頂空萃取40分鐘(55℃),取樣完畢,于250℃氣相色譜進樣口解吸附30秒,按2.1項下實驗條件進行GC-MS成分分析,經NIST98標準譜庫檢索結合人工譜圖解析,確定魚腥草注射液的揮發性成分。
3 實驗結果
魚腥草注射液揮發性成分HS-SPME-GC-MS總離子流圖見圖1;其中5種含量較高揮發性成分在加速、長期穩定性考察過程中變化情況見圖2~4;兩魚腥草注射液五種含量較高揮發性成分質量穩定性數據見表1、2。
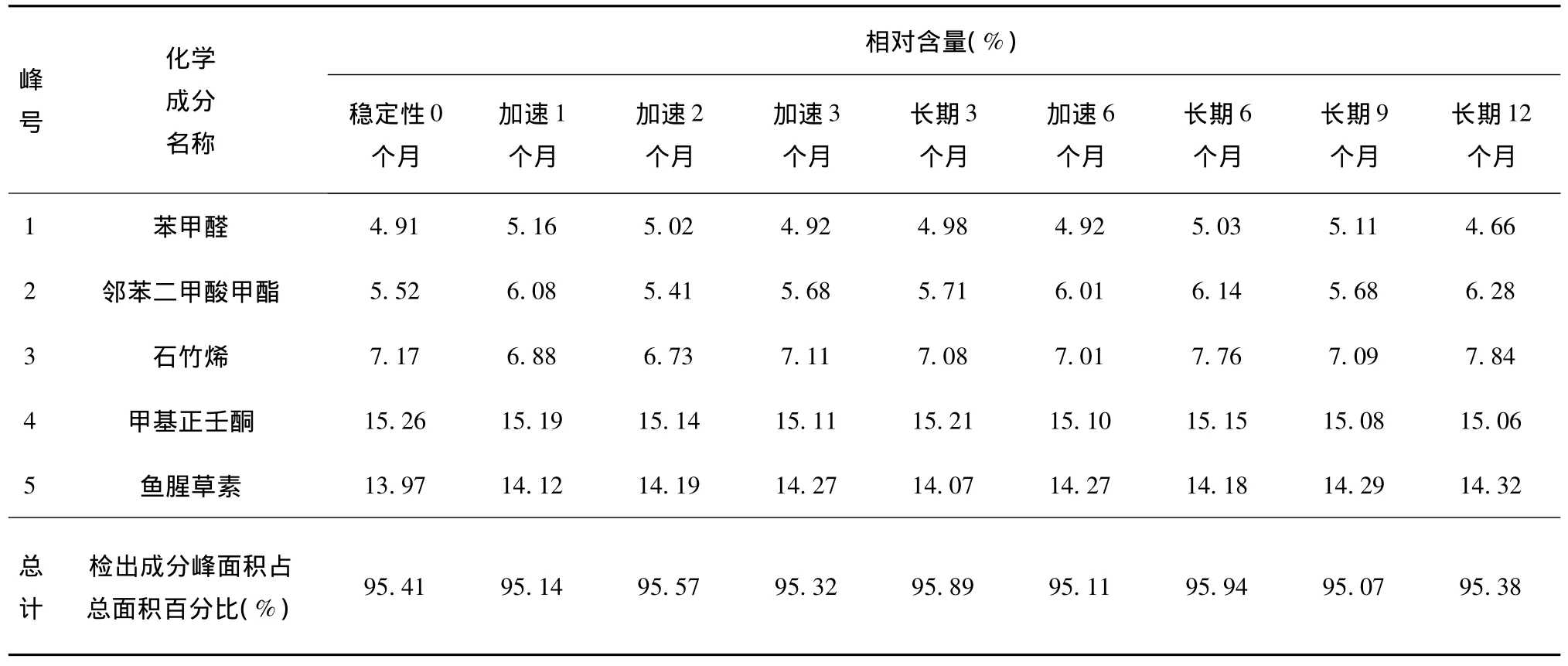
表1 HS-SPME-GC-MS對魚腥草注射液(批號:120502)揮發性成分穩定性試驗結果
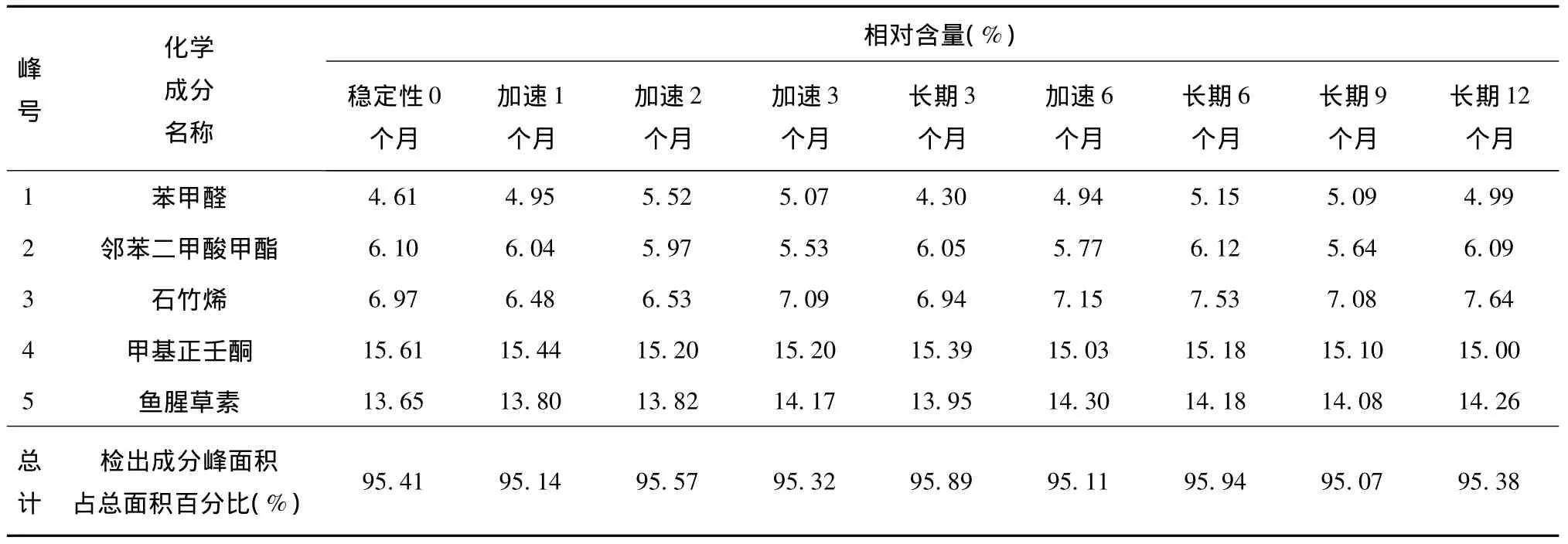
表2 HS-SPME-GC-MS對魚腥草注射液(批號:120611)揮發性成分穩定性試驗結果
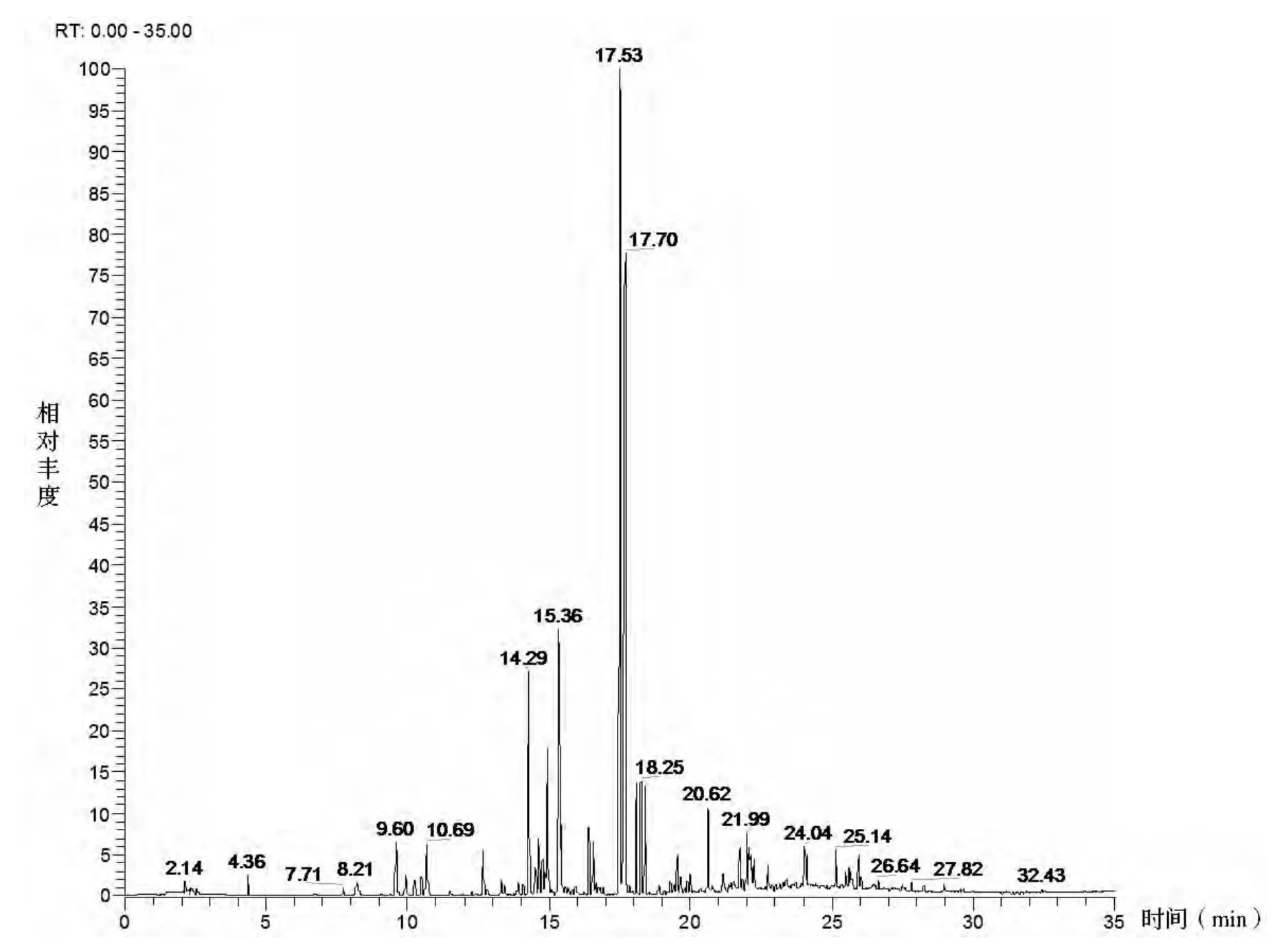
圖1 魚腥草注射液揮發性成分HS-SPME-GC-MS總離子流圖
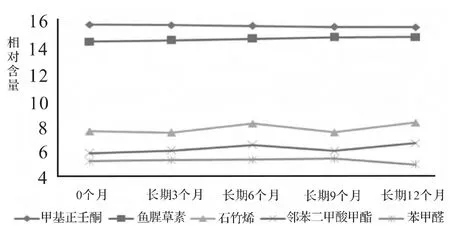
圖2 魚腥草注射液(120502)5種含量較高揮發性成分在長期穩定性考察過程中變化情況
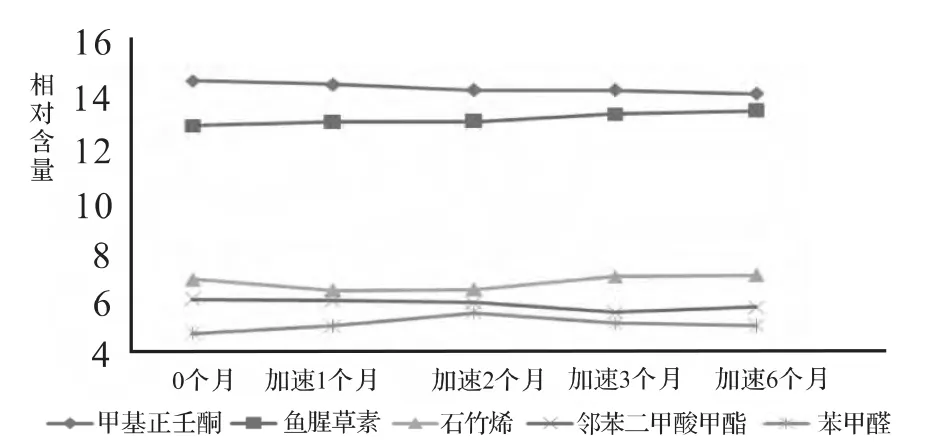
圖3 魚腥草注射液(120611)5種含量較高揮發性成分在加速穩定性考察過程中變化情況
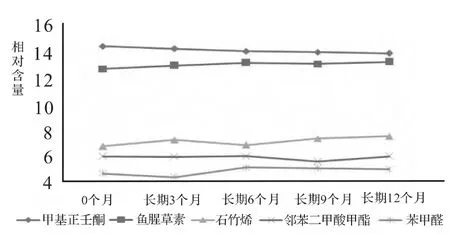
圖4 魚腥草注射液(120611)5種含量較高揮發性成分在長期穩定性考察過程中變化情況
4 小結與討論
通過HS-SPME-GC-MS技術對兩個不同批號魚腥草注射液中所含的揮發性成分進行加速、長期穩定性研究,穩定性試驗0個月時,兩批號魚腥草注射液揮發性成分種類基本一致,同種成分相對含量亦相近;從穩定性試驗過程的各個階段GC-MS鑒定的揮發性成分組成情況來看,共有組分有49種,共有化合物峰面積占檢出揮發性成分總峰面積的百分比均大于95%。實驗結果表明:魚腥草注射液中主要揮發性成分的種類沒有顯著變化,即隨著貯存時間的推移,未發現新成分產生,而原有主要揮發性成分的相對含量也未發生大的波動。本研究涉及的兩個批號魚腥草注射液中5種含量較高揮發性成分在加速、長期穩定性考察過程中的變化情況圖證實了以上結論。
魚腥草注射液中最主要的兩種藥效成分——魚腥草素和甲基正壬酮含量波動甚微,是相當穩定的。就魚腥草素而言,先前有些文獻報道[16]其質量很不穩定,易發生分解或聚合反應,是導致魚腥草注射液不良反應的原因之一。但經穩定性研究,在魚腥草注射液貯存過程中,魚腥草素相對含量變化極小,性質穩定。另有文獻報道[17]魚腥草注射液的不良反應與甲基正壬酮的含量有相關,本研究結果認為甲基正壬酮在考察期內含量基本穩定,未對制劑質量產生影響。
[3.3.1]-2-壬烯-9-醇、α-杜松醇、異欖香素等揮發性成分有時會檢測不到,但鑒于這些成分在制劑中的相對含量很低(都低于0.3%),從整體上看,可認為這樣的成分變化對魚腥草注射液的質量、安全性和療效不會產生影響。
但是針對魚腥草注射液穩定性的研究,由于時間和其它客觀因素所限,本研究僅選擇同一廠家的兩個批號制劑進行研究,樣品量較小,所得結論的確證仍需要后續研究更長時間的考察和不同廠家提供的更大樣本量的支持。
[1]《中藥辭海》編審工作委員會.中藥辭海(第二卷)[M].北京:中國醫藥科技出版社,1996.
[2]李爽,于慶海,金佩河.魚腥草的有效成分、藥理作用及臨床應用的進展[J].沈陽藥科大學學報,1997,14(2):144-147.
[3]江蘇新醫學院.中藥大辭典[M].12版.上海:上海科學技術出版社,2003:1439.
[4]梅巖.魚腥草和桑菊飲對免疫功能有影響的實驗研究[J].國外醫學中醫中藥分冊,1996,18(4):49.
[5]宋志軍,王潮臨,程建祥,等.魚腥草、田基和丁公藤注射液對大鼠免疫功能的影響[J].中草藥,1993,24(12):643.
[6]陸敏康,孟慶葉.魚腥草注射液與濕潤燒傷膏治療燒傷28例[J].湖南中醫雜志,1999,15(6):491.
[7]鞏聿清,武玉錦.魚腥草的臨床藥理研究進展[J].中國藥業,2005,14(3):73-74.
[8]趙子凱,李麗芬,石扣蘭,等.“復方養陰清肺湯”鎮咳、祛痰、抗炎及抑菌作用的實驗研究[J].中醫藥研究,1999,15(20):39-41.
[9]陳碧華.魚腥草注射液不良反應3例[J].實用藥物與臨床,2005,8(6):9.
[10]李曼,趙志恒,王忠,等.魚腥草注射液安全性的計量學評價[J].中國藥物警戒,2012,9(2):85-88.
[11]王書杰,王麗萍.魚腥草注射液不良反應126例文獻分析[J].中國藥業,2005,14(10):62.
[12]李亞莉.魚腥草注射液不良反應的回顧性分析[J].中國藥師,2005,8(2):164.
[13]王軍,姜毅,華碧春.魚腥草注射液致不良反應228例報告分析[J].中國醫藥導報,2006,3(17):192.
[14]單文治,毛飛,顧蘇俊.魚腥草注射液的嚴重不良反應分析[J].科學技術與工程,2006,6(12):1681-1682,1685.
[15]薛秀清,蔡曉虹.魚腥草注射液引起死亡1例[J].河南中醫,2006,26(9):80.
[16]魏定基.魚腥草注射液靜脈給藥不良反應分析[J].臨床合理用藥雜志,2010,3(4):60-61.
[17]葉世蕓,盧順林,李云超,等.魚腥草注射液不良反應與甲基正壬酮含量的相關性[J].中國醫院藥學雜志,2011,31(14):1166-1169.

