右美托咪啶對老年患者開胸手術后舒芬太尼靜脈自控鎮痛效果的影響
周 瓊, 趙 聰
(四川省成都市第五人民醫院 麻醉科, 四川 成都, 611130)
右美托咪啶是α2受體激動劑,具有鎮靜、鎮痛作用,可減少患者阿片類藥物的需要,且無明顯呼吸抑制作用[1]。老年患者重要組織器官代償能力減弱,且合并癥多,對阿片類鎮痛藥物敏感性、耐受性差,而開胸手術術后對鎮痛鎮靜的要求相對高,鎮痛藥的劑量加大,雖會加深鎮痛作用,但會引起其他不良反應,如呼吸抑制等[2-3]。本研究觀察右美托咪啶對老年患者開胸手術后靜脈自控鎮痛效果的影響,現報告如下。
1 資料與方法
擇期開胸手術老年患者40例,ASAⅡ~Ⅲ級。按照隨機數字表法隨機分為對照組(C組)和右美托咪啶組(D組),每組20例。 本研究經過醫院倫理委員會批準,并與家屬簽訂知情同意書。術前所有患者了解和熟悉PCIA泵的使用和和VAS評分。
麻醉方法選擇雙腔氣管插管全身麻醉,無麻醉前用藥。入手術室后,監測血壓(MAP)、心率(HR)、呼吸頻率(RR), 和脈搏血氧飽和度(SpO2), 靜脈建立輸液通路。全麻誘導靜脈注射咪達唑侖0.03 mg/kg、舒芬太尼0.3 μg/kg、依托咪酯0.3 mg/kg和順式阿曲庫銨0.15 mg/kg麻醉誘導,雙腔氣管插管置入接Ohmeda 200麻醉機行機械通氣,潮氣量設置為8~10 mL/kg。麻醉維持以吸入2%七氟醚及靜脈泵注丙泊5~10 mg/(kg·h)進行,間斷給予舒芬太尼及順式阿曲庫胺維持。手術需要時予以間斷單肺通氣。術終縫皮時,停止麻醉用藥。術后患者送麻醉恢復室觀察,待清醒自覺傷口疼痛(VAS>0)后,經輸液靜脈接PCIA鎮痛泵(內含舒芬太尼150 μg用生理鹽水稀釋至150 mL,即1 μg/mL), 并啟動PCIA(0時),同時D組以0.1 μg/(kg·h)持續輸注右旋美托咪啶至術后48 h PCIA結束,C組以D組相同速率持續輸注生理鹽水至術后48 h PCIA結束。2組PCIA均采用背景輸注速率2 mL/h, PCIA劑量2 mL/次,鎖定時間15 min。觀察30 min送返病房。術后經鼻吸O2(2~3 L/min), 48 h監測MAP、HR、RR和SpO2。
記錄2組患者年齡、體質量、性別比、ASA分級比、手術時間。記錄2組自覺傷口疼痛PCIA前(0),PCIA后4、8、12、24、48 h時VAS評分、MAP、HR、RR、SpO2和Ramsay評分(1~6分,1分為不安靜,煩躁; 2分為安靜合作; 3分為嗜睡能聽從指令; 4分為睡眠狀態,可喚醒; 5分為呼吸反應遲鈍; 6分為深睡狀態,呼喚不醒。其中3~4分為不良鎮靜,≥4分為過度鎮靜)。
2 結 果
2組年齡、體質量、性別比、ASA分級比、手術時間相比較,差異無統計學意義(P>0.05)。見表1。

表1 2組患者一般資料比較
2組術后鎮痛效果良好, D組PCIA后48 h各時點VAS評分小于C組(P<0.05), 而Ramsay鎮靜評分大于C組(P<0.05)。見表2。
術后PCIA鎮痛8 h時,D組MAP和HR低于C組,且與PCIA啟動時比較下降(P<0.05), 但2組均無低血壓或心動過緩需要處理,RR和SpO2組間比較及與PCIA啟動時比較無顯著差異。見表3。

表2 2組患者各時點VAS評分及Ramsay評分比較
與C組比較,*P<0.05。
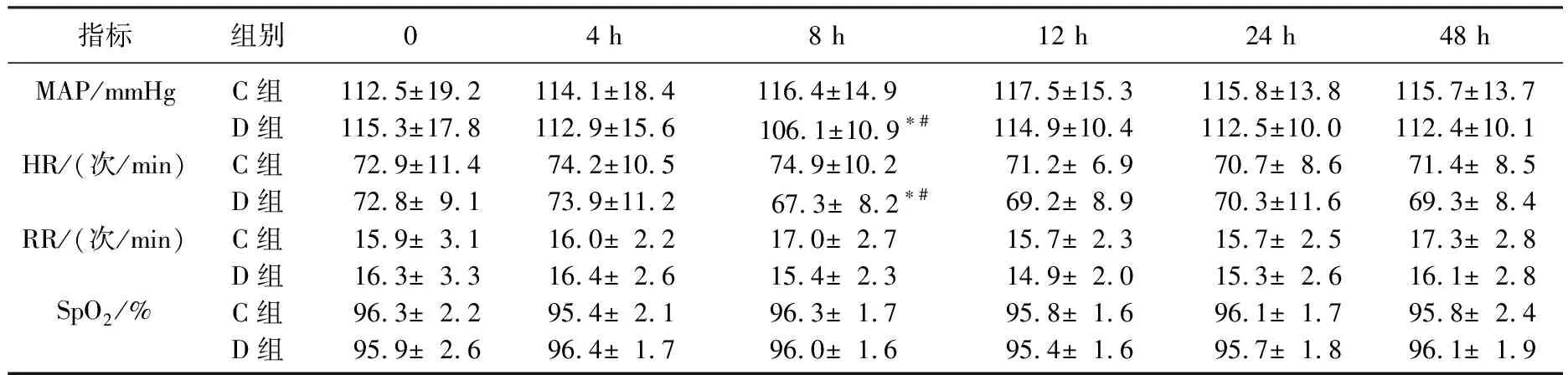
表3 2組患者平均動脈壓、心率、呼吸頻率、脈搏血氧飽和度比較
與C組比較,*P<0.05; 與基礎值(0)比較, #P<0.05。
右美托咪啶組舒芬太尼用藥總量及PCIA有效按壓次數分別為(106±8.2) μg和(15±3.6)次,較對照組的(125±7.6) μg和(19±4.1)次顯著減少(P<0.05)。
2組患者均未出現呼吸抑制。D組PCIA后發生惡心1例,嘔吐0例,瘙癢1例,頭暈1例;C組發生惡心5例,嘔吐4例,瘙癢2例,頭暈2例。D組不良反應發生率顯著低于C組(P<0.05)。
3 討 論
右旋美托咪啶對α2腎上腺素受體具有高選擇性,主要通過激動脊髓后角α2腎上腺素能受體抑制傷害性刺激向大腦傳導以及通過激動腦干藍斑核α2腎上腺素能受體降低神經興奮性減輕疼痛的不良情緒反應產生鎮痛作用[4];此外,右旋美托咪啶可能存在類可樂定的局部鎮痛機制[5]。本研究顯示,2組鎮痛效果良好,D組PCIA后VAS 評分低于C組;但Ramsay鎮靜評分高于C組,提示持續輸注右旋美托咪啶在鎮靜的同時增強了鎮痛作用,但無過度鎮靜。
舒芬太尼發揮鎮痛效應的同時可能產生呼吸抑制作用,特別是對于以后呼吸系統疾病的患者。開胸手術患者使用術后阿片類藥物靜脈自控鎮痛發生呼吸抑制的風險很高[6]。右美托咪定對呼吸系統的抑制作用較弱,與阿片類藥物相比呼吸抑制作用較輕且對其無協同作用。有研究[7]顯示,開胸手術患者術后48 h輸注右美托咪啶無明顯呼吸抑制。本研究顯示,2組患者呼吸頻率及脈搏血氧飽和度均無明顯下降。研究[8]表明,不予負荷劑量持續輸注右旋美托咪啶可避免循環波動,尤其適合危重或老年患者。本研究顯示,盡管D組術后8 h較PCIA啟動時MAP和HR下降,但未出現明顯低血壓或心動過緩,且2組患者各時點RR和SpO2組間比較無差異。本研究持續輸注右旋美托咪啶0.1 μg/(kg·h)低于臨床應用推薦劑量,用于老年患者術后多模式鎮痛可維持呼吸及循環相對穩定,是安全的。
右美托咪定可通過突觸前機制調解胃酸分泌而產生明顯的抗嘔吐作用,顯著減少術后惡心嘔吐的發生[9]。本研究顯示,持續輸注右旋美托咪啶輔助術后PCIA后,惡心嘔吐等不良反應發生率降低,提示持續輸注右旋美托咪啶達到了多模式鎮痛聯合用藥的目的,不良反應發生率降低。此外,研究表明右美托咪啶對重要器官有保護作用,可防止急性腦功能紊亂及術后譫妄。這表明右美托咪啶更適用于老年患者及高風險心臟病患者[10]。
[1] Afonso J, Reis F. Dexmedetomidine: Current role in anesthesia and intensive care[J]. Rev Bras Anestesiol, 2012, 62(1): 118.
[2] Conacher I D. Pain relief after thoracotomy[J]. Br J Anaesth, 1990, 65(6): 806.
[3] Ochroch E A, Gottschalk A. Impact of acute pain and its managementfor thoracic surgical patients[J]. Thorac Surg Clin, 2005, 15(1): 105.
[4] MacDonald E, Scheinin M. Distribution and pharmacology of alpha2-adrenoceptors in the central nervous system[J]. J Physiol Pharmacol, 1995, 46(3): 241.
[5] Zhang X, Bai X. New therapeutic uses for an alpha2 adrenergic receptor agonist-Dexmedetomidine in pain management[J]. Neurosci Lett, 2014, 561: 7.
[6] Venn R M, Hell J, Grounds RM. Respiratory effects of dexmedetomidine in the surgical patient requiring intensive care[J]. Crit Care, 2000, 4: 302.
[7] Ramsay MA, Newman KB, Leeper B, et al. Dexmedetomidine infusion for analgesia up to 48 hours after lung surgery performed by lateral thoracotomy[J]. Proc (Bayl Univ Med Cent), 2014, 27(1): 3.
[8] Ickeringill M, Shehabi Y, Adamson H, et al. Dexmedetomidine infusion without loading dose in surgical patients requiring mechanical ventilation: haemodynamic effects and efficacy[J]. Anaesth Intensive Care, 2004, 32(6): 741.
[9] Shin H W, Yoo H N, Kim D H, et al. Preanesthetic dexmedetomidine 1 g/kg single infusion is a simple, easy, and economic adjuvant for general anesthesia[J]. Korean J Anesthesiol, 2013, 65(2): 114.
[10] Pandharipande P P, Pun B T, Herr D L, et al. Effect of sedation with dexmedetomidine vs lorazepam on acute brain dysfunction in mechanically ventilated patients: the MENDS randomized controlled trial[J]. JAMA, 2007, 298(22): 2644.

