2012年奧硝唑注射劑抽驗結果與質量評價
河南省漯河市郾城區食品藥品檢驗所,河南 漯河 462300
2012年奧硝唑注射劑抽驗結果與質量評價
侯明華
河南省漯河市郾城區食品藥品檢驗所,河南 漯河 462300
目的評價國產奧硝唑注射劑的質量,分析存在的問題,為提高臨床用藥安全提供參考依據。方法按照2012年度國家評價性抽驗計劃總體要求,采用法定檢驗方法結合探索性研究對2012年度70批國產奧硝唑注射劑進行樣品檢驗,對國產奧硝唑注射劑的質量現狀進行評價。結果70批樣品均完成了全部檢驗程序,全檢率為100%,有1批奧硝唑氯化鈉注射液有關物質檢查項不符合規定,其余69批樣品結果均符合規定,合格率98.6%。結論奧硝唑注射劑總體合格率較好,現行質量標準基本可行,能夠控制該品種藥品的質量,但亟待完善。
奧硝唑注射劑;評價性抽驗;質量評價
奧硝唑是繼甲硝唑、替硝唑之后的第三代硝基咪唑類衍生物,具有良好的抗厭氧菌和抗原生質感染的作用,由于療效確切、組織刺激性小等特點,自20世紀70年代上市以來,被廣泛應用于臨床上各種感染性疾病的治療[1]。在國家食品藥品監督管理局加強對國家基本藥物質量監督管理的要求下,本所對70批奧硝唑注射劑進行評價性抽驗,統計分析檢驗結果,評價國產奧硝唑注射劑的質量,分析存在的問題,為提高臨床用藥安全提供參考依據。現報道如下。
1 抽樣情況簡介與方法
1.1 抽樣情況簡介 本次評價性抽驗樣品均由河南省各市級藥監局藥品市場監督管理辦公室自藥品生產單位、經營公司(零售藥店)及使用單位(醫院藥房、社區衛生中心)等領域抽樣,共抽取奧硝唑注射劑70批次,其中奧硝唑注射液53批(75.7%),奧硝唑氯化鈉注射液17批(24.3%)。樣品來源分布:生產企業21批(30.0%),經營公司13批(18.6%),使用單位36批(51.4%)。樣品來源涉及26個省、自治區以及直轄市,5個生產企業(SH、PD、KL、WL、JY),12個批準文號。本次的抽樣樣品覆蓋了多數的生產企業,代表廣泛,能反映目前國內奧硝唑注射劑的生產狀況;涉及樣品的生產批準文號占全國批準文號的92.31%(12/13),能較好地反映目前國產奧硝唑注射劑的質量現狀。
1.2 檢驗方法 依據國家食品藥品監督管理局頒布的國家藥品標準[1-2]和17個執行標準[3],對與產品質量密切相關的主要項目進行檢驗,如pH值,有關物質及奧硝唑、氯化鈉的含量測定等結果進行統計分析。為了更有效地評價藥品質量,在此次評價性抽驗中,還對奧硝唑注射劑的滲透壓、穩定性等開展了探索性研究。
1.3 統計學分析 采用SPSS12.0統計學軟件處理數據,對有關物質及奧硝唑、氯化鈉的含量測定等結果進行方差分析,以P<0.05為差異有統計學意義。
2 結果
2.1 法定檢驗結果 70批樣品均完成了全部檢驗程序,全檢率為100%,有1批奧硝唑氯化鈉注射液有關物質檢查項不符合規定,其余69批樣品結果均符合規定,合格率98.6%。
2.1.1 pH 70批樣品按照檢驗標準操作,奧硝唑注射液的pH值為2.30~3.60;奧硝唑氯化鈉注射液的pH值為3.10~3.90,二者差異無統計學意義(P>0.05);均符合現行標準[2](現行標準規定:奧硝唑注射液的pH為 1.8~4.0;奧硝唑氯化鈉注射液的pH 為3.0~5.5)。
2.1.2 有關物質 53批奧硝唑注射液的有關物質為0.24%~0.39%,符合注射液標準;17批奧硝唑氯化鈉注射液的有關物質檢查除有1批樣品為1.09%,不符合注射液標準中總雜質限度不超過1.0%的規定,其余樣品有關物質為0.58%~0.87%,均符合規定。
2.1.3 含量測定 五個生產廠家的奧硝唑注射劑的樣品含量為標示量的94.1%~104.7%之間,平均值為99.1%;方差分析結果為F=34.76,P<0.01,各生產廠家的注射劑含量差異有統計學意義,可能因為各廠家生產過程中投料量不同或不同規格的藥品投料量存在差異。見表1。
KL、WL、JY三個生產廠家的奧硝唑氯化鈉注射液中氯化鈉含量在標示量的98.7%~101.5%之間,平均值為99.8%(n=17) ;方差分析結果為F=1.03,P>0.05,可認為各生產廠家的注射液中氯化鈉含量差異沒有統計學意義,可能因為企業生產中氯化鈉基本按100% 投料,且工藝控制較理想。見表2。
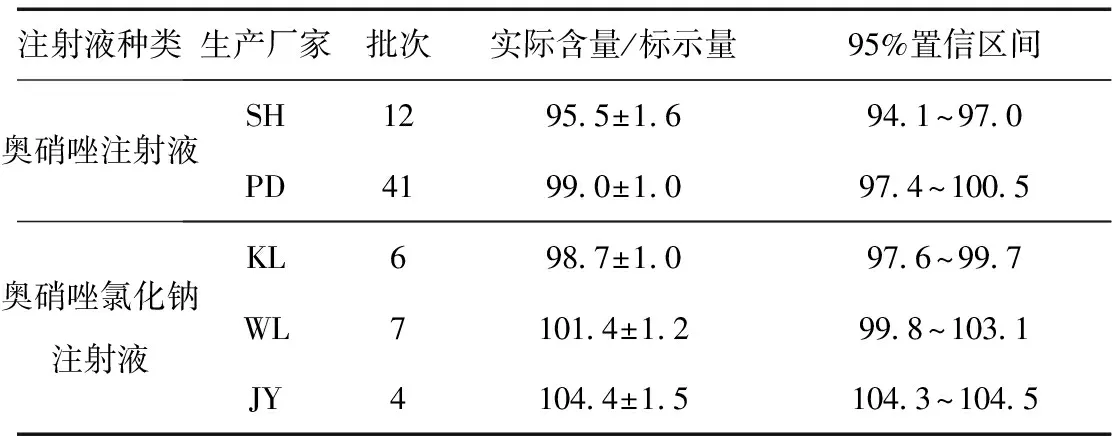
表1 奧硝唑含量測定(%)
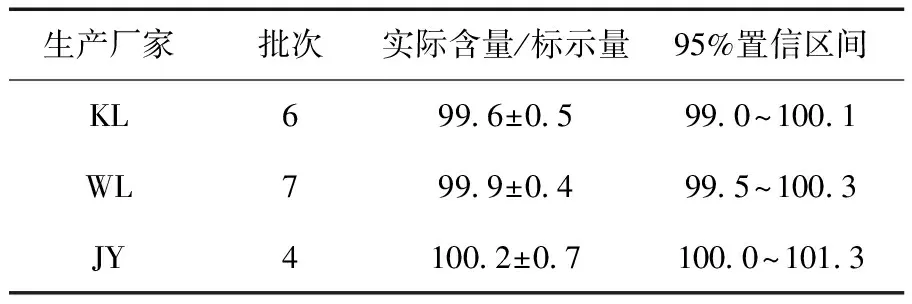
表2 氯化鈉含量測定統計表(%)
2.2 探索性研究結果
2.2.1 奧硝唑注射劑的滲透壓 采用冰點下降法測定滲透壓摩爾濃度,精密量取適量的供試品溶液,依法操作(中國藥典2010版二部附錄ⅨG[4]),測得17批奧硝唑氯化鈉注射液的毫滲透壓摩爾濃度為274~294 mOsmol·kg-1, 在正常人體血液的滲透壓摩爾濃度范圍內(285~310 mOsmol·kg-1)。不同生產企業所生產的同種規格奧硝唑注射液滲透壓摩爾濃度相差較大,可能由于各廠家生產工藝不同所致;其中,KL藥業生產的6批產品結果存在一定差異,WL藥業的7批產品結果差異不大,JY藥業的4批產品結果也差異不大,說明WL、JY藥業工藝較為穩定,KL藥業質量控制的穩定性須進一步加強。
2.2.2 穩定性試驗 取注射劑樣品分別置于3000 Lx光照下及40℃烘箱中,分別于0、5、10和20d后取樣測定,觀察樣品性狀,測定pH 值、有關物質以及奧硝唑、氯化鈉的含量。結果表明,樣品性狀、pH 值基本無變化,pH 值均穩定在2.3~3.90范圍內;但有關物質含量略有上升,奧硝唑含量略有下降,氯化鈉含量基本不變。說明光照及較高溫度(40℃)對注射液穩定性均有一定影響,需常溫避光儲存。
3 討論
藥品評價性抽驗指的是藥品監督管理部門為了掌握、了解轄區內藥品質量的總體水平與狀態而進行的抽查檢驗工作[5]。迄今為止,奧硝唑注射劑尚未收載于《中國藥典》中,關于其質量測定沒有統一的標準,本次抽驗主要依據2010年國家食品藥品監督管理局頒布的試行標準和17個執行標準進行檢驗,并結合探索性研究對其質量進行了較全面評價。由檢驗和探索性研究結果可知:奧硝唑注射劑總體合格率較好,pH值、奧硝唑氯化鈉注射液的毫滲透壓摩爾濃度符合現行標準規定。
同時,分析試驗數據,也發現存在一些問題:①文獻報道[6],當pH>4.0時,奧硝唑注射劑滅菌后產生的有關物質會超過規定限度,本研究中奧硝唑氯化鈉注射液的pH高于奧硝唑注射液,有關物質也偏高,進一步證實了文獻報道。但是人體可耐受的pH范圍為4~9,pH<4會導致疼痛或靜脈炎,而奧硝唑注射劑的pH值均低于4.0,因此建議改變制備方法或者改變奧硝唑劑型對其進行開發。②不同生產企業的產品中有關物質及主成分含量等指標差異較大,可能因為各廠家生產過程中投料量或各廠家不同規格的含量投料存在差異,因此應盡快統一并提高質量標準。③2-甲基-5-硝基咪唑為奧硝唑注射劑有關物質測定中一個主要的雜質,其含量的檢查能有效地控制其質量[7-8],穩定性試驗中發現有關物質含量略有上升,奧硝唑含量略有下降,建議對注射劑中的2-甲基-5-硝基咪唑及其他有關物質進一步考察。
[1]魏春燕,王文娣,梁艷芳,等.HPLC法測定奧硝唑注射液中2-甲基-5-硝基咪唑的含量[J].中國藥師,2012,15(9):1291-1293.
[2]國家食品藥品監督管理局.國家食品藥品監督管理局國家藥品標準(修訂)頒布件(ZGB2009-4~11)[J].中國藥品標準,2010,11(1):65-78.
[3]詹學鋒.2007年1月~2008年1月國家食品藥品監督管理局制定和發布實施的行政法規[J].醫藥導報,2008,27(4):484.
[4]The European Pharmacopoeia Commission. European Pharmacopoeia 7.0[S]. Strasbourg, France: The Directorate for the Quality of Medicine of the Council of Europe,2010.
[5]國家藥典委員會. 中華人民共和國藥典. (2010年版二部)[S]. 北京: 中國醫藥科技出版社,2010.
[6]梁鑫,劉哲丞,張杰,等.吡拉西坦氯化鈉注射液中有關物質的測定[J].齊齊哈爾醫學院學報,2010,31(6):915.
[7]張曉璐,丁建,張曉棟,等. 2011年奧硝唑注射劑抽驗結果與質量評價[J]. 藥學與臨床研究,2013,21(2):160.
[8]段燕冰,劉實,張射兵,等. pH 值對奧硝唑注射液滅菌穩定性的影響[J]. 醫學綜述,2010,16(19):3026.
[9]張京玉,侯學會,吳春麗,等. 一種奧硝唑降解雜質的分離,結構確證及制備[R].2010 年中國藥學大會暨第十屆中國藥師周論文集,2010.
R975
A
1007-8517(2014)11-0106-02
2014.04.15)

